机器学习CNN模型在心血管疾病诊疗中的临床应用及研究进展
艾克力亚尔·艾尼瓦尔 马翔,2
(1.新疆医科大学研究生院,新疆 乌鲁木齐830054; 2.新疆医科大学第一附属医院,新疆 乌鲁木齐 830054)
人工智能自20世纪60年代提出以来,发展迅速,机器学习作为实现人工智能的方法,用来解析和学习数据,通过算法完成数据整合任务。深度学习是目前最前沿的机器学习模型,其独有的自动提取特征的特点,使人工算法为临床所用。中国心血管疾病人群庞大,临床医生数量缺口大,往往无法满足患者就医需求,因此机器学习被应用到心血管疾病诊疗中。
1 机器学习
1.1 机器学习概述
机器学习近年来被广泛应用在临床诊疗中。深度学习属于机器学习的一种,通过“黑匣子”[1]自动学习数据的特征和关系,在阅读医学图像数据,诊断疾病及疾病危险分层等方面具有巨大潜力[2-3]。
机器学习通过组成简单但非线性的模块来获得,每个模块将一个层次的信息转换为一个更高、稍微抽象的层次的表示。在临床常应用的模型是卷积神经网络(convolutional neural network,CNN)模型[4-5],应用于X射线、CT、MRI和超声心动图等影像学检查,也可用于心电图的辅助诊断[6-9]。其识别图像的基本步骤为:识别图像特征,图像分类,对图像进行分割,评估图像形态结构的测量和量化、识别图像[10]。
1.2 CNN
CNN是一类指导学习网络,可以自主感知输入与输出之间的映射关系,从而分析和处理数据[11]。为了建立CNN模型,需要收集大量临床信息、影像学资料和随访资料,并根据资料特征分类。以影像学资料为例,在训练过程中(见图1),CNN[4]模型首先会看到一幅图像即输入层,计算机理解为输入若干个矩阵,会把图片光栅化,以像素形式存在,并以分数向量的形式输出结果,进入卷积层,通过多个可训练的滤波器和加权偏置进行卷积,卷积后进入池化层产生若干个映射图,特征映射图中每组多个像素进行求和、加权值和加偏置,紧接着通过一个函数得到多个下一层的特征映射,并通过与上一层相同的方法产生下一层映射,每一层都可提取上一层的局部特征,局部特征的确定意味着两层间关系的确立,最终通过特定排列检测图像边缘,将图案组合匹配更大的图案组合得到输出结果[12]。卷积层与池化层的组合可以在隐藏层出现很多次,出现次数是根据模型的需要而来的。选取的函数是根据对默认参数和二进制交叉熵的要求来进行选定,常用函数有RELU函数和sigmoid函数等。最后一次池化结束后,进入全连接层,将分布式特征映射到样本标记空间,实现对图形分类并输出结果。以上就是CNN模型对影像学资料深度学习的基本流程,对于临床资料的学习,可省去图片光栅化的过程,后面的流程与影像学资料学习过程一致。

图1 CNN模型示意图
2 在心血管疾病方面的应用
2.1 在辅助检查的应用
2.1.1 CT
CT在临床上常用于先天性心脏病、主动脉夹层和冠心病等的诊断,然而主要为二维成像,且心脏具有特殊结构,导致CT扫描无法显示清楚,对临床诊断造成干扰。Tatsugami等[13]通过深度学习混合迭代重建方法改善冠状动脉CT血管成像图像质量,Bruns等[14]使用深度学习模型,在冠状动脉CT血管成像中进行全心分割,量化心脏测量结果。深度学习模型通过训练大数据,对图片上极小的像素位置差异进行识别,也可优化影像学资料,为疾病的诊断提供极大的帮助。
2.1.2 超声心动图
超声心动图是利用超声技术获取心脏及其周围结构的高时空分辨率图像,然而心脏的结构复杂,图像固有的斑点噪声,超声图像相位及心脏轮廓模糊等因素,为临床诊疗带来不便。CNN模型可对超声心动图进行合适的分割[15],自动测量左室射血分数,对心尖二腔切面和心尖四腔切面进行准确分割,并可识别节段性室壁运动异常[16],且判读能力优于低年资医生,并达到专家水平。该模型[17]甚至可以通过超声心动图自动检测肥厚型心肌病、心脏淀粉样变和肺动脉高压(见表1)。
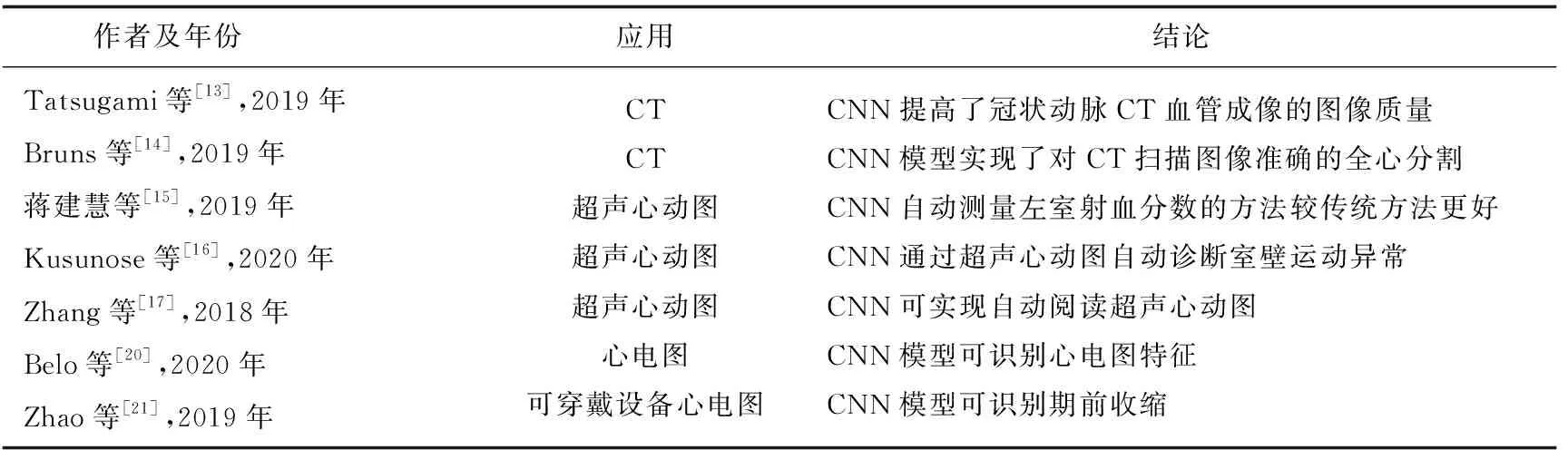
表1 CNN模型辅助检查利用
2.1.3 心电图
心电图是一种常用诊断心血管疾病的工具,但偶尔会发生漏读或误读[18]。近年来,不少研究通过深度学习模型阅读心电图[19]。心电图的自动分析依赖于两阶段的方法,首先需要人根据原始心电数据提取特征[20],然后部署决策规则或其他机器学习方法来生成最终结果。心电图还具有容易受干扰的特点,因此去噪成为了深度学习所要克服的另一大难题。Zhao等[21]采用了一种广泛应用的深度学习技术来进行心电去噪。除此之外,心电图具有一维图像的特点,分类常用的CNN有两种:一维CNN[22]和二维CNN[23]。这些模型可以做到心律失常的检测[24-25]和分析ST段的变化[26]。深度学习模型擅长阅读二维的图片如CT和MRI等,由于心电图的特殊性,往往需要必要的手段对图片进行加工或使用专用模型才能阅读。由于这些因素的限制,目前的手段只能让深度学习模型阅读简单的心电图结果,随着计算机科学的发展,在不久的将来会出现适合阅读复杂心电图的深度学习模型。
2.2 在心血管疾病危险分层的应用
在日常对心血管疾病的诊疗过程中,对心血管疾病的危险分层尤为重要,临床上常使用TIMI评分、GRACE评分及ACTION评分,然而传统评分过分依赖于实验室指标,往往无法早期评估病情[27]。心血管疾病治疗方法的发展,以及新的心血管药物的出现对心血管疾病的危险分层带来新的挑战,因此,借助深度学习模型探索心血管疾病危险分层的新方法成为近年来的热点(见表2)。Kwon等[28]对急性心肌梗死患者的数据进行分析,使用CNN模型对其危险度进行分层(DAMI评分)的表现与GRACE评分、ACTION评分以及TIMI评分进行了比较。结果发现模型评估ST段抬高心肌梗死和非ST段抬高心肌梗死危险分层的能力明显优于这三种评分。除此之外,在6个月的随访中,由DAMI定义的高危组的死亡率显著高于低危组。Huo等[29]提出了一个机器学习模型,通过分类分析将以往确诊和误诊的主动脉夹层进行分类,可帮助医师快速发现所有误诊的主动脉夹层阳性患者,评估入院后病情进展。通过对实际病例数据的训练,该预测模型可以确定患者的优先等级。深度学习参与对心血管疾病危险分层准确性更高,但在一定程度上依赖于心血管医生对患者临床信息的掌握,准确及全面的疾病信息可以使深度学习模型发挥出更好的作用。传统评分已通过大量临床病例考验并沿用至今,深度学习模型病例数较少,还需要大量临床实践验证其临床实用性。

表2 疾病风险估计及预后预测
2.3 在评估心血管疾病预后的应用
心血管疾病一级预防的关键策略是“预测”,以往用来预测心血管疾病的手段甚少,常用的心血管疾病预测手段也并非十分准确[30]。深度学习模型可以发现临床医生无法察觉的细微病情变化,并使用大数据模型很好地预测病情。Wu等[31]收集了急诊就诊的胸痛患者的数据,建立一个深度学习模型来预测患者的非ST段抬高心肌梗死。Kwon团队[32]借助深度学习模型对心力衰竭患者进行预后分析的一项研究发现,与现有的风险评分和其他机器学习模型相比,他们的这个模型能更准确地预测急性心力衰竭患者的住院和长期死亡率。Zack等[33]为了确定深度学习模型是否可以更好地预测经皮冠状动脉介入治疗后存在死亡或充血性心力衰竭再住院风险,评估了11 709例不同的患者,研究发现深度学习模型具有更好的预测能力。Commandeur等[34]在一项前瞻性研究中用CNN模型评估了心外膜脂肪组织,评估冠状动脉钙化分数,并纳入了必要的临床指标,将这些临床资料用来训练机器学习模型,用模型给受试者评分,将得分与动脉粥样硬化风险评分相比较,发现机器学习评分有更好的预测能力。心血管疾病具有发病迅猛的特点,因此通过心血管疾病危险因素预测心血管疾病的发生尤为重要,以往只能通过疾病危险因素来判断疾病发生的可能性,将深度学习模型引用到疾病预测的手段当中,可以量化疾病风险,甚至可以提前发现最危险因素,并在未病阶段进行有效干预,为疾病治疗赢取时间。然而,深度学习模型需要依赖检查结果,无法像人那样仅根据临床表现对疾病预后进行评估,该模型目前阶段仅适用于可以完善初期检查的病情变化较缓慢的疾病。
3 总结与展望
使用机器学习模型对各类心血管疾病的诊断以及评估是一种非常客观的方法,在模型训练准确的情况下,不会出现因评估医生能力不同而产生误差的情况,且这类模型对各种辅助检查图像的改善、图像的解读、心电图的阅读具有优秀表现。模型对疾病轻重缓急可以进行迅速评估,准确度普遍高于传统的评分标准,为临床治疗赢取时间。模型还可以减少临床医生的负担,提升基层医院诊断水平。深度学习模型另一个潜在应用可以将实时图像与之前影像学检查的图像进行自动比较,从而使解读的医生能够更直观地了解疾病进程。
然而,目前的模型还需更多的试验去验证,深度学习的方法是一个“黑匣子”,无法准确了解计算机模型中各个临床指标的实际作用,这种未知因素会带来一定的风险甚至会带来医疗纠纷。深度学习模型的建立往往需要大量的临床资料,而由于罕见病临床资料较少,因此机器学习模型可能无法适用于罕见病。模型对录入数据要求高,如果输入的数据质量较差或有偏差,解释的质量也会较差,此外,必须强调创建数据的统一标准,从而允许不同算法之间的集成,允许算法在不同的设备上运行。
2020年,谷歌的研究人员[35]宣布已找到破解深度学习“黑匣子”的方法,也许在不久的将来,深度学习模型会变得更加安全,机器学习将来仍是一种不可忽视的辅助医疗力量,其现有的缺点也将会渐渐被改进。