基于系统仿真的数字乳腺层析成像性能分析
邓耀宏,朱曼曼,李 穗,王永波,高 杨,马建华
1南方医科大学生物医学工程学院,广东 广州 510515;2广州市医用放射成像与检测技术重点实验室,广东广州 510515
乳腺癌是女性群体中普遍患病率和致死率最高的癌症之一,研究表明早期的乳腺癌探查能够显著地提高存活率[1]。X射线钼靶摄影技术已经兴起为目前最重要和最有效的早期筛查乳腺癌的工具。但钼靶图像中的组织重叠现象使探测乳腺微小病灶变得具有挑战性。相较于传统的2D数字钼靶摄影技术(DM),3D数字乳腺层析成像(DBT)可降低重叠的乳腺解剖结构,从而具有提升微小肿块和钙化点病灶的探测敏感性的潜力[2-6]。DBT是一种三维成像模态,在有限角度范围内获取一系列低剂量的投影数据后,以一种伪断层的方式重建3D图像[7-8]。
图像质量是受许多不同因素交互作用的产物,现有的评估DBT图像性能的研究主要可分为2类。第1类是探究比较不同乳腺成像模态在图像诊断质量方面的差异[9-12],例如实验证明:相比DM图像,DBT图像更易于检出微钙化点的病灶情况[13]。DBT图像中乳腺肿块的表征显像能力相比于DM图像有显著的提升[14]。第2类是评估扫描协议中的各项参数对于成像性能的影响[15-16],例如,Hu等[17]研究分析成像系统特征(即几何、重建参数等)同图像质量之间的联系。在一个DBT原型机上试验3个乳腺体模在3种重建算法下的对比分析结果[18]。
然而,大多数方法均利用体模数据和机器读取的重建后图像数据,并且通过仿真技术获取DBT的投影数据,然而这类数据有别于临床人体乳腺数据和原始DBT 投影测量数据,此外原始数据因归属权难以获取。因此本实验采用从DBT扫描机器中获取的物理体模和人体乳腺两类原始测量数据,从而能够更佳精准地研究辐射剂量和重建算法两大因素对于最终成像质量以及病灶信号探测的影响。首先,本实验从临床DBT系统中获取3种不同辐射剂量水平下物理体模和常规剂量下临床患者原始投影数据,并对患者数据进行低剂量仿真。然后采用3种具有代表性的DBT重建算法对这些投影数据进行图像重建与结果分析。实验结果表明,在合适的范围内,如40 milliampere-second(mAs)至120 mAs之间,增加辐射剂量可提升DBT图像信噪比和病灶可探测性;然而不同重建算法在不同解剖结构区域处的表现性能的优劣有差异,具有全变分约束的自适应最速下降凸集投影(ASDPOCS-TV)算法的结果质量一般地优于其他联合代数重建技术(SART)和Feldkamp-Davis-Kress(FDK)两算法的结果。因此,针对某个给定临床任务,平衡各影响因素、整体图像质量、临床诊断需求之间的关系是获取最优成像性能的关键。
1 方法
1.1 DBT成像系统
如图1A所示,为Hologic公司的Selenia Dimensions型号DBT系统的机型外观示例图。图1B显示该DBT系统带有平板探测器的弧形轨迹扫描几何结构示意图。其中,X射线源旋转平面平行于胸壁,平板探测器随着射线源的旋转偏转相应的角度。X射线源焦点到平板探测器的距离(SDD)是700 mm,气隙大小为25 mm。探测器整体大小为24×29 cm 其单个像素的尺寸为0.07×0.07 mm。射线源在从-7.5°到+7.5°的角度范围,每间隔1°采集一次投影数据,共采集15次投影,采集视图有首尾位(CC)和内外斜侧位(MLO)[19]。本实验中重建图像层数为50层,重建层厚为1 mm,重建图像像素大小为0.088×0.088 mm。
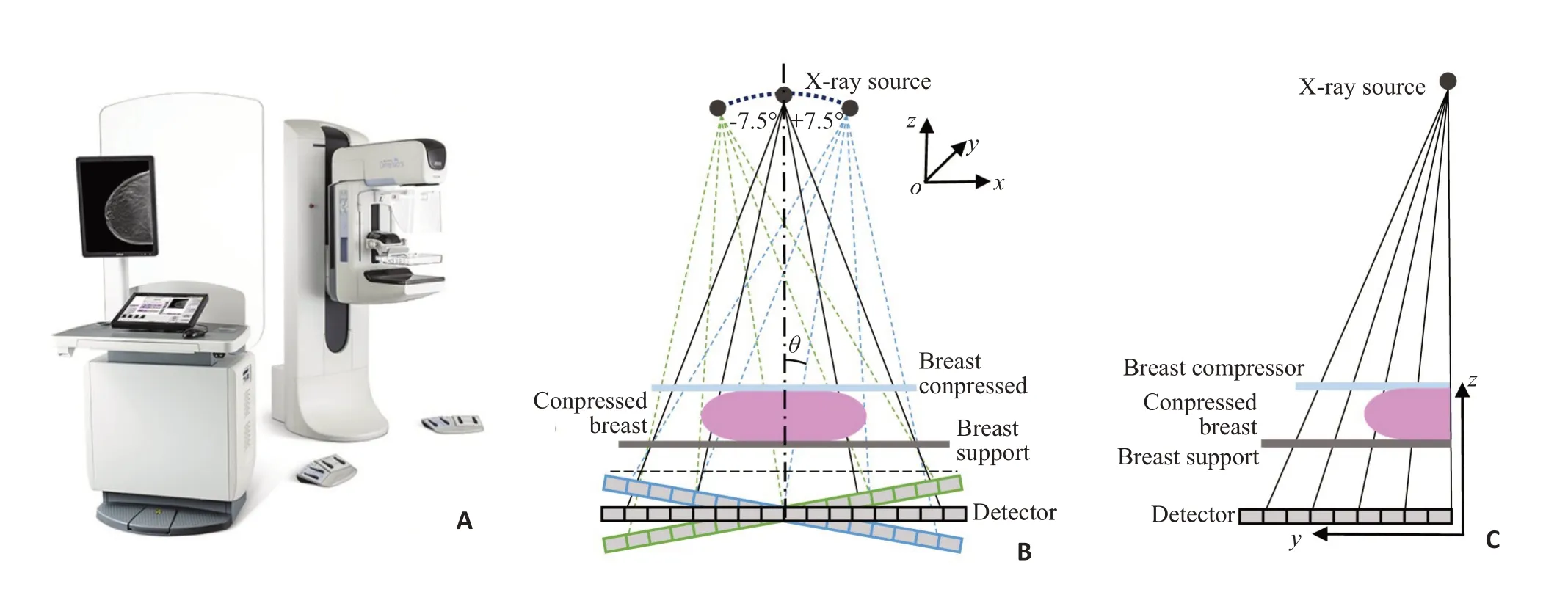
图1 DBT系统示例Fig.1 Illustration of the DBT system:A:The Hologic selenia prototype tomosynthesis system;B:Main view of standard acquisition geometry of the prototype DBT system;C:Lateral view of standard acquisition geometry of the prototype DBT system.
1.2 低剂量DBT仿真算法
Lucas等[20]提出一种低剂量DBT仿真方法,该方法将DBT图像中信号的分布以及电子噪声特性纳入仿真过程。该算法主要包括以下5个步骤:(1)将DBT原始测量数据中减去估计的偏置(offset);(2)将剩余的信号数据通过方差稳定变换(VST)进行变换处理后加入量子噪声;(3)将处理后的信号乘以剂量降低比例因子以获得所期望的低剂量水平信号;(4)然后对上一步骤得到的信号进行逆VST变换并加入电子噪声;(5)将步骤(1)中减去的offset加回处理后的信号,得到最终仿真的低剂量DBT投影数据。进一步地,像素间的串扰情况也被考虑进来,被认为是频率相关的噪声。
1.3 DBT重建算法
DBT采用有限角度锥束扫描方式采集投影数据并进行“伪断层”重建,经典的DBT重建方法包括解析和迭代两类方法,其中迭代类的重建算法进一步可分为代数迭代和统计迭代两类算法。故此,本文采用最具代表性的3种算法对不同剂量下投影数据进行DBT图像重建,分别是解析的FDK算法[21],代数迭代的SART算法[22],统计迭代的ASDPOCS-TV 算法[23]。
1.3.1 FDK算法 FDK算法基于2D滤波反投影的近似3D锥束投影重建算法。该法快速有效,应用最为广泛,然而其在低曝光剂量和曝光次数较少的情况下受噪声影响较大,且当锥角增加时,其重建误差也随之增加。
1.3.2 SART算法 SART算法基于每个投影角度下通过某个像素的投影线积分的理论计算值与实际测量投影值之间的误差来校正该像素值。该法通常可获得低剂量下的较高质量图像重建,但是迭代优化过程计算成本较高。
1.3.3 ASDPOCS-TV 算法 ASDPOCS-TV算法基于压缩感知和体积图像的值为非负的约束条件,保证投影数据在一定误差范围内,使得图像的全变分(TV)最小。该方法利用凸集投影(POCS)来实现约束,并通过自适应步长的最速下降来最小化TV目标。它对锥束伪影具有较强的鲁棒性,通常适用于角度范围有限或角度采样率较低等情况。
1.4 图像性能评价指标
1.4.1 信噪比(SNR)和峰值信噪比(PSNR)信噪比(SNR)和峰值信噪比(PSNR)评估噪声含量[24],其公式分别表达如下:
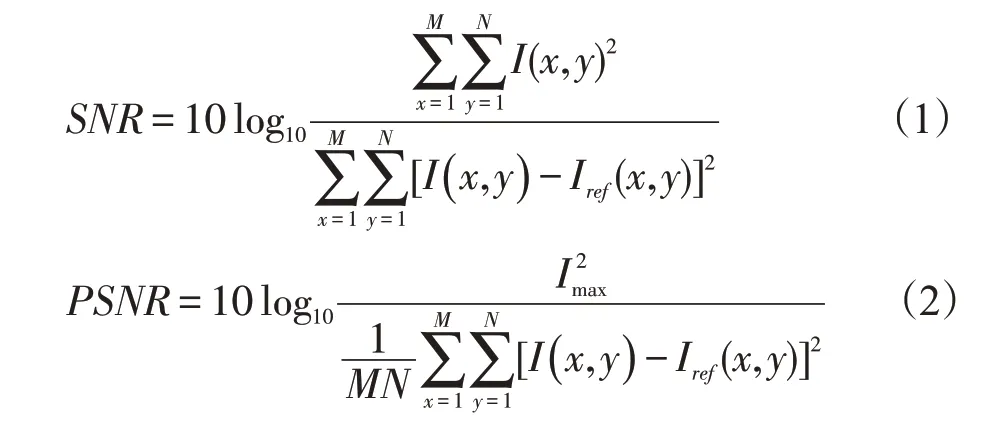
记I(x,y) 为被测量图像在位置(x,y) 处的像素值,M 和N 表示被测量图像在长和宽方向的像素个数。Iref(x,y) 通常表示无噪声的或高剂量下的参考图像,Imax是指被测量图像I(x,y) 中像素值的最大值。值得注意的是,SNR描述全图中信号的分布和噪声的强度,数值越高说明信号成分越高、噪声成分越低,失真程度越小;而PSNR基于对应像素点间的误差同时指示边缘信号对比度,数值越高说明图像的失真程度越小,图像质量越接近于参考图像。
1.4.2 噪声功率谱(NPS)此外,噪声功率谱(NPS)指示图像中不同频率信号成分的分布情况,其公式定义如下[25]:
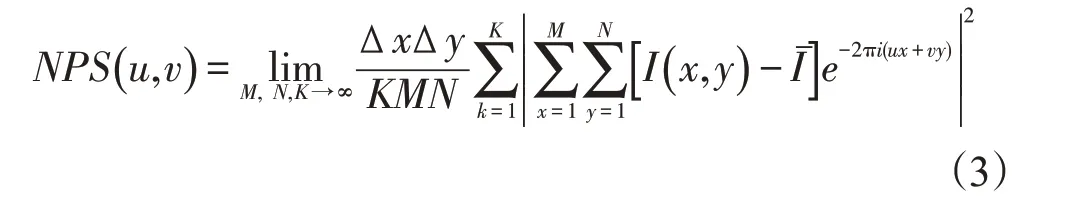
1.4.3 伪影扩散函数(ASF)和全宽半高值(FWHM)伪影扩散函数(ASF)及其全宽半高值(FWHM)指示空间分辨率和层间伪影扩散程度。在重建的3D DBT图像中,以该钙化点为中心层面的上下多个断层图像中均出现扩散的伪像信号。同时,该现象也可理解为由于图像空间分辨率低造成层间信号模糊。因此,ASF 定义为关于z 轴方向上层面索引的函数,公式定义如下[26-27]:
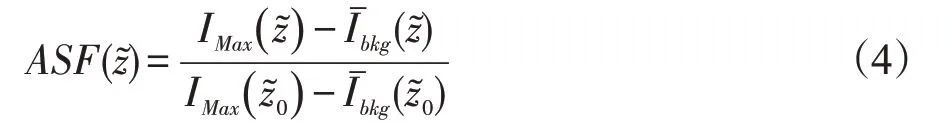
1.5 统计学分析
首先计算各项量化指标的均值和标准差等数学特征。其次,量化指标值通常在随机采样数据集中满足高斯分布,因此本文使用单因素方差分析[28-29]进行患者数据部分量化指标的统计学显著性差异分析。设定显著性置信水平为0.05,即P<0.05时说明该量化指标值关于某一因素(辐射剂量或重建算法)有显著性差异。
2 实验
2.1 实验数据集建立
实验数据包括1套物理体模和15套患者数据,均采集于同一DBT系统(南方医院,Hologic DBT)。其中,采用的物理体模(CIRS Model 015)[30-31]如图2所示,包含模拟腺体、钙化点、纤维的组成成分。该体模的尺寸是10.8×10.2×4.4 cm(长×宽×高),嵌在蜡中的条状、点状和团状分别仿真压迫状态乳腺中的纤维结构、微钙化点和肿块。体模以CC位的视角扫描3种剂量水平的投影数据,管电压固定为31 kilovolt-peak(kVp),管电流分别是120、60、30 mAs。
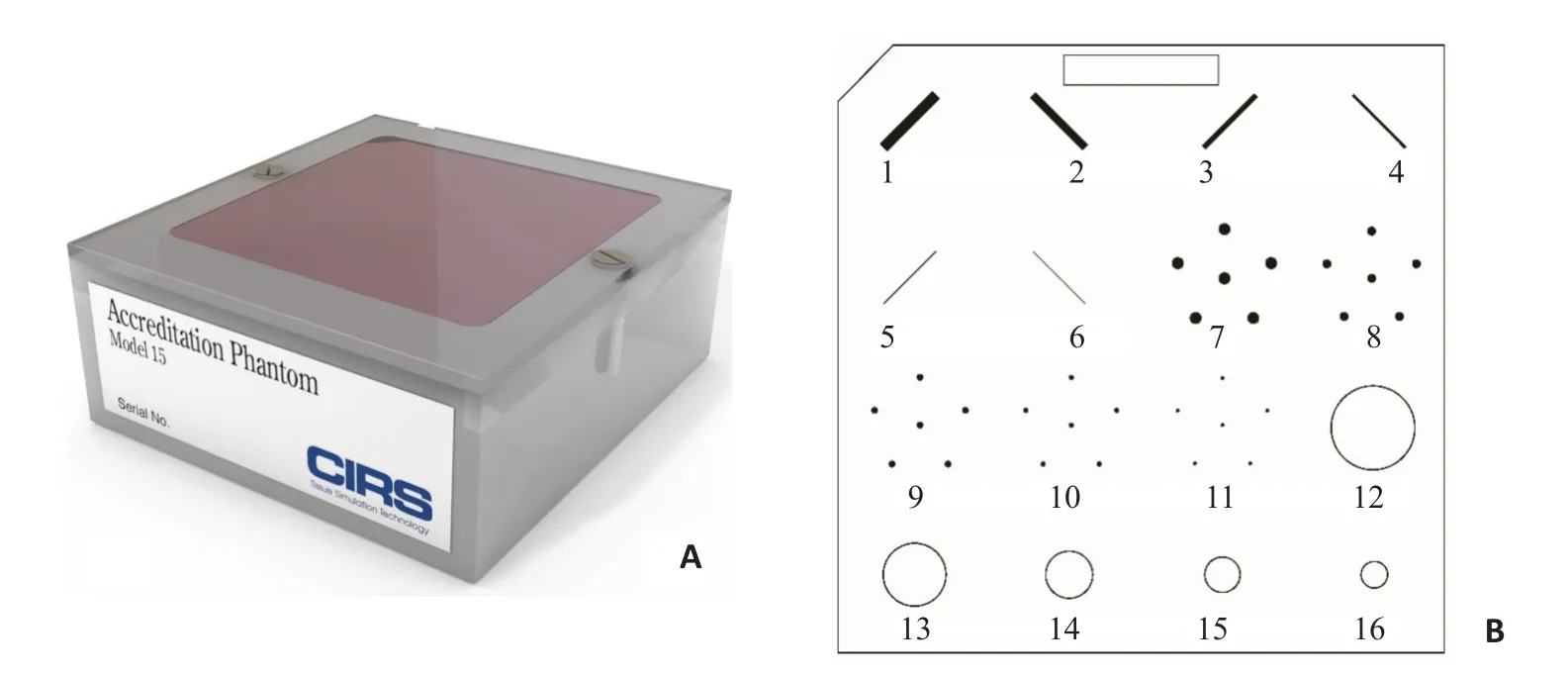
图2 物理体模示意图Fig.2 Illustration of the physical phantom:A:Appearance of the phantom;B:Diagram of the internal structure.
此外,从南方医院共收集20例乳腺钙化患者(15例良型,5例恶性)左右乳腺分别扫描CC位和MLO位2个视角的图像数据及其原始投影数据共计80套,均已签署患者知情同意书。由于自适应曝光扫描协议,于是本实验挑选其中15套数据(11套良性,4套恶性),这些数据的管电压范围为29~32 kVp,管电流范围为57~63 mAs。为简化后文描述,这些被挑选出来的数据一致地看作是管电压为30 kVp和管电流为60 mAs。
物理体模以120 mAs的投影数据为参考仿真其对应60 mAs和30 mAs的投影数据,患者数据以60 mAs的投影数据为参考仿真其对应40 mAs和25 mAs的投影数据。以上所有投影数据后续将采用3种不同的重建算法进行图像重建,并进行后续结果分析。
2.2 实验参数设置
本实验分为3部分:(1)对体模数据和患者数据进行仿真实验和结果分析,验证仿真算法的有效性;(2)利用体模数据和患者数据,在统一使用FDK算法的情况下,比较评估3种剂量下的重建图像质量;(3)利用体模数据和患者数据,比较分析3种重建算法的重建图像质量,值得注意得是,本文考虑到重建算法具有一定鲁棒性,因此对所有剂量下由同一种算法重建的图像结果看作整体,进而分析不同重建算法之间的差异(表1)。
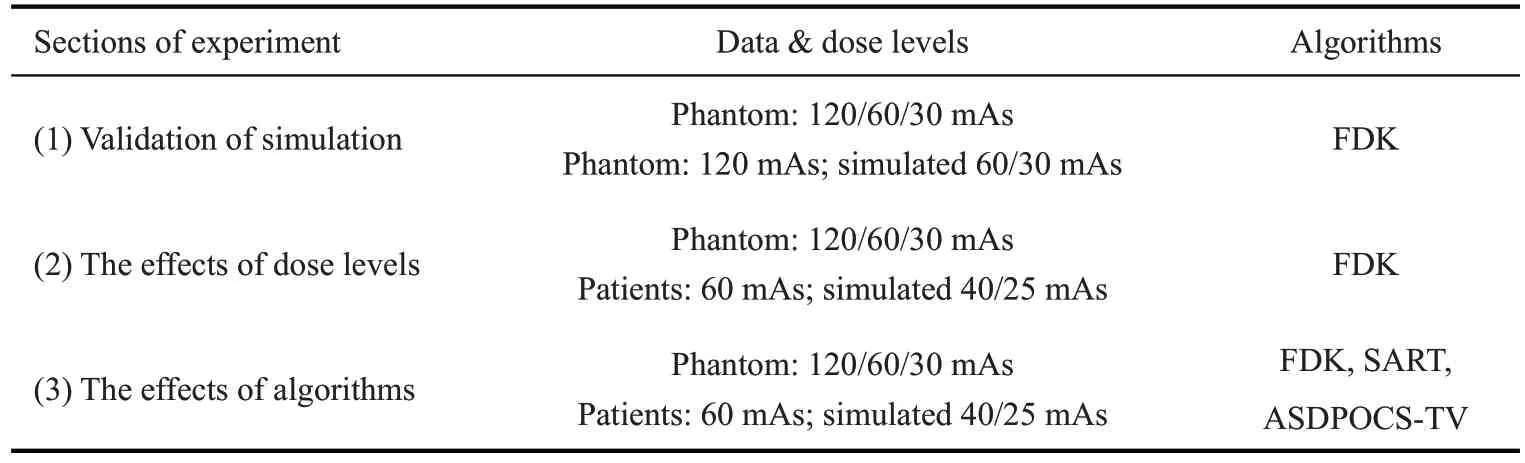
表1 实验计划总结Tab.1 Summary of the experiment protocol
第(1)部分仿真验证实验,仅使用具有真实扫描多个剂量水平的体模数据,分2个方面进行评估。首先是投影域,沿投影近胸壁端到远胸壁端方向,即沿图1C 侧视图中的y轴方向,等间距选择20个16×16像素大小的ROI,按照公式(1)计算SNR值与SNR相对误差值。其次是图像域,选择图像中6个32×32像素大小的ROI,按照公式(2)计算PSNR以指示边缘信号的对比度。沿圆形轨迹选择位于体模内部的20个大小为64×64像素的ROI,按照公式(3)计算全局NPS并转换为极坐标形式的NPS曲线。此外,采用以某个钙化点为中心的3D邻域(VOI),大小为60×60×11 像素,按照公式(4)计算ASF曲线和其FWHM值。
第(2)部分均采用FDK算法和Hamming窗滤波函数进行图像重建和图像分析。分别计算3种不同剂量水平下体模数据中团状(ROIs of mass)、点状(ROIs of calcifications)、条状(ROIs of fibre)三种ROI和患者数据中腺体(ROIs of gland,不含钙化点的腺体致密区域)、钙化点(ROIs of calcifications,含钙化点区域)、脂肪(ROIs of fat,不含钙化点的腺体稀疏区域)3种ROI的SNR值,区域大小分别为10×10、4×4、10×10像素。同时,选择图像中3种不同区域且大小为128×128像素的ROI计算局部2D NPS图像,沿圆轨迹选取20个大小为64×64像素的ROI计算全局NPS曲线。此外,分别在体模数据和每个患者数据中选择以钙化点为中心的6个和1个VOI区域计算ASF曲线及其FWHM值,区域大小为60×60×11像素。
第(3)部分选取ROI的规则与指标计算方法同第(2)部分,以比较不同算法下DBT重建图像质量的优劣情况。本实验采用基于MATLAB (MathWorks Inc,2016B)软件平台的Tomographic Iterative GPU-based Reconstruction(TIGRE)工具包[32]进行DBT图像重建工作,选用其中3种重建算法以重建三维DBT图像。其中,FDK算法采用Hamming窗滤波函数,对于迭代算法,其超参数的选择是通过最小化重建结果ASF 的FWHM值得到。于是,SART算法迭代5次且其超参数lamda设为1.85,ASDPOCS-TV算法内外层分别迭代10次且其超参数lamda和alpha分别设为1.8和3×10-8。
3 结果
3.1 仿真验证
该部分实验分别从投影域和图像域分析比较真实扫描低剂量与仿真低剂量数据之间的相似性程度。该部分实验仅采用体模数据,所有量化指标的参考图像为120 mAs投影数据及其重建图像。首先在投影域,图3A显示在不同情况下第7帧投影中随到胸壁(射线中心)距离增大的SNR曲线。其中,红色空心圆圈曲线为真实扫描60 mAs(Real 60 mAs),深蓝色星形曲线为仿真60 mAs(Sim 60 mAs),绿色空心圆圈曲线为真实扫描30 mAs(Real 30 mAs),浅蓝色星形曲线为仿真30 mAs(Sim 30 mAs)。可以看出:同一剂量水平的真实扫描和仿真投影数据的SNR曲线相互接近且真实扫描数据的SNR曲线均位于在仿真投影数据的SNR曲线上方,所有SNR曲线均呈现下降趋势。图3B显示在两种低剂量下真实扫描和仿真投影数据在1~15帧投影的SNR相对误差图,其中中间虚线为各SNR均值的变化趋势,而上下的界限分别为上下四分之一分位数。由此可知:真实扫描和仿真投影数据在60 mAs下的SNR相对误差范围从1.3%~2.3%,在30 mAs下为0.5%~0.7%,均处于一个较小的误差范围。以上结果一致表明:一方面,仿真算法比较可靠有效,能够较为准确地仿真出特定低剂量下的投影数据,接近于真实扫描的低剂量投影数据。另一方面,仿真算法不是完美的,因此导致仿真投影数据的图像信噪比略低于真实扫描的投影数据。此外,由于DBT中的X射线束是一个以乳腺为中心的半锥形线束,随着到射线中心的距离增大,入射X射线光子数相应减少,因此造成SNR曲线随距离增大而呈现下降趋势。
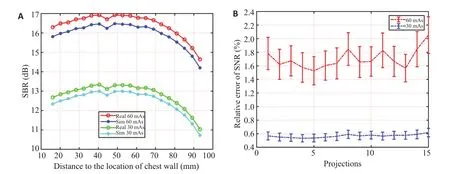
图3 比较真实扫描和仿真数据在不同剂量水平下单帧投影和全部15帧投影的SNRFig.3 Comparison of the SNR on the single projection and all 15 projections from scanned and simulated data at different dose levels.A:The SNR curves of the 7th frame projections (the x-axis represents the vertical distance to the chest wall);B:The relative SNR error curves of the 1st-15th frames projections.
其次在图像域,图4展示4种情况下的投影数据使用FDK算法的重建结果图像,左上角红色ROI为放大的图像块。可以看出:在同一显示范围内,两类重建图像视觉方面具有较高的一致性。选择图4A中6个黄色ROI 计算不同剂量下两类重建图像的PSNR 值,两者PSNR均相互接近,差异最大处在ROI 3(0.71),且ROI 2/3/4/5处仿真数据的PSNR高于真实扫描数据,可能的原因是FDK重建算法可弥补仿真算法的不足(表2)。图5描绘两类数据在两种低剂量水平下的NPS曲线,同时计算NPS曲线对应的平均能量频率和峰值能量频率记录于表3中。图6展示了两类数据在两种剂量水平下的ASF曲线,其平均相对误差分别是60 mAs下3.52%和30 mAs下6.18%。计算其ASF的FWHM值,FWHM值的均值与标准差如表4中所列。图5、表3、图6、表4结果均表明扫描与仿真两类数据的重建图像表现出相近的空间分辨率与纹理特征,且仿真较扫描具有略高的峰值信噪比和噪声含量以及略重的层间伪影扩散程度。综上所述,两类数据之间差异较小,处于可接受范围内。

图4 两类投影数据在不同剂量水平的FDK重建图像结果(第37层)Fig.4 The reconstructed results of two kinds of projections at various dose (the 37th slice).A:Real scanned 60 mAs;B:Simulated 60 mAs;C:Real scanned 30 mAs;D:Simulated 30 mAs.Display range:[0.05,0.12].
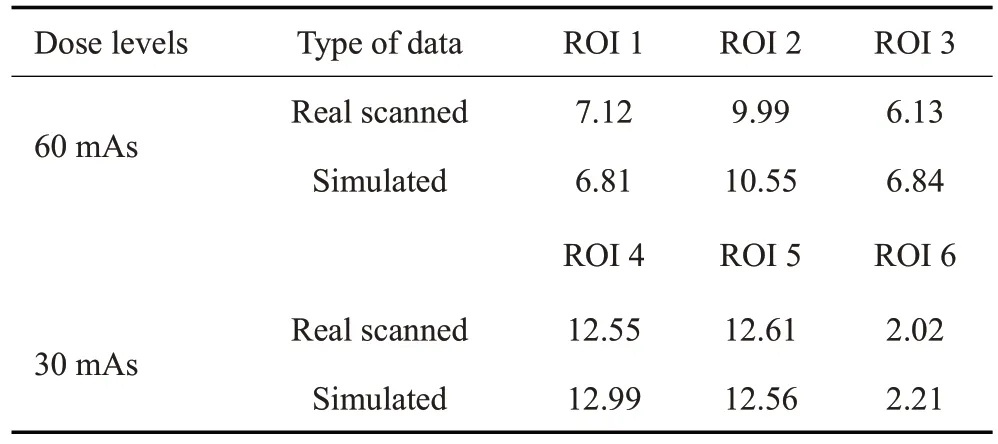
表2 两类重建图像在不同低剂量水平下多个ROI内PSNR值(/dB)Tab.2 The PSNR (/dB) values of several ROIs on reconstructed images at various dose
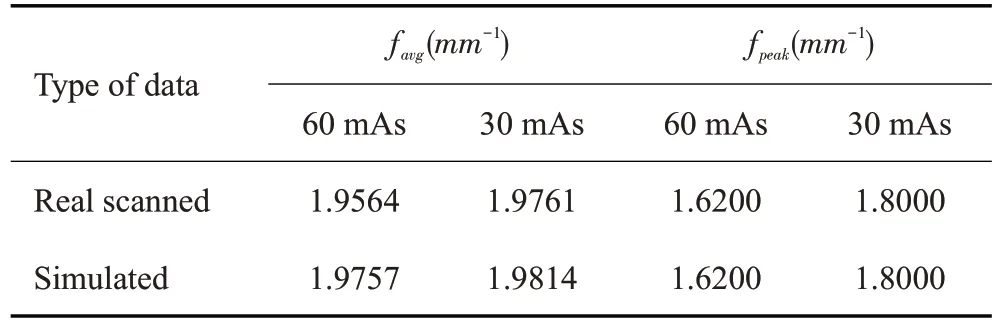
表3 两类图像在不同剂量水平下NPS曲线的平均频率和峰值频率Tab.3 Average frequency and peak frequency of the NPS curves on two kinds of images at different dose levels
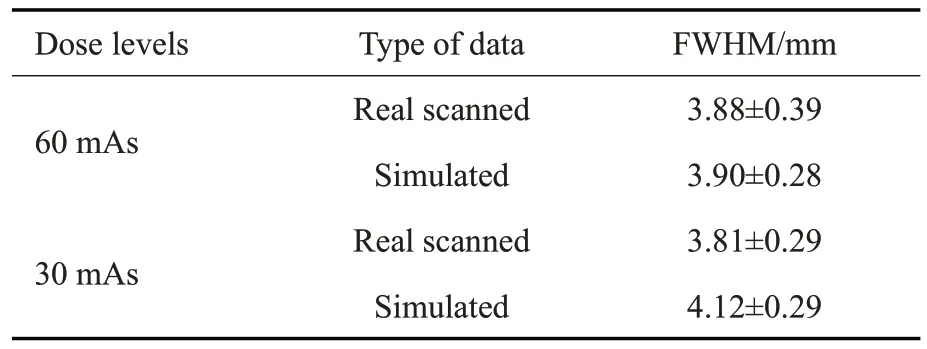
表4 比较扫描与仿真重建图像在不同剂量水平下FWHM值Tab.4 Comparison of FWHM values (Mean±SD) of scanned and simulated reconstructed images at different dose levels
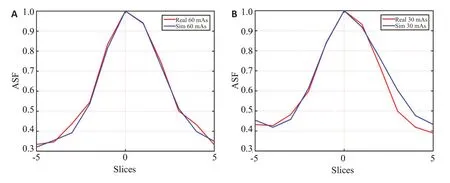
图6 两类重建图像的ASF曲线Fig.6 ASF curves of two kinds of reconstructed images:A:60 mAs;B:30 mAs;("0"represents the 37th slice of reconstructed images,the 32th-42th slices are selected).
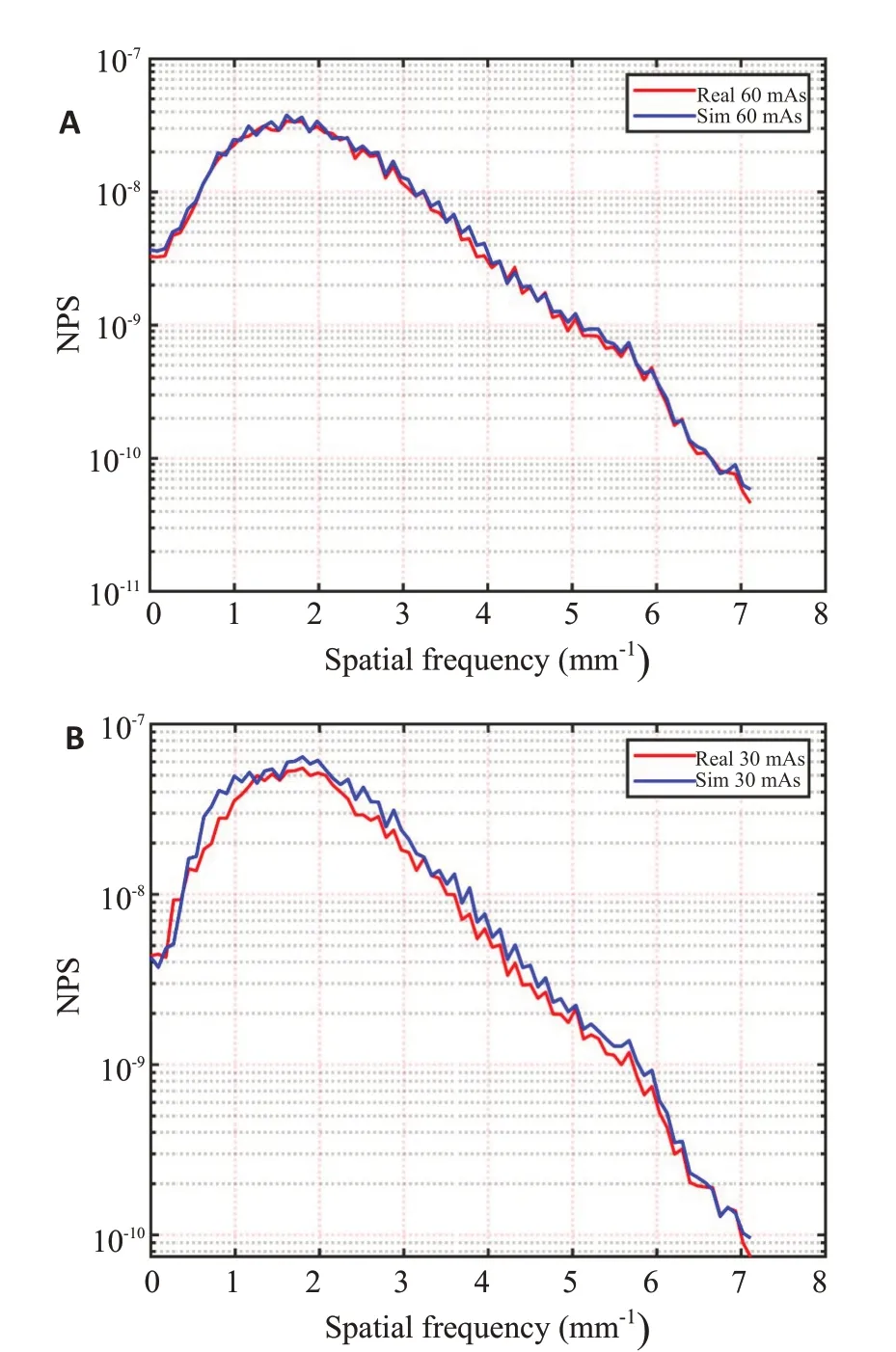
图5 两类重建图像的NPS曲线Fig.5 The NPS curves on two kinds of reconstructed images.A:60 mAs;B:30 mAs.
3.2 剂量与重建算法双因素定性分析
图7和图8分别展示体模和一例患者数据在3种剂量和3种算法下的重建结果图像。在视觉方面,基于ASDPOCS-TV算法的体模图像重建结果中噪声和伪影最少,图像表征最平滑,图像对比度最佳(图7)。此外,基于FDK算法的重建结果比基于SART算法的重建结果具有更清晰的边缘,但同时在高衰减嵌入物质的周围附近具有较强的上冲伪影和下冲伪影。患者图像的边缘锐利度从高到低依次为FDK算法、ASDPOCS-TV算法、SART算法,但同时钙化点附近的伪影严重程度从高到低(图8)。

图7 体模在不同剂量和不同重建算法下的结果图像Fig.7 The reconstructed images of the phantom under various doses and different reconstruction algorithms.
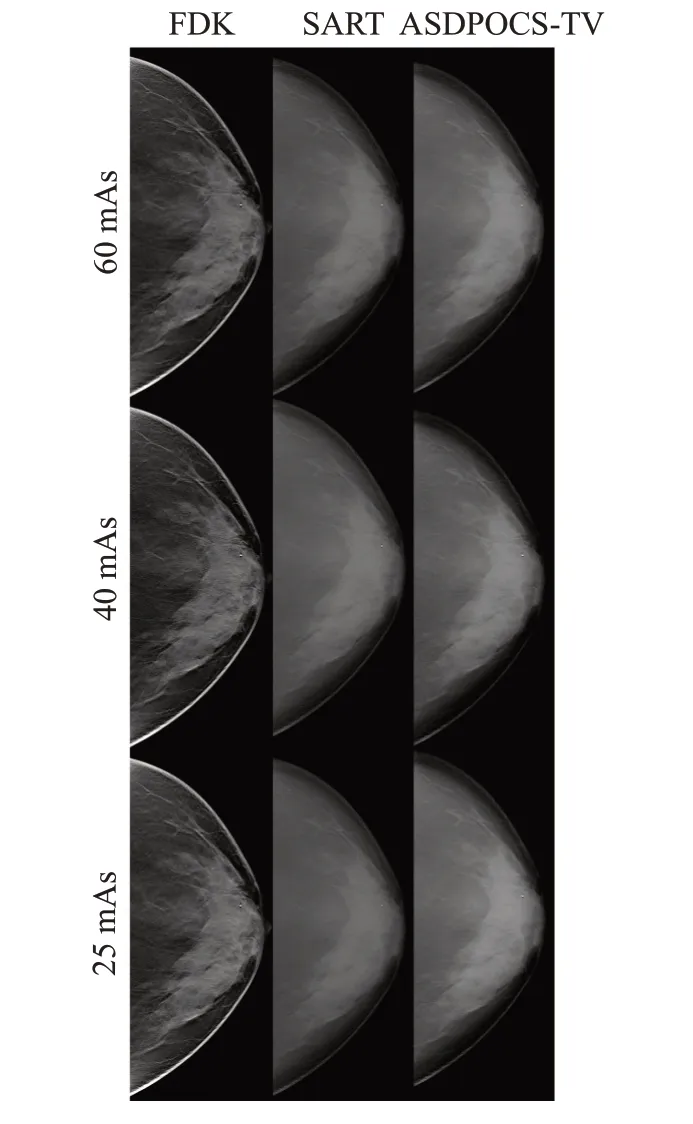
图8 良性乳腺钙化患者在不同剂量和不同重建算法下的结果图像Fig.8 Image results of a patient with benign breast calcifications under different doses and different reconstruction algorithms.
3.3 剂量因素定量分析
图9分别展示体模和患者数据为计算图10和图11中2D NPS而选取的3种不同的ROI。图10和图11分别显示不同剂量水平下体模数据和患者数据3种ROI对应的2D NPS,显示的空间频率范围是[-1.925,1.925]mm-1,图像中心处的空间频率为0 mm-1。如图所示,2D NPS是各向异性的且与图像中背景内容物相关,其中,中心区域代表低频信号,外围区域表示高频信号,蓝色表示信号强度值越低,黄色表示信号强度值越高。由此可见,降低剂量会导致NPS图像的外围区域出现更强的高频信号,提示噪声信号成分的增加。为进一步分析辐射剂量对成像质量的影响,3种剂量下的全局NPS曲线。剂量越低,其对应的NPS曲线更高,而高NPS曲线表示图像中包含更多的噪声与伪影成分(图12)。特别地,仿真40 mAs 与仿真20 mAs 的2D NPS 视觉差异较小(图11),且图12B中代表仿真40 mAs的蓝色曲线和代表仿真20 mAs的绿色曲线因过于接近而重叠,因此仅显示绿色NPS曲线。实际上,两者数值有细微差异,这一现象提示仿真算法可能在仿真精度不足。表5和表6分别列出不同剂量水平下体模数据和患者数据3 种ROI 的SNR 与FWHM 指标的均值和标准差,以120 mAs 或60 mAs 的FDK 重建图像为参考图像,并对FWHM值进行单因素方差分析,加粗显示的数值表示最优结果。其中,表6中“-”处表示该值无法计算,因SNR指标计算时以60 mAs的图像作为参考图像,因此,60 mAs图像的SNR值无法计算,也不能和40 mAs及25 mAs图像的SNR值进行统计学分析。由表5和表6可知,对于体模数据,60 mAs的重建图像明显比30 mAs具有更高的SNR值;对于患者数据,40 mAs与25 mAs的重建图像在SNR方面具有显著性的差异(P<0.05),而且60 mAs的伪影扩散程度低于40 mAs和25 mAs,但三者之间均无显著性的差异。
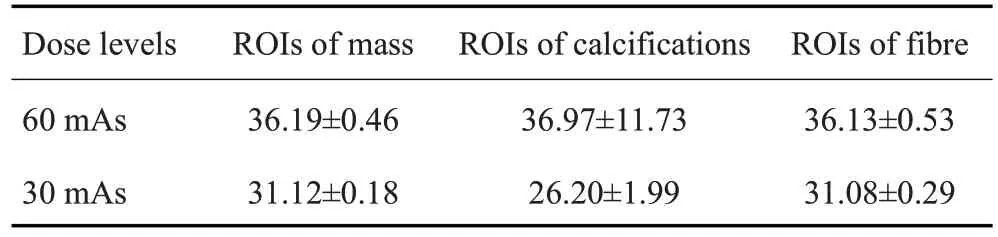
表5 不同剂量下体模图像在3种ROI内的SNR值(/dB)Tab.5 SNR values/dB (Mean±SD) on three ROIs of the phantom images under different doses
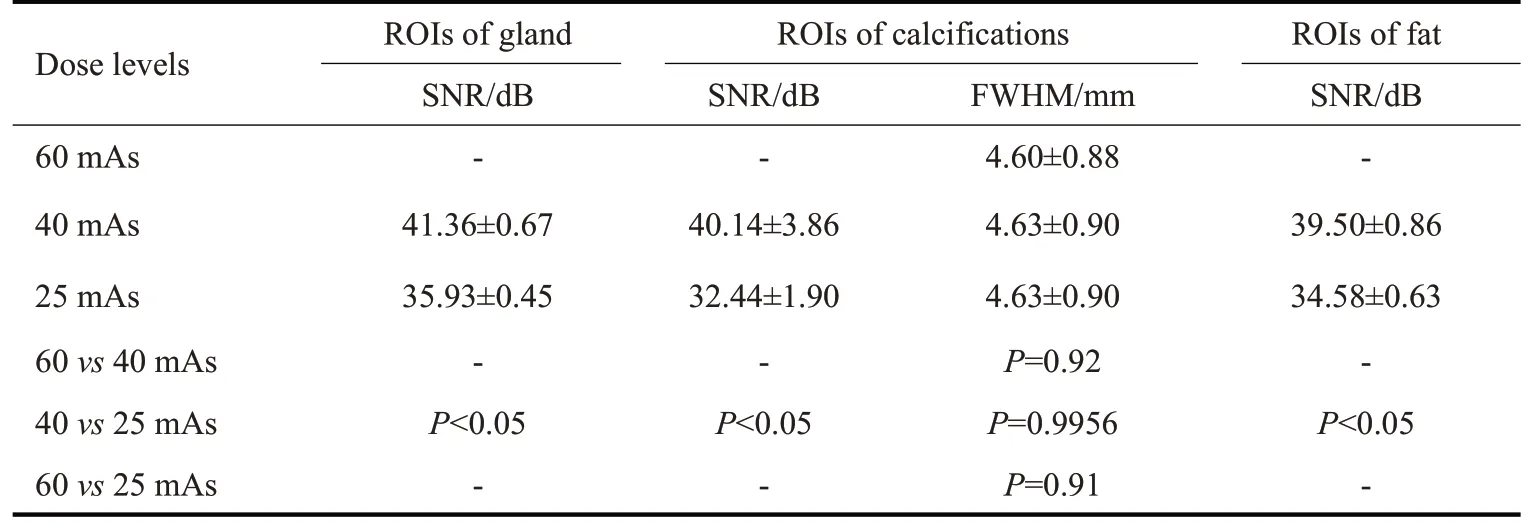
表6 不同剂量下患者数据图像在3种ROI内的SNR 和FWHW 值Tab.6 SNR and FWHM values(Mean±SD)of patient data images on three kinds of ROIs under different doses
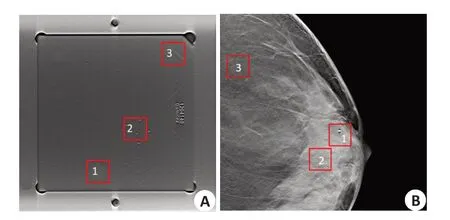
图9 选取计算2D NPS的ROI图示Fig.9 ROIs for calculating 2D NPs:A:3 ROIs(37th slice image)of the phantom data;B:3 ROIs of one patient case (benign,19th slice image).
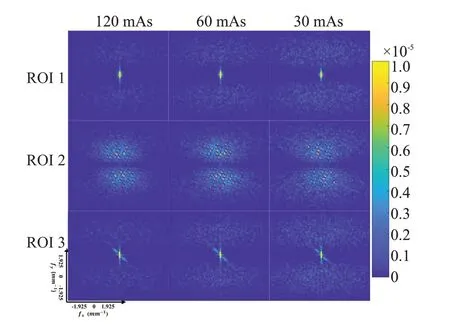
图10 体模数据在不同剂量水平下3个ROI对应的2D NPS(37层图像,FDK算法)Fig.10 NPS corresponding to three ROIs of the phantom data at different dose levels (37th slice image with FDK algorithm).
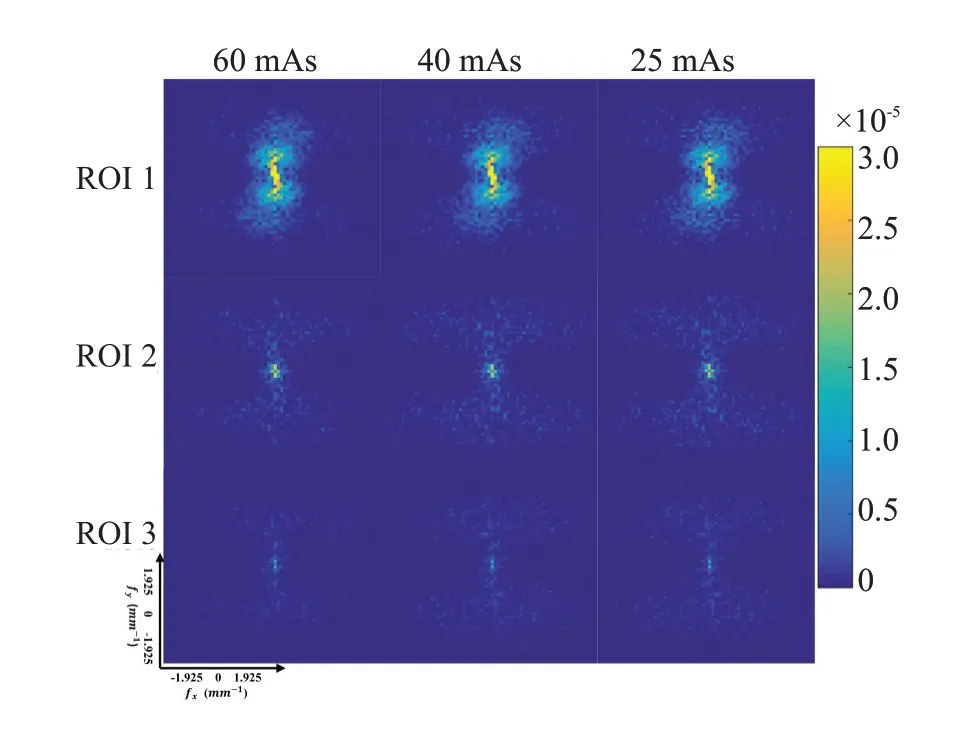
图11 患者数据在不同剂量水平下3个ROI对应的2D NPS(良性,第19层图像,FDK算法)Fig.11 NPS corresponding to three ROIs of one patient case at different dose levels (benign,19th slice image,with FDK algorithm).
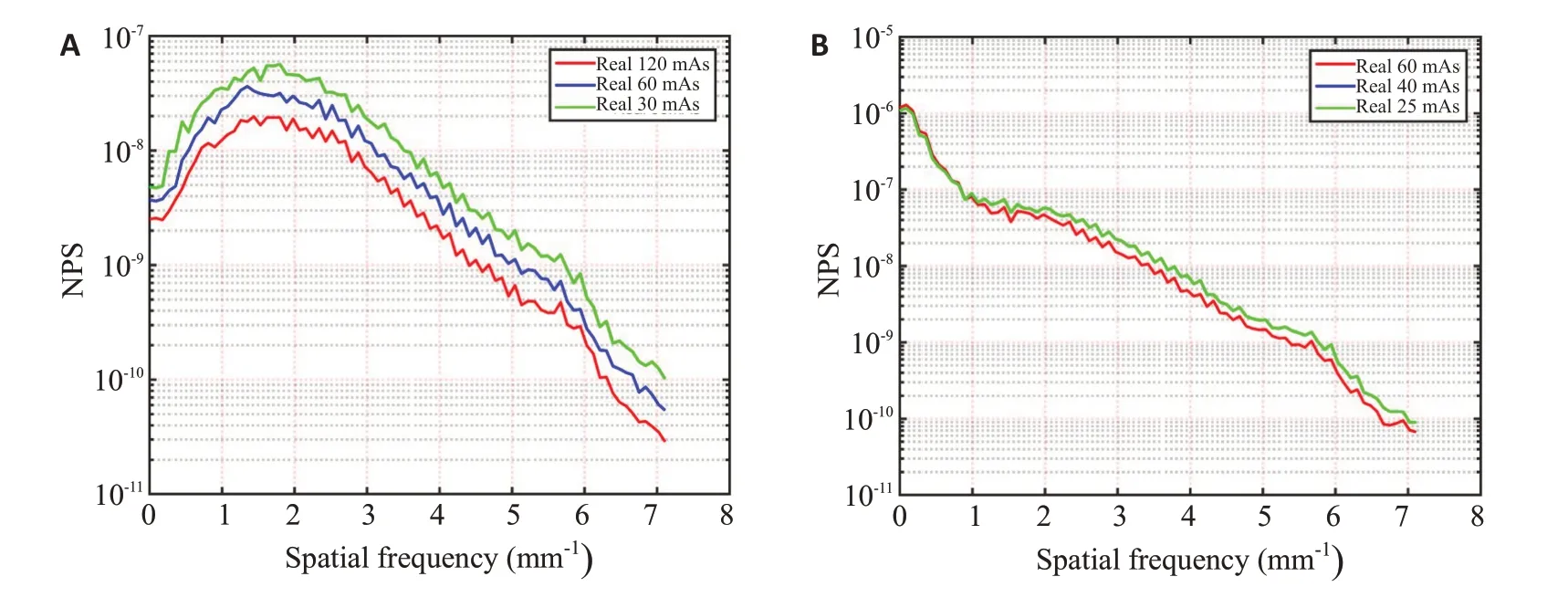
图12 不同剂量水平下的重建图像的全局NPS曲线Fig.12 The global NPS curves of reconstructed images at different dose levels:A:phantom data;B:patient data.
3.4 重建算法定量分析
图13和图14分别显示了3种算法重建的体模图像和良性乳腺钙化患者图像中3个ROI对应的噪声功率谱,同样对应图9所示ROI位置。FDK算法的重建结果具有最高亮的信号值,其次是SART 算法,最后是ASDPOCS-TV算法,更亮的外围区域指示更强烈的噪声和伪影信号成分。3种算法重建结果的全局NPS曲线如图15所示,一般地,FDK算法重建结果的NPS曲线高于SART算法高于ASDPOCS-TV算法,反映噪声信号强度由强至弱。以120 mAs 体模数据或者60 mAs患者数据分别作为参考图像,计算3种ROI的SNR指标及其均值和标准差记录于表7和表8中。同时计算患者数据的ASF曲线FWHM值的均值与方差,并进行单因素方差分析。由表7 和表8 可知:对于体模数据,ASDPOCS-TV算法的重建结果具有更高的SNR值,明显优于其他两算法。对于患者数据,在钙化点区域,ASDPOCS-TV 算法具有最高的SNR 值和更低的FWHM 值,SART 算法次最优;在腺体和脂肪区域,SART 算法表现最优,ASDPOCS-TV 算法表现次最优。除钙化点区域的FWHM指标外(P=0.18),其余各项指标方面,FDK 算法与SART 算法、FDK 算法和ASDPOCS-TV算法之间均存在显著性差异(P<0.05);而SART算法和ASDPOCS-TV算法在所有指标方面均无显著性的差异(P>0.05)。
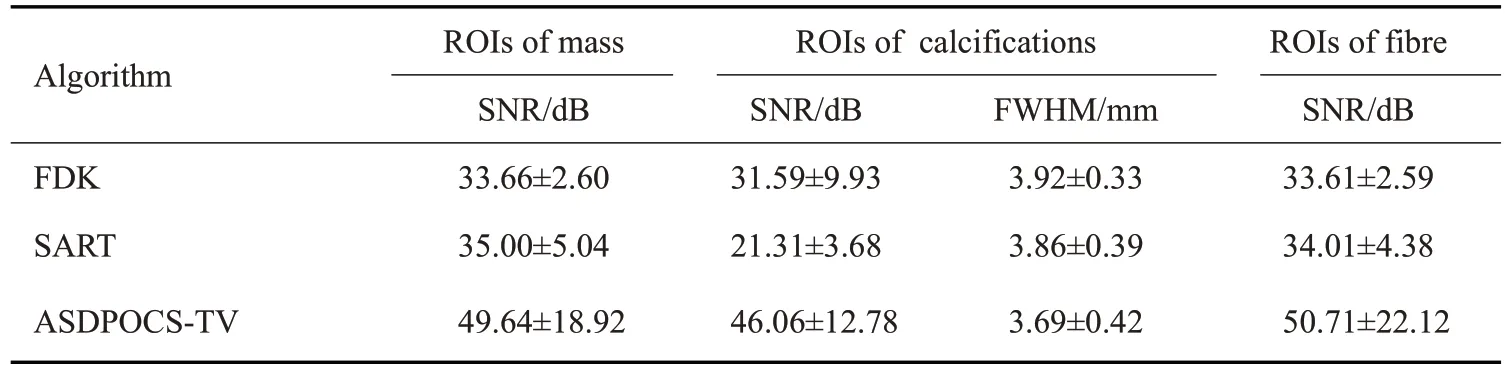
表7 不同重建算法下体模图像的SNR和FWHM值Tab.7 SNR and FWHM values (Mean±SD) of the phantom images under different reconstruction algorithms
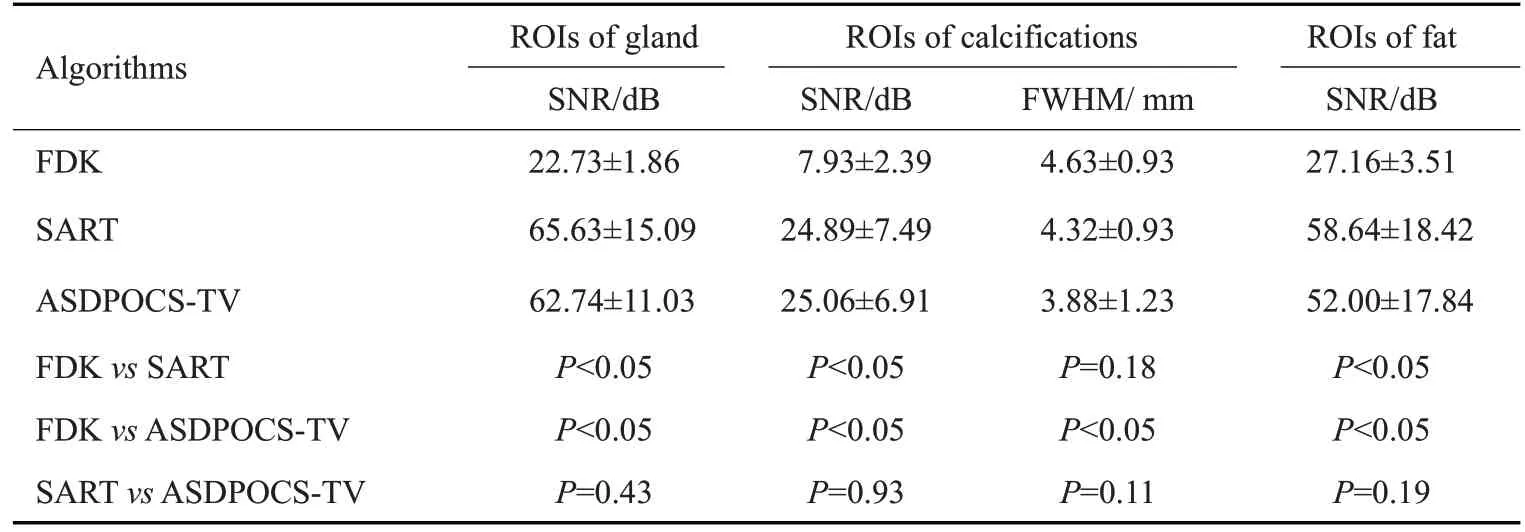
表8 不同重建算法对应患者图像的SNR和FWHM值Tab.8 SNR and FWHM values(Mean±SD)of patient images under different reconstruction algorithms
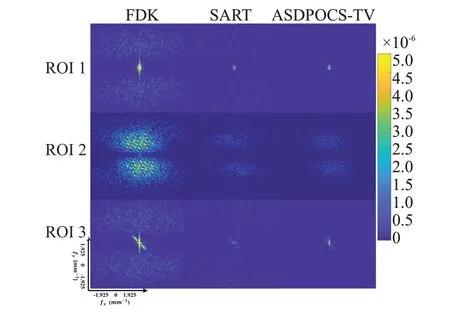
图13 体模数据在不同重建算法下3个ROI对应的2D NPS(第37层图像,120 mAs)Fig.13 2D NPS corresponding to three ROIs of the phantom data under different reconstruction algorithms(the 37th slice image,120 mAs).
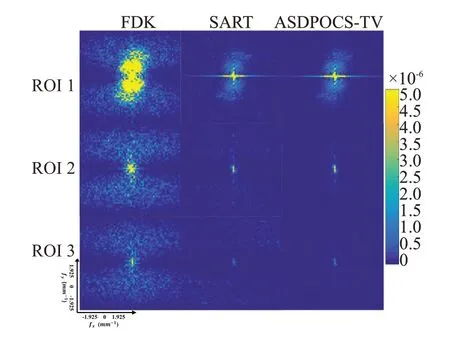
图14 患者数据在不同重建算法下3个ROI对应的2D NPS(良性,第19层图像,60mAs)Fig.14 2D NPS corresponding to three ROIS of one patient data under different reconstruction algorithms(benign,the 19th slice image,60 mAs).
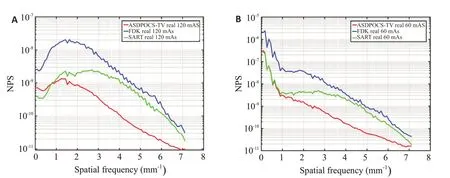
图15 不同算法重建图像的全局NPS曲线Fig.15 The global NPS curves of reconstructed images with different reconstruction algorithms:A:the phantom data(120 mAs);B:one patient data(60 mAs).
4 讨论
本文采用难以获取的原始测量数据,包括物理体模和患者,探究辐射剂量和重建算法两大影响因素对DBT成像质量的影响。本研究将指标SNR、PSNR和NPS用于噪声评估,指标ASF和FWHM用于指示空间分辨率和伪影分布,进而多方面评估DBT成像质量。
各项实验结果表明:(1)该DBT仿真算法切实有效,扫描与仿真数据从投影域和图像域两方面均表现出相近的图像表征,可用于其他需要进行DBT仿真的实验中;(2)剂量因素,随着剂量的降低,DBT图像中的噪声水平和伪影扩散程度相应增加。这一方面可能降低视觉方面对病灶的可视性,另一方面可能造成基于DBT图像的计算机视觉任务模型性能退化,如计算机辅助诊断系统(CAD);(3)重建算法因素,ASDPOCSTV算法和SART算法的DBT重建图像相较于FDK算法在噪声和伪影抑制方面表现出更优越的性能。特别地,ASDPOCS-TV算法的重建结果在体模数据的3种区域都表现最优,而仅在患者数据的含钙化点区域表现为最优,在腺体和脂肪区域表现为次最优,考虑原因可能为全变分正则化(TV)对于无锐利边缘处的DBT图像不敏感。这一结论提示基于不同临床诊断任务可选择最合适的剂量与重建算法。
本实验仍有一些局限性:(1)独立的患者数据测试集较小,仅包含15套数据;(2)实验中仅采用客观量化评价指标,未考虑放射医师的主观评价和基于诊断任务的评估方案;(3)数据来源单一,实验回顾性收集的数据均出自同一个中心的同一台扫描仪器。未来,更大量的、多中心的数据有待于收集、实验与分析。