基于HPLC多指标成分含量测定结合化学计量学的小儿康颗粒质量评价
王紫洁,马灵珍
0 引言
小儿康颗粒由太子参、山楂、白芍、白术、茯苓等12味中药材按照“君、臣、佐、使”中医药理论配伍而成,主要用于食滞虫痢、烦躁不安、精神疲倦、脘腹胀满、面色萎黄等病症的治疗[1]。现代药理和临床研究表明,小儿康颗粒可有效改善功能性腹痛[2]、再发性腹痛[3]的临床症状,对小儿腹泻[4]、小儿功能性便秘[5]治疗效果显著,同时还具有增强小儿厌食症患者食欲[6]、降低高血铅和轻度铅中毒患儿的血铅水平[7]等作用。小儿康颗粒现收载于卫生部药品标准中药成方制剂第六册[1],质量标准中尚未对其所含成分进行定量控制,文献报道[8]中也仅对其佐药白芍所含的芍药苷进行了定量研究。中药及其制剂所含成分繁多且复杂,具有多靶点、多组分协同增效、多点微调等特点,为全面评价中成药复方制剂整体质量,多指标成分质量控制模式近年来已广泛应用于其质量控制中。本实验根据中医配伍理论,结合中药质量标志物确定原则,采用HPLC梯度洗脱法对小儿康颗粒中君药太子参的主要活性成分太子参环肽B,臣药山楂的代表性成分牡荆素葡萄糖苷、牡荆素鼠李糖苷和金丝桃苷,佐药白芍的代表性成分氧化芍药苷、芍药苷和苯甲酰芍药苷含量进行同时测定,采用化学计量学分析方法对不同生产企业生产的小儿康颗粒目标成分含量进行聚类分析和主成分分析,为全面评价小儿康颗粒整体质量、提高其质量控制标准提供数据支持。
1 仪器与试药
1.1 仪器 Waters2695型高效液相色谱仪(美国Waters公司);AE240型电子天平(瑞士Mettler Toledo公司);KQ-300DA型数控超声波清洗仪(昆山市超声仪器有限公司)。
1.2 试药 芍药苷对照品(批号:110736-201943,含量95.1%,CAS号23180-57-6)、金丝桃苷对照品(批号:111521-201809,含量94.9%,CAS号482-36-0)和牡荆素葡萄糖苷对照品(批号:111979-201501,含量92.8%,CAS号178468-00-3)均来源于中国食品药品检定研究院;牡荆素鼠李糖苷对照品(批号:16042941,含量98.1%,CAS号64820-99-1)、氧化芍药苷对照品(批号:18031641,含量98.8%,CAS号:39011-91-1)、苯甲酰芍药苷对照品(批号:18031622,含量99.3%,CAS号38642-49-8)和太子参环肽B对照品(批号:18031328,含量99.9%,CAS号145459-19-4)均来源于上海同田生物技术股份有限公司;乙腈为色谱纯,其他试剂为分析纯。小儿康颗粒(规格:每袋装10 g;批号:190303、190305、190801,编号依次为S1~S3,来源于海南葫芦娃药业集团股份有限公司,简称企业1;批号:7381902、7382201、7382401、7382801、8381802、8382203、8382501,编号依次为S4~S10,来源于广州诺金制药有限公司,简称企业2;批号:1902002、200101,编号依次为S11~S12,来源于江西佑美制药有限公司,简称企业3)。
2 方法与结果
2.1 溶液的制备
2.1.1 混合对照品储备液 精密称取牡荆素葡萄糖苷、牡荆素鼠李糖苷、金丝桃苷、氧化芍药苷、芍药苷、苯甲酰芍药苷、太子参环肽B对照品适量,用甲醇制成质量浓度分别为0.436、3.178、0.544、0.278、2.536、0.192、0.158 mg/ml的混合对照品储备液。
2.1.2 混合对照品溶液 精密吸取混合对照品储备液0.1、0.2、0.5、1.0、2.0和2.5 ml,分别置于6个20 ml量瓶中,用甲醇稀释至刻度,制成6个系列质量浓度线性考察混对溶液Ⅰ~Ⅵ;取混对溶液Ⅳ作为混合对照品溶液(牡荆素葡萄糖苷21.8 μg/ml、牡荆素鼠李糖苷158.9 μg/ml、金丝桃苷27.2 μg/ml、氧化芍药苷13.9 μg/ml、芍药苷126.8 μg/ml、苯甲酰芍药苷9.6 μg/ml、太子参环肽B 7.9 μg/ml)。
2.1.3 供试品溶液和阴性样品溶液 取小儿康颗粒样品适量,除去内包装,取内容物研成细粉,取约2.0 g,精密称定,置25 ml量瓶中,精密加入甲醇25 ml,超声处理45 min,放冷后用甲醇补重,摇匀,经0.45 μm微孔滤膜滤过,制成小儿康颗粒供试品溶液。按小儿康颗粒的处方工艺[1],分别制备缺山楂、缺白芍和缺太子参的阴性样品,再按上述方法制成阴性样品溶液。
2.2 色谱条件及专属性试验 以Waters SunFire C18柱(250 mm×4.6 mm,5 μm)为液相色谱柱,柱温:30 ℃;流动相:乙腈(A)-0.1%磷酸溶液(B),梯度洗脱(0~14.0 min,15.0%A;14.0~25.0 min,15.0%A→27.0%A;25.0~41.0 min,27.0%A→39.0%A;41.0~47.0 min,39.0%A→52.0%A;47.0~55.0 min,52.0%A→15.0%A),流速:1.0 ml/min;进样量:10 μl;检测波长分别为340 nm (0~25.0 min检测牡荆素葡萄糖苷、牡荆素鼠李糖苷和金丝桃苷)[9-11],230 nm (25.0~41.0 min检测氧化芍药苷、芍药苷和苯甲酰芍药苷)[12-14]和203 nm (41.0~55.0 min检测太子参环肽B)[15-17]。精密吸取混合对照品溶液、小儿康颗粒供试品溶液和各阴性样品溶液各10 μl,进样检测,记录色谱图。结果小儿康颗粒供试品色谱图中牡荆素葡萄糖苷、牡荆素鼠李糖苷、金丝桃苷、氧化芍药苷、芍药苷、苯甲酰芍药苷、太子参环肽B色谱峰峰形对称,分离度均>1.5,理论板数按各目标化合物色谱峰计均≥3 500,阴性样品对小儿康颗粒中太子参环肽B等7种目标成分的测定不干扰,色谱图见图1。

图1 HPLC色谱图
2.3 线性关系考察 精密吸取“2.1.2”项下系列质量浓度线性考察混对溶液Ⅰ~Ⅵ各10 μl,依次进样测定小儿康颗粒中太子参环肽B等7种目标化合物的峰面积,以牡荆素葡萄糖苷、牡荆素鼠李糖苷、金丝桃苷、氧化芍药苷、芍药苷、苯甲酰芍药苷、太子参环肽B质量浓度(X,μg/ml)为横坐标,峰面积(Y)为纵坐标进行线性回归,得7种成分的回归方程、线性范围及r值见表1。
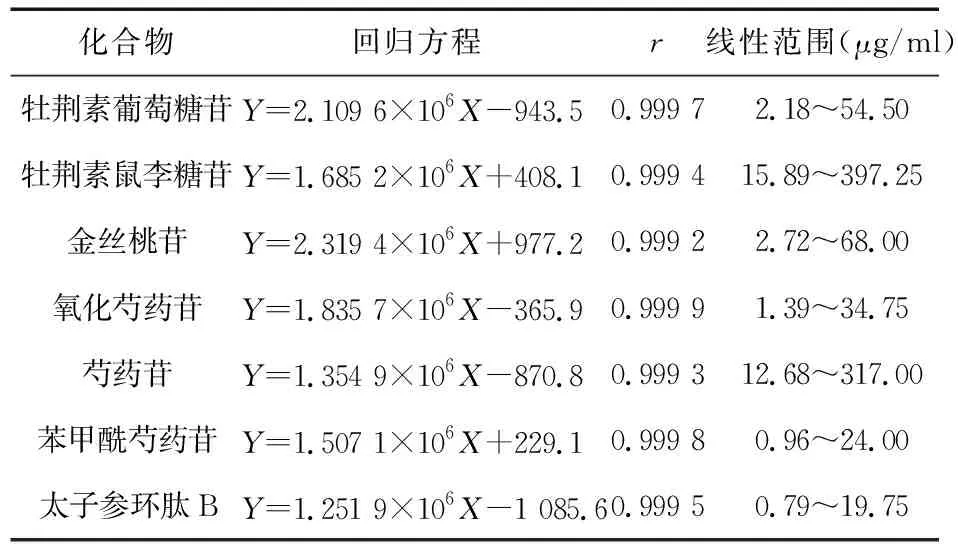
表1 7种化合物的回归方程、相关系数和线性范围
2.4 精密度、重复性、稳定性考察
2.4.1 精密度考察 取“2.1.2”项下混合对照品溶液连续进样6次,记录牡荆素葡萄糖苷、牡荆素鼠李糖苷、金丝桃苷、氧化芍药苷、芍药苷、苯甲酰芍药苷、太子参环肽B的峰面积,结果仪器精密度良好,太子参环肽B等7种目标成分峰面积的RSD分别为1.05%、0.52%、1.06%、1.09%、0.57%、1.10%和1.22%。
2.4.2 重复性考察 取小儿康颗粒样品,按“2.1.3”项下方法配制6份小儿康颗粒供试品溶液,依法进样分析,记录牡荆素葡萄糖苷、牡荆素鼠李糖苷、金丝桃苷、氧化芍药苷、芍药苷、苯甲酰芍药苷、太子参环肽B的峰面积并计算各目标化合物的含量,结果方法重复性良好,太子参环肽B等7种目标成分含量的RSD分别为1.82%、0.86%、1.61%、0.73%、1.08%、1.75%和1.89%。
2.4.3 稳定性考察 临用新配1份小儿康颗粒供试品溶液,于0、2、4、8、18和24 h进样检测牡荆素葡萄糖苷、牡荆素鼠李糖苷、金丝桃苷、氧化芍药苷、芍药苷、苯甲酰芍药苷、太子参环肽B的峰面积,结果小儿康颗粒供试品溶液24 h内稳定,太子参环肽B等7种目标成分峰面积的RSD分别为0.99%、0.56%、1.07%、1.12%、0.60%、1.15%和1.18%。
2.5 加样回收率试验 取牡荆素葡萄糖苷、牡荆素鼠李糖苷、金丝桃苷、氧化芍药苷、芍药苷、苯甲酰芍药苷、太子参环肽B含量均已知的同一批次小儿康颗粒样品适量,除去内包装取内容物研成细粉,取约1.0 g,精密称定(共称取9份,3份随机分为1组),依据《中国药典》2015年版四部规定(对照品加入量约为样品原有量的50%、100%和150%),分别精密加入混合对照品溶液(另行配制,牡荆素葡萄糖苷、牡荆素鼠李糖苷、金丝桃苷、氧化芍药苷、芍药苷、苯甲酰芍药苷、太子参环肽B的质量浓度分别为0.127、0.863、0.159、0.078、0.715、0.057、0.043 mg/ml)1.0、2.0和3.0 ml,再按“2.1.3”项下方法制成加样回收样品溶液,依法进样测定牡荆素葡萄糖苷、牡荆素鼠李糖苷、金丝桃苷、氧化芍药苷、芍药苷、苯甲酰芍药苷、太子参环肽B的峰面积,并计算其含量,用测得量与样品原有量之差除以对照品加入量,计算太子参环肽B等7种目标成分的回收率及RSD值,结果见表2。
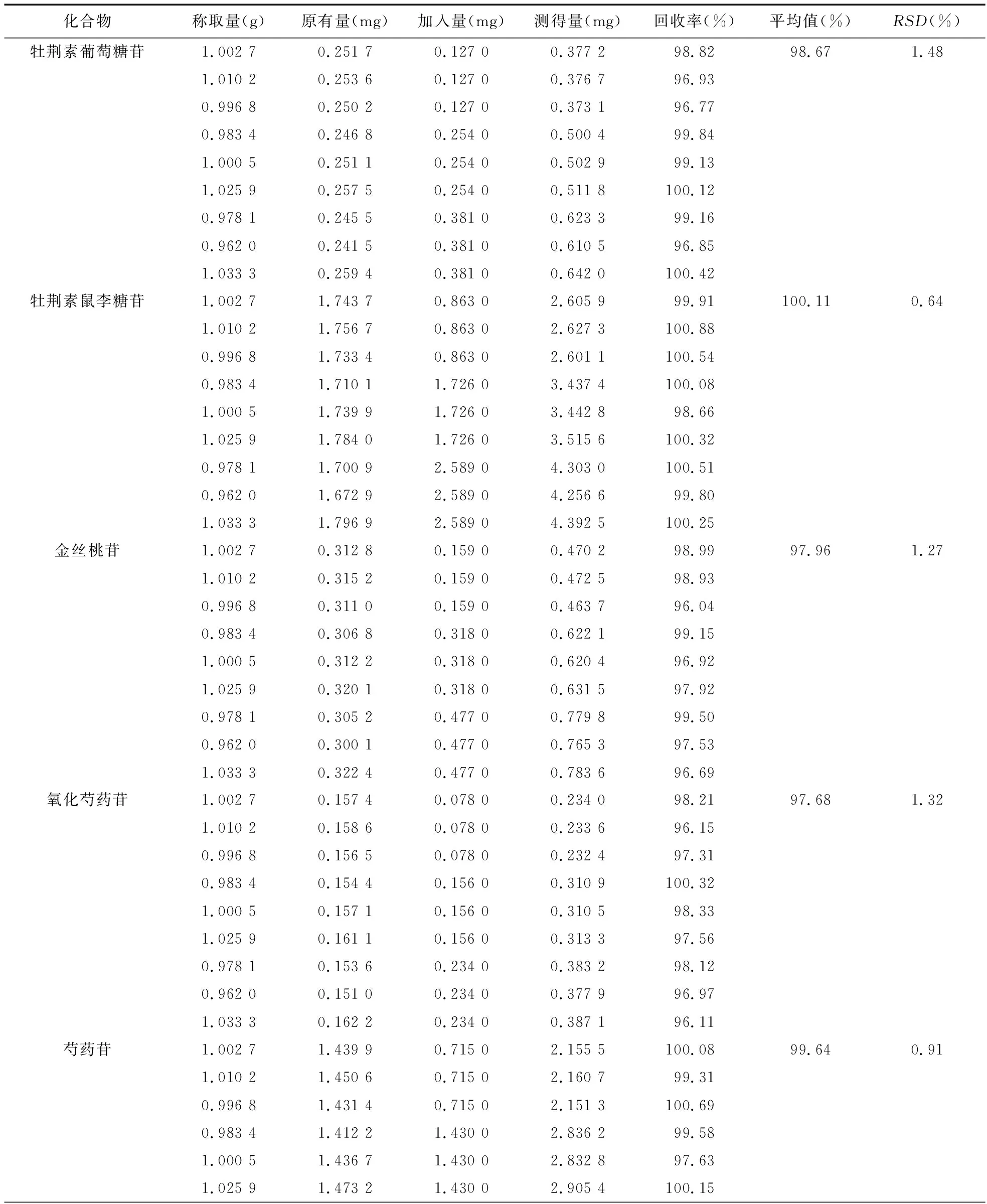
表2 小儿康颗粒中7种成分的加样回收率试验结果
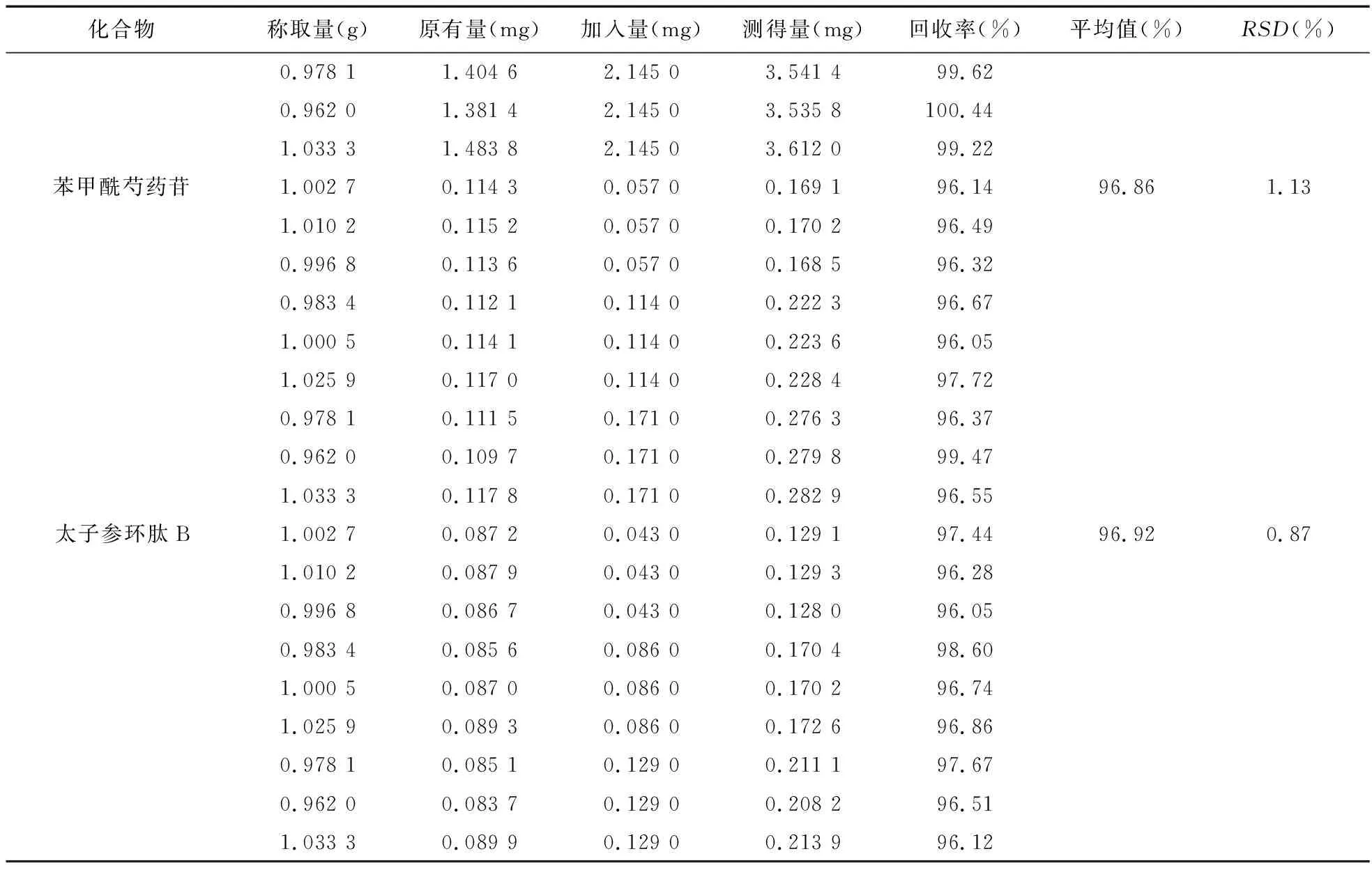
续表
2.6 样品含量测定 取12个批次的小儿康颗粒样品(编号S1~S12),按“2.1.3”项下方法制成供试品溶液(每个批次平行制备3份),依法进样测定牡荆素葡萄糖苷、牡荆素鼠李糖苷、金丝桃苷、氧化芍药苷、芍药苷、苯甲酰芍药苷、太子参环肽B的峰面积,并计算目标成分的含量,结果见表3。
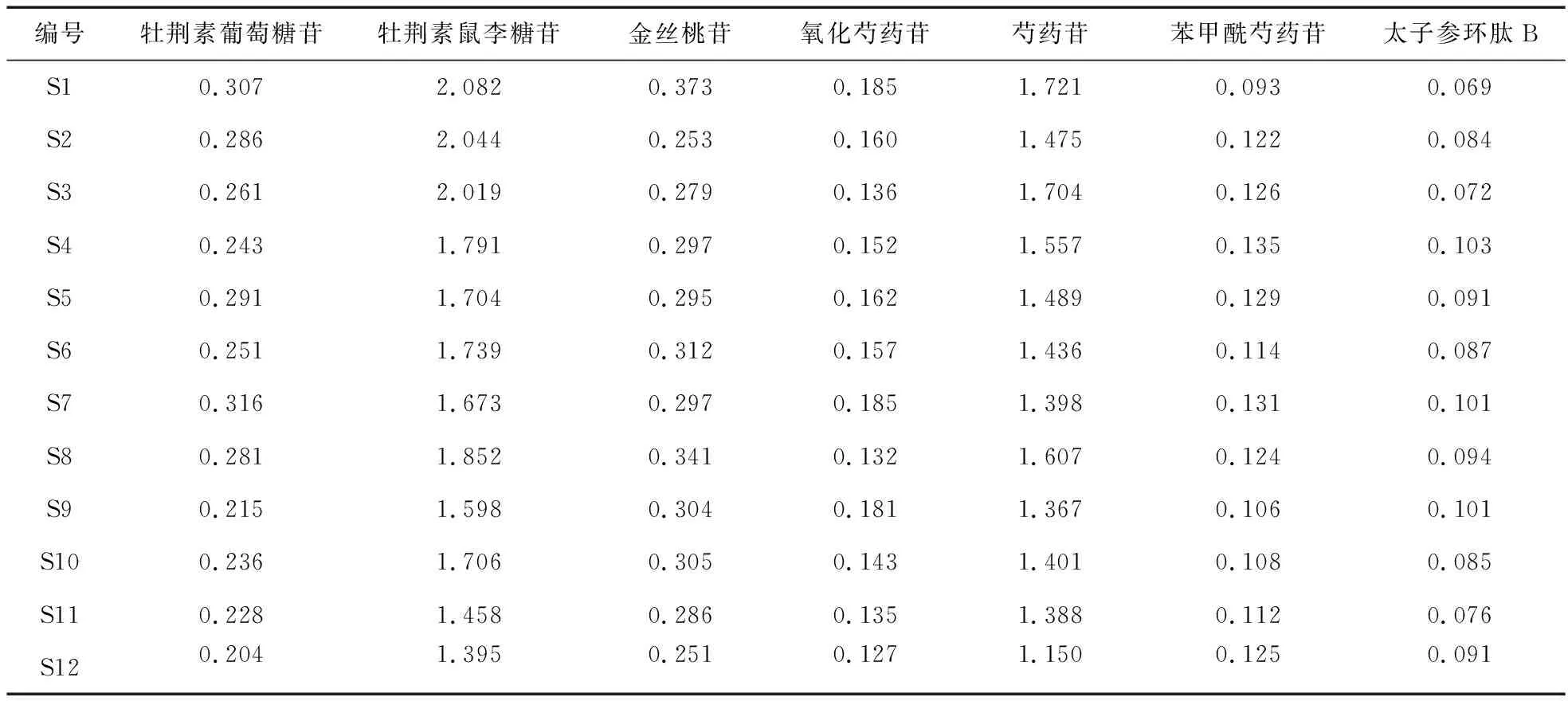
表3 样品含量测定结果(mg/g)
2.7 聚类分析 为考察不同批次小儿康颗粒中太子参环肽B等7种目标成分的含量差异,采用SPSS 26.0软件系统聚类分析法(聚类方法:组间联接,测度:欧氏距离)对12个批次小儿康颗粒样品进行聚类分析,结果见图2。由图2所得结果可知,当类间距离为15时,12批小儿康颗粒样品聚为3类,样品S6、S10、S5、S7、S9、S4和S8聚为一类,样品S11和S12聚为一类,样品S1、S3和S2聚为一类。从分类结果可以看出,同一生产企业生产的小儿康颗粒样品聚为一类,表明同一生产企业样品各成分含量相对稳定、均匀,企业2样品质量较为稳定,而不同生产企业样品间存在一定差异。
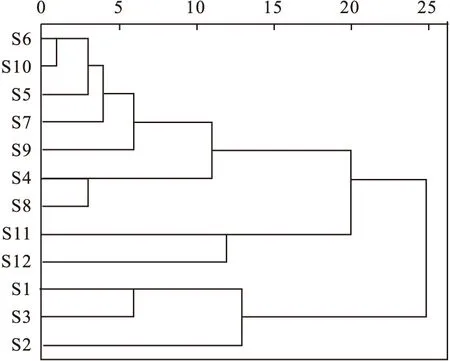
图2 12批小儿康颗粒聚类分析树状图
2.8 主成分分析 采用SPSS 26.0软件对12批小儿康颗粒中太子参环肽B等7种目标成分的含量数据进行主成分分析,将表3测得数值导入分析软件,得样品主成分分析碎石图见图3,主成分特征值和方差贡献率结果见表4。

表4 主成分特征值和方差贡献率
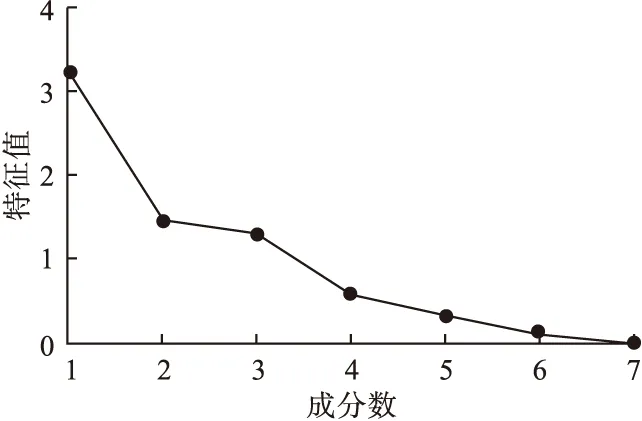
图3 主成分分析碎石图
根据累积贡献率>85%的原则,以初始特征值>1为提取标准,前3个主成分分别为3.219、1.461、1.282,初始特征值均>1,对方差贡献率分别为45.987%、20.869%和18.312%,累积贡献率为85.168%,大于85%,表明提取前3个主成分即可代表小儿康颗粒中太子参环肽B等7种目标成分85.168%的信息,可以用于对小儿康颗粒的质量评价。
3 讨论
3.1 多指标成分的选择 小儿康颗粒由太子参、山楂、白芍、白术、茯苓等12味中药材组方而来,方中太子参益气健脾、生津润肺,白术健脾益气、燥湿利水,共为君药;山楂消食健胃、化浊降脂,茯苓健脾渗湿,葫芦茶消痰散瘀,麦芽行气消食、健脾开胃,合为臣药;白芍养血敛阴、柔肝止痛,乌梅敛肺生津,蝉蜕敛肺止痛,榧子消积润肺、润燥通便,槟榔行气消积,合为佐药;陈皮健脾和胃、行气宽中,引药达病所,为使药。诸药合用,共奏健脾开胃、消食化滞、驱虫止痛之功。太子参环肽B为君药太子参特征成分;牡荆素葡萄糖苷、牡荆素鼠李糖苷、金丝桃苷等黄酮类为臣药山楂主要活性成分;氧化芍药苷、芍药苷、苯甲酰芍药苷等单萜类化合物为佐药白芍主要药效成分。本实验根据中药质量标志物确认原则选取牡荆素葡萄糖苷、牡荆素鼠李糖苷、金丝桃苷、氧化芍药苷、芍药苷、苯甲酰芍药苷、太子参环肽B为小儿康颗粒多指标定量测定成分,以期全面评价小儿康颗粒的整体质量。
3.2 供试品溶液制备方法的优化 在确定供试品溶液制备方法时,以小儿康颗粒中牡荆素葡萄糖苷、牡荆素鼠李糖苷、金丝桃苷、氧化芍药苷、芍药苷、苯甲酰芍药苷、太子参环肽B的综合提取率为指标,同时结合杂质干扰程度,对比考察了50%甲醇[11]、70%甲醇[9]、甲醇[13,15-17]和50%乙醇[12,14]提取溶剂以及超声提取[9-11,13-17]、加热回流[12]提取方式对考察指标的影响,结果显示,以甲醇超声提取时,小儿康颗粒中太子参环肽B等7种目标成分综合提取率最佳,杂质成分干扰较小,在此基础上对提取时间进行优化,最终确定采用甲醇超声提取45 min对小儿康颗粒进行供试品溶液的制备。
3.3 流动相的优化选择 在流动相优化选择时,参考相关文献,依次考察了乙腈-水[15,17]、乙腈-0.1%甲酸溶液[10-11,16]和乙腈-0.1%磷酸溶液[12-14]流动相体系对小儿康颗粒中牡荆素葡萄糖苷、牡荆素鼠李糖苷、金丝桃苷、氧化芍药苷、芍药苷、苯甲酰芍药苷、太子参环肽B色谱峰峰形、分离度的影响。结果显示,以乙腈-0.1%磷酸溶液为流动相系统进行梯度洗脱时,色谱图基线平稳,太子参环肽B等7种目标成分色谱峰峰形对称,与相邻色谱峰均能有效分离。在此基础上对流动相中有机相和水相比例进行优化,最终确定采用“2.2”项色谱条件下的流动相梯度洗脱程序对小儿康颗粒中牡荆素葡萄糖苷、牡荆素鼠李糖苷、金丝桃苷、氧化芍药苷、芍药苷、苯甲酰芍药苷、太子参环肽B含量进行同时检测。
本实验采用HPLC法对小儿康颗粒中牡荆素葡萄糖苷、牡荆素鼠李糖苷、金丝桃苷、氧化芍药苷、芍药苷、苯甲酰芍药苷、太子参环肽B含量进行了同时测定,建立了该制剂的多指标成分质量控制评价模式,所建立的方法操作简便、结果准确,为全面评价小儿康颗粒的整体质量提供了参考依据,同时采用聚类分析、主成分分析对3个不同生产企业生产的12批次小儿康颗粒样品质量进行了综合评价。结果显示,同一生产企业样品相对稳定,不同生产企业样品间存在一定差异,可能与各生产企业原药材质量控制和生产过程参数控制存在一定差异有关,提示药品生产企业应加强原药材产地、采收季节等源头控制,不断提升原药材内控质量标准,优化制剂生产过程控制参数,确保产品质量和临床疗效的一致性。

