微电子肌电桥技术对颈脊髓损伤患者桡侧腕长伸肌运动功能康复的效果
王冲,杜良杰,王志功,李建军,李军,刘宏炜,丛芳,林歆
1.首都医科大学康复医学院,北京市 100068;2.中国康复研究中心北京博爱医院,a.理疗科;b.脊柱脊髓神经功能重建科,北京市 100068;3.中国康复科学所,神经损伤与康复北京市重点实验室,北京脑重大疾病研究院神经损伤与修复研究所,北京市 100068;4.东南大学射频与光电集成电路研究所,江苏南京市210000
外伤、疾病等原因会导致脊髓损伤,颈脊髓损伤会导致严重的四肢感觉、运动以及二便障碍。上肢功能是颈脊髓损伤患者优先考虑改善的功能[1-3]。手功能可分为粗大和精细两种,其中腕关节的主动背伸和手指主动屈伸是手功能的基础。因此,腕背伸功能障碍是影响手功能恢复的主要原因,对于C5脊髓损伤患者来说,腕背伸功能的恢复会带来手的被动抓握功能,也能为今后手功能重建手术创造良好的条件。目前用于手功能康复的方法大致包括物理运动、矫形器、普通的电刺激、功能性电刺激(functional electrical stimulation,FES)、肌电生物反馈(electromyographic biofeedback,EMGBF)和手术等,其中FES是目前常用的瘫痪肢体康复方法之一,其优势在于使用电刺激的方法使得瘫痪肢体肌肉得到一定强度的康复训练,但传统的FES 信号来源单一,病患参与性较弱,目的性不强,得不到积极意义的反馈,往往仅能起到防止肌肉萎缩的作用。
本研究所涉及的“微电子肌电桥”(microelectronic electromyography bridge,EMGB)技术引入健康肢体控制瘫痪肢体的训练机制,其信号来源于正常肢体,产生的信号与人体的肌肉收缩脉冲信号和谐度更高,且可以根据患侧肌肉疲劳的程度随时调整刺激的强度及刺激持续的时间。本研究观察该技术对患者瘫痪的桡侧腕长伸肌进行康复训练的疗效。
1 资料与方法
1.1 一般资料
选取2016 年3 月至2017 年3 月在北京博爱医院脊柱脊髓神经功能重建科住院的男性C5完全性脊髓损患者,诊断依据脊髓损伤神经学分类国际标准(2011版)[4]。
纳入标准:①男性;②临床诊断确诊的C5完全性脊髓损;③病程≤6个月;④签署知情同意书。
排除标准:①带有心脏起搏器等植入式电子装置;②并发其他脊柱疾病,如脊髓肿瘤、强直性脊柱炎等;③手及腕关节被动活动明显受限;④并发上肢骨折、骨化性肌炎、周围神经损伤等损害;⑤认知功能障碍(简易精神状态检查评分≤24 分);⑥严重抑郁(汉密尔顿抑郁量表评分≥24 分);⑦改良Ashworth 肌张力评分患侧上肢肌张力≥2 级;⑧并发严重心、脑、肝、肾和造血系统等严重原发性疾病,全身情况较差;⑨肌肉明显萎缩,对FES无反应。
剔除与脱落标准:①提前出院;②病情加重,不能继续配合训练;③不愿意继续参与训练。
共纳入20例,随机数字分组方法分为对照组和试验组。两组一般资料比较均无显著性差异(P>0.05)。见表1。
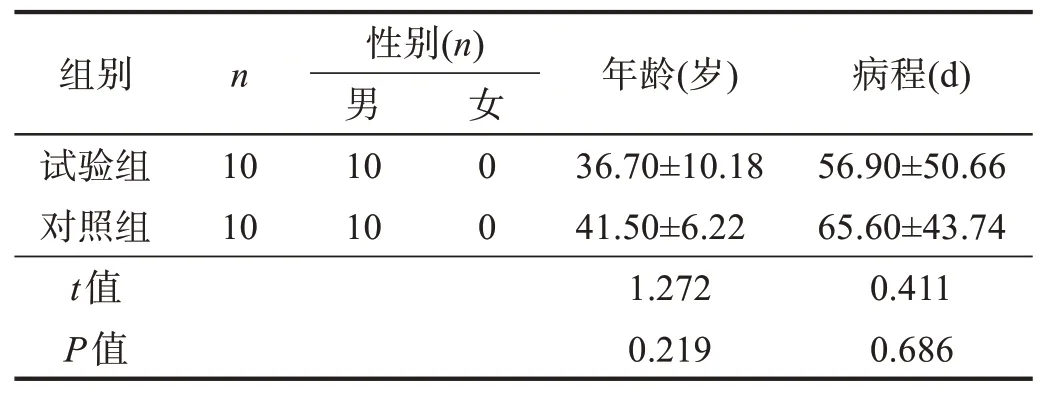
表1 两组一般资料比较
本研究取得北京博爱医院药物临床试验机构伦理委员会批准(No.2015-4-48-1)。
1.2 方法
两组均给予常规康复训练,试验组在常规康复训练的基础上增加EMGB康复训练。
1.2.1常规康复训练
①作业治疗训练:上肢及手部关节活动度的维持,生活自理能力训练等。②肌力增强训练:徒手抗阻活动,双侧本体感觉神经肌肉促进,易化、使用沙袋、哑铃的渐进性抗阻训练。③卧床训练:以手部活动为主,充分训练屈肘等未瘫痪上肢及背部肌的肌力,进而练习翻身、坐起等能力。④坐位训练:练习长腿坐位及短腿坐位平衡。
每次训练30 min,每天1次,每周5 d。
1.2.2EMGB康复训练
应用SQMN-1.0 双通道瘫痪肢体运动功能重建仪(南京神桥医疗器械有限公司)进行康复训练。该产品采用微处理器控制技术和肌电生物反馈电刺激技术,根据健康肢体运动时所产生的肌电信号,经过微处理器计算后启动相应的动作模式程序,通过功能性神经电刺激作用于患侧肢体,产生有效的刺激电流作用于瘫痪肢体并激发其运动,实现健康肢体控制瘫痪肢体运动练习。动作电位脉冲频率1~50 Hz。
在安静的环境中,将与上述仪器相连的探测电极贴附在健康研究者的桡侧腕长伸肌肌腹收缩明显处进行肌电信号采集,输出电极贴附在试验组患者双侧桡侧伸腕肌刺激敏感部位;由患者主动发出抬腕指令,由研究者最大程度抬腕,输出电极刺激患者双侧桡侧腕长伸肌,使患者在直视下同步进行最大程度抬腕;每次在最大抬腕位坚持10 s,停止刺激,间歇10 s 后再次给予刺激;20 s 为1 个循环;每次治疗20 min,每周5次,持续180 d。
1.3 评定方法
1.3.1表面肌电图(surface electromyography,sEMG)
采用sEMG 肌电指标中的均方根值(root mean square,RMS)定量反映治疗前后运动功能的改善,取等长收缩最大RMS 和平均RMS,其值越高,提示肌肉活动时运动单位激活的数量、参与活动的运动单位的类型越多,同步化程度越高,肌肉的运动功能越好[5-7]。
1.3.2徒手肌力检查(Manual Muscle Test,MMT)
MMT 采用Lovett 分级法,包括0~5 级,级别越高,分值越高,肌力越强[8]。
1.3.3Wolf 运动功能评定量表(Wolf Motor Function Test,WMFT)
WMFT 由15 个项目组成,1~6 为简单的关节运动,7~15为复合功能动作。对所有动作当场进行计时和动作质量打分(0~5分),分值越高功能越好[9-11]。
1.3.4脊髓损伤独立性量表(Spinal Cord Lesion Independence Measure,SCIM)
SCIM 评定包括自我照顾、呼吸和括约肌管理、移动能力3 个方面,共17 项。分值不统一,从0~1 分至0~15 分不等。最低分为0 分,总分为100 分。分值越高,患者日常生活自理能力越好[12-16]。
在治疗前和治疗180 d 后,分别采用以上方法评定患者上肢功能。
1.4 统计学分析
采用SPSS 20.0 统计软件进行数据处理。所有试验数据经单样本Kolmogorov-Smirnov检验结果符合正态分布,以()表示。组内采用配对样本t检验,组间采用独立样本t检验。显著性水平α=0.05。
2 结果
2.1 sEMG
治疗前,两组RMS 值均无显著性差异(P>0.05)。治疗后,两组RMS 峰值和平均值均提高(P<0.05);试验组左侧RMS 峰值和平均值优于对照组(P<0.05),试验组右侧RMS 峰值优于对照组(P<0.05),而平均值与对照组比较无显著性差异(P>0.05)。见表2。

表2 两组治疗前、后桡侧腕长伸肌sEMG的RMS比较(μV)
2.2 MMT评分
治疗前,两组MMT评分无显著性差异(P>0.05)。治疗后,两组MMT 评分均提高(P<0.05),且试验组优于对照组(P<0.05)。见表3。
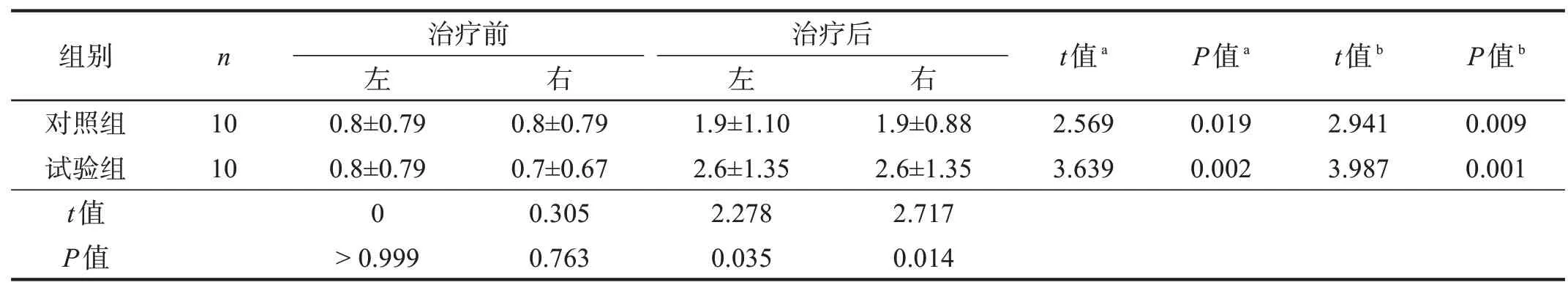
表3 两组治疗前后桡侧腕长伸肌MMT评分比较
2.3 WMFT评分
治疗前,两组WMFT 评分无显著性差异(P>0.05)。治疗后,两组WMFT 评分均明显提高(P<0.01);两组间比较无显著性差异(P>0.05)。见表4。
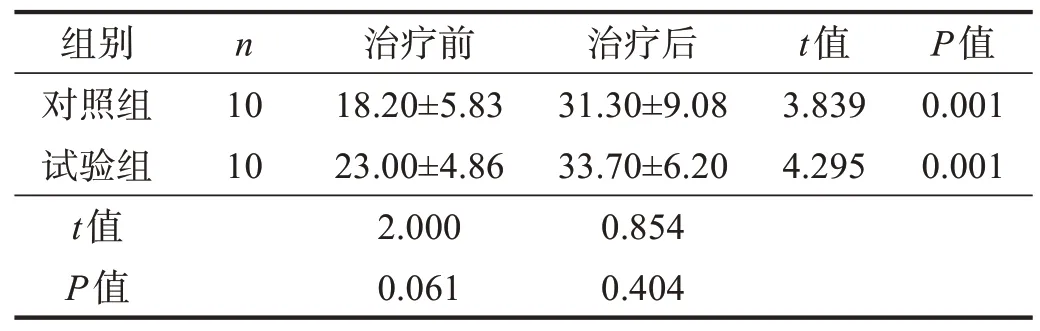
表4 两组治疗前后WMFT评分比较
2.4 SCIM评分
治疗前,两组SCIM评分无显著性差异(P>0.05)。治疗后,两组SCIM评分均显著提高(P<0.001);两组间比较无显著性差异(P>0.05)。见表5。
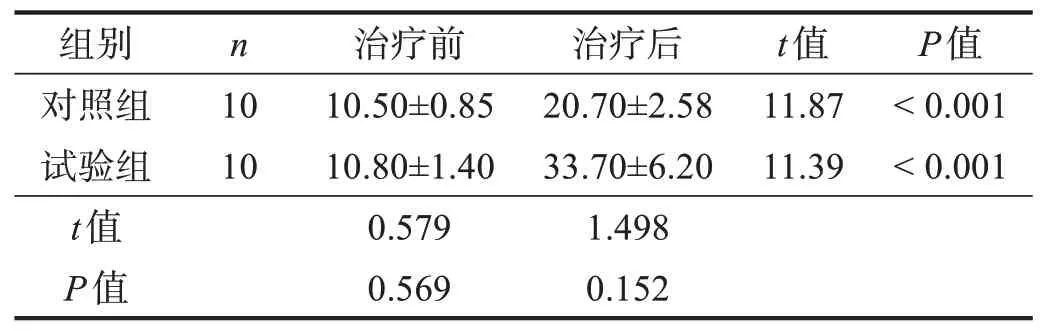
表5 两组治疗前后SCIM评分比较
3 讨论
与既往对于患者自身sEMG 信号的研究不同,本研究是基于健康人肌电信号刺激训练技术的研究。本研究显示,EMGB 具有一定的康复作用;但两组右手桡侧腕长伸肌sEMG 均值、SCIM 评分和WMFT 评分无差异,考虑其可能原因为:①试验组右手肌电RMS较对照组有所增高,但统计结果显示其P值为0.054,略高于0.05,可能与样本量较小、试验时间较短有关,有待今后进一步研究;②患者SCIM 评分和WMFT评分与很多因素有关,如屈肘力量的加强、床上翻身动作的练习、个人自我认知、主动参与积极性的改善等,而伸腕肌肌力的恢复只能在一定程度上改善患者部分腕部功能,而提高日常生活自理能力的其他功能仍需要相应的康复训练才能得到明显提高。
本研究还显示,常规康复训练和EMGB 训练均对颈脊髓损伤患者的桡侧腕长伸肌有增强作用,增加EMGB康复训练可以获得更好的康复疗效。
王志功等[17-19]首次提出微电子神经桥(microelectronics neural bridge,MENB)的概念[17],其原理为:在受损神经纤维的近端采集其微弱神经信号,再经前置放大器放大后,传输至滤波器等神经信号处理器;再利用所提取的神经信号控制FES 信号发生器;最后,在刺激电极上施加FES 信号,从而将信号传递给受损的远端神经,并产生肢体的运动。在此基础上,其团队进一步提出EMGB的概念,其实质就是采集与瘫痪肢体相同部位的健康人的sEMG,应用射频传输通信技术原理,经过加工处理后输出以刺激瘫痪肢体的肌肉,实现瘫痪肢体与健康人肢体的同步运动[18-19]。在上述过程中,患者可看到肢体运动,可听到自己或陪练者发出的运动指令,并可以随着训练进行最大程度的自主肌肉收缩运动[20]。其工作频率为1~50 Hz,既属于低频电刺激范畴又与低频电刺激有着很大差异。
低频电刺激作为一种物理因子治疗,其机制可能是电流刺激瘫痪肢体肌肉引起反复的被动运动,通过这种训练,可增加肌肉的血液循环及营养代谢,促进神经兴奋性及传导功能恢复,加快运动功能的恢复[21]。持续的电刺激可以实现神经系统的结构重塑;同时也可以使处于休眠状态的突触被代偿使用;还能通过将脊髓自发可塑性和训练任务依赖性可塑性策略相结合[22-25],达到改善肢体运动功能的目的。在既往的临床康复中低频电刺激对于偏瘫患者的中枢结构和功能重塑发挥了重要作用[26]。
FES 已在临床广泛应用。第一代FES 只产生最简单的波形,如双相脉冲,完全人工的脉冲参数由医生设定,患者完全被动,没有任何主动参与。第二代FES 根据预定义的阈值,应用检测到的患者自己的肢体sEMG 信号控制开关对肢体进行刺激。第三代FES应用sEMG 既控制开关状态,又控制肌电信号的振幅,由脉冲发生器产生FES 脉冲对肢体进行刺激;然而其sEMG信号和FES脉冲信号之间没有时序关系。
总之,传统的低频电刺激和FES 刺激信号与正常的肌肉收缩工作模式存在很大差异。本研究所采用的EMGB 不同于以往的低频电刺激和FES,因为其信号来源并非人工设置,而是从健康人肢体相同部位肌肉的肌电信号“复制”而来,通过射频传输通信技术处理,再通过输出电极作用于瘫痪肢体,诱发出与健康肢体相同的肌肉运动;该技术可以模拟正常的自主收缩运动模式,其刺激信号与正常肌肉的电信号特征相符,与人体的肌肉收缩脉冲信号和谐度更高,且可以根据患侧肌肉疲劳的程度随时调整刺激强度及持续时间,以达到改善或者恢复被刺激肌肉或肌群功能的目的。既往研究证明[27],该技术对偏瘫患者腕、手运动功能的康复疗效优于普通的FES,且不增加局部肌肉痉挛。王志功团队[28]利用该技术提出一种可穿戴电刺激装置,实现偏瘫患者手部运动功能的实时控制,建立高精度的腕、手运动控制。本研究首次将该技术应用到脊髓损伤患者,证明其对于脊髓损伤患者伸腕功能的康复也有较为理想的作用。
神经功能存在一定的恢复潜力。脊髓损伤后,脊髓灰质周围长传导束可以不全损伤,骨折脱位节段的神经根可以不全损伤并能够不同程度地恢复;因此,对于C5完全性脊髓损伤患者来说,仍具有C6神经根功能恢复的潜力;而C6神经根的功能恢复的结果就是伸腕功能的恢复。大量临床实践证明,很多完全性脊髓损伤的患者都具备运动平面下降的可能[29-30];而对颈脊髓损伤患者来说,即使运动平面下降一个节段,对手功能恢复也常常具有很大的意义[31-32]。脊髓损伤后,脊髓具有自发可塑性(损伤诱导的可塑性)和训练任务依赖性可塑性两种类型的可塑性[33];这些神经恢复的潜力是患者伸腕功能恢复的基础[34-35]。
运动再学习是上世纪80年代初由Carr等[36]提出的一种运动疗法,它把中枢神经系统损伤后运动功能的恢复训练视为一种再学习或再训练过程,强调患者的主动参与性。本研究应用EMGB技术进行瘫痪肢体的运动功能训练。在康复训练中由患者发出抬腕指令,健康研究者做出抬腕动作,其肌电信号经过仪器采集、加工、输出后作用于患者的桡侧腕长伸肌,患者同时努力做出主动抬腕动作,二人几乎同时完成抬腕;该过程中患者可以实现主动参与运动再学习。在此康复训练过程中,也可以结合作业疗法进行患肢的运动再学习,如让患者抬腕的同时完成抓握水杯的任务。研究表明[37],主动训练及其不断强化训练有益于神经重塑和运动功能的恢复;如能够结合作业疗法,增加患肢在日常生活中的使用,进行目标导向性及任务特异性的训练,则能促进中枢神经的重塑,并获得更好的运动再学习的效果[38-40]。
目前康复训练中常用的生物反馈技术包括视觉反馈和听觉反馈等多种形式;其中视觉反馈训练因其直观和有效等优点而备受关注[41]。镜像神经元(mirror neurons)是一类特殊的神经元,可在人类执行某种动作时或当观察到其他同类执行某种动作(如言语刺激)时被激活。分布于不同脑区的所有镜像神经元构成了镜像神经元系统。视觉反馈训练可通过镜像神经元系统的激活,促使大脑发生可塑性改变和功能重组,进而促进运动功能恢复,因此可称其为基于镜像神经元理论的康复疗法[42-43]。视觉反馈激活镜像神经元是目前研究的热点。Dohle 等[44]证实基于镜像神经元的视觉反馈训练有助于提高脑卒中患者的日常生活能力及上肢功能。国内朱美红等[45]的研究也证明了视觉反馈训练有助于促进脑卒中偏瘫患者上肢的运动功能恢复。在目标运动时,镜像反馈能够增强同侧皮质脊髓束的兴奋性[46-48]。本研究由患者发出共同抬腕指令,在特殊仪器帮助下,实现了健康研究者与患者的同步全关节范围的伸腕活动;整个过程可视可听,为患者构建了一个丰富的视觉反馈和听觉反馈环境;如此反复训练就能够激活镜像神经元系统,从而促进患者运动功能的恢复。
综上所述,EMGB 技术能够提高C5完全性脊髓损患者桡侧腕长伸肌的运动功能;具有刺激信号同源、刺激信号模式与健康肌肉工作模式一致的优势;能够充分调动患者的主动参与性;且在康复训练中能够调动视觉反馈和听觉反馈;激发镜像神经元康复活力;对于脊髓损伤后的肢体功能具有较好的康复作用,也为今后临床康复提供了一个较好的发展方向。
本研究属于临床研究,受到较多因素的干扰。①患者本身受伤程度、手术方式、既往健康状况以及训练积极性的差异均会在一定程度上影响研究结果;②患者住院期间并发症的产生亦会影响患者的整体状况以及康复训练的进程。③因肌肉疲劳间歇时间的调整亦会给试验结果带来一定的差异性。④可能存在其他影响试验结果的未知因素,如人文因素、社会因素和经济因素等。
本实验属于小样本研究,亦受研究时间、地点的限制,下一步希望进行大样本、多中心的研究,亦可进行脑部或脊髓功能磁共振,进一步深入探索中枢的可塑性。
利益冲突声明:所有作者声明不存在利益冲突。

