基于UPLC多指标成分含量测定的柴胡不同部位质量评价研究
周丽娟,孙欣光*,王雅芝,3,王玉龙,杨晓宁*(.北京振东光明药物研究院有限公司,北京 00085;.山西振东道地药材开发有限公司,山西 长治 04700;3.遵义医科大学药学院,贵州 遵义 563000)
柴胡为伞形科植物柴胡Bupleurum chinenseDC.或狭叶柴胡Bupleurum scorzonerifoliumwilld.的干燥根,具有疏散退热,疏肝解郁,升举阳气等功效[1]。研究表明,柴胡具有解热、抗炎、抗肿瘤、保肝、免疫调节等药理作用[2-4]。柴胡中主要含有皂苷、黄酮、挥发油、多糖等成分[2,5-6],其中柴胡皂苷为其主要活性成分,也是目前评价柴胡质量的主要指标成分[4]。柴胡具有显著的临床疗效而被广泛使用,含柴胡的中成药品种约500个[7],《中国药典》2015年版及增补版收载含柴胡中成药品种共105个,常见品种有柴黄片、柴胡疏肝丸、小柴胡泡腾片、小柴胡颗粒、柴胡疏肝丸等[8]。
由于柴胡药材的市场需求量较大,导致柴胡药材资源短缺,曾出现供不应求的局面。目前柴胡药材野生资源很少,市场上流通的柴胡药材以栽培品种为主,且大多会保留部分地上残茎。柴胡的药用部位为根,文献报道柴胡茎叶与根的化学成分存在差异[6],但关于地上残茎的化学成分研究鲜有报道,地上残茎与根之间主要柴胡皂苷类成分的含量差异情况不明确,从而导致市场流通的柴胡药材质量参差不齐,影响其疗效。
多指标的含量测定来评价柴胡药材质量的研究已有报道,但所需对照品用量大,价格昂贵且难以获得。一测多评(quantitative analysis of multi-components by single-maker,QAMS)以中药中某一种成分对照品为内参物,利用相对校正因子实现多指标成分的同时测定,可以很好地解决这类难题[9-14],被《中国药典》收载用于多种中药的多成分含量测定及质量评价,具有重要的指导意义[15]。
本研究建立QAMS法同时测定柴胡药材根和地上残茎中6种柴胡皂苷成分的含量,以柴胡皂苷d为内参物,建立其与柴胡皂苷a、b2、c、e和f的相对校正因子,并计算5种柴胡皂苷的含量;采用外标法(ESM)验证QAMS的可行性和准确性,最终建立QAMS法测定柴胡药材中6 种主要皂苷成分的含量,并测定 8批柴胡药材根及残茎不同分段部位中6种成分的含量,比较各柴胡皂苷成分差异,阐明地上残茎对柴胡药材质量的影响,为柴胡药材的质量控制提供新的方法和依据。
1 材料
1.1 试药
柴胡皂苷a(批号:110777-201912,含量:94.8%)、柴胡皂苷d(批号:110778-201912,含量:96.3%)(中国食品药品检定研究院);柴胡皂苷b2(批号:7383,含量:99.6%)、柴胡皂苷c(批号:4237,含量:100%)、柴胡皂苷e(批号:4157,含量:99.9%,)、柴胡皂苷f(批号:6131,含量:99.7%)(施丹德生物科技有限公司);色谱乙腈(批号:JB091230,默克);色谱甲醇(批号:5021403,上海星可高纯溶剂有限公司);氨水(批号:20200302,福晨化学试剂有限公司);纯水(Milli-Q 制备)。
1.2 药材
不同产地的柴胡药材,经山西医科大学高建平教授鉴定为伞形科植物柴胡Bupleurum chinenseDC.的干燥根及少量地上残留茎,其产地来源信息见表1,均购自安国药材市场。带有地上残茎的柴胡药材从芦头处分开,分为根和残茎两部分;残茎从芦头处开始分为茎0~1 cm(J1)、茎1~2 cm(J2)、茎2 cm以上(J3)三部分,根从芦头处开始分为根0~1 cm(G1)、根1~2 cm(G2)、根2 cm以下(G3)三部分。
表1 柴胡药材样品来源信息表Tab 1 Source information of Bupleuri Radix
1.3 仪器
Waters Acquity UPLC H-Class 系统(PDA 检测器,Waters 公司);色谱柱:Waters ACQUITY UPLC HSS T3(100 mm×2.1 mm,1.8 μm);Agilent ZORBAX Eclipse Plus C18(100 mm×2.1 mm,1.8 μm);Waters ACQUITY UPLC BEH C18(100 mm×2.1 mm,1.7 μm);TLE204/02电子天平、XSE205DU电子天平(METTLER TOLEDO);电子天平(MSA36S-OCE-DH,Sartorius)。
2 方法与结果
2.1 色谱条件
色谱柱Waters ACQUITY UPLC BEH C18(100 mm×2.1 mm,1.7 μm);流动相乙腈(A)-水(B),梯度洗脱(0~1 min,5%A;1~2 min,5%→30%A;2~5 min,30%→32%A;5~8 min,32%→35%A;8~12 min,35%→40%A;12~15 min,40%→45%A;15~20 min,45%A);流速0.45 mL·min-1;柱温40℃,进样量3 μL,检测波长为205 nm(柴胡皂苷a、c、d、e、f)和254 nm(柴胡皂苷b2)。
2.2 对照品溶液的制备
取柴胡皂苷a、b2、c、d、e、f对照品适量,分别精密称定,加甲醇制成每1 mL含柴胡皂苷a 0.20 mg、柴胡皂苷b20.0075 mg、柴胡皂苷c 0.08 mg、柴胡皂苷d 0.30 mg、柴胡皂苷e 0.020 mg、柴胡皂苷f 0.05 mg的混合对照品溶液,即得。
2.3 供试品溶液的制备
取柴胡药材粉末(过3号筛),约1.0 g,精密称定,置具塞锥形瓶中,加含5%氨水的甲醇25 mL,密塞,称重,超声处理(功率500 W,频率40 kHz)30 min,取出,放冷,用含5%氨水的甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。
2.4 方法学考察
2.4.1 专属性 取空白溶液(含5%氨水的甲醇)、混合对照品溶液、供试品溶液,分别注入液相色谱仪,记录色谱图。结果显示空白溶液在与混合对照品溶液和供试品溶液相应位置没有色谱峰,表明空白溶液对6种皂苷成分的检测无干扰,方法专属性良好,见图1。

图1 柴胡6种皂苷的高效液相色谱图Fig 1 HPLC chromatogram of 6 saikosaponins in Bupleuri Radix
2.4.2 线性关系、检测限和定量限考察 取混合对照品储备液,用甲醇稀释成不同浓度的混合对照品溶液,按“2.1”项下方法检测,以柴胡皂苷进样量(x)与峰面积(y)绘制标准曲线。以信噪比S/N为 3∶1时的质量浓度为检测限和S/N为10∶1时的质量浓度为定量限,结果见表2。

表2 线性范围Tab 2 Linearity
2.4.3 精密度试验 取对照品溶液,按“2.1”项下色谱条件连续进样6次,记录色谱图,计算柴胡皂苷a、b2、c、d、e、f 的峰面积RSD(n=6),结果对照品溶液RSD分别是0.39%、0.13%、0.61%、0.14%、1.5%、1.1%,表明仪器精密度良好。
2.4.4 重复性试验 取同一批号药材,精密称定6份,按“2.3”项下方法制备供试品溶液,按“2.1”项下色谱条件测定,记录色谱图,测得含柴胡皂苷a 6.29 mg·g-1、柴胡皂苷b20.0933 mg·g-1、柴胡皂苷c 1.94 mg·g-1、柴胡皂苷d 7.86 mg·g-1、柴胡皂苷e 0.639 mg·g-1、柴胡皂苷f 1.42 mg·g-1,RSD分别为0.50%、0.43%、0.89%、0.71%、1.8%、1.4%,结果表明本方法重复性良好。
2.4.5 稳定性考察 取同一供试品溶液分别在0、4、8、12、18、24、48 h 按照“2.1”项下色谱条件进样测定,记录色谱图,计算柴胡皂苷a、b2、c、d、e、f峰面积的RSD,结果为2.1%、1.7%、2.0%、1.6%、2.2%、2.6%,表明供试品溶液在48 h 内稳定性良好。
2.4.6 准确度试验 取柴胡皂苷a、b2、c、d、e、f对照品,精密称定,加含5%浓氨溶液的甲醇溶解,配制成每1 mL含柴胡皂苷a 0.1204 mg、柴胡皂苷b20.0018 mg、柴胡皂苷c 0.0398 mg、柴胡皂苷d 0.1503 mg、柴胡皂苷e 0.0127 mg、柴胡皂苷f 0.0290 mg的回收率对照品溶液;取柴胡药材粉末0.5 g,精密称定,共6份,置具塞锥形瓶中,分别精密加入回收率对照品溶液25 mL(相当于药材含量100%),按“2.3”项下方法处理,按“2.1”项下色谱条件测定,记录色谱图,结果6种成分的回收率均在95.56%~104.91%,RSD均在0.61%~2.4%,说明本方法准确度良好。
2.5 相对校正因子测定
2.5.1 相对校正因子 采用多点校正法[16-18],即以多个浓度点计算所得的相对校正因子的平均值作为定量用相对校正因子f,公式为Fs/k=(Ms×Ak)/(Mk×As)(Ms为内参物质量,Mk为待测物质质量,As为内参物峰面积,Ak为待测物质峰面积)。取柴胡皂苷a、b2、c、d、e、f 对照品,精密称定,加甲醇配制成混合对照品溶液,并稀释成不同质量浓度的对照品溶液。按“2.1”项下色谱条件测定,记录色谱图,以柴胡皂苷d为内参物,分别计算待测成分柴胡皂苷a、b2、c、e、f 的相对校正因子,结果5个待测成分的相对校正因子分别为0.9990、4.4151、0.7235、0.9614、0.7972。
2.5.2 耐用性考察 分别考察柱温38、42℃,流速0.40、0.50 mL·min-1对相对校正因子的影响,结果见表3。不同色谱条件下各皂苷的相对校正因子RSD均小于3.0%,耐用性良好。

表3 相对校正因子的耐用性结果Tab 3 Durability of relative correction factors
2.6 QAMS与ESM的测定结果比较
取8批市场购买的柴胡药材,把地下部位和残茎分开处理,分别按“2.3”项下方法制备供试品溶液,以“2.1”项下色谱条件测定,分别采用ESM和QAMS方法进行计算,结果见表4。采用SPSS 20.0软件对两种方法计算的结果进行t检验,结果两组5个成分之间均无显著性差异(Pssa=0.95、Pssb2=0.77、Pssc=0.75、Psse=0.94、Pssf=0.99,均大于0.05),证明QAMS 在柴胡药材的多指标成分质量评价中的应用是可行的。
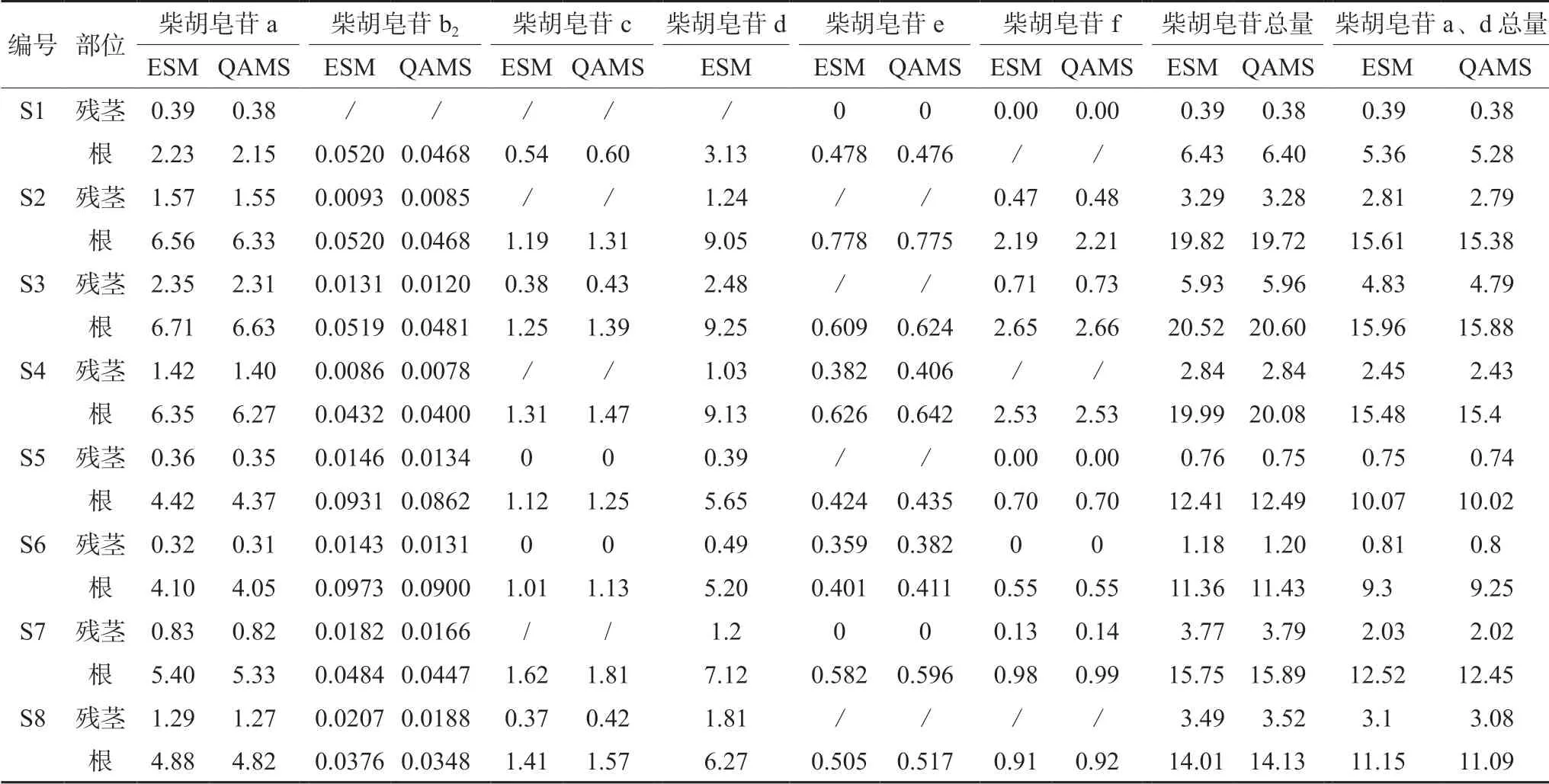
表4 一测多评法与外标法含量测定结果(mg·g-1)Tab 4 Content determination results of QAMS and ESM (mg·g-1)
2.7 柴胡药材不同部位皂苷类成分含量差异研究
2.7.1 柴胡药材不同部位主成分分析 柴胡药材不同部位皂苷类成分含量见表5。以柴胡皂苷a、b2、c、d、e、f 的含量为变量,采用PCA法对表5中8批柴胡药材的根和残留茎进行分析。PCA得分图见图2。整体来看,8批柴胡药材的根和残留茎在PCA 得分图中可被明显区分为2个区域。根和残留茎被明显区分,说明柴胡药材的根和残留茎在化学成分方面具有差异性。

图2 8批柴胡药材的PCA 得分图Fig 2 PCA score of 8 batches of Bupleuri Radix
2.7.2 柴胡药材皂苷类成分分布规律研究 基于上述结果,柴胡药材残茎中的柴胡皂苷含量要远低于根。为研究柴胡药材中皂苷类成分的分布规律,对市购的8批柴胡药材根和残茎分别进行了分段处理,检测其中的皂苷类成分含量,结果显示柴胡皂苷总量,柴胡皂苷a、d的总量以及柴胡皂苷a、b2、c、d、e、f 6个成分的含量分布规律均为:茎2 cm以上<茎1~2 cm<茎0~1 cm<根0~1 cm<根1~2 cm<根2 cm以下,见表5、图3。

图3 柴胡不同部位皂苷含量Fig 3 Content of saikosaponins in different parts of Bupleuri Radix

表5 柴胡不同部位皂苷含量结果(mg·g-1)Tab 5 Content of saikosaponin in different parts of Bupleuri Radix (mg·g-1)
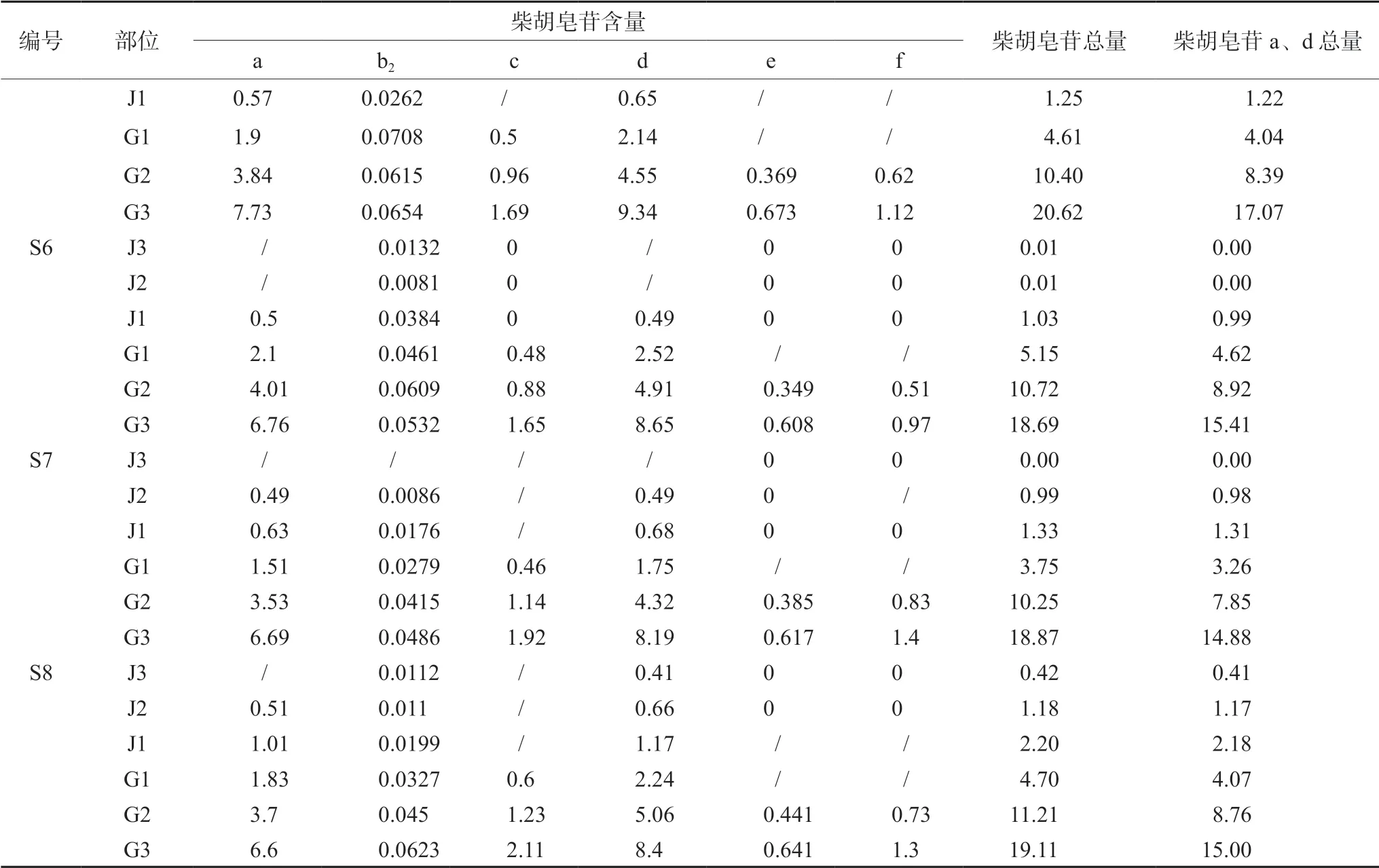
续表5
3 讨论
3.1 色谱条件的考察
UPLC具有灵敏度高、分离度好等特点,与HPLC相比缩短了分析时间,同时减少了溶剂用量,降低了分析成本,适用于解决中药组分复杂、分离困难等问题。因此,本试验建立了UPLC-PDA同时测定柴胡中6种皂苷含量的分析方法。对比了含5% 氨水的甲醇溶液、100%甲醇溶液对柴胡药材中柴胡皂苷类的提取效率,结果表明含5% 氨水的甲醇溶液提取效率明显高于100%甲醇溶液。在流动相的选择上,考察了乙腈-水、乙腈-0.1%乙酸溶剂系统,以乙腈-水为流动相时,色谱峰分离效果好,基线平稳。同时,考察了Waters ACQUITY UPLC HSS T3(100 mm×2.1 mm,1.8 μm)、Agilent ZORBAX Eclipse Plus C18(100 mm×2.1 mm,1.8 μm)、Waters ACQUITY UPLC BEH C18(100 mm×2.1 mm,1.7 μm)3种型号的色谱柱,最终发现色谱柱Waters ACQUITY UPLC BEH C18(100 mm×2.1 mm,1.7 μm)对各峰分离效果优于其余色谱柱,故选择其用于含量测定方法的建立。
柴胡皂苷a、c、d、e、f最大吸收波长为205 nm,而柴胡皂苷b2在254 nm 有最大吸收,为确保6 种柴胡皂苷均能很好地响应,综合考虑确定在双波长下同时测定6种柴胡皂苷的含量。
3.2 一测多评法质量评价
柴胡皂苷d是柴胡药材的主要特征成分之一,含量较高,其对照品容易获得,质量稳定,本试验采用QAMS法对柴胡药材中6种皂苷类成分进行含量测定,选用柴胡皂苷d作为内参物,对8批柴胡药材的不同部位中6种皂苷类成分进行测定,分别采用ESM和QAMS计算,结果两种方法差异无统计学意义,说明QAMS可以用于柴胡药材中6种皂苷类成分的含量测定。
3.3 柴胡药材药用部位的讨论
柴胡药材的地上部分和地下部分的皂苷含量差异较大,地下部分皂苷含量要远高于地上部分。文献报道柴胡药材的根和茎叶中的化学成分具有明显区别[19-21],地上部分的黄酮类成分含量较高[22-23];另外柴胡地上和地下部分在药效学上存在差异[24-26],如北柴胡地下部分根具有保肝作用,而其地上部分无此作用,在解热、抗炎等作用方面也有区别[27-29]。
本研究的8个样品中地下部分柴胡皂苷a、d含量在0.53%~1.60%,全部符合《中国药典》总量不得低于0.30%的规定;地上残留茎部分只有2个样品的柴胡皂苷a,d 总量在0.30%~0.49%,其余均不符合药典规定,因此,地上残留茎部分不可以作为柴胡的药用部位。
研究发现残茎中柴胡皂苷的含量是随着长度的增加呈递减趋势的,然而即使是靠近根部的茎0~1 cm部分的6个柴胡皂苷的总量也只有地下根部的14%,建议柴胡药材加工过程中应尽量除去残茎,减少残茎掺杂,保证药材的质量。

