TCH新辅助化疗方案对HER2阳性乳腺癌的疗效及对患者ER、PR、HER2表达的影响
温润耀

【摘要】 目的:探討TCH新辅助化疗方案对人表皮生长因子受体2(HER2)阳性乳腺癌的疗效及对患者ER、PR、HER2表达的影响。方法:选择2019年1月-2020年3月在本院进行治疗的78例乳腺癌患者。按照随机数字表法将患者分为观察组和对照组,每组39例。对照组接受TAC方案,观察组接受TCH方案。比较两组患者的疗效、FACT-B评分、不良反应发生情况。结果:观察组干预后ER、PR水平均高于干预前和对照组,Ki-67、HER2、CEA、CA15-3水平均低于干预前和对照组,差异均有统计学意义(P<0.05)。观察组干预后TGF-β1、VEGF水平均低于干预前和对照组,差异均有统计学意义(P<0.05)。观察组总有效率为97.44%,高于对照组的76.92%,差异有统计学意义(P<0.05)。治疗后,两组FACT-B评分均高于治疗前,且观察组高于对照组,差异均有统计学意义(P<0.05)。观察组不良反应发生率为7.69%,低于对照组的25.64%,差异有统计学意义(P<0.05)。结论:TCH新辅助化疗方案治疗HER2阳性乳腺癌疗效显著,能够促进HER2下降和ER、PR升高,且安全性良好。
【关键词】 HER2阳性乳腺癌 TCH新辅助化疗 ER PR
Influence of Efficacy and Levels of ER, PR, HER2 in HER2 Positive Breast Cancer by TCH Neoadjuvant Chemotherapy Regimen/WEN Runyao. //Medical Innovation of China, 2021, 18(13): 0-019
[Abstract] Objective: To investigate the efficacy of TCH neoadjuvant chemotherapy regimen on human epidermal growth factor receptor 2 (HER2) positive breast cancer and its effect on ER, PR and HER2 expression in patients. Method: A total of 78 patients with breast cancer who received treatment in our hospital from January 2019 to March 2020 were selected. According to random number table method, the patients were divided into observation group and control group, 39 cases in each group. The control group received TAC regimen, and the observation group received TCH regimen. The efficacy, FACT-B score and the incidence of ADR were compared between the two groups. Result: After intervention, the levels of ER and PR in the observation group were higher than those of before intervention and the control group, and the levels of Ki-67, HER2, CEA and CA15-3 in the observation group were lower than those of before intervention and the control group, the differences were statistically significant (P<0.05). The levels of TGF-β1 and VEGF in the observation group after intervention were lower than those before intervention and control group, the differences were statistically significant (P<0.05). The total effective rate of the observation group was 97.44%, which was higher than 76.92% of the control group, the difference was statistically significant (P<0.05). After treatment, FACT-B scores of both groups were higher than before treatment, and observation group was higher than control group, the differences were statistically significant (P<0.05). The incidence of ADR in the observation group was 7.69%, which was lower than 25.64% in the control group, the difference was statistically significant (P<0.05). Conclusion: The TCH neoadjuvant chemotherapy regimen has significant efficacy in the treatment of breast cancer with positive HER2, and can promote the decrease of HER2 and the increase of ER and PR, with good safety.
[Key words] HER2 positive breast cancer TCH neoadjuvant chemotherapy ER PR
First-authors address: Dongguan Peoples Hospital, Dongguan 523059, China
doi:10.3969/j.issn.1674-4985.2021.13.004
乳腺癌在女性中有着比较高的发病率,属于恶性肿瘤之一,转移率和死亡率均较高的,该疾病的发生发展严重威胁者女性健康。人表皮生长因子受体2(HER2)阳性乳腺癌作为一种特殊疾病,为乳腺癌的常见类型,恶性程度和侵袭性均高于其他类型乳腺癌,目前主要采取化疗进行治疗[1]。近几年,TCH新辅助化疗在该疾病治疗中的效果逐渐得到了临床医师的认可,化疗敏感性较好[2]。随着国外对于HER2阳性乳腺癌发病机制研究的不断深入,有报道指出雌激素受体(ER)以及HER2均在该病的发病中发挥着重要作用,经过化疗后也会出现明显的改变,但国内对此研究较少[3-4]。本研究即对这一方案与常规TAC方案治疗效果差异及对ER、PR、HER2等的影响进行分析。现报道如下。
1 资料与方法
1.1 一般资料 选择2019年1月-2020年3月在本院进行治疗的78例乳腺癌患者。(1)纳入标准:符合乳腺癌诊断标准[5],经病理检查和免疫组化染色检查明确为HER2阳性乳腺癌;初次确诊,入选前未接受过任何方案化疗治疗;TNM分期为Ⅱ~Ⅲ期;预计生存期>6个月;均为女性。(2)排除标准:有远处转移情况者;合并其他恶性肿瘤或重要脏器功能障碍者;有血液系统或免疫系统疾病者;无法耐受本研究治疗方案者。按照随机数字表法将患者分为观察组和对照组,每组39例。患者均知情同意并签署相关文件,研究经伦理学委员会批准。
1.2 方法 (1)对照组接受TAC方案化疗:多西他赛注射液(生产厂家:正大天晴药业集团股份有限公司;批准文号:国药准字H20183209;规格:1 mL︰20 mg)75 mg/m2,第1天静脉滴注;注射用盐酸表柔比星(生产厂家:浙江海正药业股份有限公司,批准文号:国药准字H19990279,规格:10 mg/支)80 mg/m2,第2天静脉滴注;注射用环磷酰胺(生产厂家:山西普德药业有限公司,批准文号:国药准字H14023686,规格:0.2 g/瓶)500 mg/m2,第1、2天静脉滴注。21 d
为1个疗程,共治疗6个疗程。(2)观察组接受TCH方案化疗:多西他赛注射液75 mg/m2,第1天静脉滴注;注射用卡铂(生产厂家:齐鲁制药有限公司,批准文号:国药准字H20020180,规格:10 mL︰100 mg)AUC=6,第1天静脉滴注;注射用曲妥珠单抗(生产厂家:Genentech Inc.,批准文号:注册证号S20060026,规格:440 mg︰20 mL)8 mg/kg,第1~7天静脉滴注。21 d为1个疗程,从第2个疗程开始曲妥珠单抗剂量下调至6 mg/kg。共治疗6个疗程。
1.3 观察指标及判定标准 比较两组患者的雌激素受体(ER)、孕激素受体(PR)、Ki-67、HER2、癌胚抗原(CEA)、糖类抗原15-3(CA15-3)、TGF-β1、VEGF水平、生命质量评分、疗效、不良反应发生情况。治疗效果评估具体如下,完全缓解:MRI检查结果显示,患者的相关的肿瘤病灶,都达到完全消失的程度;部分缓解:病灶体积缩小≥50%,表明患者的临床症状达到了部分缓解的效果;稳定:病灶体积缩小<50%或增大<25%,表明患者的临床症状达到了稳定的治疗效果;进展:病灶体积增大≥25%或有新病灶出现[6];总有效率=(完全缓解例数+部分缓解例数)/总例数×100%。生命质量评估使用FACT-B评分,涉及5项内容,总分为0~144分,评分越高表示生命质量越好[7]。
1.4 统计学处理 采用SPSS 22.0软件对所得数据进行统计分析,计量资料用(x±s)表示,组间比较采用t检验,组内比较采用配对t检验;计数资料以率(%)表示,比较采用字2检验。以P<0.05为差异有统计学意义。
2 结果
2.1 两组一般资料比较 观察组年龄32~68岁,平均(45.25±6.38)岁;体质量指数(BMI)18.52~25.41 kg/m2,平均(22.05±2.71)kg/m2。对照组年龄33~69岁,平均(45.64±6.44)岁;BMI 18.52~25.41 kg/m2,平均(21.93±2.82)kg/m2。两组一般资料比较,差异均无统计学意义(P>0.05),具有可比性。
2.2 两组干预前后ER、PR、Ki-67、HER2、CEA、CA15-3水平比较 干预前,两组ER、PR、Ki-67、HER2、CEA、CA15-3水平比较,差异均无统计学意义(P>0.05);观察组干预后ER、PR水平均高于干预前和对照组,Ki-67、HER2、CEA、CA15-3水平均低于干预前和对照组,差异均有统计学意义(P<0.05)。见表1。
2.3 两组干预前后TGF-β1、VEGF水平比较 干预前,两组TGF-β1、VEGF水平比较,差异均无统计学意义(P>0.05);观察組干预后TGF-β1、VEGF水平均低于干预前和对照组,差异均有统计学意义(P<0.05)。见表2。
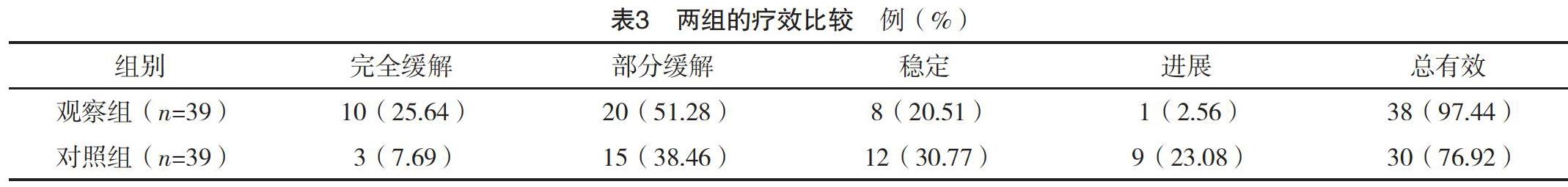
2.4 两组的疗效比较 观察组总有效率为97.44%,高于对照组的76.92%,差异有统计学意义(字2=8.251,P<0.05),见表3。
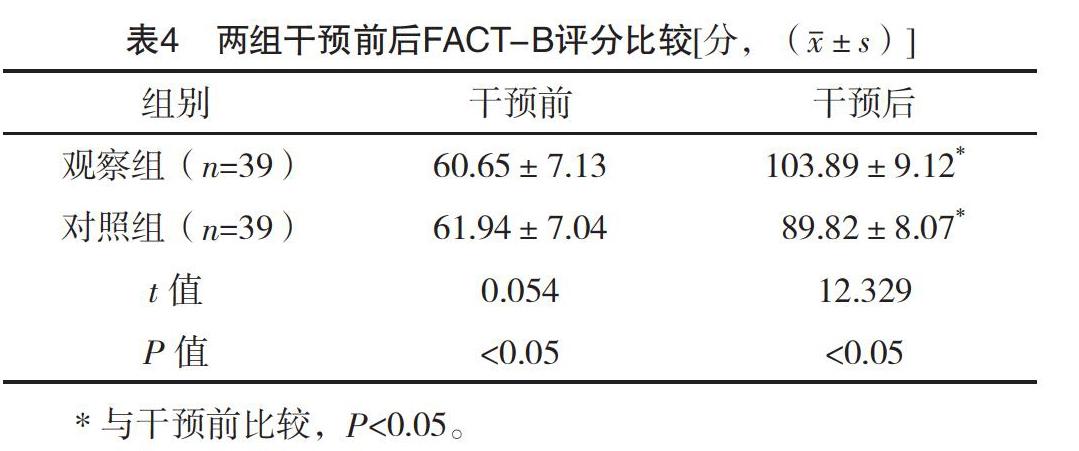
2.5 两组干预前后FACT-B评分比较 干预后,两组FACT-B评分均高于干预前,且观察组高于对照组,差异均有统计学意义(P<0.05),见表4。
2.6 两组不良反应发生情况比较 观察组不良反应发生率为7.69%,低于对照组的25.64%,差异有统计学意义(字2=6.324,P<0.05),见表5。
3 讨论
我国是世界上乳腺癌的高发地区,且该病的发病正呈现年轻化趋势,严重威胁女性健康。调查研究显示,HER2阳性乳腺癌约占所有乳腺癌的20%,属于一种难治且恶性程度较高的乳腺癌类型[8]。目前,临床上对于HER2阳性乳腺癌早期主要采取手术切除,但单纯手术的临床疗效仍难以满足患者日益增长的治疗需求,因此以手术为主,化疗为辅的治疗方式逐渐成了临床研究的热点[9]。
在HER2阳性乳腺癌的化疗方面,由于该病具有确切的驱动基因,因此多采取抗HER2靶向治疗,曲妥珠单抗即为一线化疗药物[10]。近几年,大量文献报道也指出采取曲妥珠单抗联合化疗在这一疾病的治疗中显示出了良好的临床优势和安全性,由多西他赛、卡铂和曲妥珠单抗组成的TCH新辅助化疗方案的临床效果也得到了临床医师的认可[11-12]。临床研究表明,曲妥珠单抗以癌基因为治疗靶点,对于HER2受体的靶向作用明确;多西他赛则为强效抗癌药物,能够有效抑制癌细胞的分裂,并调节雌激素受体的表达,为相关治疗提供了有利条件[13]。有研究报道指出,曲妥珠单抗与多西他赛联合使用,有良好的协同作用,在控制乳腺癌病情进展,提高治疗总有效率方面效果显著[14-16]。本研究结果也显示,观察组总有效率较高,且CEA、CA15-3等常见肿瘤标志物的抑制效果也优于对照组,证实了TCH的治疗作用,与上述研究报道相符。
国外研究报道指出,ER、PR、HER2与乳腺癌的发生和病情进展有紧密联系,其中HER2与多种恶性肿瘤的癌细胞转化密切相关,乳腺癌患者出现癌变后HER2水平会在短时间内异常升高,诱导癌细胞进行大量繁殖,促进病灶扩大,加剧病情,可用于评估HER2阳性乳腺癌的治疗预后[17-18];乳腺癌患者出现癌变后PR与ER则会出现下降的情况[19-20]。本研究中两组干预后ER、PR水平均高于同组治疗前,HER2水平低于同组干预前(P<0.05),且观察组干预后ER、PR水平均高于对照组(P<0.05),HER2水平低于对照组,则表明经过有效的化疗治疗患者的病情得到控制,癌细胞生长、增殖、分化得到有效抑制,而TCH新辅助化疗方案对ER、PR、HER2表达的影响则更为显著。另外,在生命质量和安全性方面,观察组治疗后FACT-B评分高于对照组,化疗相关不良反应总发生率低于对照组(P<0.05),也表明TCH新辅助化疗方案能够有效改善患者的生命质量,且有更好的安全性。
综上所述,TCH新辅助化疗方案治疗HER2阳性乳腺癌疗效显著,能够促进HER2下降和ER、PR升高,且安全性良好。
参考文献
[1]李佳圆,郝宇,吴雪瑶.基于多组学数据的流行病学研究策略及其在乳腺癌研究中的应用[J].中国普外基础与临床杂志,2020,27(11):1344-1347.
[2] Loibl S,Gianni L.HER2-positive breast cancer[J].Lancet,2017,389(10087):2415-2429.
[3] Agnieszka K,Marzena K,Katarzyna S,et al.Primary and secondary prevention of breast cancer[J].Ann Agric Environ Med,2017,24(4):549-553.
[4]江水娥,许海莺.乳腺癌ER、PR、Ki67表达与临床病理的关系[J].深圳中西医结合杂志,2019,29(24):93-95.
[5]中国抗癌协会乳腺癌专业委员会.中国抗癌协会乳腺癌诊治指南与规范(2019年版)[J].中国癌症杂志,2019,29(8):609-680.
[6] Aras M,Erdil T Y,Dane F,et al.Comparison of WHO, RECIST 1.1, EORTC, and PERCIST criteria in the evaluation of treatment response in malignant solid tumors[J].Nucl Med Commun,2016,37(1):9-15.
[7] Matthies L M,Taran F A,Keilmann L,et al.An Electronic Patient-Reported Outcome Tool for the FACT-B (Functional Assessment of Cancer Therapy-Breast) Questionnaire for Measuring the Health-Related Quality of Life in Patients With Breast Cancer: Reliability Study[J].Journal of Medical Internet Research,2019,21(1):e10004.
[8] Waks A G,Winer E P.Breast Cancer Treatment: A Review[J].JAMA,2019,321(3):288-300.
[9]高晓洁.HER2阳性乳腺癌靶向治疗的研究进展[J].中国城乡企业卫生,2020,35(11):49-51.
[10]李莹,刘芯,曾伟燃,等.曲妥珠单抗靶向治疗联合新辅助化疗对HER2阳性表达乳腺癌的治疗效果[J].临床医学研究与实践,2019,4(35):85-87.
[11]冯凌飞,贺曾.赫赛汀联合多西他赛对人表皮生长因子受体-2阳性转移性乳腺癌的臨床疗效[J].安徽医药,2020,24(10):2095-2098.
[12]陈魏威,权广前,王金津.曲妥珠单抗联合多西他赛治療乳腺癌的疗效及安全性评价[J].中国老年保健医学,2019,17(6):67-69.
[13]谢林浩.曲妥珠单抗联合多西他赛和铂类对HER-2阳性转移性乳腺癌的临床疗效和不良反应[J].北方药学,2016,13(10):149,177.
[14] Wildiers H,Tryfonidis K,Dal L,et al.PertuzumabandtrastuzumabwithorwithoutmetronomicchemotherapyforolderpatientswithHER2-positivemetastaticbreastcancer(EORTC75111-10114):anopen-label,randomised,phase2trialfromtheElderlyTaskForce/BreastCancerGroup[J].Lancet Oncol,2018,19(3):323-336.
[15]崔志超,周立芝,马杰,等.乳腺癌患者新辅助化疗后ER、PR、HER2、Ki67表达变化及临床意义[J].现代生物医学进展,2020,20(10):1997-2000,1960.
[16] Kolarova I,Vanasek J,Odrazka K,et al.Therapeutic significance of hormone receptor positivity in patients with HER-2 positive breast cancer[J].Biomed Pap Med Fac Univ Palacky Olomouc Czech Repub,2019,163(4):285-292.
[17]郑书楷,凌飞海,崔世恩,等.TCH新辅助化疗治疗HER-2阳性乳腺癌的临床有效性分析[J].中外女性健康研究,2018,11(13):180,188.
[18]石峰.曲妥珠单抗联合紫杉醇卡铂方案新辅助化疗治疗HER-2阳性乳腺癌疗效及不良反应分析[J].医学理论与实践,2016,29(17):3017-3019.
[19]刘志.序贯和同步曲妥珠单抗联合蒽环类方案对人表皮生长因子受体-2阳性乳腺癌患者新辅助化疗效果及安全性的影响[J].中国医学工程,2019,27(7):96-99.
[20]徐巧萍,朱洁瑾,刘坚,等.HER-2阳性乳腺癌患者2种新辅助化疗方案的药物经济学评价[J].中国现代应用药学,2019,36(8):985-992.
(收稿日期:2021-04-09) (本文编辑:姬思雨)

