河南部分地区番茄黄化曲叶病毒和番茄褪绿病毒复合侵染的分子鉴定
王东 刘帅 张燕 杨世玮 苏玉静 陈红旭 丁飞 薛东齐 贾芝琪


摘 要:为调查河南省部分地区番茄病毒病危害情况,于2019年10月采集16份表现黄化、曲叶症状的番茄植株,利用分子生物学技术对其进行鉴定。结果表明:供试样品均被TYLCV(Tomato yellow leaf curl virus)侵染,31.75%的样品被TYLCV和ToCV(Tomato chlorosis virus)复合侵染;DNA全序列比对分析发现,供试样品中分离的TYLCV河南菌株与TYLCV-Is等地区的核苷酸序列同源性均达到94%以上,其中TYLCV-HN-AY-1分离物与TYLCV-Almeria(NC004005.1)序列相似性最高,为99.5%;对供试样品TYLCV抗病基因分子检测发现,部分番茄样品含有Ty-1、Ty-2、Ty-3/Ty-3a,表明部分TYLCV株系已突破Ty-1、Ty-2、Ty-3/Ty-3a的抗性。该结果对指导河南省番茄的安全生产具有重要意义。
关键词:番茄;黄化曲叶病毒;番茄褪绿病毒;复合侵染
中图分类号:S641.2+S436.412.1+1 文献标志码:A 文章编号:1673-2871(2021)02-012-006
Molecular identification of Tomato yellow leaf curl virus and Tomato chlorosis virus in some areas of Henan province
WANG Dong, LIU Shuai , ZHANG Yan, YANG Shiwei, SU Yujing, CHEN Hongxu, DING Fei, XUE Dongqi, JIA ZhiqiA
(College of Horticulture, Henan Agricultural University, Zhengzhou 450002, Henan, China)
Abstract: In order to investigate the damage of tomato virus disease in some areas of Henan province, 16 tomato samples with symptoms of yellow leaf curl were collected in October 2019 and identified by molecular biology techniques.Results showed that the samples were all infected by TYLCV(tomato yellow leaf curl virus), and 31.75% of the samples were infected by TYLCV and ToCV(tomato chlorosis virus). DNA sequence alignment analysis showed that the nucleotide sequence homology between the Henan isolates and other regions reached over 94%. The sequence identity between TYLCV-HN-AY-1 and TYLCV-Almeria (NC004005.1) isolation is 99.5%. The detection of TYLCV resistance genes found that some tomato samples contained TYLCV resistance genes Ty-1, Ty-2 and Ty-3/Ty-3a, indicating that TYLCV Henan strains have broken the resistance of Ty-1, Ty-2 and Ty-3/Ty-3a. The results are of great significance to guide the safe production of tomato in Henan Province.
Key words: Tomato; Tomato yellow leaf curl virus(TYLCV); Tomato chlorosis virus(ToCV); Mixed infections
番茄黃化曲叶病毒(Tomato yellow leaf curl virus,TYLCV)属于双生病毒科(Geminiviridiae)菜豆金色花叶病毒属(Begomovirus)。该病毒由烟粉虱传播,发病迅速,严重危害番茄生产,甚至导致番茄绝产[1]。番茄感病植株表现为植株生长发育缓慢、矮化,节间明显变短,叶片变厚、变小,叶片边缘至叶脉区域黄化,叶缘向上卷曲,果实坐果数量明显减少,且易出现变小和畸形[2]。TYLCV首次在以色列被发现,然后随着媒介烟粉虱的传播在全球范围内大暴发,我国在2006年首次在上海检测到TYLCV后,北京、河北、河南、浙江等20个省市的番茄产区陆续检测到该病毒,给番茄生产带来巨大影响,造成严重的经济损失[1,3-5]。番茄褪绿病毒(Tomato chlorosis virus,ToCV)是由烟粉虱传播的单链RNA病毒,属于长线型病毒科(Closteroviridae)毛形病毒属(Crinivirus),番茄感病植株主要表现为叶片褪绿和黄化症状,在番茄生产上常被误认为缺素症,导致诊断和防治的延误。番茄褪绿病毒于1998年首次在美国佛罗里达州被发现,之后在意大利、巴西、以色列等国也相继被报道[6-8]。番茄褪绿病毒在2004年传播到我国台湾,随后在江苏、北京、南京、河南、河北、天津、湖南等设施番茄产区陆续有该病毒的报道,并且造成严重损失[9-11]。
TYLCV和ToCV的单独侵染或复合侵染均能够对番茄造成严重损失,因此对病害的检测和防治就显得尤为必要。目前在ToCV和TYLCV的检测方法上主要有目测法、分子生物学方法、组织印迹杂交法、血清学检测技术等[10,12-16]。分子生物学方法通过检测病毒核酸来检测病毒的存在,其特异性更强,检测病毒的范围更广,并可以进行大批量样本检测。在TYLCV抗病基因挖掘方面,现已发现的TYLCV抗病基因有Ty-1、Ty-2、Ty-3、Ty-4、Ty-5、Ty-6;在抗病品种选育方面,我国育成的一系列抗TYLCV番茄品种中大多数含有Ty-1,少数含有Ty-2或Ty-3抗病基因[16]。ToCV虽然发现较早,但是番茄抗ToCV的种质资源筛选和育种进展则相对缓慢,目前国内外尚未有抗ToCV的番茄品种的报道。越来越多的田间观察结果发现,很多含有Ty抗病基因的番茄品种和材料表现感病,推测原因可能是病毒菌株发生变异,或是其他病毒的复合侵染降低了抗病基因的抗病性[17-18]。
本研究于2019年10月在河南省部分番茄产区收集出现叶脉褪绿、心叶黄化、曲叶等症状的番茄样品,对其进行了病原物分析、测序鉴定和序列分析,并分析了ToCV与TYLCV复合侵染的情况,对样品携带的抗病基因进行了分子标记鉴定。该结果对探究番茄黄化曲叶病毒抗病基因抗病性丧失原因及指導河南省番茄的安全生产具有重要意义。
1 材料与方法
1.1 材料
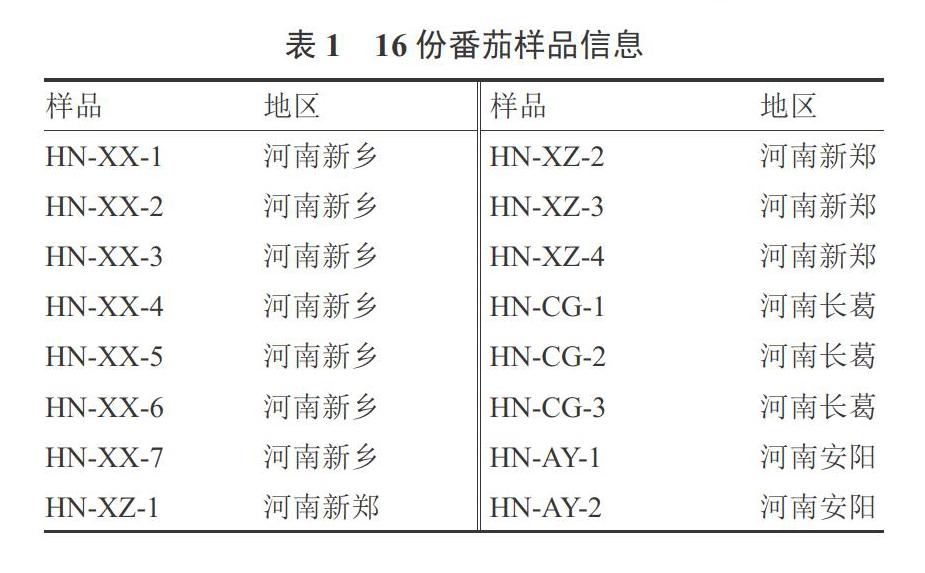
16份表现黄化、曲叶症状的番茄样品于2019年10月采自河南省番茄主要产区,具体信息见表1。
1.2 番茄黄化曲叶病毒分子鉴定
番茄样品总DNA提取采用CTAB法,利用TYLCV特异性引物(表2)进行PCR扩增,PCR体系:2X San Taq PCR Mix 12.5 ?L,上下游引物各1.5 ?L,模板DNA 1 ?L,ddH2O 8.5 ?L。PCR程序为95 ℃预变性4 min,94 ℃变性45 s,50 ℃ 45 s,72 ℃延伸3 min,35次循环,72 ℃延伸10 min,4 ℃保存。PCR产物纯化回收送生工生物工程(上海)股份有限公司测序。
1.3 番茄褪绿病毒分子鉴定
番茄样品采用北京华越洋植物多糖多酚植物RNA提取试剂盒提取RNA,反转录采用莫纳反转录试剂盒,反转录体系:RNA 1 ?L,MonScriptTM 5×RTIII AII-in-One Mix 4 ?L,MonScriptTM dsDNase 1 ?L,Nuclease-Free Water 14 ?L。反转录程序:37 ℃ 2 min,55 ℃15 min,85 ℃ 5 min。反转录完成后的cDNA于-80 ℃保存。采用ToCV特异性引物ToCV-F/R(表2)进行PCR扩增,PCR体系:2× San Taq PCR Mix 12.5 ?L,上下游引物各1.5 ?L,cDNA第一链1 ?L,ddH2O 8.5 ?L。PCR程序为94 ℃预变性3 min,94 ℃变性30 s,57 ℃30 s,72 ℃延伸30 s,35次循环,72 ℃延伸10 min,4 ℃保存。
1.4 TYLCV抗病基因Ty-1、Ty-2、Ty-3的PCR分子检测
利用Ty-1、Ty-2、Ty-3抗性基因分子标记引物(表2)进行PCR扩增,PCR体系:2× San Taq PCR Mix 12.5 ?L,上下游引物各1.5 ?L,模板DNA 1 ?L,ddH2O 8.5 ?L。PCR程序为94 ℃预变性3 min,随后94 ℃变性30 s,57.5 ℃ 30 s,72 ℃延伸45 s,35次循环,72 ℃延伸10 min,4 ℃保存。PCR产物经1%(w)的琼脂糖凝胶检测或7%(w)的聚丙烯酰胺凝胶电泳检测。
2 结果与分析
2.1 番茄TYLCV的鉴定
16份番茄样品经TYLCV特异引物扩增,全部样品均检测出2 800 bp左右的目的条带(表3,图1-a),PCR产物测序结果证实为TYLCV病毒,感染率为100%;测序获得的番茄TYLCV河南分离物的全长为2 781 bp。从NCBI中选取各地区TYLCV分离物,其中包括国内分离物20个,国外分离物6个,与本次分离得到TYLCV分离物进行比较,结果表明,该基因的核苷酸序列与TYLCV-Is(X15656.1)、TYLCV-Almeria(NC004005.1)、TYLCV- California(EF539831.1)、TYLCV-Florida-3.1 (KY971328.1)、TYLCV-JSNJ1(FN256259.1)、TYLCV-SH3(FN256258.1)、TYLCV-ZJ3(AM698117.1)、TYLCV-HBWH(MF590732.1)、TYLCV-BJ03(KT338293.1)、TYLCV-XX (JQ004048.1、MF668139.1、MF668140.1、MF668141.1)、TYLCV-AY(JQ034613.1、KX034539.1)、TYLCV-JZ(KX034541.1、KX034542.1、KX034546.1)、TYLCV-ZZ(MF590734.1)等分离物的相似性均在94%以上,其中TYLCV-Almeria(NC004005.1)分离物与TYLCV-HN-AY-1序列相似性最高,为99.5%,TYLCV-HN-XX-6与TYLCV-AY(JQ034613.1)序列相似性最低,为94.82%。
系统进化树分析表明(图2),所选择的序列共分为几大分支,其中此次分离到的TYLCV河南分离物与来自中国广东、广西、云南大理和以色列、泰国等国家或地区的TYLCV分离物聚在一个大分支,与TYLCV-XX(MF668139.1、MF668141.1)、TYLCV-JZ(KX034541.1、KX034542.1、KX034546.1)、TYLCV-AY(KX034539.1)、TYLCV-ZZ(MF590734.1)等分离物亲缘关系相对较近,与TYLCV-California(EF539831.1)、TYLCV-JSNJ1(FN256259.1)、TYLCV-XX(JQ004048.1)分离物亲缘关系相对较远,与TYLCV-BJ03(KT338293.1)、TYLCV-HBWH(MF590732.1)、TYLCV-SH3(FN256258.1)、TYLCV-ZJ3(AM698117.1)4个分离物的亲缘关系最远。
2.2 番茄ToCV的鉴定
16份番茄样品经ToCV特异性引物检测并测序验证,有5株番茄样品检测出239 bp的ToCV目的条带(表3,图1-b),其中新乡、安阳和长葛地区分别有2个、2个和1个样品检测到ToCV。这5株番茄样品为TYLCV和ToCV复合侵染,复合侵染率31.75%,新郑地区番茄样品没有检测到ToCV。
2.3 番茄TYLCV抗病基因分子标记分析
对16份番茄样品进行Ty-1基因检测,发现所有样品均检测到252 bp(Ty-1,抗病条带)和264 bp(ty-1,感病条带)的特异性条带(表3,图1-c);其中Ty-1/Ty-1纯合基因型番茄样品3份、Ty-1/ty-1杂合基因型番茄样品7份、ty-1/ty-1感病基因型番茄样品6份。对Ty-2基因的检测发现,所有样品均检测到295 bp(Ty-2,抗病条带)和619 bp(ty-2,感病条带)的特异性条带(表3,图1-d);其中Ty-2/Ty-2基因型番茄样品2份、Ty-2/ty-2基因型番茄样品3份、ty-2/ty-2基因型番茄样品11份。对Ty-3基因的检测发现,所有样品均检测到630 bp(Ty-3a,抗病条带)、450 bp(Ty-3,抗病条带)或320 bp(ty-3,感病条带)的特异性条带(表3,图1-e);其中Ty-3a的纯合基因型番茄样品1份、Ty-3a的杂合基因型番茄样品6份、不含Ty-3基因的番茄样品6份、Ty-3纯合基因型番茄样品1份、Ty-3杂合基因型番茄样品1份、同时含有Ty-3和Ty-3a基因型番茄样品1份。
3 讨论和结论
赵黎明等[24]首次在山东发现TYLCV和ToCV的复合侵染,随后吴淑华等[25]在江苏再次发现TYLCV和ToCV的复合侵染。在此期间TYLCV和ToCV的复合侵染已从我国华南地区扩散到全国各地,造成这种现象的原因可能与农艺生产活动相关联[24-26]。但ToCV的侵染会不会造成寄主植株对TYLCV抗性的减弱值得进一步研究。
本研究样品TYLCV分离物测序结果经NCBI比对验证为TYLCV。本研究结果与之前河南地区报道的TYLCV-XX(JQ004048.1、MF668139.1、MF668140.1、MF668141.1)、TYLCV-JZ(KX034541.1、KX034542.1、KX034546.1)、TYLCV-AY(JQ034613.1、KX034539.1)、TYLCV-ZZ(MF590734.1)均与TYLCV-Is(X15656.1)进行两两序列比对,结果发现序列相似性均在94%以上,依据双生病毒分类标准,同种双生病毒基因组序列同源性大于 94% 被认为是同一株系的不同变种,判断这6个分离物属于TYLCV-Is株系[27],研究结果表明TYLCV在河南并没有发生新的病毒菌株。
对河南16份番茄样品Ty抗病基因的检测发现,被TYLCV侵染的HN-XX-4、HN-XX-5番茄样品中同时含有Ty-1、Ty-2、Ty-3/Ty-3a抗性基因(表3),表明TYLCV已经突破Ty-1、Ty-2、Ty3/Ty3a的抗性。但抗病基因抗病性丧失的原因有待进一步研究,可能的原因是随着病毒长时间的传播以及含有Ty-1、Ty-2、Ty3/Ty3a抗病品种的广泛种植,而造成变异菌株的流行,但具体是哪些位点突变所引起的还有待进一步实验证实。本研究中含有Ty-1、Ty-2、Ty-3抗性基因的部分样品具有感病症状并检测到TYLCV,却并未检测到ToCV,暗示了TYLCV和ToCV的复合侵染不是抗病性降低的主要原因。田兆丰等[17]为了解不同抗病品种中番茄黄化曲叶病毒基因变异的情况,对感染 TYLCV 的番茄抗病品种进行了TYLCV全长基因克隆和测序,未发现新的病毒菌株,推测是原有菌株的变异引起抗病基因的抗病性丧失,与本研究结果一致。Torre等[28]在含有Ty-1基因的番茄抗性品种上接种TYLCV病毒18 d后,将其与对照相比观察到轻微的花叶症状,表明不同抗病基因型对TYLCV抗性水平不同,接种压力、株龄、温度和光照强度均可能对疾病症状产生非常重要的影响[29]。但环境因素是否会影响抗病基因的抗病性也待更进一步的研究。
本研究为了解河南省部分番茄产区TYLCV和ToCV的分布、序列变异、进化等情况提供了研究基础,同时该研究结果对探究番茄黄化曲叶病毒抗病基因抗病性丧失原因以及指导河南省番茄品种选择和安全生产都具有重要意义。
参考文献
[1] WU J B, DAI F M, ZHOU X P. First report of Tomato yellow leaf curl virus in China[J].Plant Disease,2006,90(10):1359-1359.
[2] 汤亚飞,何自福,杜振国,等.番茄黄化曲叶病毒在湖北首次报道[J].植物保护,2015,41(5):233-236.
[3] 季英华,熊如意,程兆榜,等.江苏省番茄黄化曲叶病的病原分子诊断[J].园艺学报,2008,35(12):1815-1818.
[4] GHANIM M,MORIN S,ZEIDAN M,et al.Evidence for transovarial transmission of Tomato yellow leaf curl virus by its vector,the white fly Bemisia tabaci[J].Virology,1998,240(2):295-303.
[5] 楊欢欢,赵婷婷,刘冠,等.番茄黄化曲叶病抗病基因与抗病育种的最新进展[J].分子植物育种,2016,14(8):2044-2049.
[6] ACCOTTO G P,VAIRA A M,VECCHIATI M,et al.First report of Tomato chlorosis virus in Italy[J].Plant Disease,2001,85(11):1208-1208.
[7] SEGEV L, WINTERMANTEL W M,POLSTON J E,et al.First report of Tomato chlorosis virus in Israel.[J].Plant Disease,2004,88(10):1160-1160.
[8] FREITAS D M,NARDIN I,SHIMOYAMMA N,et al. First report of Tomato chlorosis virus in potato in Brazil[J].Plant Disease,2012,96(4):593-593.
[9] ZHAO R N,WANG R,WANG N,et al.First report of Tomato chlorosis virus in China[J]. Plant Disease,2013,97(8):1123-1123.
[10] KARWITHA M,FENG Z,YAO M,et al.The complete nucleotide sequence of the RNA1 of a Chinese isolate of Tomato chlorosis virus[J].Journal of Phytopathology,2014,162(6):411-415.
[11] 高利利,孙国珍,王勇,等.天津地区番茄褪绿病毒的分子检测和鉴定[J].华北农学报,2015,30(3):211-215.
[12] TSAI W S,SHIH S L,GREEN S K,et al.First report of the occurrence of Tomato chlorosis virus and Tomato infectious chlorosis virus in Taiwan[J].Plant Disease,2004, 88(3): 311-311.
[13] ZhAO L M,LI G,GAO Y,et al.Molecular detection and complete genome sequences of Tomato chlorosis virus isolates from infectious outbreaks in China[J].Journal of Phytopathology,2014,162(10):627-634.
[14] PICO B,DIEZ M J,NUEZ F.Improved diagnostic techniques for Tomato yellow leaf curl virus in tomato breeding programs[J].Plant Disease,1999,83(11):1006-1012.
[15] JACQUEMOND M,VERDIN E,DALMON A,et al.Serological and molecular detection of Tomato chlorosis virus and Tomato infectious chlorosis virus in tomato[J].Plant Pathology,2008,58(2):210-220.
[16] 胡恩美,余文贵,王银磊,等.番茄抗黄化曲叶病基因研究进展[J].江苏农业学报,2013,29(6):1496-1502.
[17] 田兆豐,杨天琦,董丹,等.感染番茄抗病品种的番茄黄化曲叶病毒的基因变异[J].科学技术与工程,2018,18(8):21-26.
[18] GARCIACANO E,RESENDE R O,FERNANDEZMUNOZ R,et al. Synergistic interaction between Tomato chlorosis virus and Tomato spotted wilt virus results in breakdown of resistance in tomato[J].Phytopathology,2006,96(11):1263-1269.
[19] 胡霞,王蓉,李菲菲,等.番茄抗TYLCV基因新标记的开发及其在多抗聚合选择中的应用[J].中国蔬菜,2014 (10):18-23.
[20] JI Y,SCOTT J W,SCHUSTER D J,et al.Fine mapping of the Tomato yellow leaf curl virus resistance gene Ty-2 on chromosome 11 of tomato[J].Molecular Breeding,2009,34(2):749-760.
[21] 薛东齐.中国番茄黄化曲叶病毒株系分化及侵染性克隆的构建[D].哈尔滨:东北农业大学,2013.
[22] 王志荣,李晓东,朱玉,等.陕西杨凌番茄褪绿病毒的分子检测[J].植物保护,2018,46(2):81-88.
[23] 刘燕,尚春明,高振江,等.番茄新品种黄化曲叶病毒病抗性基因Ty1、Ty3的分子标记[J].北方农业学报,2018,46(1):33-35.
[24] 赵黎明,李刚,刘永杰,等.侵染番茄的番茄褪绿病毒山东泰安分离物的分子鉴定和序列分析[J].植物保护,2014,40(5):34-39.
[25] 吴淑华,李廷芳,赵文浩,等.江苏省番茄黄化曲叶病毒和褪绿病毒复合侵染的分子检测[J].园艺学报,2016,43(1):89-99.
[26] 刘微,史晓斌,唐鑫,等.云南番茄褪绿病毒和番茄黄化曲叶病毒复合侵染的分子鉴定[J].园艺学报,2018,45(3):552-560.
[27] FAUQUET C M,BRIDDON R W,BROWN J K,et al.Geminivirus strain demarcation and nomenclature[J].Archives of Virology,2008,153(4):783-821.
[28] TORRE C,DONAIRE L,GOMEZAIX C,et al.Characterization of begomoviruses sampled during severe epidemics in tomato cultivars carrying the Ty-1 gene[J].International Journal of Molecular Sciences,2018,19(9):2614.
[29] PICO B,DIEZ M J,NUEZ F.Viral diseases causing the greatest economic losses to the tomato crop II.The Tomato yellow leaf curl virus -a review[J].Scientia Horticulturae,1996,67(3/4):151-196.

