多级结构MoS2/C复合材料的储锂性能
杨子川项佳楠王霞霞田建华单忠强
(天津大学化工学院,天津 300072)
锂离子电池的传统负极材料是石墨,其具有资源丰富、电导率高及体积变化小等优点,但是它的理论比容量仅为372 mA·h·g-1。近几年的研究热点硅负极材料具有3 580 mA·h·g-1高比容量,而且电压平台低、资源丰富且环境友好,但是本征电导率低、嵌/脱锂过程中体积变化大(~300%)以及首圈库伦效率低等问题限制了其实际应用。MoS2理论比容量约为670 mA·h·g-1,体积膨胀率较低(~103%),而且和碳材具有很好的协同效应,近年来得到许多关注[1-3]。
MoS2本身具有片层结构,存在着不可忽略的体积膨胀。因此,研究人员采用很多方法来改进MoS2的电化学性能。首先是材料的制备方法,采用物理和化学剥离合成MoS2的方法制备规模小且重复性差,化学气相沉积成本又过高[4-6],所以通过湿法化学合成MoS2复合材料,成为改善电极材料性能的重要手段[7-8]。Jiang等[9]利用蔗糖通过水热法,合成了MoS2/C复合材料,调控MoS2/C复合材料的形貌。在200 mA·g-1电流密度下循环150次后,可逆比容量为705 mA·h·g-1。Xu等[10]通过在反应体系中加入氨基葡萄糖,调控MoS2在石墨烯片层上的生长,制备了MoS2/C复合材料,在100 mA·h·g-1的电流密度下循环100次后容量为896 mA·h·g-1。Cai等[11]利用MoO3制备Mo-MOFs,并在反应体系中加入葡萄糖作为碳源,制备了MoS2/C复合材料。在100 mA·h·g-1的电流密度下循环100次后容量约为500 mA·h·g-1。
本研究通过一步水热法将葡萄糖与MoS2复合制备MoS2/C复合材料,方法简单易操作,通过对溶剂组成和碳含量的调控,得到具有多级花状片层结构的MoS2/C复合材料,为锂离子和电子传输提供了更丰富的通道,材料的电化学性能明显改善。
1 实验部分
1.1 材料与试剂
钼酸钠,天津市科密欧化学试剂有限公司;硫脲,天津市元立化工有限公司;葡萄糖,天津市大茂化学试剂厂;导电炭黑 Super P,瑞士Timcal公司;聚偏氟乙烯,阿科玛化工有限公司。
1.2 MoS2/C复合材料的制备
以葡萄糖为碳源,采用乙醇/水复合溶剂热法合成MoS2/C复合材料。首先,按照物质的量之比为1.00∶4.25分别称取0.15 g钼酸钠和0.2 g硫脲,并将它们依次溶解在30 mL的乙醇/水复合溶剂体系中,搅拌均匀后,称取一定质量的葡萄糖加入上述混合溶液中并持续磁力搅拌30 min,然后将上述混合溶液转移至100 mL聚四氟乙烯制成的高压水热反应釜内,密封并置于电热恒温鼓风干燥箱中200 ℃下反应24 h。待水热釜自然冷却至室温后,通过减压抽滤获得黑色粉末状反应产物,并分别用蒸馏水和无水乙醇洗涤产物3次,之后将产物置于55 ℃电热鼓风干燥箱中干燥过夜。最后,将产物研磨并转移至Ar气氛管式炉内以3 ℃ min-1的升温速率升温至700 ℃下热处理3 h,以形成具有多级绣球花状结构的MoS2/C复合材料。
1.3 材料的物化性能表征
采用德国Bruker公司的D8 Focus X射线衍射仪进行材料物相分析,铜靶Kα,工作电压40 kV,电流200 mA,扫描范围10°~80°,扫速8(°)·min-1。采用日本Hitachi公司的S4800场发射扫描电子显微镜进行材料微观形貌观察。采用日本JEM 2100F场发射透射电子显微镜进行材料的微观结构分析。采用德国TG209热重分析仪对材料进行C含量的分析。采用美国热电公司的DXR Microscope来表征MoS2及其复合材料的特征Raman光谱,激发波长为λ=532 nm,拉曼位移的测试范围为250~3 000 cm-1。
1.4 电极的制备和电化学性能表征
电极的制备:复合材料、导电剂SuperP和黏结剂聚偏氟乙烯(PVDF)按照质量比8∶1∶1分别加入到研钵中,以N-甲基吡咯烷酮(NMP)为溶剂研磨合膏。然后均匀涂覆在预处理后的铜箔上,经110 ℃下真空干燥12 h,将极片在9 MPa下压实,再冲成Φ14 mm的电极圆片备用。实验中由于复合材料所含碳质量不同,经称量计算后,得出电极极片单位面积活性物质的质量为0.85~0.99 mg·cm-2。
电池的制作:以金属锂片(质量分数99.9%,天津中能锂业)为负极,多孔聚丙烯膜(美国Celgard公司)为隔膜,电解液为浓度1 mol·L-1的LiPF6的碳酸乙烯酯(EC)-碳酸二甲酯(DMC)混合溶液[V(EC)∶V(DEC)=1∶1],在Ar气氛的手套箱中组装成CR2032型扣式电池,静置12 h后进行电化学性能测试。
采用武汉蓝电CT2001A型测试仪对电池进行恒流充放电循环以及倍率性能测试;采用上海辰华CHI660E型电化学工作站测量电池的循环伏安曲线,扫描速度是0.2 mV·s-1,扫描范围是0.01~1.50 V(vs.Li+/Li)。采用德国ZahnerIM6电化学工作站测量电池的交流阻抗并进行数据拟合,测量频率在1.0×10-2~1.0×105Hz范围内,振幅为5 mV。
2 结果与讨论
2.1 溶剂组成对MoS2/C复合材料性能的影响
溶剂组成会影响反应物和中间体的分散性和溶解度,从而影响具有各向异性的MoS2晶体的晶粒形成和生长速度。本研究首先研究不同体积比的乙醇/水溶剂对复合材料物化性能和形貌结构的影响。
图1是在不同体积比的乙醇/水反应体系下制备的MoS2/C复合材料的SEM图。如图1a)所示,当溶液总体积为30 mL,V(乙醇)∶V(水)为1∶5时,MoS2/C复合材料为松散的无规则银耳状球,其尺寸约为100~200 nm,且分布不均匀。当V(乙醇)∶V(水)为1∶2时[见图1b)],MoS2/C复合材料呈现出均匀的多级绣球花状形貌,尺寸约为300~350 nm。当V(乙醇)∶V(水)为1∶1时[见图1c)],MoS2/C复合材料的尺寸与V(乙醇)∶V(水)为1∶2时相比变化不明显,但尺寸分布变得不均匀,并且出现团聚现象,这不利于锂离子在电极材料中的传输。结果可见,在溶剂中加入一定量的乙醇能够调节优化MoS2/C的微观结构。

图1 不同溶剂组成制备的MoS2/C的SEM图Fig.1 SEM images of MoS2/C composites with different solvent compositions
图2a)是在不同V(乙醇)∶V(水)反应体系下所制备的MoS2/C复合材料的充放电循环曲线。电流密度为200 mA·h·g-1,循环次数为100次。当V(乙醇)∶V(水)为1∶5时,MoS2/C电极的首圈充电比容量为1 099.4 mA·h·g-1,循环100次后比容量下降为633.7 mA·h·g-1,容量保持率为57.6%。当V(乙醇)∶V(水)为1∶1时,充放电循环100次后比容量降低为626.3 mA·h·g-1,这是因为当溶剂中乙醇量过多时MoS2/C纳米粒子堆积密度过大。当V(乙醇)∶V(水)为1∶2时,首次库伦效率为72.6%,第2次和第3次库仑效率分别为95.2%和96.8%,循环100次后库伦效率为99.2%。首次库伦效率低可能是由于MoS2/C表面SEI膜的形成和无定形碳中残余的含氧官能团造成了不可逆的储锂位点[12-14];首次充电比容量为1 236.9 mA·h·g-1,循环100次后比容量保持为762.7 mA·h·g-1,性能最好,说明适当提高乙醇比例可使MoS2/C复合材料的比容量提高。
图2b)是在不同V(乙醇)∶V(水)的反应体系下制备的MoS2/C复合材料的倍率性能曲线。由图2b)可知,当V(乙醇)∶V(水)为1∶2时,电极材料的倍率性能在3者中最好,该电极材料在0.1、0.2、0.5、1.0和2.0 A·g-1的电流密度下的平均可逆比容量为857.05、731.20、661.90、490.10和821.10 mA·h·g-1;当电流密度再次回到0.2 A·g-1时,电极材料的比容量回到815 mA·h·g-1,约占初始容量的95%。这可能是由于MoS2/C电极材料的片层间距和片层厚度适中,孔结构丰富且较为稳定,为锂离子传输提供稳定的通道,因而具有良好的倍率性能。

图2 不同溶剂组成MoS2/C电极的充放电性能a)和b)倍率性能Fig.2 Cycling performance a) and rate performance b) of MoS2/C electrodes with different solvent compositions at 0.2 A·g-1
2.2 碳含量对复合材料的结构和性能的影响
MoS2/C复合材料中的碳含量受到溶剂中钼酸钠和葡萄糖质量比例的影响。制备MoS2/C-1、MoS2/C-2和MoS2/C-3的初始溶剂中葡萄糖含量分别为0.008、0.016和0.024 g·mL-1。当钼酸钠质量不变时,葡萄糖的量越高,复合材料中碳含量越高。图3是MoS2和不同碳含量的MoS2/C复合材料在空气气氛下的TGA曲线,通过TGA曲线可以得到MoS2/C复合材料中碳的相对含量[15]。计算可得MoS2/C复合材料中碳的质量分数分别为14%、50%和56%,对应的3个样品依次标记为MoS2/C-1、MoS2/C-2和MoS2/C-3。
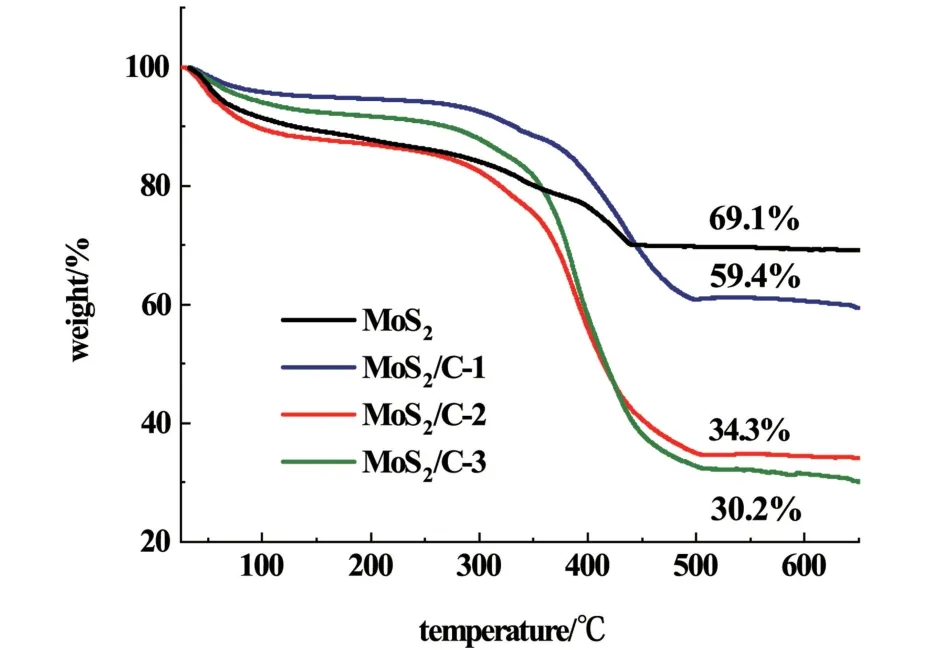
图3 MoS2和不同碳质量分数的MoS2/C在空气中的TGA曲线Fig.3 TGA curves of MoS2 and MoS2/C composite with different carbon contents
图4是MoS2和不同碳含量的MoS2/C复合材料的XRD图。MoS2的特征峰与2H-MoS2的物相匹配良好。位于33.2°,39.6°,58.9°附近的衍射峰分别归属于2H-MoS2的(100)、(103)和(110)晶面。与MoS2相比,MoS2/C复合材料位于14.1°的(002)特征峰消失,并且在8.6°和17.2°处出现2个新的弱特征峰,根据Bragg方程计算相应的层间距分别为1.01和0.52 nm,它们分别归属于碳层插入MoS2层内形成的层间距离和相邻的MoS2层与碳层之间的距离。这是由于蔗糖衍生的碳层插入到MoS2层内导致的[16-17]。
图5是不同碳含量MoS2/C复合材料的SEM图。如图5a)所示,纯MoS2是由较大较厚的纳米片组装成的微球,其尺寸超过1 μm。在反应体系内加入葡萄糖碳源时,微球的尺寸变小。当碳含量质量分数较少(14%)时,如图5b)所示,MoS2/C-1尺寸约为350~400 nm,复合材料表面出现明显的团聚现象。当碳质量分数增大(50%)时,如图5c)所示,MoS2/C-2的尺寸减小为300~350 nm,并且团聚现象得到明显的缓解。进一步增加碳质量分数(56%),如图5c)所示MoS2呈微球状,尺寸进一步减小,尺寸约为200~250 nm,但纳米片堆积过于密实,且有团聚现象,不利于Li+的传输和扩散。

图5 不同碳含量MoS2/C复合材料SEM图Fig.5 SEM images of MoS2/C composite with different carbon contents
如图6a)所示,纯MoS2样品是由多层MoS2紧密堆叠形成的厚片,层间距为0.63 nm。加入适量的葡萄糖后所制备的MoS2/C-2没有明显的片层堆叠现象,片层呈分散状分布,由于葡萄糖衍生的碳层插入,MoS2片层间距增大至1.01 nm,这与图4 XRD的测量结果一致。结果说明,葡萄糖的引入成功地抑制了MoS2纳米片的堆叠,扩大了层间距,有利于Li+的传输和扩散。
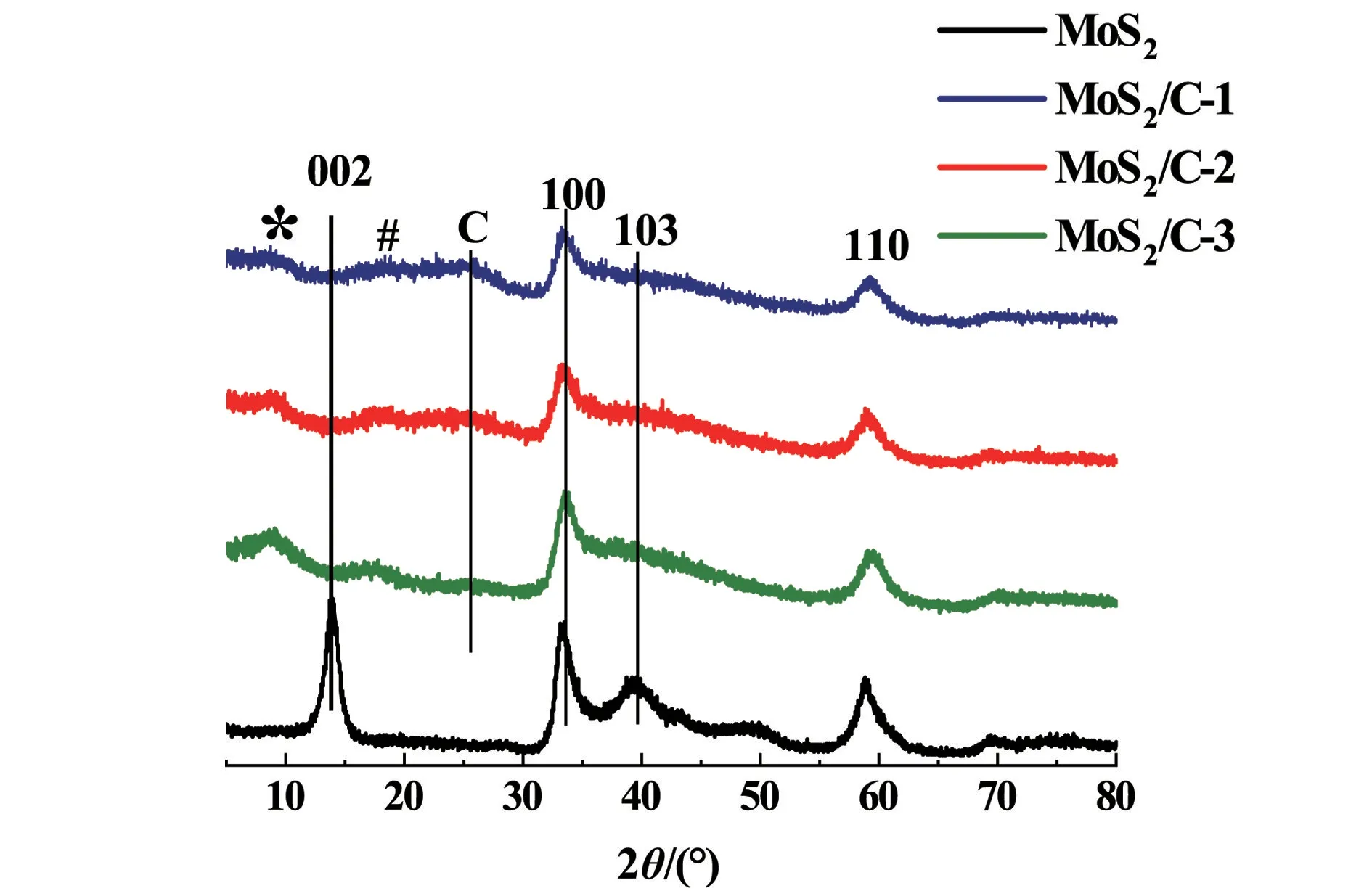
图4 MoS2和不同碳含量的MoS2/C复合材料的XRD图Fig.4 XRD of MoS2 and MoS2/C composite with different carbon contents
图7为MoS2/C-2和MoS2的Raman光谱图。如图所示MoS2位于374和400 cm-1的双峰分别代表层状MoS2结构的面内振动模和面外振动模A1g。MoS2/C-2中移动至378 cm-1,A1g移动至402 cm-1。和A1g的峰间距△k会随着MoS2堆叠层数的增加而增加。此外,在MoS2/C-2复合材料中出现在1 350和1 580 cm-1处的2个峰分别代表碳的D-带和G-带。在Raman光谱中,D-带与sp3-杂化碳的缺陷和无序程度有关,而G-带代表有序sp2-杂化碳的振动。通常,峰强度之比ID/IG表示碳材料中的缺陷程度,根据图6计算值为1.14,较高的ID/IG表明复合材料具有更多的活性缺陷位点可用于可逆地储锂,从而提高其电化学性能[18]。
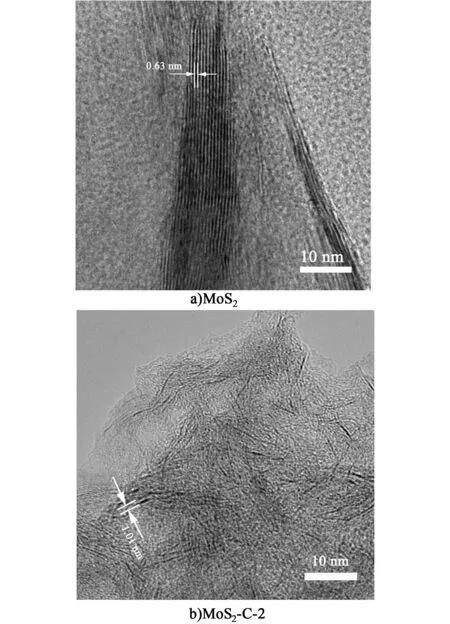
图6 MoS2和MoS2/C-2复合材料的TEM图Fig.6 TEM images of MoS2 and MoS2/C-2 composites
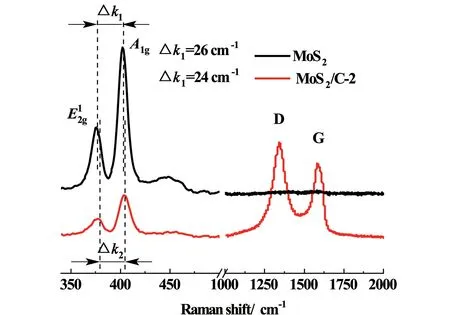
图7 MoS2和MoS2/C-2复合材料的拉曼光谱图Fig.7 Raman spectrum of MoS2 and MoS2/C-2 composites
图8a)为MoS2/C复合电极的循环伏安(CV)图。从图8a)中可以看到,首圈负向电位扫描在 0.6 V附近出现1个还原峰,对应LixMoS2与Li+转化反应生成Mo和Li2S的过程[19],在第2次循环后此峰消失,说明该过程不可逆;正向扫描过程中,在2.2 V附近出现的强氧化峰对应的是Li2S脱锂反应,1.4 V左右的弱氧化峰对应于Mo的不完全氧化反应[20]。第2次循环起,首圈负向扫描出现的还原峰消失,而在1.2和1.8 V附近出现2个新的还原峰,分别对应S向LiS2转化和MoS2向LixMoS2转化的反应。在第5次循环时,CV曲线上各峰的性质不再发生明显变化,说明电极电化学性能趋于稳定。
图8b)为MoS2/C-2复合材料在200 mA·h·g-1电流密度下的充放电性能曲线。从图8b)中首次充放电曲线可以观察到位于0.6 V的放电平台,这对应着Li+与MoS2反应生成Mo和Li2S的过程。在后续充放电过程中,位于2.2 V左右的充电电压平台对应于Li2S转换为S的过程;放电电压平台不太明显,这是由于MoS2/C复合材料低的结晶度以及分散相无定型碳的无序性导致的[16]
图8c)是不同C含量的MoS2/C复合材料在电流密度为200 mA·h·g-1下循环100次的充放电循环性能曲线。从图8c)中可以看出,纯MoS2电极在循环40次时容量已开始衰减,在充放电循环100次后由924.8 mA·h·g-1衰减至86.0 mA·h·g-1,容量保持率仅为9.2%。而C含量为50 wt% 的MoS2/C-2电极首圈充电比容量为1 236.9 mA·h·g-1,循环100次后比容量保持为762.7 mA·h·g-1,容量保持率为61.6%,这归因于MoS2与碳具有良好的协同作用。
图8d)为不同C含量的MoS2/C复合材料在电流密度为0.1、0.2、0.5、1.0和2.0 A·g-1电流密度下的倍率性能曲线。从图8d)中可看出,相比纯MoS2电极,MoS2/C-2复合电极在各种电流密度下具有更好的比容量和循环稳定性。
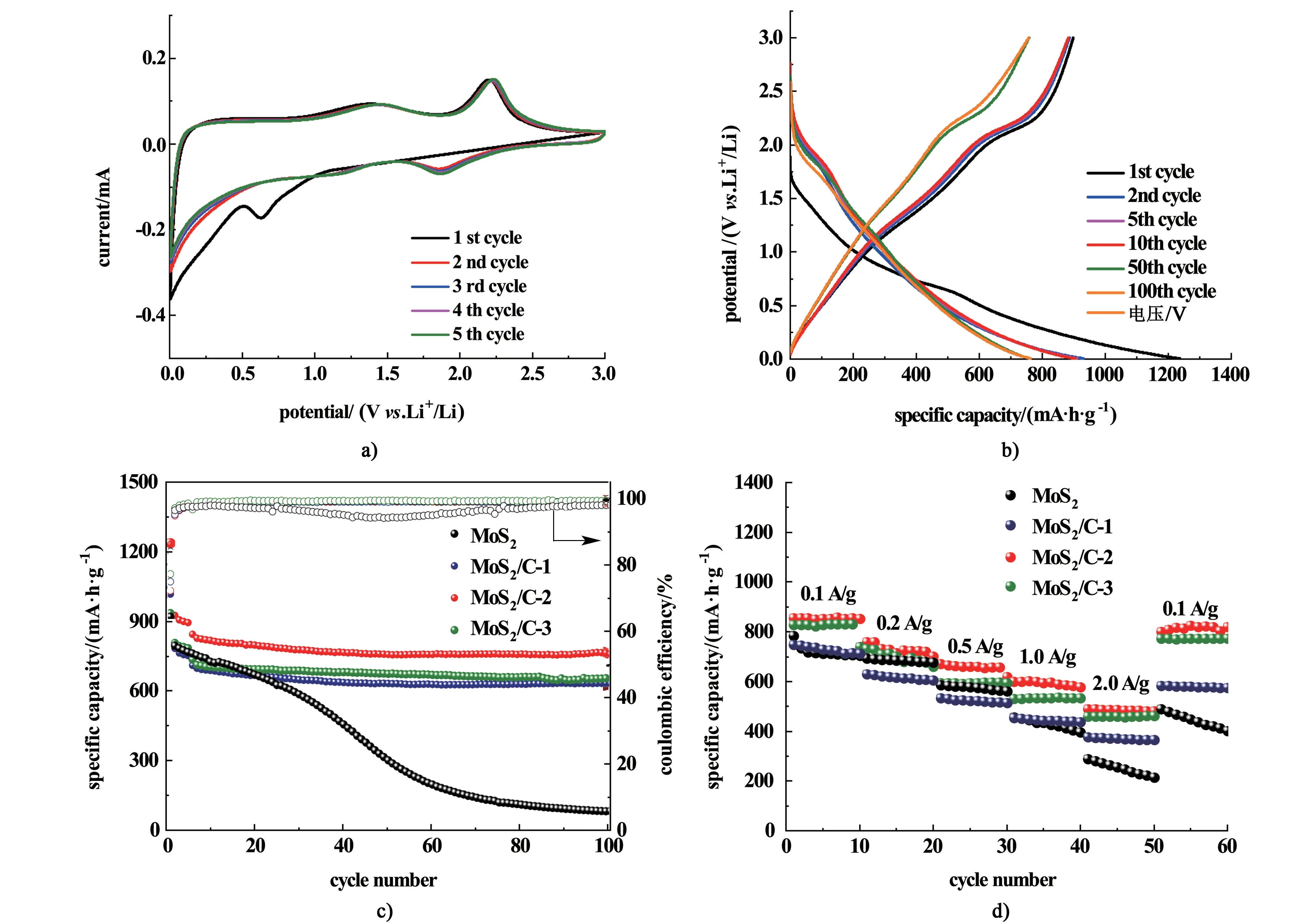
图8 MoS2/C复合电极的a) CV曲线;b) 充放电曲线;c)充放电循环性能和d)倍率性能Fig.8 Voltage profiles of MoS2/C electrode at 0.2 A·g-1 a); cyclic voltammetry profiles b); cycling performance at 0.2 A·g-1 c) and rate performance of different MoS2/C composite electrodes d)
图9为不同碳含量的MoS2/C复合材料的交流阻抗图谱,该电极是在200 mA·g-1的电流密度下充放电循环100次后进行测量的,频率范围为1.0×105~1.0×10-1Hz。图9中位于高频区域的半圆对应于在电极/电解质界面处产生的电荷转移阻抗(Rct)和恒相元(CPE),位于低频区域的斜线代表与Li+向电极材料内部扩散有关的Warburg阻抗(Zw)[21]。主要的动力学参数Re和Rct可以通过插图中的等效电路拟合获得。拟合结果(表1)表明,电极的Re差别不大而MoS2/C的Rct值显著减小,MoS2/C-2的Rct值最小,说明电极对电子和Li+的传输能力提高[22]。
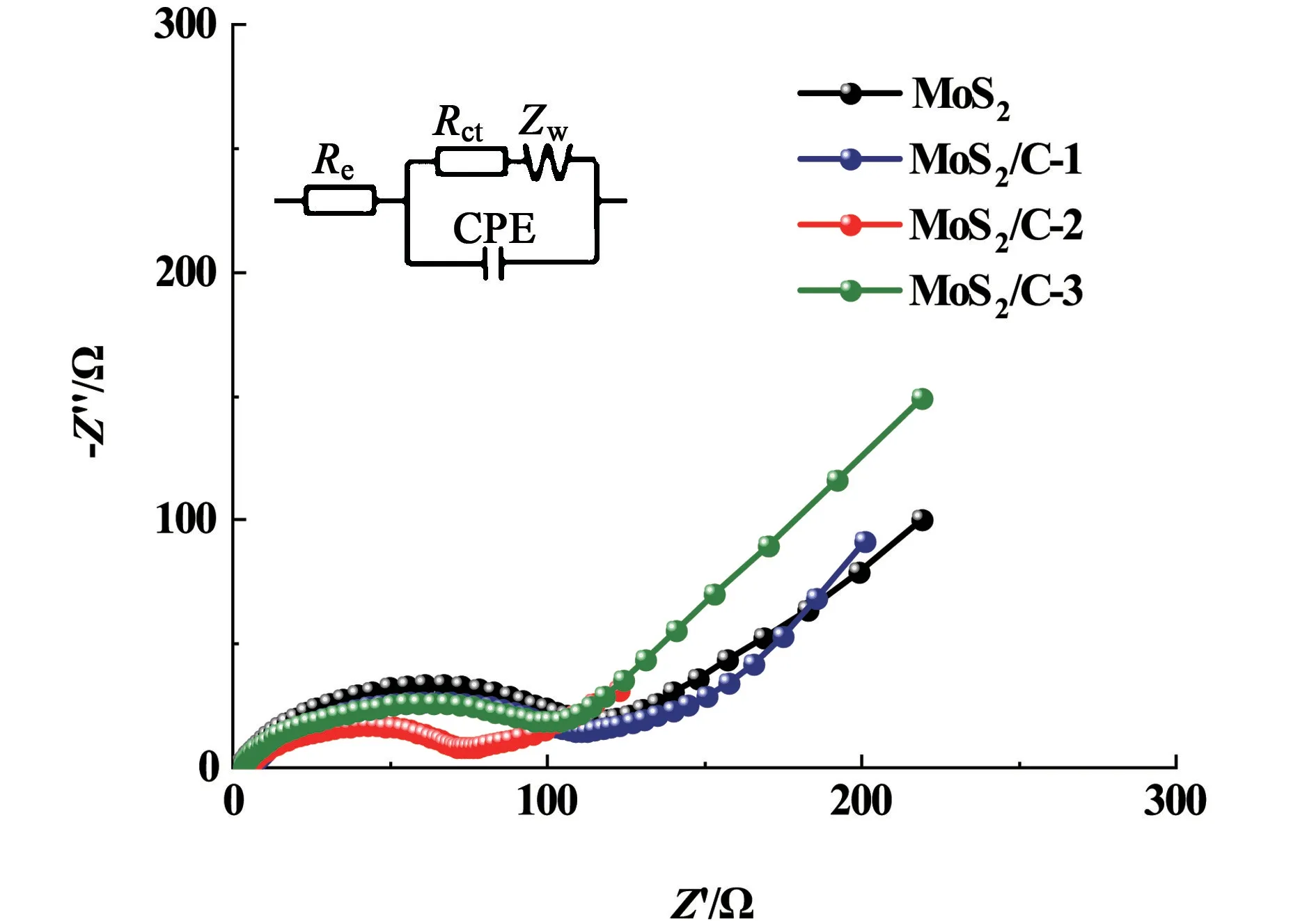
图9 MoS2和不同碳含量的MoS2/C电极的交流阻抗图谱(内插图为等效电路图)Fig.9 Nyquist plots of MoS2 and MoS2/C electrodes with different carbon contents (the inset is the equivalent circuit)

表1 MoS2及不同碳含量的3种MoS2/C电极EIS图谱的Re和Rct拟合值Table 1 Re and Rct fitting values of EIS patterns of MoS2 and three MoS2/C electrodes with different carbon contents
3 结论
采用乙醇/水复合溶剂热法合成了MoS2/C复合材料,复合溶剂中乙醇的适量添加对MoS2/C的多级结构的形成起着关键性作用。当V(乙醇)∶V(水)为1∶2、碳质量分数为50%时,MoS2/C复合材料呈现出尺寸均匀的多级花状微球结构,增大了层间距,丰富了材料的电子和离子传输通道。在200 mA·g-1的电流密度下,复合电极充放电循环100次后可逆容量达到762 mA·h·g-1,具有较好的比容量和稳定性。

