铁基普鲁士蓝正极材料的宏量制备及电化学储钠性能
孙 瑜 孙云坡 刘春丽 谢 健*, 赵新兵裘吕超 梅 简 徐雄文 涂 健
(1浙江大学材料科学与工程学院,杭州 310027)
(2国网浙江省电力有限公司电力科学研究院,杭州 310014)
(3湖南立方新能源科技有限责任公司,株洲 412000)
0 引 言
随着科技的进步和社会的发展,能源已经成为现代社会的关键因素。煤、石油等化石能源的过度消耗使得能源短缺和环境污染等问题日益严重,而太阳能、风能、潮汐能等清洁能源也存在间歇性以及受自然条件和地域条件制约等问题。因此,开发高效的储能技术成为清洁能量发展的关键因素。近年来,锂离子电池凭借其优开的电化学性能,在各领域得到了广泛应用[1-3]。但是,由于锂资源稀缺且地域分布不均,导致锂离子电池成本高昂,不利于其在大规模储能领域的广泛应用。而与锂元素具有相似物化性质的钠元素在地壳中储量丰富、分布广泛、价格低廉,因此开发钠离子电池对大规模储能具有重要的意义[4-8]。
由于钠离子半径比锂离子大,钠离子在晶格中的扩散较为困难,嵌入时更易引起材料体积的变化,因此在锂电池体系中具有优开性能的正极材料的类似体应用于钠离子电池时,往往呈现低劣的电化学性能,如工作电压低、循环寿命差等。因此,开发适合钠离子电池的正极材料成为研究的重点和难点[9]。常见的钠离子电池正极材料主要包括层状氧化物、聚阴离子化合物、普鲁士蓝类似体等[10-16]。其中,普鲁士蓝类化合物由于相对低廉的原料成本、简单易行的制备方法、开放的三维框架结构及优开的电化学性能,引起了研究者的关注[17-21]。因此,普鲁士蓝类材料被认为是钠离子电池最理想的正极材料之一。
一般来说,普鲁士蓝类化合物是在水溶液中、室温下通过共沉淀方法制备。因此,晶体结构中往往含有较多的缺陷、间隙水和结晶水。这导致材料中钠的实际含量较低,从而降低可得容量,且众多的晶体缺陷也导致循环寿命较差。研究表明,通过引入配位剂、提高反应温度等手段可提高晶体的完整性,从而提高容量和循环性能[22-24]。但是,以往的普鲁士蓝材料合成往往基于低前驱体浓度、低滴速、小体积反应装置,且材料的电化学性能评价一般基于纽扣型半电池,其合成工艺和性能评价很难应用于实际生产中。
在本工作中,使用高浓度的前驱体溶液,以20 L的反应釜为反应装置,模拟实际生产的反应条件,探索了铁基普鲁士蓝材料(FePB)的宏量制备。通过在反应前驱体中加入适量的柠檬酸钠作为配位剂,减缓了共沉淀反应速率,减少了晶体中的缺陷,所得FePB具有较高的容量、优开的倍率性能和良好的循环稳定性。以商业硬碳为负极,制作了软包钠离子全电池,所得电池具有较长的循环寿命。该工作可为规模化制备普鲁士蓝材料提供指导意义。
1 实验部分
1.1 主要试剂
硫酸钠(Na2SO4,99.5%,国药集团化学试剂有限公司),十水合亚铁氰化钠(Na4[Fe(CN)6]·10H2O,99%,国药集团化学试剂有限公司),七水合硫酸亚铁(FeSO4·7H2O,99%,Aladdin),无水乙醇(99.7%,国药集团化学试剂有限公司),聚偏氟乙烯(PVDF,Mr=1 000 000,上海东氟化工科技有限公司),科琴黑(工业级,广州新稀冶金化工有限公司),N-甲基吡咯烷酮(NMP,99.5%,Aladdin),玻璃纤维隔膜(GF/D,Whatman),金属钠(99%,国药集团化学试剂有限公司),电解液为1 mol·L-1的 NaPF6的碳酸丙烯酯(PC)和碳酸甲乙酯(EMC)溶液(体积比1∶1),并含有体积分数为5%的氟代碳酸乙烯酯(FEC),电解液购自苏州佛赛,纯度为电池级。
1.2 材料制备
使用图1a所示的20 L容量的反应釜作为合成装置,室温下在水溶液中采用共沉淀法宏量制备FePB材料。首先,按照化学计量比称取1.5 mol十水合亚铁氰化钠,溶于去离子水中配制3 L亚铁氰化钠溶液(0.5 mol·L-1),记为溶液A;再称取1.65 mol七水合硫酸亚铁和6 mol柠檬酸钠,配制13 L水溶液,记为溶液B;然后,称取3 mol硫酸钠,配制3 L水溶液,记为溶液C。反应时,先将溶液C转移至20 L反应釜中,通入氮气,并搅拌(转速为400 r·min-1);再将4 L的B溶液加入到反应釜中;接着使用蠕动泵,分别将剩余的B溶液按9 mL·min-1和A溶液按3 mL·min-1的速度同时滴入反应釜中,直至滴完;反应完成后,在氮气气氛和搅拌下陈化2 h,最后进行洗涤和离心分离。将分离所得产物置于烘箱中先110℃下常压干燥12 h,再真空干燥12 h,得到蓝色粉末样品。
1.3 材料表征
采用X射线粉末衍射(XRD)对合成产物进行物相分析,使用仪器为日本理学电机Rigaku D/Max-2550pc粉末衍射仪,测试时以CuKα为辐射源,波长λ=0.154 06 nm,管压40 kV,管流250 mA,扫描步长0.02°,扫描范围2θ=10°~60°。采用扫描电子显微镜(SEM)对产物进行形貌观察,所用仪器为日立Hitachi S-4800扫描电子显微镜,加速电压为5 kV,测试前对样品进行1 min喷金处理。采用透射电镜(TEM)和高角度环形暗场-扫描透射电镜(HAADFSTEM)对样品进行微结构分析,所用仪器为FEI Titan G2 80-200 ChemiSTEM,加速电压为200 kV,同时采用X射线能量色散谱仪(EDS,Phoenix)对样品进行元素面扫分析。采用热重(TG)分析测定样品中的水含量,所用仪器型为德国Netzsch LFA467,测试时,在氮气气氛下,将样品从室温以10℃·min-1的升温速率升温至500℃,再冷却至室温。采用电感耦合等离子体-原子发射光谱(ICP-AES)测定试样中Na、Fe元素的含量,使用仪器型号为IRIS IntrepidⅡXSP。采用元素分析仪测定样品中的C、N元素的含量,使用仪器型号为Flash EA 1110。
1.4 电化学性能测试
按照质量比7∶2∶1分别称取FePB、导电剂科琴黑、黏结剂PVDF,在研钵中混合均匀后,转移至称量瓶,注入NMP,经磁力搅拌得到均匀的浆料。使用小型涂布机将浆料均匀涂覆于铝箔上,再在110℃下真空干燥24 h,并经10 MPa压力压片后,得到FePB电极。在氩气氛的手套箱中进行CR2025型纽扣半电池的装配,以FePB电极为工作电极,金属钠片为对电极,玻璃纤维膜为隔膜,1 mol·L-1NaPF6PC/EMC+5%FEC溶液为电解液。将装配好的纽扣电池在室温下静置12 h后,采用新威电池测试仪进行恒电流充放电测试。使用电化学工作站(上海辰华)对电池进行循环伏安(CV)和交流阻抗(EIS)测试。CV测试电压范围为2.0~4.2 V,扫描速率为0.1 mV·s-1;EIS测试频率范围为10-2~105Hz,振幅为10 mV。以上电化学测试均在室温下进行。软包全电池的制作和测试详见正文。
2 结果与讨论
2.1 材料的制备、物相和组成分析
图1a是FePB的合成装置图,反应釜为玻璃材质。反应前,反应釜中底液为硫酸钠溶液和部分硫酸亚铁溶液。反应开始时,使用2台蠕动泵将高浓度的亚铁氰化钠(0.5 mol·L-1)和硫酸亚铁溶液同时注入反应釜中,进行共沉淀反应,合成温度为室温,反应过程中悬浮液颜色为白中泛绿。图1b是所得产物的外观图,产物呈现蓝色,与反应过程中悬浮液的颜色不同,这是由于在贫钠环境下,离心洗涤时FePB发生表面失钠所致[25]。按本实验条件,一次反应所得产物重量大于500 g。图1c是宏量制备产物的XRD图,从图中可知,FePB样品呈现立方相结构,空间群为Fmm,具有良好的结晶性,与文献报道相吻合[26]。为分析FePB的结晶水含量,进行了TG分析(图1d)。TG曲线显示,所得样品的结晶水质量分数为14.1%。结合TG、ICP-AES和C、N元素分析可知,所得FePB的结构式为Na1.30Fe[Fe(CN)6]0.98·2.7H2O。由此可见,产物具有相对较高的钠含量。
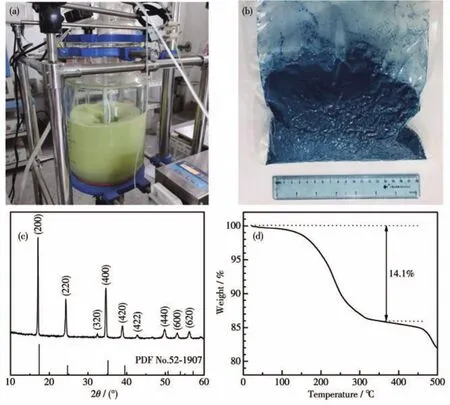
图1 宏量制备的FePB样品的(a)合成装置、(b)外观、(c)XRD图和(d)TG曲线Fig.1 (a)Synthesis device,(b)appearance,(c)XRD pattern and(d)TG curve of the FePB sample prepared by a scalable route
2.2 材料的形貌与微观结构
图2a是FePB样品的低倍SEM照片,由图可知,样品呈现近似立方结构,颗粒尺寸为微米级,粒度分布较为均匀,形状总体比较规整,但仍有少数无规则颗粒。图2b是FePB样品的高倍SEM照片,从图可知,颗粒尺寸为2~3 μm,颗粒表面整体较为光滑。此外,FePB颗粒呈现明显的多层边界,这与柠檬酸钠配位二价铁离子,使得二价铁离子与亚铁氰根离子的沉淀反应速度减慢有关。多个颗粒在同一个晶核上相互嵌套、穿插生长,有利于大颗粒产物的形成,大颗粒产物抗电解液腐蚀能力较强,具有更优良的循环稳定性,且极片的涂布性能较好。另外,大颗粒有利于固液分离,且电池组装时消耗较少的电解液。图2c是FePB样品的粒度分布曲线,其D50值为2.330 μm(D50是指一个样品的累计粒度分布百分数达到50%时所对应的粒径),所有颗粒的尺寸均大于1 μm,小于10 μm,尺寸分布比较均匀,与SEM结果相吻合。在本工作中通过使用合适的柠檬酸钠量及控制加料工艺,在较高浓度下,仍得到了颗粒较大的产物。图3为FePB样品的TEM和HAADF-STEM照片,以及Na、Fe、C和N元素的EDS面扫图。由图可知,FePB中的各元素在颗粒中均匀分布,这表明所得普鲁士蓝材料具有良好的均匀性。比较图3c和图3d发现,Na元素的分布面积要少于Fe元素,这是由于FePB颗粒表面失Na有关[25],与产物颜色和元素分析相符。
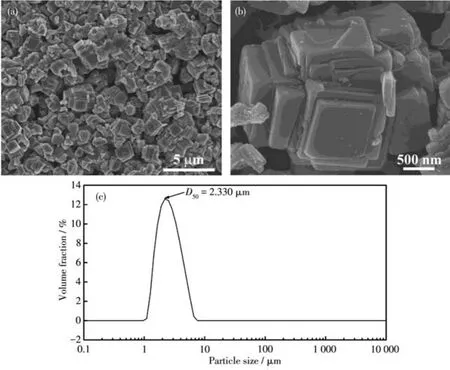
图2 FePB样品的(a)低倍SEM照片、(b)高倍SEM照片和(c)粒度分布曲线Fig.2 SEM images at(a)low and(b)high magnification and(c)size distribution curve of the FePB sample

图3 FePB样品的(a)TEM照片、(b)HAADF-STEM照片和(c~f)EDS面扫Fig.3 (a)TEM image,(b)HAADF-STEM images and(c~f)EDS mappings of the FePB sample
2.3 材料的电化学性能
图4a为FePB样品在0.1C(1C=150 mA·g-1)电流密度下的前3次充放电曲线,从图中可知,宏量合成的FePB样品首次充电比容量为92 mAh·g-1,首次放电比容量为117 mAh·g-1。材料合成因在富钠环境及惰性气氛下进行,产物的钠含量较高,但离心分离因在贫钠和开放气氛下进行,导致Fe2+被氧化成Fe3+,并伴随FePB颗粒表面的钠损失。在首次放电时,样品起始态中的Fe3+也被还原为Fe2+,因此,出现首次放电容量高于充电容量的现象。在实际钠离子电池制作时,可对硬碳负极进行预钠化,来补偿首次低库仑效率。经过首次循环后,放电容量与充电容量基本一致,表现出较高的库仑效率。图4b为FePB样品的CV曲线图,图中3.05/2.82 V和3.43/3.31 V处出现2对氧化/还原峰,分别对应与N结合的高自旋态的Fe2+/Fe3+和与C结合的低自旋态的Fe2+/Fe3+的氧化还原反应[17,27-28],这与图4a中的2个充放电平台相对应。
图4c和图4d分别为FePB样品在不同电流下的充放电曲线和容量,即倍率性能。由图可知,电池在0.1C、0.5C、1C、2C、5C和10C下的比容量分别为110、102、100、97、95和 92 mAh·g-1。随着电流密度的增加,比容量降低,放电电压平台逐渐下降,电池的极化增大,但充电电压随电流变化不大。值得注意的是,当电流密度增加时,比容量的下降并不明显,在10C大电流密度下比容量仍可保持在92 mAh·g-1,显示出该材料优开的倍率性能。这与普鲁士蓝类化合物独特的结构有关,其开放的三维框架结构中空隙尺寸较大,有利于钠离子的快速脱嵌,此外,特殊的多边界结构增加了材料表面积,有利于钠离子在电极/电解液界面处的快速迁移。图4e为FePB样品在1C电流密度下的循环性能,测试结果显示,该材料具有优开的循环稳定性,经过500次循环后,容量从初始的 98 mAh·g-1降至 87 mAh·g-1,容量保持率达到89%。普鲁士蓝类化合物的循环稳定性与缺陷含量和形貌有关,FePB优开的循环稳定性一方面得益于其较为完整的晶体结构,另一方面也得益于其较大的粒径,可一定程度上减缓被电解液腐蚀[17,29]。

图4 FePB样品(a)在0.1C电流下前3次充放电曲线、(b)在0.1 mV·s-1扫描速率下的CV曲线、(c)不同电流下的充放电曲线、(d)倍率性能和(e)1C电流下的循环性能Fig.4 (a)First three voltage profiles at 0.1C rate,(b)CV plots at 0.1 mV·s-1,(c)voltage profiles at various current rates,(d)rate capability and(e)cycling performance at 1C rate of the FePB sample
图5a~5c为使用FePB样品所制成的极片在循环前、循环50次后和循环100次后的SEM照片。由图可知,随着循环的进行,微米级的多层边界结构没有出现明显被电解液腐蚀的迹象,说明该材料具有较好的抗电解液腐蚀的能力,与上述的优开的循环稳定性相吻合。但是,随着循环次数的增加,电极中出现了形状不规则、尺寸较小的颗粒。如图5d所示,对比初始电极,循环后电极的XRD图在24°和39°(2θ)处出现了分峰现象,说明随着循环的进行,材料结构的对称性下降,部分材料由立方相转化为单斜相,可能与上述的小颗粒生成有关。图5e是FePB样品不同循环后的电化学阻抗谱,谱图采用插图中的等效电路进行拟合,拟合结果如表1所示。该谱图由高频区和中频区的2个部分重叠的半圆和低频区的斜线组成。等效电路中,Re代表欧姆电阻,对应谱图与实轴在高频区的交点,包含活性颗粒间的接触电阻、电解液电阻和集流体及活性颗粒的接触电阻等;Rf和Q1分别是固态电解质膜(SEI)电阻和相应的松弛电容,与阻抗谱中的高频半圆相对应;Rct和Q2分别代表电荷转移电阻和电解液与正极间的双电层电容,与阻抗谱中的中频半圆相对应;Zw是钠离子在电极内部的扩散电阻,与低频的斜线相对应[3,6]。表中Y代表恒相位元件的电容,n代表由表面缺陷或粗糙度引起的电流分布不均的指数,当n=1时,Q1(或Q2)为纯电容,当 0<n<1时,Q1(或Q2)为非理想电容[30]。分析拟合结果可知,随着循环次数的增加,Re和Rf变化并不明显,但均有所增加;Rct明显增加,从270.5 Ω增加到450.9 Ω,总阻抗呈现增加的趋势。说明随着循环的进行,FePB电极的电化学动力学性能有所减弱,这与电化学性能衰减相符合。
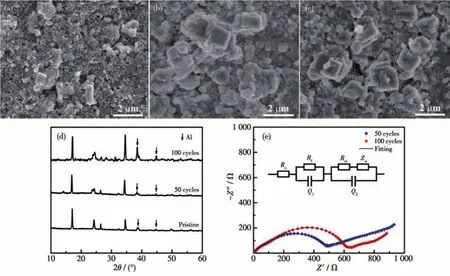
图5 FePB极片(a)循环前、(b)50次和(c)100次循环后的SEM照片;FePB极片(d)循环前后的XRD图和(e)不同循环次数后的EIS谱图Fig.5 SEM images of the FePB electrodes(a)before cycling,(b)after 50 cycles and(c)100 cycles;(d)XRD patterns of FePB electrodes before and after cycling,and(e)EIS spectra of FePB electrode after different cycles

表1 FePB样品EIS谱图的拟合结果Table 1 Fitting results of the EIS spectra of FePB sample
为了测试该FePB样品实际应用性能,将所得FePB正极和商业硬碳(HC,日本可乐丽公司)负极相匹配,组装了软包全电池(FePB/HC),并对FePB/HC电池的电化学性能进行了测试,使用同FePB/Na半电池相同的电解液。FePB正极由质量分数90%的活性物质、4%的PVDF黏结剂和6%的导电剂组成,电极经涂布、干燥(170℃真空烘干48 h)后得到如图6a所示的正极极片。负极极片由质量分数88%的HC、8%的黏结剂和4%的导电剂组成。正极单面活性材料负载为10 mg·cm-2,负极单面活性材料负载为3.3 mg·cm-2。经叠片、注液、封装,得到图6b所示的FePB/HC软包全电池。图6c为软包电池在10 mA的电流下的充放电曲线(经过化成后),其放电比容量为40 mAh,库仑效率接近100%。图6d为软包电池的循环性能,在50 mA的电流下,软包电池经过400次循环后仍然具有75%的容量保持率,表现出较为优开的循环稳定性。软包全电池的测试结果表明,所得普鲁士蓝材料显示出良好的实际应用前景,特别是在大规模储能领域。

图6 (a)FePB极片外观、(b)FePB/HC软包电池外观和FePB/HC软包电池的(c)充放电曲线与(d)循环性能Fig.6 (a)Appearance of the FePB electrode and(b)FePB/HC punch battery,and(c)charging/discharging curves and(d)cycling performance of the FePB/HC punch battery
3 结 论
采用水溶液共沉淀法在室温下宏量制备了铁基普鲁士蓝(FePB)材料。通过引入适量的柠檬酸钠作为配位剂,得到了钠含量较高且结晶较完整的FePB材料。所得FePB材料用作钠离子电池正极时,显示出较高的容量、优开的倍率性能和较长的循环寿命。0.1C放电时比容量能够达到117 mAh·g-1,在10C的大电流密度下比容量仍保持在92 mAh·g-1,在1C电流密度下循环500次,比容量仍保持在87 mAh·g-1,容量保持率达到89%。在纽扣型半电池组装和测试基础上,组装了FePB/HC软包全电池,该电池在50 mA的电流下,经过400次循环仍然具有75%的容量保持率。该材料优开的倍率性能和循环稳定性为钠离子电池在大规模储能中的应用提供了可能性;同时,该FePB合成工艺对于普鲁士蓝类材料的大规模生产具有重要的借鉴意义。
- 无机化学学报的其它文章
- Synthesis and Characterization of Palladium Nanoparticles with High Proportion of Exposed(111)Facet for Hydrogenation Performance
- Dielectric Phase Transition Induced by Halogen Substitution Based on 1,4-Diazabicyclo[2.2.2]octane-Derivatives
- 不同晶体生长活化能对SrZrO3∶Ce发光性能及微观组织影响
- 炭球修饰g-C3N4材料的制备及其可见光光催化性能
- Er3+掺杂 Li2O-SrO-ZnO-Bi2O3玻璃中 Er3+离子在1.53 μm处的荧光发射特性
- 3-((5-(3-吡啶基)-2-(1,3,4-噁二唑基))硫代)-2,4-戊二酮Cu(Ⅱ)/Zn(Ⅱ)/Mn(Ⅱ)配合物的合成及其晶体结构

