分散固相萃取-超高效液相色谱-三重四极杆串联质谱测定樱桃中的苯丁锡和三苯锡的方法研究
◎ 陈佩佩,陈琳珊,何雯倩,陈 茹
(1.广东省食品工业公共实验室,广东 广州 511442;2.广东省食品工业研究所有限公司,广东 广州 511442;3.广东省质量监督食品检验站,广东 广州 511442)
苯丁锡和三苯锡是一类感温型抑制神经组织的有机锡杀螨剂,化学结构见图1,其特点为高效、毒性低、效果持续时间长,对防治果树、茶树、柑橘、葡萄和樱桃等作物虫害有显著效果,因此,近年来在农作物中应用广泛,同时在木材防腐方面也有较大的作用[1-2]。目前,对于苯丁锡和三苯锡的相关毒理性研究尚不充分,有研究表明,苯丁锡和三苯基锡具有一定的毒性,对牡蛎和其他贝类的生长有一定的影响[3],而三苯基锡毒性比较大,低浓度就能引发生物体的内分泌紊乱[4]。因此,对消费者也产生了一定的潜在风险。美国、日本、欧盟等国家也制定了相关的限量标准。GB 2763—2019中明确规定,苯丁锡在柑橘中的限量为1 mg·kg-1,而在苹果、梨、葡萄等水果中,限量为5 mg·kg-1,樱桃、香蕉、草莓则是10 mg·kg-1,同时也增加了动物肉类的限量[5]。因此,建立高效快捷的测定方法具有重要的意义。
近年来,研究者对有机锡的测定方法进行了大量的研究。目前检测有机锡的方法主要有高效液相色谱-电感耦合等离子体质谱法[6-7]、气相色谱法[8]、气相色谱-串联质谱法[9-10]、高效液相色谱法[11-12]和高效液相色谱-串联质谱法[13]。高效液相色谱-电感耦合等离子体质谱法操作烦琐,所需试剂多,气相色谱及质谱法需对样品进行衍生,同样操作烦琐,且重复性差,液相色谱法则存在灵敏度低,目标物受杂质干扰严重等缺点。本文建立了分散固相萃取-超高效液相色谱-串联质谱法同时测定樱桃中的苯丁锡和三苯锡,前处理简单高效,且峰型好,灵敏度高,分析时间短,可进行日常实验室大批量的测定。

图1 苯丁锡和三苯锡的化学结构图
1 材料与方法
1.1 仪器与设备
API4000Q质谱仪(美国AB SCIEX公司);岛津LC-20AD液相色谱系统(日本岛津公司);Milli-Q Advantage A10超纯水系统(法国Merck Millipore公司);4k-15离心机(北京卓明贸易有限公司);IKA Vortex4涡旋混匀器(广州仪科实验室技术有限公司)。
1.2 试剂及耗材
樱桃样品购自广州市市场;苯丁锡和三苯锡(纯度≥98.5%,德国Dr.Ehrenstorfer公司);无水硫酸镁和氯化钠(分析纯,广州化学试剂厂);甲酸、乙腈(HPLC级,美国Thermo Fisher公司);C18、PSA、GCB、NH2粉和中性氧化铝(分析纯,上海安谱公司);实验用水为经Milli-Q净化系统过滤的超纯水(电阻率为18.2 MΩ·cm-1)。
1.3 样品前处理
樱桃样品均质后称取2 g样品于50 mL离心管中,加入5 mL 水和10 mL乙腈,涡旋混匀后加入4 g无水硫酸镁和1 g氯化钠粉末,涡旋提取10 min后,置于离心机中以10 000 r·min-1离心5 min-1,转移上清液1 mL至2 mL离心管中,加入30 mg C18粉末,涡旋2 min,10 000 r·min-1离心5 min,上清液过0.22 μm有机相滤膜上机。
1.4 标准溶液的配制
分别准确称取适量的苯丁锡和三苯锡标准品于10 mL容量瓶中,用乙腈稀释至刻度,再分别吸取一定量体积的标准溶液于同一10 mL容量瓶中,用乙腈定容,折算后混合标准溶液浓度均为10 mg·L-1。
取阴性樱桃样品进行前处理,得到空白基质液,用所得基质液配制基质曲线,浓度分别为5.0 μg·L-1、10 μg·L-1、20 μg·L-1、50 μg·L-1、100 μg·L-1、200 μg·L-1和500 μg·L-1。
1.5 色谱及质谱条件
1.5.1 色谱条件
色谱柱:Xbridge BEH C18(100 mm×2.1 mm,1.7 μm);流 动 相A(甲 醇)-B(0.3%甲 酸 含10 mmol·L-1甲酸铵);流速:0.30 mL·min-1;进样量:10 μL;柱温:40 ℃;梯度洗脱程序:0.0~2.0 min,40%→95%A;2.0~8.0 min,95%A;8.0~9.0 min,95%→40%A;9.0~13.0 min,40%A。
1.5.2 质谱条件
离子源:电喷雾电离源;扫描方式:正离子模式;气帘气:25 psi;电离电压(IS):5 500 V;离子源温度(TEM):550 ℃;雾化气(GAS1):50 psi;加热辅助气(GAS2):50 psi;碰撞气(CAD):medium;采集模式:多反应监测(MRM)模式。
2 结果与分析
2.1 色谱条件的优化
实验尝试使用乙腈和甲醇作为有机相,0.3%甲酸溶液和0.3%甲酸含10 mmol·L-1甲酸铵溶液作为水相进行了对比。结果发现,甲酸铵的加入对峰型影响较大,当水相中没有甲酸铵作为缓冲盐时,苯丁锡在流动相中扩散严重,峰型影响尤其明显,峰宽较宽,拖尾严重。而乙腈和甲醇相比,峰型影响不是很大,苯丁锡和三苯锡均能有较好的峰型,但考虑到乙腈洗脱能力较强,可能造成的基质效应相比甲醇更严重,所以综合考虑,选择甲醇-0.3%甲酸含10 mmol·L-1甲酸铵体系作为流动相。苯丁锡和三苯锡的MRM色谱图见图2。
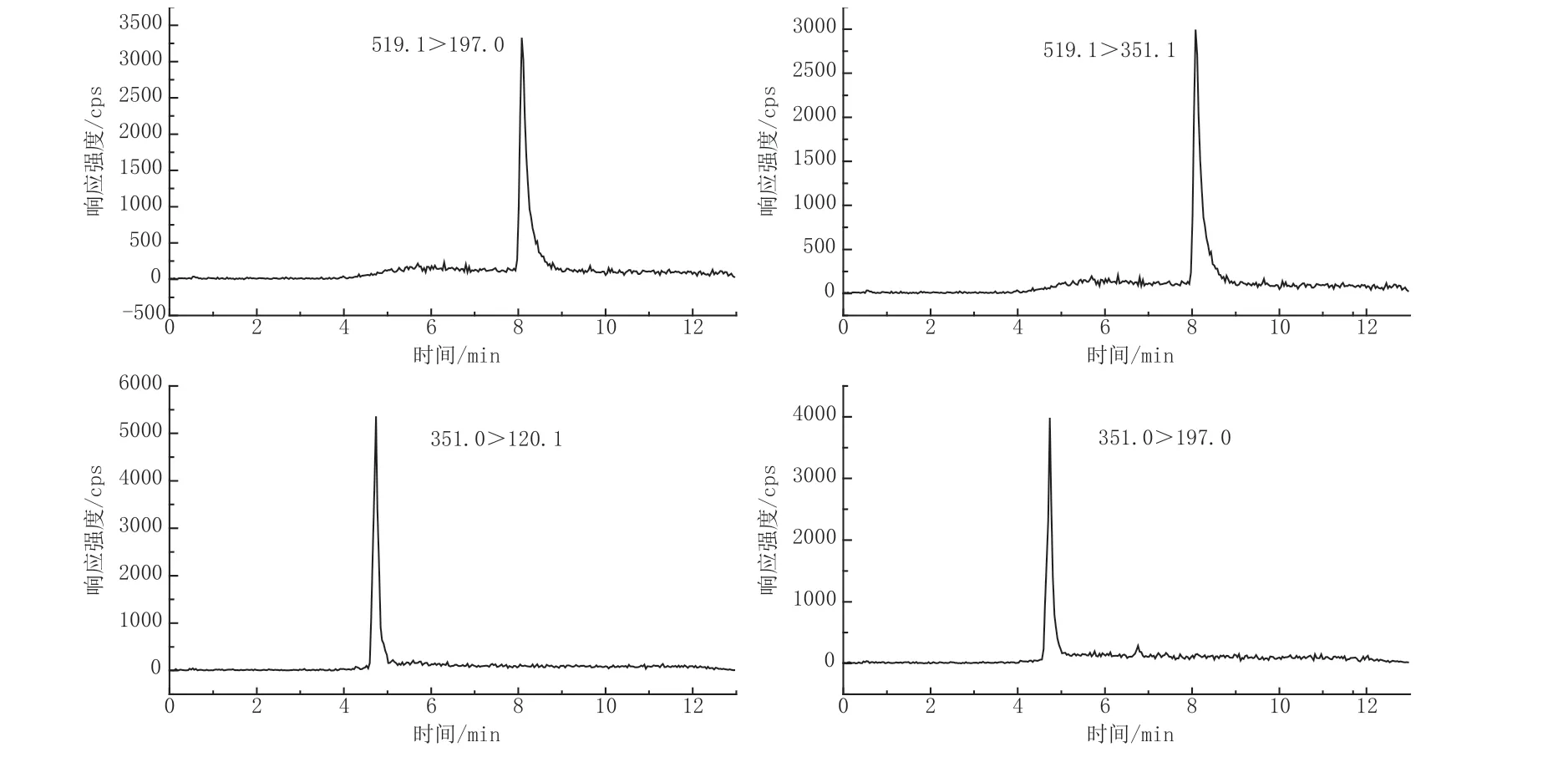
图2 苯丁锡与三苯锡的MRM色谱图
2.2 质谱条件的确定
实验初期发现,苯丁锡和三苯锡的母离子均是由O-Sn键断裂,产生对应的脱电子正离子,同时因为Sn的同位素较多,所以得到的母离子也较多,最终选择响应较高的作为母离子。进一步采用流动注射方式,优化去簇电压DP,使母离子响应达到最优,确定DP后,进一步优化各碎片离子的碰撞电压CE,选择响应较高的两个离子对作为定性定量依据,响应最高的为定量离子,另外的为定性离子。详细的质谱参数见表1,质谱图见图3。
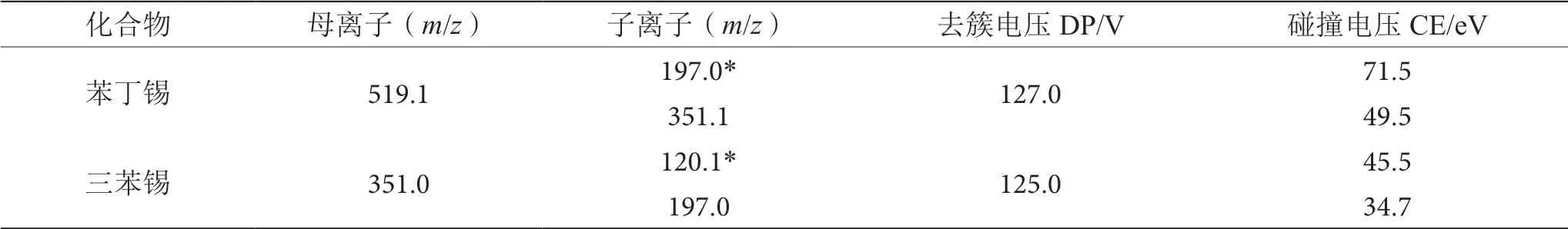
表1 多反应监测测定二级碎片的质谱参数表
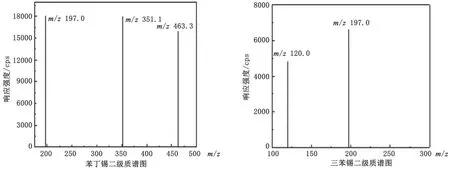
图3 苯丁锡和三苯锡的二级质谱图
2.3 固相萃取剂种类的选择
为了降低基质效应对结果的影响,同时保证回收率,实验前期对固相萃取剂的种类对回收率的影响进行了探究,选取了C18、PSA、GCB、NH2和中性氧化铝作为固相萃取剂,使用量均为25 mg。结果显示,在两次平行实验中,C18和PSA的回收率最高,其次是NH2,对苯丁锡和三苯锡的吸附也相对较小。而GCB和中性氧化铝对苯丁锡和三苯锡吸附严重,导致回收率低。虽然C18和PSA吸附的杂质类型不同,但由于两者回收率均较高,且C18的回收率要略高于PSA,因此为了简化实验,最终选择只使用C18作为固相萃取剂。回收率结果见图4。

图4 固相萃取剂对回收率的影响图
2.4 基质效应的探讨
樱桃中含有大量的糖和色素,在提取过程中易被提取到乙腈层引起较大的基质效应,从而增强或抑制苯丁锡和三苯锡的离子化程度,因此,需要对基质效应进行研究和定量结果校正。实验分别用乙腈和空白基质液配制100 μg·L-1的单点混合标准溶液,按优化后的方法测定,以基质单点和溶剂单点的峰面积比值K为判断依据。当K值小于80%,则说明基质抑制效应明显,大于120%则说明基质增强效应明显。测定结果为苯丁锡38.5%,三苯锡39.8%,基质抑制效应较为严重,因此,最终使用基质曲线进行定量。
2.5 定量分析依据
用空白基质溶液配制线性范围为5.0~500 μg·L-1的基质曲线对苯丁锡和三苯锡进行定量。将基质曲线按前处理方法上机测定后,以浓度为横坐标(X)和定量离子对峰面积为纵坐标(Y)绘图,所得方程为苯丁锡:Y=38.86X+2 304,相关系数R2为0.999 1;三苯锡:Y=40.21X+2 553,相关系数R2为0.999 2。结果表明苯丁锡和三苯锡的基质曲线在5.0~500 μg·L-1的浓度范围内呈良好线性关系。同时以低浓度加标进行测定,按照信噪比RS/N=3和RS/N=10分别计算出方法检出限和方法定量限,苯丁锡和三苯锡的检出限均为25 μg·kg-1,定量限均为100 μg·kg-1,方法灵敏度达到分析测定要求,满足样品一般含量的测定。
2.6 回收试验及精密度
选用苯丁锡和三苯锡呈阴性的樱桃样品,进行加标回收实验。根据方法定量限的1、2、5倍进行标准添加,每个水平平行测定6次,并计算出相应的相对标准偏差RSD。结果得出,苯丁锡和三苯锡在樱桃中的平均回收率范围在80.7%~94.5%,RSD在1.26%~4.52%。表明方法回收率好,精密度高,能够准确定量樱桃中的苯丁锡和三苯锡含量,具体结果见表2。

表2 樱桃中苯丁锡和三苯锡的回收率和精密度(n=6)表
2.7 方法的实际应用测定
随机选取实验室日常样品30个,用建立的方法进行测定,测定结果为三苯锡均低于检出限,而有一个样品检出了苯丁锡,含量为1.51 mg·kg-1,高于定限量,但符合GB 2763—2019中樱桃样品苯丁锡的检出限量10 mg·kg-1规定。同时,说明目前市面上的樱桃存在一定的苯丁锡残留风险,需要加大监管力度。
3 结论
本研究以分散固相萃取为前处理基础,建立了超高效液相色谱-串联质谱法同时测定樱桃中的苯丁锡和三苯锡。乙腈-水体系提取,过程快速高效,提取率高,结合C18固相萃取剂进行净化,回收率高;使用超高效液相色谱柱,梯度洗脱分离,在优化后的流动相和洗脱程序下,苯丁锡和三苯锡在9 min内出峰,且拖尾现象不严重,峰型较好;利用基质曲线对定量结果进行校正,加标回收实验结果表明,方法回收率好、重现性好,可用于实际测定樱桃中的苯丁锡和三苯锡。

