关于富液式蓄电池内化成工艺的研究
孙言行,邓亮,侯康,刁涵,曹云鹏
(陕西凌云蓄电池有限公司,陕西 宝鸡 721304)
0 引言
铅酸蓄电池的化成分为内化成和外化成两种。外化成是将固化干燥后的生极板装在含有稀硫酸电解液的化成槽中进行充电的化成方式。内化成是将固化干燥后的生极板装配成蓄电池,加入电解液进行充电的化成方式。与外化成相比,蓄电池内化成工艺的优点是,工序少,生产周期短,节能降耗,制造成本低[1-3]。内化成基本有两种方式:一种是先加入较低密度的硫酸电解液,然后待化成结束,将电解液倒出,注入较高密度的电解液,使蓄电池内部的电解液密度控制在1.29 g/cm3左右;另一种是加入较高密度的电解液,且化成结束后不倒酸,而电解液密度控制在1.29 g/cm3或将密度调整到1.29 g/cm3左右[4]。
本文中,笔者主要对电解液添加剂、电解液密度、化成过程中温度、化成充电制度等工艺参数进行研究,以确定最佳的富液式蓄电池内化成工艺。
1 试验
1.1 样品蓄电池制作
将连续冲孔工艺批量生产的免维护蓄电池正负生极板与PE隔板配组,装配为6-QW-165型蓄电池。正负极板栅合金为Pb-Ca-Sn-Al四元合金。灌酸量为10.5 ml/Ah。所有电解液均由浓硫酸(分析纯)与纯水配置,并添加一定量的无水硫酸钠(分析纯)。
1.2 静置过程中电解液密度对蓄电池温度的影响
分别给两只样品蓄电池加入温度为20℃密度为1.24 g/cm3、1.05 g/ cm3的电解液,然后静置。当把电解液加入蓄电池后,H2SO4与铅膏中的PbO发生中和反应,释放出中和热,使蓄电池内的温度升高。电解液的密度越高,反应速度越快,蓄电池的温度越高。如图1所示,密度为1.24 g/cm3的电解液使蓄电池的温度在1.5 h内上升至60℃、2.5 h上升至65℃以上。相应地,加入密度为1.05 g/ cm3的电解液的蓄电池在3 h内的最高温度不足40℃。

图 1 静置过程中蓄电池温度的变化曲线
据报道[5],化成初期的温度将影响蓄电池的低温性能。化成温度过高,会使有机膨胀剂木素磺酸钠的溶解度增加。木素磺酸钠溶出后,有一部分会在正极发生电化学氧化,使负极板中的有机膨胀剂的含量减少,导致负极活物质的逐渐收缩、板结,丧失多孔性,最终使蓄电池的低温性能降低。对于该6-QW-165型蓄电池,采用1.24 g/cm3的电解液化成的风险较大,宜采用密度为1.05 g/cm3的电解液进行化成。
1.3 测试静置过程中电解液密度的变化情况
将温度为20 ℃密度为1.05 g/cm3的硫酸电解液加入样品蓄电池中静置。在静置过程中电解液密度的变化情况如图2所示。由于中和反应使H2SO4不断消耗,电解液的密度持续降低,在5 h内降到了1.010 g/cm3左右。在电解液中,PbSO4的溶解度随着SO42-浓度的减小而升高,即化成过程电解液的密度越低,PbSO4的溶解度越高,枝晶短路现象发生的几率越大。为防止枝晶短路现象的发生,在实际的操作过程中最有效的办法是,向电解液中添加一定量的硫酸盐,提高电解液中SO42-的浓度。由于同离子效应的存在,可降低PbSO4的溶解度。目前常用的添加剂为Na2SO4,但该添加剂在富液式蓄电池中应用的研究较少。
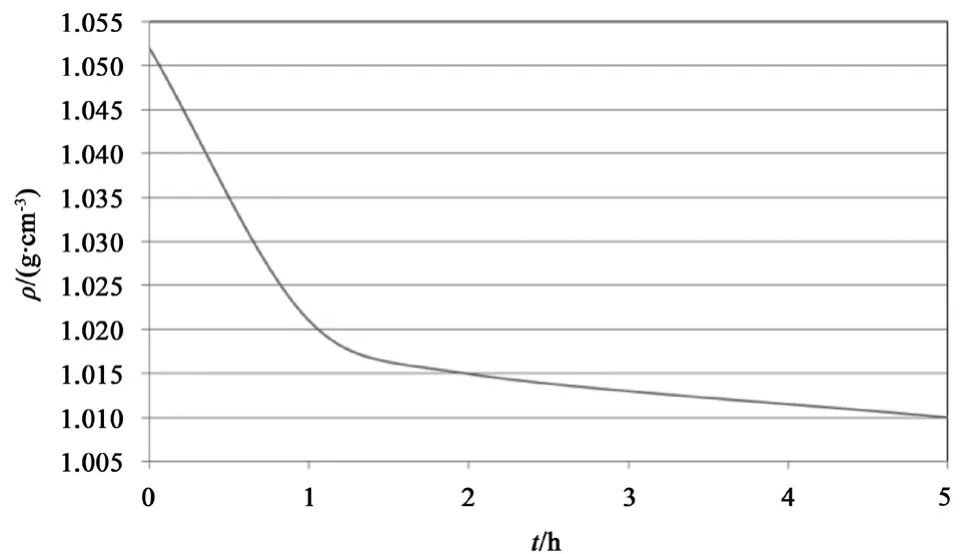
图 2 静置过程中电解液密度的变化曲线
1.4 化成充电制度的确定
在化成过程,充电电流密度越大,化成时间越短,但在化成后期由于析气量增加,电流有效转化的效率降低。当电流密度过高时,正极上化成得到的二氧化铅将继续被氧化,向更高价态的铅氧化物转化;负极上除了单质铅的生成外,还将有大量的氢气生成,以及其他不可预知的还原反应发生。换句话说,化成电流密度过高将导致副反应大量发生,严重削减蓄电池实际放出的容量[6]。并且,由于气体析出过程的冲刷作用,铅膏与板栅以及铅膏之间的结合力降低,影响蓄电池的使用寿命。另外,在蓄电池内化成过程中,电解液中 H2SO4的量制约了中和反应的进程。由于化成初期铅膏的转化效率较高,当化成的电流密度较大时,中和反应产生热量的速度增加。中和热与欧姆热共同作用将引起蓄电池温度升高。
鉴于以上考虑,确定采用五段式化成充电制度。第一阶段用2 mA/cm2电流密度持续充电30 min,使极板中形成导电的通道。第二阶段用12 mA/cm2的电流密度,充入蓄电池负极活性物质理论容量的电量。之后分别用6、5、3 mA/cm2的电流密度持续充电,使总化成时间控制在20 h左右。
1.5 Na2SO4对纯铅电极负极析气的影响
电化学分析采用三电极体系,工作电极为自制的纯铅电极(工作面积为9 mm2),参比电极为Hg/Hg2SO4/K2SO4(MSE)电极,辅助电极为面积为36 mm2自制铅板电极,电解液为添加不同质量Na2SO4的密度为1.28 g/cm3的硫酸水溶液。
以10 mV/s 的速度分别对Na2SO4含量为0、0.014、0.028、0.042、0.056、0.070 mol/L的电解液进行负向线性电位扫描5次,扫描区间为-1.2~-1.8 V,取第5次数据进行分析。从图3可以看出,在-1.2~-1.8 V范围内,当Na2SO4添加量为0.028 mol/L时,析氢电流最小,小于空白值,而其它浓度时析氢电流均高于空白值,说明添加0.028 mol/L的Na2SO4可抑制析氢。

图 3 线性电位扫描(LSV)曲线
1.6 蓄电池化成
采用密度为1.05 g/cm3的电解液,在30 ℃的水浴中用预定的充电制度进行化成。化成结束后,倒出电解液,用浓硫酸调配密度为1.350 g/cm3的电解液,再次灌入蓄电池中,使蓄电池电解的密度控制在1.285 g/cm3±0.005 g/cm3。为防止化成过程中有枝晶短路现象发生,在1.05 g/cm3的电解液中添加Na2SO4。根据线性电位扫描分析结果和化成过程的物料变化情况,Na2SO4的浓度控制在0.030 mol/L,以保证成品蓄电池电解液中Na2SO4的浓度为0.028 mol/L。
化成过程中蓄电池温度随时间的变化趋势如图4。从图4可以看出,由于所加的电解液密度较低,加液后蓄电池内的温度相对较低,但随着化成的进行,温度不断升高。在化成进行至第5h时温度达到最大值52℃。之后随着化成的进行,蓄电池内部的热量由负极析出的气体带出,温度开始下降。由此可以说明,用密度1.05 g/cm3的电解液以及30℃水浴冷却进行化成,可将蓄电池的温度控制在预定的要求。在炎热的夏季将水浴温度控制在30℃比较容易实施。
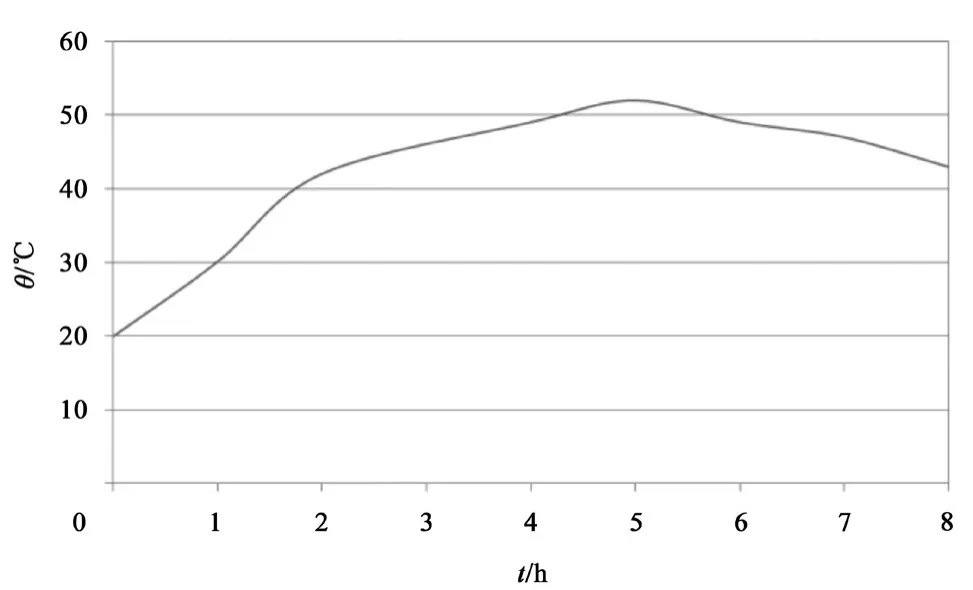
图 4 化成过程中电池的温度
1.7 蓄电池性能测试
化成结束后抽取蓄电池,进行表1所列性能测试。蓄电池过放电能力测试方法为:在25℃将蓄电池以In的电流放电至端电压为10.5 V,不经充电,用10 mm2的铜导线短路21 d。然后用恒压16 V限流4In充电24 h,再次用In的电流放电至端电压为10.5 V,记录Ce,并计算Ce与额定容量Cn的比值。其它性能测试按照GB/T 5008.1—2013对长寿命耐振动蓄电池的要求进行。蓄电池寿命测试结束后,解剖发现蓄电池的失效模式为缺液,这可能与测试方法有关。经过21 d的短路过放电后,蓄电池容量恢复到20小时率额定容量的92%,未发生枝晶短路现象。表1中,蓄电池各项性能均达到了 GB/T 5008.1—2013对长寿命耐振动蓄电池的要求。说明所设计的化成工艺可满足蓄电池生产的需要。
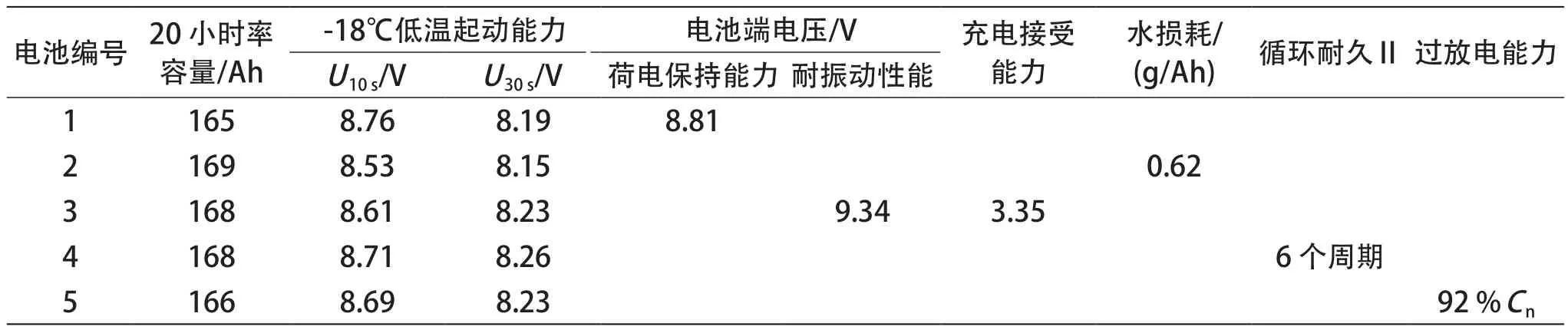
表 1 蓄电池性能测试结果
2 结论
通过上述试验可以确定:(1)采用密度为1.05 g/cm3的电解液进行内化成时,蓄电池化成过程的最高温度可控制在55℃以下。(2)化成过程中电解液添加剂 Na2SO4的最佳浓度为 0.030 mol/L,可防止枝晶短路发生。(3)蓄电池的化成充电制度为五段式模式,其中第二阶段的充电电流密度为12 mA/cm2。

