含双PNP和O-烷基二硫代磷酸配体的双核镍配合物的合成及其电化学性能
曹家熙,白晓雪,张栋梁,李涛,谢斌,,
(四川轻化工大学a.化学与环境工程学院;b.材料科学与工程学院;c.化学工程学院,四川 自贡643000)
引言
氢能作为一种高效、清洁的能源载体,是人们寻求的理想清洁能源之一,其中电催化分解水产氢是目前氢能研究的热点[1-2]。尽管贵金属Pt、Pd等催化制氢的效果优越,但是其催化制氢成本昂贵,故它们仅用于航天航空等特殊领域。而利用第四周期的过渡金属配合物作为催化剂实现大规模制氢是氢能未来发展的关键方向之一[3],已报道了具有高效催化活性的锰[4]、镍[5-8]、钴[9]、铜[10]等金属配合物。双膦化合物和O-烃基二硫代磷酸均是构筑配合物最常见的有机配体[11-18],研究表明含双膦和O-烃基二硫代磷酸的镍配合物具有电催化质子还原制氢的能力[16,18],并提出了镍配合物(dcpf)Ni(S2P{O}OR)的电催化制氢机理[18]。双(二苯基膦)胺(简称为PNP)是一类特殊的双膦配体,含PNP配体的镍配合物也被证明具有电催化制氢活性[13-15]。最近,人们报道了部分双核配合物也可作为电催化制氢催化剂,如双核铜[19]、双核钴配合物[20]。Collin课题组报道了含两个四氮杂大环的双核镍配合物用作水溶液中制氢催化剂,在pH=7的水溶液中施加-1.5 V的电位时,其电催化制氢活性比相应的四氮杂大环单核镍配合物的活性增强了8倍,提出了二聚体镍大环化合物之间可能存在协同作用[21]。但是,目前还没有人报道含双PNP配体的双核配合物的合成及其性质研究,为此,本文报道4个含双PNP配体和O-烷基二硫代磷酸配体的双核镍配合物((CH2)n(N(PPh2)2)2)Ni(S2P{O}OR)2(1:n=4,R=CH3;2:n=4,R=C2H5;3:n=3,R=CH3;4:n=3,R=C2H5)的合成、结构表征及其电化学性能,研究结果表明配合物1~配合物4是一类新颖的电催化制氢催化剂,在催化制氢领域具有潜在的应用前景,如图1所示。
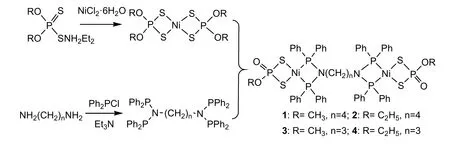
图1 配合物1~配合物4的合成路线
1 实验部分
1.1 试剂与仪器
所有试剂均为市购分析纯,未作进一步纯化处理。配合物((CH3O)2PS2)2Ni和((C2H5O)2PS2)2Ni按文献方法合成[16],双PNP化合物(CH2)3(N(PPh2)2)2和(CH2)4(N(PPh2)2)2按文献方法改进合成[17]。
在Nicolet 6700红外分光光度计上,用KBr压片法测定红外光谱。在Bruker AV 400核磁共振谱仪上测定核磁共振谱。用TU-1950紫外-可见分光光度计和1cm石英比色皿测量配合物在乙腈溶液中的紫外-可见吸收光谱。在Bruker Smart Apex CCD单晶衍射仪上测定配合物的晶体结构。电化学性能是在CHI660E电化学工作站上用三电极系统(直径为3 mm的玻璃碳工作电极、铂丝对电极和非水溶液的Ag/AgNO3参比电极),以n-Bu4NPF6为支持电解质,乙腈为溶剂,氮气气氛下测定。所有电位均用Fc+/Fc进行校准。
1.2 配合物的合成
1.2.1配合物1的合成
在100 mL的三口烧瓶中加入0.372 g((CH3O)2PS2)2Ni(1 mmol)和20 mL二氯甲烷(CH2Cl2),搅拌使固体完全溶解,再加入0.412 g(CH2)4(N(PPh2)2)2(0.5 mmol),溶液迅速变为黄色,在室温下搅拌4 h。尔后用旋转蒸发仪减压去除溶剂,用适量CH2Cl2溶解,以体积比15∶1的二氯甲烷/甲醇混合溶剂作展开剂,进行薄层色谱分离,得黄色固体0.477 g,产率78%。Anal.Calcd(%)for C54H54N2Ni2O4P6S4:C,52.88;H,4.44;N,2.28。Found(%):C,52.98;H,4.65;N,2.19。FTIR(KBr disk,cm-1):νP=O1209(s),vP-O-(C)1035(m),v(P)-O-C831(m),vP-N-P748(s),vP-S571(m),691(s)。1H NMR(400 MHz,CF3COOD,ppm):δ0.66(s,4H,2CH2),2.45~2.67(m,4H,2NCH2),3.61(d,J=13.9 Hz,6H,2OCH3),7.43~7.53(m,16H,PPh),7.64(dt,J=13.2 Hz,6.4 Hz,24H,PPh)。13C NMR(101 MHz,CF3COOD,ppm)δ136.61(s,i-Ph),135.17(d,J=26.5 Hz,m-Ph),132.28(t,J=5.8 Hz,o-Ph),128.88(dd,J=39.2 Hz,12.5 Hz,p-Ph),56.38(s,2OCH3),50.21(s,2NCH2),28.97(s,2CH2)。31P{1H}NMR(162 MHz,CF3COOD,85%H3PO4,ppm)δ55.80(d,J=5.8 Hz,NP),88.16(d,J=11.9 Hz,P=O)。UV-vis(MeCN,λmax,nm):209,278,321。
1.2.2配合物2的合成
用0.428 g((C2H5O)2PS2)2Ni(1 mmol)代 替((CH3O)2PS2)2Ni与0.412 g(CH2)4(N(PPh2)2)2(0.5 mmol)反应,得黄色固体0.513 g,产率82%。
Anal.Calcd(%)for C56H58N2Ni2O4P6S4:C,53.61;H,4.66;N,2.23。Found(%):C,53.98;H,5.05;N,2.41。FTIR(KBr disk,cm-1):νP=O1209(s),vP-O-(C)1041(m),v(P)-O-C836(w),vP-N-P753(s),vP-S567(w),699(s)。1H NMR(400 MHz,CF3COOD,ppm):δ0.70(s,4H,2CH2),1.24(t,J=6.8 Hz,6H,2CH3),2.50~2.69(m,4H,2NCH2),3.98~4.09(m,4H,2OCH2),7.53(d,J=5.9 Hz,16H,PPh),7.60~7.78(m,24H,PPh)。13C NMR(101 MHz,CF3COOD,ppm)δ136.21(d,J=7.5 Hz,i-Ph),134.75(dt,J=27.6 Hz,5.9 Hz,m-Ph),131.87(t,J=5.4 Hz,o-Ph),128.51(td,J=26.1 Hz,13.3 Hz,p-Ph),67.47(s,2OCH2),49.80(s,2NCH2),28.59(s,2CH2),16.30(d,J=7.1 Hz,2CH3)。31P{1H}NMR(162 MHz,CF3COOD,85%H3PO4,ppm)δ55.82(d,J=5.7 Hz,NP),85.79(d,J=11.9 Hz,P=O)。UV-vis(MeCN,λmax,nm):208,278,322。
1.2.3配合物3的合成
与1合 成 方 法 相 似,用0.405 g(CH2)3(N(PPh2)2)2(0.5 mmol)代替(CH2)4(N(PPh2)2)2与((CH3O)2PS2)2Ni反应,得黄色固体0.472 g,产率78%。Anal.Calcd(%)for C53H52N2Ni2O4P6S4:C,52.50;H,4.32;N,2.31。Found(%):C,53.56;H,4.46;N,2.01。FTIR(KBr disk,cm-1):νP=O1199(s),vP-O-(C)1017(m),v(P)-O-C872(m),vP-N-P752(s),vP-S562(w),650(w)。1H NMR(400 MHz,DMSO-d6,ppm):δ0.53~0.76(m,2H,CH2),2.75~2.88(m,4H,2NCH2),3.35(d,J=4.0 Hz,6H,2OCH3),7.46~7.60(m,32H,PPh),7.71(d,J=19.2 Hz,8H,PPh)。13C NMR(101 MHz,DMSO-d6,ppm)δ133.15(s,i-Ph),132.22(t,J=6.0 Hz,m-Ph),129.55(t,J=5.5 Hz,o-Ph),127.96(q,J=24.0 Hz,p-Ph),52.94(d,J=7.0 Hz,2OCH3),44.83(s,2NCH2),29.33(s,CH2)。31P{1H}NMR(162 MHz,DMSO-d6,85%H3PO4,ppm)δ57.47~57.82(m,NP),58.02(d,J=11.9 Hz,P=O)。UV-vis(MeCN,λmax,nm):204,277,320。
1.2.4配合物4的合成
与配合物合成2的合成方法相似,用0.405 g(CH2)3(N(PPh2)2)2(0.5 mmol)代 替(CH2)4(N(PPh2)2)2,得到黄色固体0.402 g,产率65%。Anal.Calcd(%)for C55H56N2Ni2O4P6S4:C,53.25;H,4.55;N,2.26。Found(%):C,53.32;H,4.95;N,2.31。FTIR(KBr disk,cm-1):νP=O1204(s),vP-O-(C)1040(m),v(P)-O-C859(m),vP-N-P753(s),vP-S561(w),653(w)。1H NMR(400 MHz,DMSO-d6,ppm):δ0.56~0.70(m,2H,CH2),1.05(t,J=7.1 Hz,6H,2CH3),2.72~2.90(m,4H,2NCH2),3.71(dt,J=9.6 Hz,7.1 Hz,4H,2OCH2),7.47~7.58(m,32H,PPh),7.71(t,J=7.2 Hz,8H,PPh)。13CNMR(101 MHz,DMSO-d6,ppm)δ133.12(s,i-Ph),132.38~132.04(m,m-Ph),129.52(t,J=5.6 Hz,o-Ph),128.00(dd,J=47.5 Hz,24.1 Hz,p-Ph),61.69(d,J=7.1 Hz,2OCH2),44.84(s,2NCH2),29.33(s,CH2),15.92(d,J=7.6 Hz,2CH3)。31P{1H}NMR(162 MHz,DMSO-d6,85%H3PO4,ppm)δ55.19(t,J=11.9 Hz,NP),58.15(d,J=11.9 Hz,P=O)。UV-vis(MeCN,λmax,nm):208,279,321。
1.3 晶体结构测定
将尺寸为0.19 mm×0.18 mm×0.17 mm的配合物1的单晶置于Bruker Smart Apex CCD上,用经石墨单色化的Mo Kα(λ=0.071 073 nm)为辐射光源,在100 K下,以ω/2θ方式进行扫描,在2.124°≤2θ≤50.018°范围内,共收集到20 068个衍射点,其中有10 549个独立衍射点(Rint=0.0912)。用ShelX程序[22]解析配合物的晶体结构,结构精修使用ShelXL程序[23]来完成。非氢原子坐标及各向异性参数进行全矩阵最小二乘法修正,对氢原子则采用跨骑方式修正。最终偏离因子R1=0.0937(I>2σ(I)),wR2=0.2764(所有数据)。在最终的差值Fourier图中,最高残余电子密度峰1.78 e·Å-3,最低残余电子密度峰-1.55 e·Å-3。
配合物1的晶体数据为:C54H54ClN2Ni2O4P6S4(M=1226.47 g/mol),单斜晶系,P21/c空间群,a=19.447(4)Å,b=17.783(4)Å,c=17.677(4)Å,β=99.989(4)°,V=6020(2)Å3,Z=4,μ(Mo Kα)=0.967 mm-1,Dcalc=1.353 g·cm-3,F(000)=2536(CCDC:2051375)。
2 结果与讨论
2.1 配合物1的晶体结构
配合物1的主要键长和键角见表1,其晶体结构如图2所示。从图2可知,配合物1存在一个分子对称中心,两个镍原子的配位环境相同。每个镍原子由双PNP配体的同一双(二苯基膦基)胺的两个磷原子和O-甲基二硫代磷酸配体的两个硫原子配位,形成了NiS2P2的配位环境。Ni-P的键长为2.1295Å~2.1690Å,Ni-S的键长为2.2090Å~2.2242Å。围绕Ni1和Ni2原子的配位键角之和分别为360.02°和360.06°,说明两个镍原子的配位环境近似于平面四方形,与含PNP和O-烷基二硫代磷酸配体的单核镍配合物的结构相似[24]。

图2 配合物1的晶体结构(椭球率为50%,删去了氢原子)
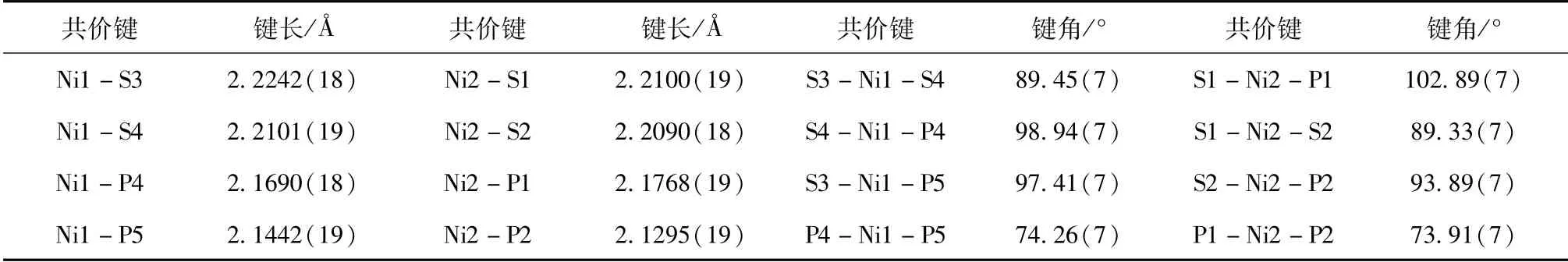
表1 配合物1的主要键长和键角
2.2 配合物的谱学表征
2.2.1红外光谱
配合物1~配合物4的特征红外数据见表2,配合物分别在831 cm-1~872 cm-1和1017 cm-1~1041 cm-1出现了分别归属于(P)-O-C键和P-O-(C)键的两个强伸缩振动吸收峰,在561 cm-1~571 cm-1的吸收谱峰归属于P-S键的对称伸缩振动,而650 cm-1~699 cm-1的吸收谱带为P-S键的不对称伸缩振动;在1199 cm-1~1209 cm-1范围内出现了P=O键的伸缩振动吸收带。另外在748 cm-1~753 cm-1出现了双PNP配体的P-N-P的骨架伸缩振动吸收峰[14-15,24-25]。

表2 配合物1~配合物4的主要红外光谱数据/cm-1
2.2.2核磁共振谱
配合物1~配合物4的1H NMR测定表明:双PNP上的CH2N在2.45 ppm~2.90 ppm出现多重峰,相应的苯环氢化学位移在7.43 ppm~7.78 ppm。配合物1和配合物3的P{O}OCH3分别在3.61 ppm和3.35 ppm出现一双重峰,归属于配合物4的P{O}OCH2的双峰在3.71 ppm,而配合物3的P{O}OCH2在3.98 ppm~4.09 ppm出现多重峰;在13C NMR上,配合物1和配合物3的P{O}OCH3的碳化学位移分别在56.38 ppm和52.94 ppm,配合物4的P{O}OCH2的碳化学位移为61.69 ppm,而配合物3的P{O}OCH2出现在67.47 ppm;相应的31P NMR谱在57.47 ppm~57.82 ppm出现了双PNP的多重峰,而归属于P=O键的31P NMR在58.02 ppm~88.16 ppm范围内[16,18]。
2.2.3紫外-可见吸收光谱
图3为配合物1~配合物4的紫外-可见吸收光谱图,它们的紫外-可见吸收光谱非常相似,分别在208 nm、278 nm和322 nm附近呈现出三条吸收带。在208 nm和278 nm吸收带可归属于双PNP配体和O-烷基二硫代磷酸根配体中的π→π*跃迁,在322 nm吸收带为配体内的电荷转移(ILCT/LLCT)吸收峰[24-27]。
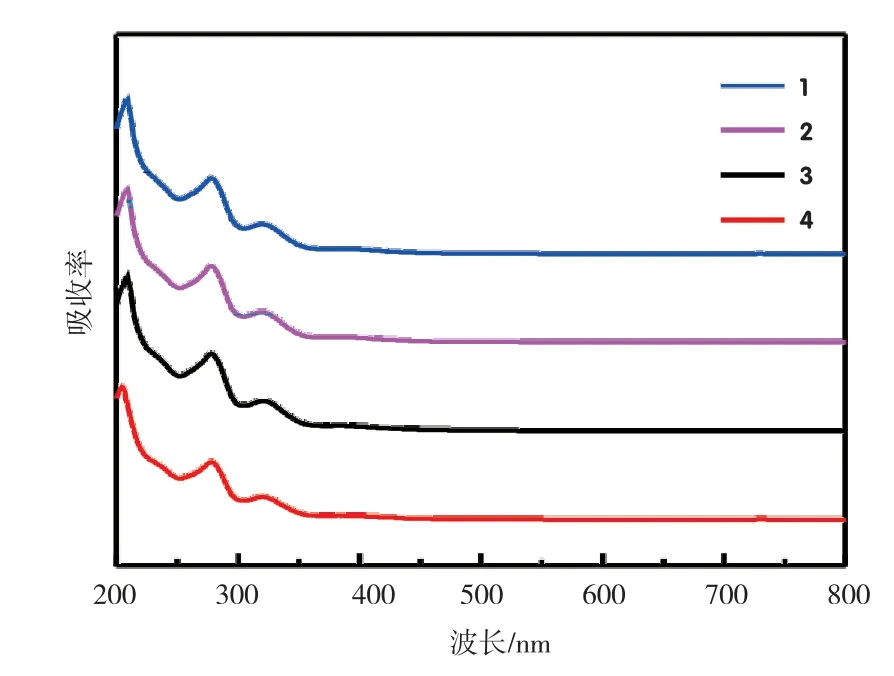
图3 配合物1~配合物4在乙腈溶液中紫外-可见吸收光谱
2.3 电化学性能
2.3.1循环伏安配合物1~配合物4的乙腈溶液的循环伏安图见图4。
从图3可知,配合物1在Epc=-1.63 V的可逆还原峰为NiⅡNiⅡ/NiⅡNiⅠ的 单 电 子 还 原 过 程[16,18,27-29],在Epa=+0.59 V的不可逆氧化峰为双PNP配体的氧化峰。同样地,配合物2~配合物4分别在Epc=-1.64 V和Epa=+0.61 V附近也分别出现了NiⅡNiⅡ/NiⅡNiⅠ的单电子还原过程和双PNP配体的氧化峰(图4和表3)。

图4 1 mmol·L-1的配合物1~配合物4的乙腈溶液的循环伏安图(条件:0.1 mol·L-1 n-Bu4 NPF6支持电解质,扫描速率为100 mV·s-1)
在不同扫描速度下的配合物1的循环伏安图如图5所示,由图5(a)可知:配合物的所有氧化还原峰的电流强度(Ipc和Ipa)均随扫描速度的增加而增强,其电流强度与扫描速率的平方根呈线性关系(图5(b)),表明配合物1的电化学过程是扩散控制过程,电化学活性物质在溶液中是自由扩散的[24,27-29]。其扩散系数(D0)为1.51×10-5cm2·s-1。同样的配合物2~配合物4的电化学过程也是受扩散控制的,相应的D0列在表3中。

表3 配合物1~配合物4在乙腈溶液中的电化学数据
2.3.2电催化制氢活性
如图6(a)所示,配合物1在添加10 mmol·L-1三氟乙酸(TFA)后,Epc=-1.63 V处的还原峰向正移到-1.38 V处,另外在-1.76 V产生一个新还原峰。随TFA的浓度增加,第一个还原峰电流强度增加不明显,且在50 mmol·L-1TFA时被第二个催化还原峰所覆盖。可以观察到:Epc=-1.76 V的催化还原峰的电流强度随TFA浓度的增加而增加,说明配合物1可有效地催化质子还原成H2[1
8
,24,31]。由图6(b)可以看出,该催化还原峰的电流强度与未添加TFA的配合物的还原峰电流强度的比值(Icat/Ipc)与TFA的浓度的平方根呈线性相关,表明该催化制氢反应对TFA为一级反应。

图5 1 mmol·L-1的配合物1的乙腈溶液在不同扫描速度下的循环伏安图(a)及其在NiⅡNiⅡ/NiⅡNiⅠ还原峰的电流强度与扫描速率的平方根的关系图(b)(条件:0.1 mol·L-1 n-Bu4 NPF6支持电解质,扫描速率为50 mV·s-1、100 mV·s-1、200 mV·s-1、300 mV·s-1、400 mV·s-1和500 mV·s-1)

图6 添加有0-120 mmol·L-1 TFA的1 mmol·L-1配合物1的乙腈溶液循环伏安图(a)及其催化还原峰电流强度与未添加TFA的还原峰电流强度的比值(I cat/I pc)与扫描速率的平方根的关系图(b)(条件:0.1 mol·L-1 n-Bu4NPF6支持电解质,扫描速率为100 mV·s-1)
同样地,配合物2~配合物4也具有催化还原TFA制氢的活性,相应的电催化数据列在表3中。由表3可知,在添加120 mmol·L-1TFA后,配合物1~配合物4的Icat/Ipc值为48.31~49.71,可以用转换频率(TOF)来表征催化活性,利用Icat/Ipc值可计算出催化剂的TOF值[28]。从表3可以看出:当添加120 mmol·L-1TFA时,配合物1~配合物4的电催化制氢反应的TOF分别为442.5 s-1、458.1 s-1、462.4 s-1、469.5 s-1。说明配合物催化还原制氢的活性顺序为:配合物4>配合物3>配合物2>配合物1,表明配合物4的乙腈溶液催化还原TFA制氢的效率最高。采用Fourmond方法[33],可以计算出催化制氢反应的过电位(η),当添加120 mmol·L-1TFA时,配合物1~配合物4的电催化制氢反应的η值为0.89 V~0.98 V。
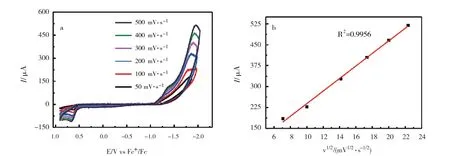
图7 添加有30 mmol·L-1 TFA的1 mmol配合物1的乙腈溶液在不同扫描速度的循环伏安图(a)及其还原峰电流强度与扫描速率的平方根的关系图(b)(条件:0.1 mol·L-1 n-Bu4 NPF6支持电解质,扫描速率为50 mV·s-1、100 mV·s-1、200 mV·s-1、300 mV·s-1、400 mV·s-1和500 mV·s-1)
图7(a)为配合物1在添加30 mmol·L-1TFA后在不同扫描速度下的循环伏安图,其催化还原峰的电流强度与扫描速率的平方根呈现线性关系(见图7(b)),表明配合物1的催化还原电流是由TFA在电极表面的扩散速度决定的,其扩散系数D1为1.43×10-3cm2·s-1。同样地,配合物2~配合物4在添加30 mmol·L-1TFA后的电化学过程也是扩散控制的过程,其D1列在表3中。
采用双(O,O’-二烷基二硫代磷酸)镍配合物与双PNP反应合成了4个新颖的含双PNP和O-烷基二硫代磷酸配体的双核镍配合物((CH2)n(N(PPh2)2)2)Ni(S2P{O}OR)2(1:n=4,R=CH3;2:n=4,R=C2H5;3:n=3,R=CH3;4:n=3,R=C2H5),对配合物的结构进行了全面表征。测定了配合物1的单晶结构,配合物1为含有两个畸变平面四边形NiS2N2的双核配合物。配合物1~配合物4的乙腈溶液在Epc=-1.63 V处存在归属于NiIINiII/NiIINiI的可逆氧化还原峰,在Epa=0.60 V附近有双PNP配体的不可逆氧化峰。在TFA存在下,配合物1~配合物4均能电催化还原质子,均具有催化制氢的活性,在添加120 mmol·L-1TFA时的制氢TOF和(分别为442.5 s-1~469.5 s-1和0.89 V~0.98 V,其中配合物4的TOF值达到469.5 s-1,具有最好的电催化制氢能力。另外无论是否存在TFA,配合物1~配合物4的电化学过程均受扩散控制。

