高氧还原稳定性的非金属掺杂Pt基催化剂制备及其稳定机理研究
熊云杰涂吴轩王添毅晏根平
高氧还原稳定性的非金属掺杂Pt基催化剂制备及其稳定机理研究
熊云杰1,2,涂吴轩2,王添毅2,晏根平2
(1. 江西省环保材料与装备工程技术研究中心;2. 萍乡学院 材料与化学工程学院,江西 萍乡 337000)
近年来,阴极催化剂较低的氧还原稳定性已成为限制质子交换膜燃料电池实际应用与发展的瓶颈。文章以尿素和氯铂酸钾为前驱体,通过简单的无表面活性剂合成方法,得到一种非金属N掺杂的Pt纳米颗粒。物理表征结果清楚地显示了N在Pt晶格内的掺杂导致了Pt纳米粒子的拉伸应变,电化学测试结果表明,这种N掺杂的Pt纳米催化剂具有高的氧还原活性与稳定性,其20000圈循环加速测试后活性衰减仅为商业化Pt/C的14.4 %。实验结果表明,通过该合成方法制备的N掺杂的Pt纳米粒子为燃料电池催化剂的实际运用提供了广阔前景。。
燃料电池;铂基催化剂;氧还原;非金属掺杂
随着不可再生资源的日益枯竭及人类需求的急剧增加,寻找一种环境友好、成本低廉的创新解决方案已经迫在眉睫。燃料电池作为一种能将化学能直接转换为电能的装置,具有能量效率高、比功率高、绿色环保等优点,是目前解决能源危机和环境污染的重要途径之一。但是,阴极缓慢的氧还原反应(ORR)动力学是限制高效燃料电池开发的主要因素。催化剂作为燃料电池中的关键材料,既是决定燃料电池性能的关键因素,也是其高成本的突出体现。目前,贵金属铂(Pt)仍然是燃料电池中阴极ORR催化剂的最佳选择[1–3]。然而,由于Pt储量有限、成本过高,严重地制约了燃料电池的发展。因此,在减少Pt用量的同时,维持催化剂的高活性,是降低成本,实现燃料电池商业化的关键之一。目前使用的燃料电池需要在严苛的酸性条件下运行,高电势条件下碳载体腐蚀和铂催化剂的溶解、长大都会造成催化剂活性的损失,使燃料电池循环性能衰减。基于以上考虑,在降低Pt催化剂用量的同时,保证其催化活性、大幅提升稳定性,是当今燃料电池催化剂研究发展的方向[2–4]。
研究表明,通过形貌控制、合金化以及形成核壳结构等方法,可以提高Pt基ORR催化剂的稳定性[5]。但值得注意的是,通过这些方法合成的Pt基电催化剂绝大多数为Pt-过渡金属合金[5],而在燃料电池的工作过程中,Pt-金属合金中过渡金属的不断溶出会降低其和原有 Pt 表面原子间的相互作用,造成Pt原子流失,从而导致催化剂的性能不断降低。目前,已有部分研究报道了具有较高氧还原稳定性的非金属元素掺杂的Pt基氧还原催化剂。例如,Adzic[6]等人在510℃下用NH3处理PtNi前驱体,得到了具有核壳结构的PtNiN催化剂,经35000次循环加速测试后,其LSV半波电位仅损11 mV(商业化Pt/C为55mV),DFT计算认为核中N原子的存在使Pt更容易地从内层扩散到表层,填补了ORR过程中造成的催化剂表面的空位,从而提高了催化剂的耐久性。Xia等人在650℃通过NH3热处理,在Pt3Fe[7]、PtTe[8]等Pt基金属间化合物中引入N原子,新引入的N原子对原有组分有锚定作用,增强了催化剂的结构稳定性,提升了ORR稳定性的。除掺杂N元素外,P、B等非金属元素同样被用于提升Pt基ORR催化剂的稳定性。Zhang[9]等人利用电沉积法,以ZnO纳米棒阵列为模板,合成了PtP多孔合金纳米管阵列,该PtP纳米管阵列在酸性介质中具有较好的ORR电催化活性和稳定性,经过10000次循环后,该催化剂的ORR活性几乎没有衰减。利用NaH2PO2作为磷源,研究者们合成三元PtNiP[10]、PtCoP[11]以及四元PtPdNiP[12]等一系列具有较高ORR稳定性的P掺杂的催化剂。此外,Dong[13]等人利用二甲胺硼烷用作还原剂和硼源,液相合成得到了B掺杂的Pt3Ni催化剂,经10000次加速测试后,该催化剂展现出较商业化Pt/C更高的ORR活性。
尽管非金属掺杂的Pt基催化剂研究已经取得了一定进展,但Pt与非金属元素成键的键能较低,大多数非金属掺杂的Pt基催化剂的合成往往需要高温热处理,而过高的热处理温度容易导致纳米粒子的烧结和团聚,一定程度上影响催化剂的活性和稳定性,因此,降低掺杂温度成为非金属掺杂的Pt基催化剂合成的关键;与此同时,如何精准地调控非金属在Pt中的掺杂量,也是一个亟待解决的问题。
本文通过溶剂热法,制备得到尺寸均一、粒径小、分散度高的N掺杂Pt黑和Pt/C催化剂,XRD、球差矫正电镜、EELS能谱等结果均证实了N已成功掺杂进入了Pt的晶格中。通过此方法制备的催化剂展现出能与商业化Pt催化剂相媲美的活性以及极其优异的稳定性。该方法步骤简单,没有使用表面活性剂,可以实现催化剂单批次百克级制备。因此,这种具有前景的制备策略为经济高效地生产Pt基催化剂提供了巨大潜力。
1 实验部分
1.1 氮掺杂的Pt NPs/C催化剂的制备与物理表征
氮掺杂的Pt NPs/C的具体合成步骤如下:将20.42mg的K2PtCl4、118mg的尿素、6.4mg的炭黑加至400mL的超纯水中溶解并混匀,将混合溶液移入回流装置中在90℃下搅拌回流6h。冷却至室温后,悬浮液通过过滤回收,用超纯水洗涤数次后真空干燥。接着将干燥后得到的粉末通入氢气/氮气(氢气占体积分数为10%)在110℃下热处理2h,将处理后的样品用稀硫酸、超纯水、乙醇洗涤数次,除去残留在催化剂表面上的杂质,并在60℃下真空干燥,得到氮掺杂的Pt NPs/C(铂负载量为60%)。将此氮掺杂的Pt NPs/C在200℃下热处理后通入氢气/氮气下1h(标记为氮掺杂的Pt NPs/C-H2)。
催化剂的物理表征:采用透射电子显微镜(TEM)(FEI Tecnai 30F)分析催化剂颗粒的分布以及粒径,同时进行线扫和面扫获得了催化剂元素的分布。采用X射线粉末衍射(XRD)(D8 ADVANCE)分析催化剂的结构和组分。采用X-射线光电子能谱(XPS)(Quantum 2000),得到催化剂中各元素的原子价态信息以及各种化合物元素的组成、含量以及化学状态。
1.2 催化剂电化学体系与工作电极的制备
1.2.1 电化学测试体系
本文使用三电极体系进行催化剂电化学性能测试,以涂有催化剂的圆盘玻碳(GC,直径3nm)电极为工作电极,GC为对电极,饱和Hg/Hg2SO4电极(MSE)为参比电极,实验测试时的电位与可逆氢电极(RHE)相对比。实验通过控制循环水的温度将测试体系的温度稳定在25℃,实验仪器为上海辰华仪器公司的CHI630E电化学工作站和法国Radiometer Analytical公司的旋转圆盘电极。
1.2.2 工作电极的制备
将实验中用到的工作电极依次用Al2O3粉末打磨干净,然后在异丙醇溶液和超纯水中超声10min,用N2(≥99.99 %)吹干备用。用称量天平称取5 mg催化剂与用移液枪移取的50μL的Nafion溶液(5wt%)、2.95mL的超纯水混合,超声1h使催化剂溶液均匀分散得到悬浊液。接着将3μg的混合悬浊液转移至铂碳电极表面,室温下干燥过夜得到42μgPt•cm-2的催化剂涂层。以涂有催化剂的电极为工作电极,GC为对电极,MSE为参比电极,在三电极体系的电化学工作站上对催化剂进行电化学测试
1.3 催化剂的电化学性能测试
1.3.1 循环伏安法
循环伏安法(CV)通过控制电极电势使得电极上发生电化学反应,电位扫描得到循环、封闭的氧化还原波,得到的电流电压图即为循环伏安图。通过循环伏安图中氧化还原峰的位置以及曲线形状可以分析催化剂的活性强弱。本实验所采用的电解质溶液是0.1M的HClO4溶液,测试前向溶液通入高纯N2(约0.5h)以除去电解质溶液中的溶解氧,CV扫描电位上限为1.1V,为降低金属的氧化对催化剂电化学性能的影响,扫速设为50 mV•s-1。
1.3.2 线性扫描
旋转圆盘电极使电解液通过旋转产生离心力,电极表面覆盖的液体在离心力作用下形成厚度均匀的扩散层以及均一的扩散电流密度。通过线性扫描(LSV)在电极上施加线性变化的电压使电极电位随着外加电压变化,得到工作电极上的电解电流。电流随电极电位变化的曲线为线性扫描伏安图。本实验在O2饱和的0.1M的HClO4溶液中进行LSV测试,扫描速度为10mV•s-1,旋转速度为1600rpm。
2 实验结果与讨论
2.1 氮掺杂的Pt NPs/C催化剂元素分析
利用XPS检测获得了实验合成出的氮掺杂的Pt NPs/C表面的元素组成的详细信息,通过外标法由C 1s峰(284.8 eV)对原子结合能大小进行校准,修正各元素的灵敏系数。由图1(A)可知,实验合成出的氮掺杂的Pt NPs/C表面检测出了Pt 4f、C 1s、N 1s、O 1s信号。为了更深入研究氮元素在Pt NPs/C经中的分布状态,使用Ar+离子体对样品进行刻蚀(蚀刻速率为0.3nm/s),经过60s、600s的刻蚀之后,再分别进行XPS检测,结果如图1(B—C)所示。由图1(B—C)可知,XPS检测中仍然可以观察到N信号,表明N元素不仅存在于氮掺杂的Pt NPs/C的表面,也存在于氮掺杂的Pt NPs/C内部。
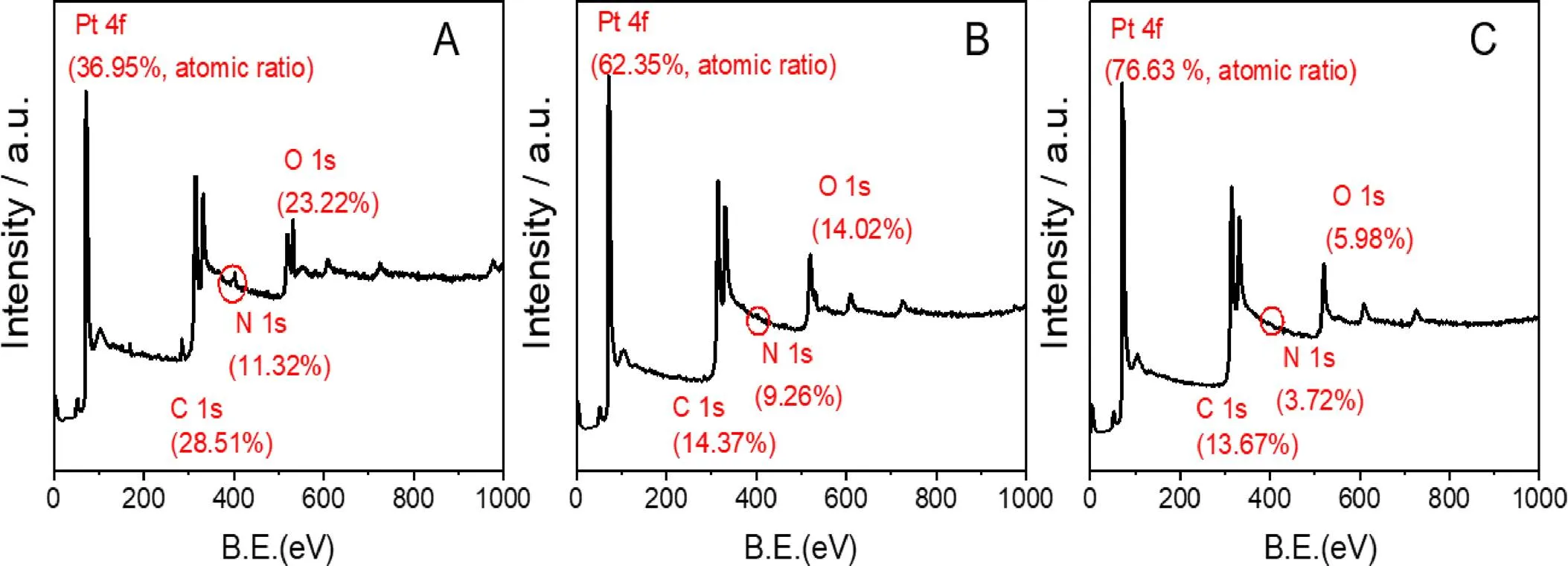
(A)0s;(B)60s;(C)600s
2.2 氮掺杂的Pt NPs/C催化剂XRD分析
为了研究氮掺杂的Pt NPs/C结构上的信息,实验对商业化的Pt/C与实验合成的氮掺杂的Pt NPs/C进行XRD检测,结果如图2所示。从图2(A)可以看出,商业化的Pt/C与实验合成的氮掺杂的Pt NPs/C都具有对应于面心立方结构(FCC)金属Pt的(111)、(200)、(220)、(311)面对应的特征衍射峰。而如图2(B)所示,与商业化的Pt/C相比,氮掺杂的Pt NPs/C的Pt(111)面对应的XRD峰从39.67°移至39.82°,即对应于Pt(111)晶格间距从2.254 Å增加至2.270Å,说明氮掺杂的Pt NPs/C中产生了拉伸应变效应。
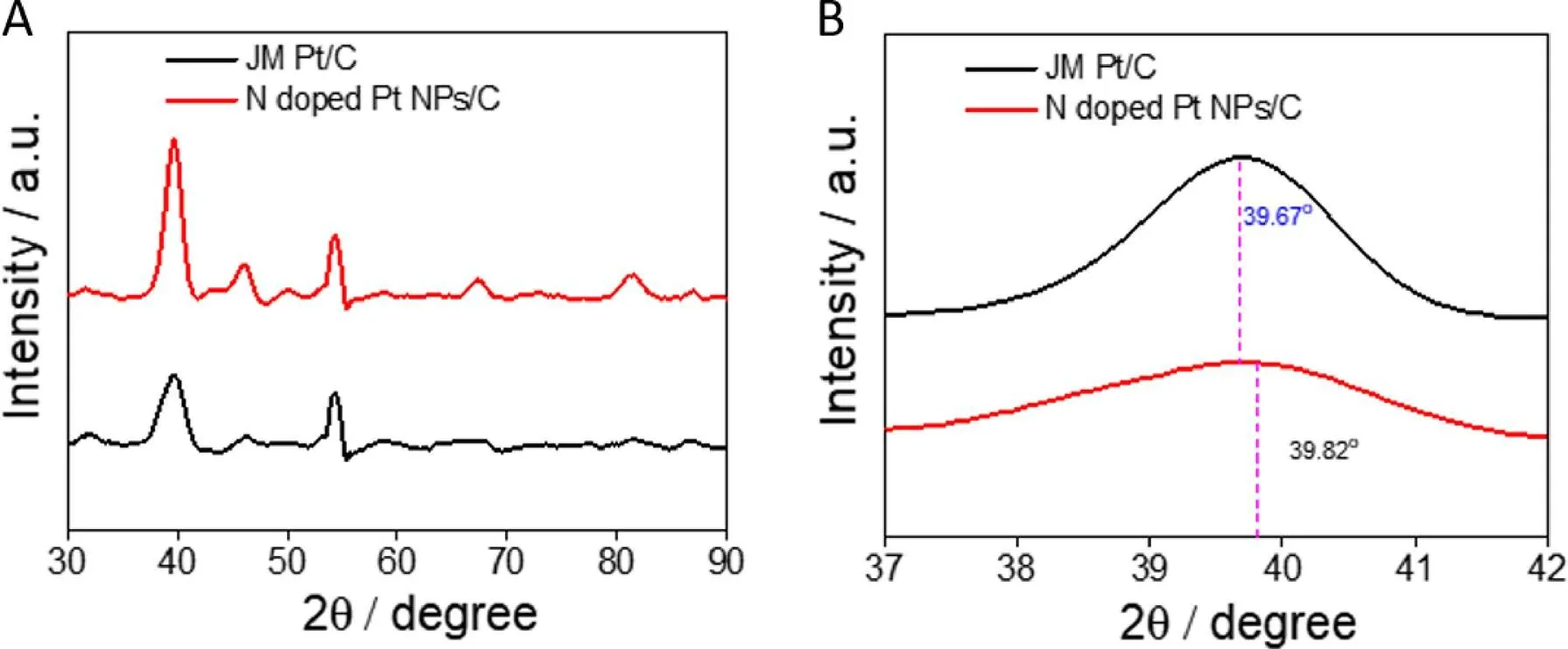
图2 氮掺杂的Pt NPs/C和商业化Pt/C催化剂XRD图(B为A图中37o∽42o范围的放大)
2.3 氮掺杂的Pt NPs/C催化剂透射电镜分析
如图3(A)所示,通过HAADF-STEM表征氮掺杂的Pt NPs/C,可以观察到明显的球状粒子,且形状较为均一。如图3(B—C),通过TEM元素面扫分布,Pt(绿色),N(蓝色),可以清晰地观察到N元素均匀分布在Pt粒子上。如图3(D)所示,从TEM元素面扫分布可得Pt粒子上的N元素的原子含量是6.52%。
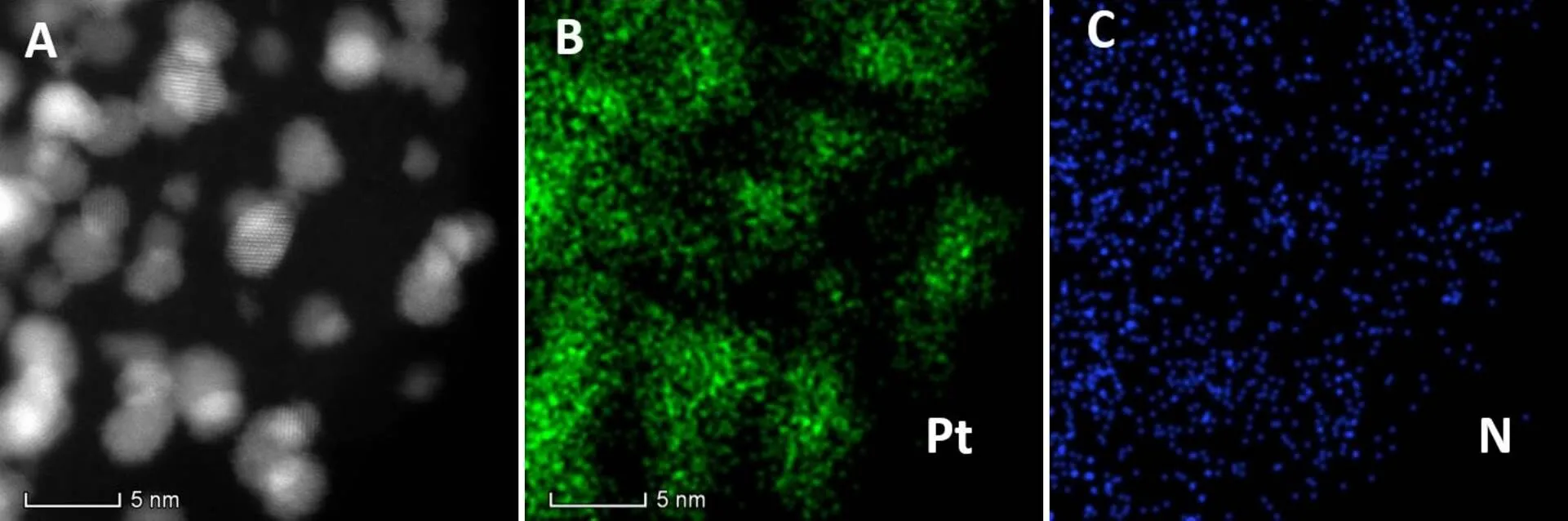
(A)暗场分布;(B)Pt元素分布;(C)N元素分布
2.4 催化剂电化学性能表征
为了评估催化剂的ORR催化活性,实验首先通过循环伏安法(CV)测试了不同催化剂的电化学活性表面积(ECSA),结果如图4(A)所示。图4(A)显示了不同催化剂在25℃下,在N2饱和的0.1 M HClO4溶液中的CV曲线。通过计算可以得到氮掺杂的Pt NPs/C比表面积为68.7m2•g-1,其比表面积与商业化的Pt/C的比表面积72.1m2•g-1相近。
通过线性扫描(LSV)法检测了氮掺杂的Pt NPs/C以及商业化的Pt/C在O2饱和的0.1 M的HClO4溶液中,在0.6∽1.1 V(vs. RHE)下的氧还原极化曲线,结果如图4(B)所示。氮掺杂的Pt NPs/C在0.9 V(vs. RHE)处的动力学电流密度为3.06 mA∙cm-2,高于商业化Pt/C催化剂的2.78 mA∙cm-2,展现出更高的ORR活性。
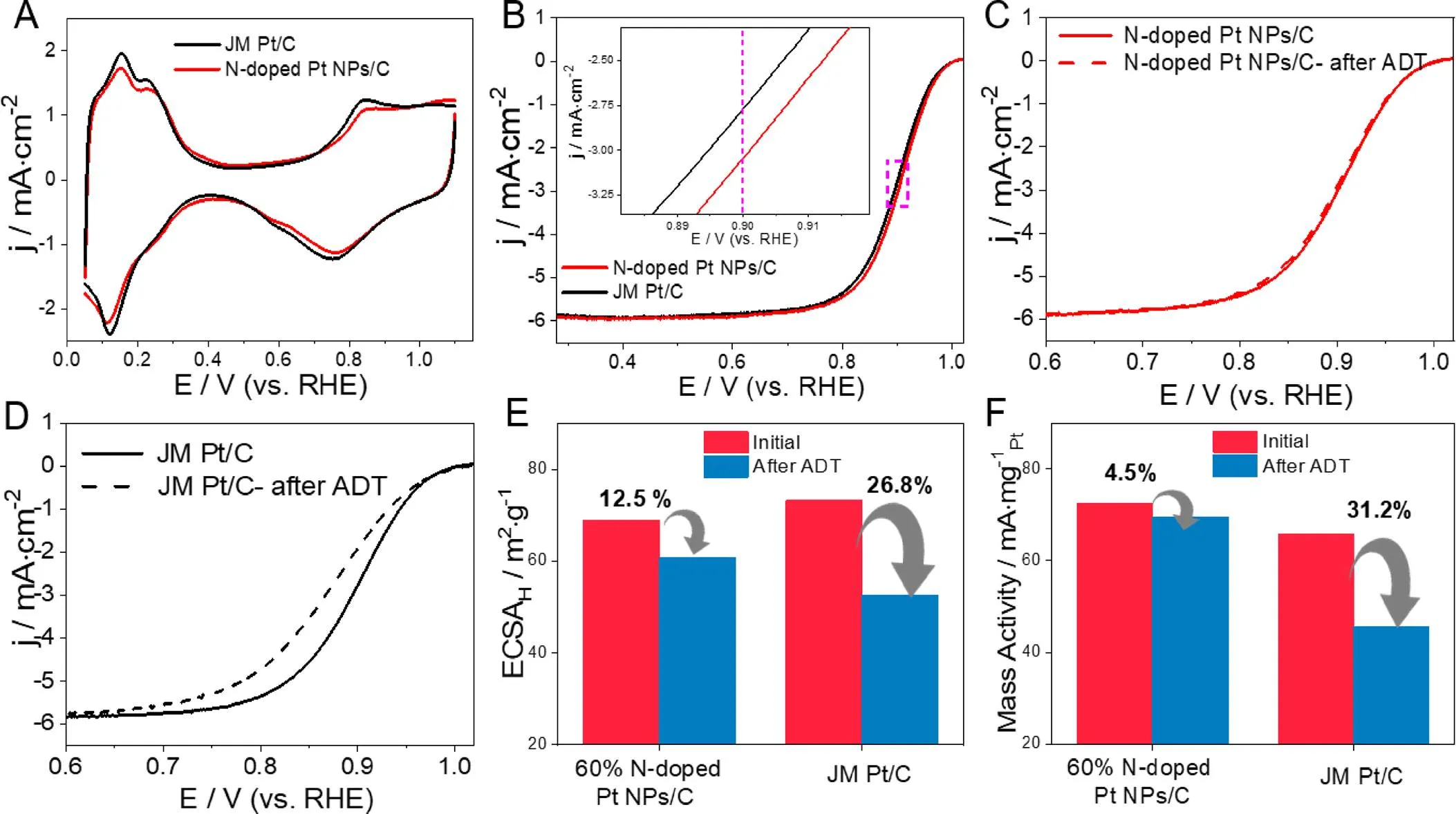
(A)CV图;(B)LSV曲线;(C)ADT前后N掺杂Pt/C的 LSV曲线;(D)ADT前后JM Pt/C的 LSV曲线;(E)ADT前后催化剂ECSA的比较;(F)ADT前后催化剂MA的比较
耐久性是评估ORR催化剂性能的另一个重要指标,具有良好耐久性的电化学催化剂具有更长的使用寿命。为探究氮掺杂的Pt NPs/C催化剂的ORR稳定性,我们在O2饱和的0.1M HClO4溶液中,电位在0.6∽1.1V(vs. RHE)之间,以50 mV•s-1的扫速进行了加速耐久性测试。通过20000圈循环耐久性测试后,由图4(C—D)可得,氮掺杂的Pt NPs/C的半波电位下降比例比商业化的Pt/C的半波电位下降比例更小。通过进一步计算,如图4(E—F)所示,经历了20000圈循环耐久性测试后,氮掺杂的Pt NPs/C的电化学活性比表面积(ECSA)和在0.9V时的质量比活性(MA),分别下降了12.5%和4.5%,远小于商业化Pt/C催化剂的26.8%和31.2%。这些结果证明了氮掺杂的Pt NPs/C具有更好的耐久性。
为了探究N掺杂的Pt基催化剂稳定性提升机理,构建了纯Pt纳米粒子和N原子掺杂的Pt纳米粒子结构模型,如图5(A—B)。密度泛函(DFT)理论计算表明,N原子的掺杂,会使得Pt晶格的晶面间距增大。如图5(C—D)所示,由于电负性大的N原子的引入,使得Pt上的电子转移到N上,Pt原子间因电子斥力而产生的相互作用减弱。与纯Pt相比,N掺杂的Pt纳米粒子中Pt原子间的结合能以及原子脱附能更高,因此在ORR过程中,纳米粒子中Pt原子更难被溶解,稳定性更高。

图5 催化剂理论模拟计算
3 结论
本文探讨PEMFC中铂基催化剂的铂负载量大、耐久度低等问题,通过在铂中掺杂氮元素改变催化材料的性质,以提高铂基催化剂的催化性能。实验利用简单的表面活性剂与聚合物自由合成的方法,得到非金属氮掺杂的铂纳米颗粒。通过XPS、XRD、TEM等表征手段对氮掺杂的Pt NPs/C的物理性质进行表征。利用旋转圆盘电极体系评价Pt NPs/C电化学催化活性。实验结果表明,合成的N掺杂Pt NPs/C催化剂形貌均一,氮元素分布均匀且无明显团聚现象,在0.9 V(vs. RHE)处的动力学电流密度为3.06 mA∙cm-2,经历了20000圈循环耐久性测试后,0.9V处的质量比活性(MA)下降4.5%。其氧还原活性和稳定性均优于商业化的Pt/C催化剂。DFT理论计算表明,由于电负性大的N原子的引入,使得Pt上的电子转移到N上,Pt原子间因电子斥力而产生的相互作用减弱。与纯Pt相比,N掺杂的Pt纳米粒子中Pt原子间的结合能以及原子脱附能更高,因此在ORR过程中,纳米粒子中Pt原子更难被溶解,稳定性更高。本催化剂的成功制备为铂基燃料电池催化剂的实际运用提供了广阔前景。
[1] ZHANG X, LI H, YANG J, et al. Recent advances in Pt-based electrocatalysts for PEMFCs[J]. RSC Advances, 2021, 11(22): 13316–13328.
[2] WANG X X, SOKOLOWSKI J, LIU H, et al. Pt alloy oxygen-reduction electrocatalysts: Synthesis, structure, and property[J]. Chinese journal of catalysis, 2020, 41(5): 739–755.
[3] MA Z, CANO Z P, YU A, et al. Enhancing Oxygen Reduction Activity of Pt-based Electrocatalysts: from Theoretical Mechanisms to Practical Methods[J]. Angewandte chemie international edition, 2020, 132(42): 18490–18504.
[4] WANG X, LI Z, QU Y, et al. Review of metal catalysts for oxygen reduction reaction: from nanoscale engineering to atomic design[J]. Chem, 2019, 5(6): 1486–1511.
[5] SINGH K, TETTEH E B, LEE H-Y, et al. Tailor-Made Pt catalysts with improved oxygen reduction reaction stability/durability[J]. ACS catalysis, 2019, 9(9): 8622–8645.
[6] KUTTIYIEL K A, SASAKI K, CHOI Y, et al. Nitride Stabilized PtNi Core–Shell Nanocatalyst for high Oxygen Reduction Activity[J]. Nano Letters, 2012, 12(12): 6266–6271.
[7] LI X, AN L, CHEN X, et al. Durability enhancement of intermetallics electrocatalysts via N-anchor effect for fuel cells[J]. Scientific reports, 2013, 3(1): 1–6.
[8] AN L, YAN H J, LI B, et al. Highly active N-PtTe/reduced graphene oxide intermetallic catalyst for formic acid oxidation[J]. Nano energy, 2015, 15: 24–32.
[9] ZHANG L L, WEI M, WANG S Q, et al. Highly stable PtP alloy nanotube arrays as a catalyst for the oxygen reduction reaction in acidic medium[J]. Chemical science, 2015, 6(5): 3211–3216.
[10] DENG K, XU Y, YANG D, et al. Pt–Ni–P nanocages with surface porosity as efficient bifunctional electrocatalysts for oxygen reduction and methanol oxidation[J]. Journal of materials chemistry A, 2019, 7(16): 9791–9797.
[11] SUN J, DOU M, ZHANG Z, et al. Carbon nanotubes supported Pt-Co-P ultrafine nanoparticle electrocatalysts with superior activity and stability for methanol electro-oxidation[J]. Electrochimica acta, 2016, 215: 447–454.
[12] LI C, XU Y, DENG K, et al. Metal–nonmetal nanoarchitectures: quaternary PtPdNiP mesoporous nanospheres for enhanced oxygen reduction electrocatalysis [J]. Journal of materials chemistry A, 2019, 7(8): 3910–3916.
[13] DONG Y, ZHOU Y-W, WANG M-Z, et al. Facile aqueous phase synthesis of carbon supported B-doped Pt3Ni nanocatalyst for efficient oxygen reduction reaction[J]. Electrochimica acta, 2017, 246: 242–250.
Preparation of Non-Metallic Doped Pt-Based Catalysts with High Oxygen Reduction Stability and Its Stabilization Mechanism
XIONG Yun-jie1,2, TU Wu-xuan2, WANG Tian-yi2, YAN Gen-ping2
(1. Jiangxi Engineering and Technology Research Center for Environmental Protection Materials and Equipment; 2. School of Materials and Chemical Engineering, Pingxiang University, Pingxiang, Jiangxi 337000, China)
In recent years, the low oxygen reduction stability of cathode catalysts has become a bottleneck limiting the practical application and development of Proton Exchange Membrane Fuel Cells (PEMFCs). In the paper, a non-metallic N-doped Pt nanoparticle was obtained by a simple surfactant-free synthesis method using urea and potassium chloroplatinate as precursors. The physical characterization results clearly show that the doping of N within the Pt lattice leads to the tensile strain of Pt nanoparticles, and the electrochemical test results indicate that this N-doped Pt nanocatalyst has high oxygen reduction activity and stability, and its activity decay after 20,000 cycles of accelerated testing is only 14.4 % of that of commercial Pt/C. The experimental results indicate that the N-doped Pt nanoparticles prepared by this synthetic method offer a promising future for the practical application of fuel cell catalysts.
fuel cell; platinum-based catalyst; oxygen reduction; non-metallic doping
O643.36
A
2095-9249(2021)06-0045-06
2021-11-17
江西省教育厅科学技术项目(GJJ181098)
熊云杰(1991—),男,江西萍乡人,讲师,博士,研究方向:燃料电池催化剂。
〔责任编校:吴侃民〕

