基于电化学热耦合模型的富镍锂离子电池产热分析
李夔宁,谢运成,谢 翌,白庆华,郑锦涛
(1重庆大学低品位能源利用技术及系统教育部重点实验室;2重庆大学能源与动力工程学院;3重庆大学汽车工程学院,重庆400044)
为了减少污染物和温室气体的排放,人们日益关注清洁能源汽车的发展,包括纯电动汽车、混合动力汽车和插电式混合动力汽车,它们比传统的内燃机系统更节能、更环保,被认为是未来交通最可持续的解决方案之一[1]。近年来,锂离子电池由于具有较高的比能量和比功率密度以及标称电压高、自放电率低、循环寿命长、无记忆效应等优异的性能,在新能源汽车开发中得到了广泛的应用[2-5]。
锂离子电池在充放电的过程中会发生电化学反应同时伴随着热量产生,主要包括可逆熵热、极化热、欧姆热、副反应热等[6]。在充放电期间,巨大的温度上升和不均匀的温度分布会大大降低电池组的使用寿命和输出性能,甚至会引起热失控或热安全问题[7-8]。国内外众多学者基于不同的产热模型分析了各种因素对锂离子电池性能的影响。李维平等[9]以商用圆柱形18650 电池为研究对象,利用Bernardi简化生热模型研究了不可逆热、可逆热与电池单体直流内阻的关系,分析得到了不同温度与SOC(state of charge)以及电池单体生热之间的经验关系式。陈军等[10]以18650锂离子电池为研究对象,建立电化学热耦合模型分别从产热角度和散热角度对电池热性能进行了仿真分析,系统地比较了各种因素对温度及温差的影响。Yang等[11]为锂离子电池开发了一种改进的半经验热模型,基于实验拟合方程确定可逆熵热和欧姆热,由锂扩散过程的近似模型得出极化热,改进的模型虽然简化了电池发热率的计算过程但内部产热特性却无法分析。Du等[12]研究了高放电速率下软包装磷酸铁锂电池的热行为,分析了不可逆热产生的规律和不同电极材料颗粒形态下的热演化。结果表明,不可逆热量的产生随着放电速率的增加而迅速增加,而极化热量的产生是主要的影响因素。Amiribavandpour 等[13]提出了一种改进的理论电化学热模型准确预测了锂离子电池组内锂离子电池的发热率、散热率和温升,并用实验数据验证了该模型在恒放电电流时的准确性。
综上所述,国内外众多学者主要关注于磷酸铁锂和低镍三元锂等电池的产热估算与分析,事实上富镍锂离子电池[LiNixCoyMnzO2(x≥0.5)]由于具有较高的镍含量会使得循环性能变差、热稳定性降低[14],给实际使用带来一定的安全隐患,然而针对富镍三元锂离子电池热行为的影响研究尚不够充分。因此,本文选取富镍三元锂离子电池为对象,基于动态参数响应及正交各向异性导热系数完善了电化学热耦合模型,分别从宏观角度对电池产热进行了定性分析,从微观角度对生热来源速率进行了定量分析,研究结果能够为锂离子电池的热性能评估和电池组的热管理系统设计提供一定的指导意义。
1 模型建立与验证
1.1 电化学模型
工作以市售某50 A·h富镍方形硬壳锂离子电池为研究对象,其正极材料为LiNi0.5Co0.2Mn0.3O2,负极材料为石墨,电解液体系LiPF6/EC∶EMC 比例为3∶7。锂离子电池的工作过程一般包括内部电化学反应和发热过程。因此,锂离子电池模型的开发应同时考虑电化学反应和传热两方面。采用Newman 等[15-16]基于多孔电极理论和浓溶液理论提出的电化学模型,包括质量守恒、电荷守恒和电化学动力学方程。本文建立的伪二维模型如图1所示。该模型包括五个部分:正极集流体、正极、隔膜、负极和负极集流体。其中在模型建立过程中做出了如下假设:①多孔电极活性物质是尺寸均匀的球形颗粒;②不考虑双电层效应和副反应;③忽略集流体上的接触电阻;④充放电过程中不产生气体。

图1 锂离子电池伪二维模型结构示意图Fig.1 Structure diagram of pseudo two dimensional model of Li ion battery
本研究电化学模型控制方程中所用到的参数主要包括电池结构设计参数、电化学性能参数及动态响应参数。结构设计参数通过厂商提供与实验测量获取,电化学性能参数及动态响应参数参考相同体系电池文献,详细参数类型[17-20]及其取值如表1所示。
正、负电极材料平衡电势与熵热系数分别取自文献[21-22],见图2。
电化学参数的准确性直接影响模型的准确以及合理性,考虑到固液相扩散系数、离子电导率等参数与温度、浓度相关性较大。因此,对模型中动态响应参数进行精确的描述以提高模型准确性。动态响应参数表达式分别如式(1)~(4)所示。
离子电导率

正极固相扩散系数

负极固相扩散系数

液相扩散系数

1.1.1 固相电荷守恒
固体电极材料中的电荷守恒方程式(5)遵循欧姆定律。σeff为固相中的有效电导率;ϕs为固相中的电势;as为粒子的比表面积;F为法拉第常数;j为局部电流密度。在外边界(x = 0,Lp+ Lsep+ Ln),电荷通量等于施加的电流密度iapp,如式(6)所示,而在内边界(x = Lp,Lp+ Lsep)没有电荷通量,如等式(7)所示。

表1 电池结构设计与性能参数Table 1 Battery structure design and performance parameters

图2 负、正电极材料平衡电势与熵热系数Fig.2 Equilibrium potential and entropy heat coefficient of negative and positive electrode materials

1.1.2 液相电荷守恒
电解质相的电势守恒由式(8)给出,式中κeff为有效离子电导率;ϕe为电解质相电势;t+为锂离子迁移数;R 为摩尔气体常数;ce为电解质相的锂离子浓度,在正负集流体处边界条件为零通量。

1.1.3 固相锂离子质量守恒
锂离子在电极活性材料球形颗粒中的质量守恒用菲克第二扩散定律描述,如式(10)所示。cs为电极颗粒内部固相锂离子浓度;Ds为固相扩散系数;r 为球形颗粒粒子半径,锂离子在粒子中心的通量为0,如式(11)所示。而表面的通量(r=Rs)由电化学反应的局部电流密度决定,如等式(12)所示。


1.1.4 液相锂离子质量守恒
电解质相的锂离子浓度分布遵循式(13),εe为电解质相的体积分数;Deffe为有效电解质相扩散系数,如式(14)所示,电解质相中锂离子通量在外边界(x = 0,Lp+ Lsep+ Ln)处设为0,而在内边界(x =Lp,Lp+ Lsep)处的锂离子浓度被认为是连续的。

1.1.5 电化学动力学


1.2 传热模型
电池的热物性参数是热仿真必不可少的输入,且电池导热系数值直接影响电池的散热特性,直接影响计算结果的准确程度。考虑到根据其电芯内部串并联特性分别计算电芯垂直和平行方向的导热系数值不能完全代表电池的物性参数。因此本文基于文献[23]提出的仿真和热网格模型法获取电池3 个方向的等效导热系数值及相关热物性参数。

表2 热模型参数Table 2 Thermal model parameters
锂离子电池的传热模型涉及能量平衡方程、产热方程、散热方程。能量平衡方程式可以给出电池内的温度分布表示为式(19)。其中Q̇为总产热速率;Qp、Qr和Qj分别代表活性极化热、反应热和欧姆热;ρbat是电池平均密度;Cp是电池平均比热容,h是电池与环境之间的综合对流系数;abat是电池的比表面积,Tamb是环境温度。
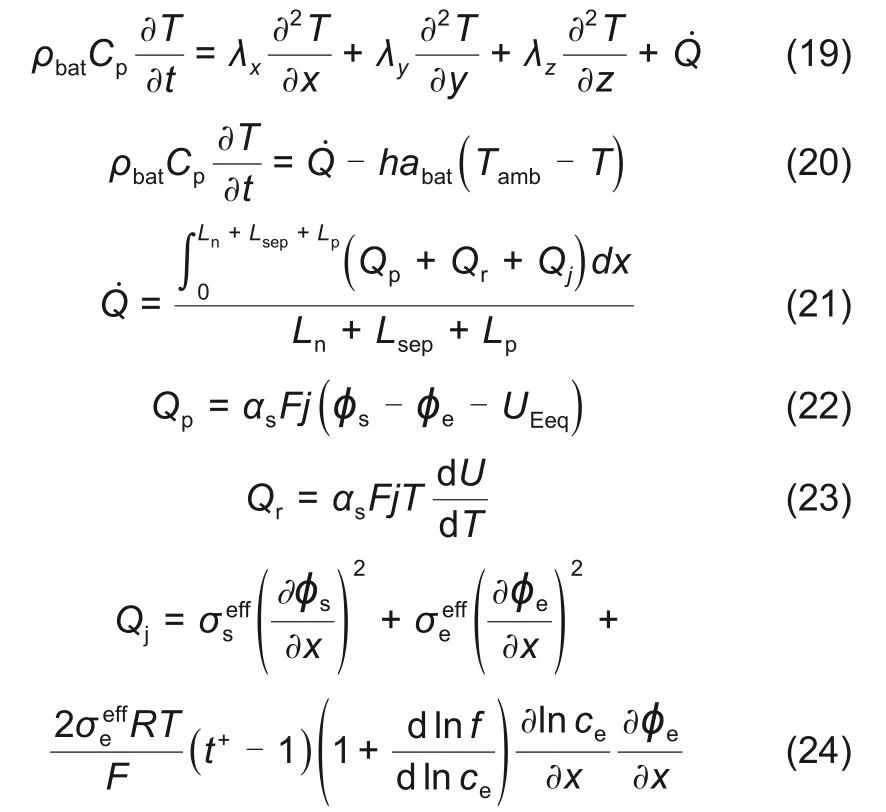
1.3 电化学-热耦合关系
模型耦合机理是将一维电化学模型中计算的热源耦合到三维热模型中引起热模型中的温度变化。热模型反馈到电化学模型中导致与温度相关的参数发生变化,并用Arrhenius 公式(25)定量描述,两者相互耦合关系如图3所示。
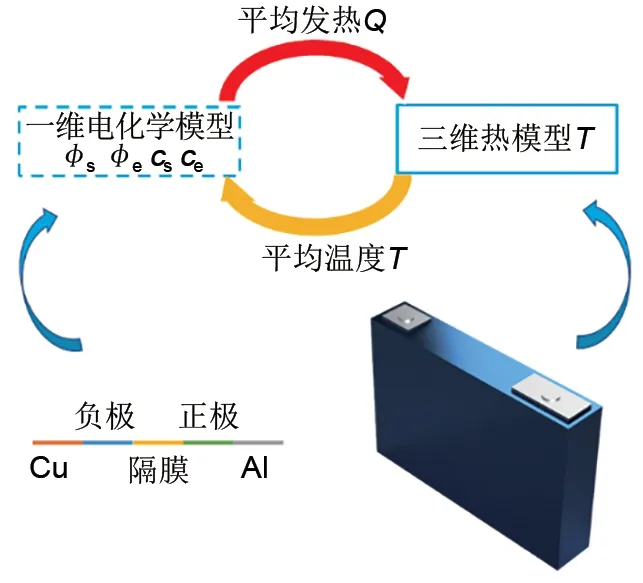
图3 电化学热耦合关系示意图Fig.3 Schematic diagram of electrochemical thermal coupling relationship

式中,Y 代表与温度有关的参数;Yref为参考温度Tref下的参数值;Ea,Y为与参数Y 相对应的活化能。
1.4 模型精度验证
为了验证电化学热耦合模型的精度,试验采用CK-150G型可程式恒温恒湿设备、新威BTS-8000型充放电测试仪、34972A 型安捷伦数据采集仪、并将K 型热电偶按照如图4 所示布置在电池表面,对电池按照表3所示的测试步骤进行充放电测试并记录试验测试的数据,然后分别进行电化学和热性能验证进而验证耦合模型的精确性和可靠性。

图4 实验测试平台Fig.4 Experimental test platform
电化学验证如图5 所示,在0 ℃和40 ℃环境温度下,0.3 C、1 C仿真与实验放电曲线之间的对比图显示出很好的一致性。其中0 ℃放电曲线验证图最大相对误差为2.21%,40 ℃放电曲线验证图最大相对误差为3.97%。
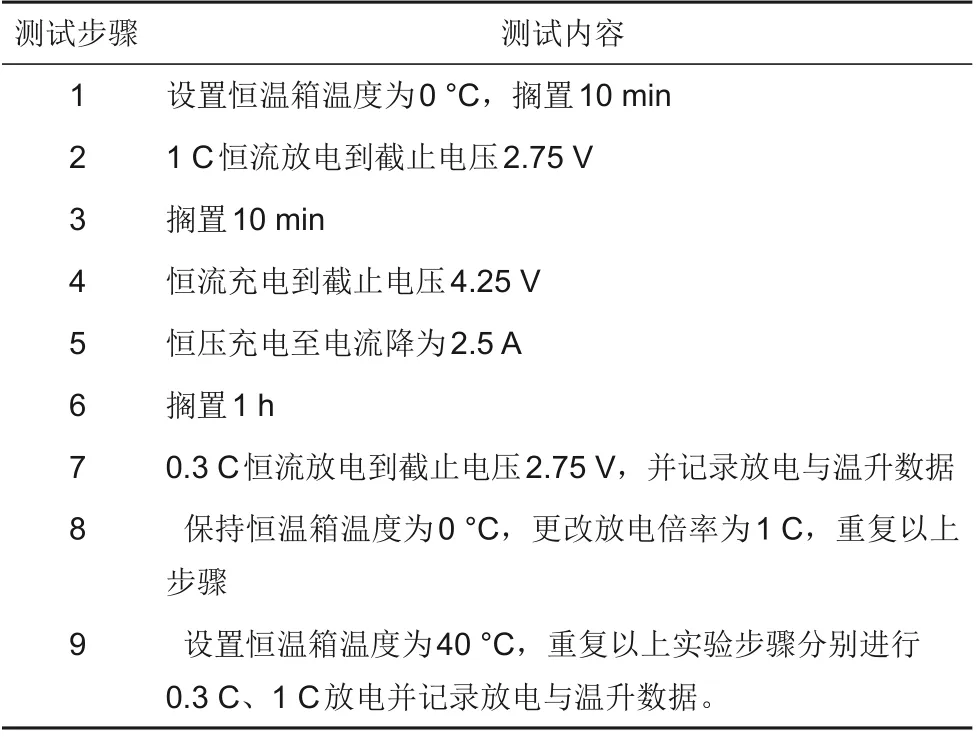
表3 电池充放电试验测试步骤Table 3 Battery charging and discharging test steps
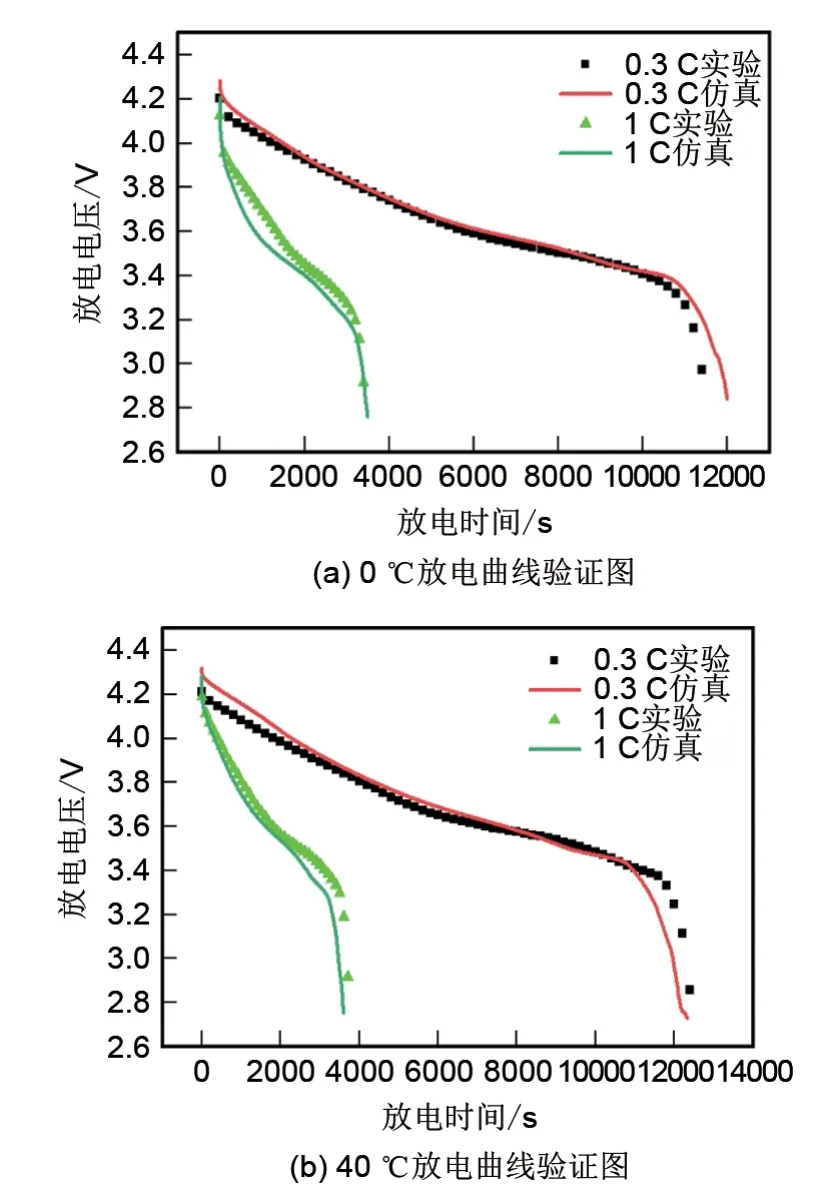
图5 0 ℃和40 ℃环境温度下0.3 C、1 C放电曲线验证图Fig.5 Verification diagram of 0.3 C and 1 C discharge curves at ambient temperatures of 0 ℃and 40 ℃
热性能验证如图6所示,在0 ℃、40 ℃环境温度下,仿真与实验温升曲线基本吻合。在0 ℃环境温度下,0.3 C 放电温升最大相对误差为3.15%,而在40 ℃环境温度下,放电温升最大相对温差仅为1.16%,整体吻合度优于文献[24]中(5 ℃最大相对误差约为9.81%,55 ℃最大相对误差约为1.42%)建立的电化学耦合模型。
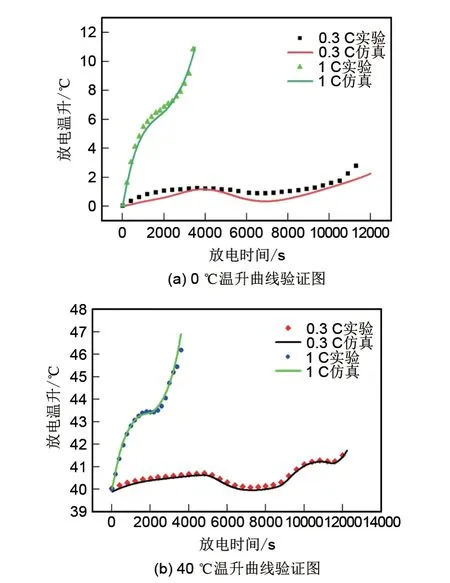
图6 0 ℃和40 ℃环境温度下0.3 C、1 C温升曲线验证图Fig.6 Verification diagram of 0.3 C and 1 C temperature rise curves at ambient temperatures of 0 ℃and 40 ℃
考虑到本文仿真所选取的部分电化学与热参数来自于相同类型电池体系的参考文献与实际研究电池参数存在些许偏差,且在模型建立过程中忽略了电池内部对流传热以及与外界的辐射传热等因素的影响使得模型精度存在部分偏差。总体而言,本研究所建立的电化学热耦合模型能够准确地分析电池热特性。
2 结果分析与讨论
2.1 锂离子电池温升特性分析
2.1.1 放电倍率对锂离子电池温升特性的影响
为了研究放电倍率对单体电池温升特性的影响,考察了环境温度为20 ℃、对流换热系数为20 W (m2·K) 的状况下,单体电池分别以0.3、0.5、1、2 C 不同倍率放电到截止电压情形下的温升变化,其仿真结果如图7所示。
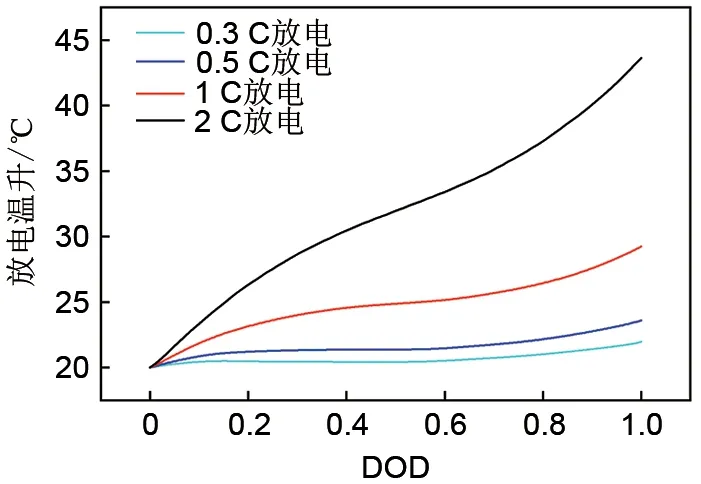
图7 不同放电倍率下电池温升变化Fig.7 Temperature rise of battery under different discharge rate
当电池以0.3、0.5、1 C 放电时,随着放电的进行电池温度曲线呈S 型变化趋势。当电池以2 C放电时,随着放电深度的增大,电池温升近似线性增长。放电结束后电池的表面平均温升随着电池的放电倍率增大而提高分别为:2、3.7、9.5、23.7 ℃。这是由于当电池以低倍率放电时电池发热量较小、可逆热占比较大、欧姆热占比较小,电池可以进行很好的散热,而当放电倍率提高时电流增大,电池产生的反应热以及欧姆产热增加,外部自然对流换热不足以将产热导出导致电池温度升高。电池内部的温度差也随着电池放电倍率的提高而增大,分别是0.2、0.4、0.9、2.1 ℃。
2.1.2 环境温度对锂离子电池温升特性的影响


图8 不同环境温度下电池温升变化Fig.8 Changes of battery temperature rise under different ambient temperatures
由温升图可分析出随着放电深度的增加,单体电池温度基本呈S型变化趋势增加。当环境温度分别为0、10、20、40 ℃时,1 C放电时温升分别为10.9、9.8、9.5、8.2 ℃,当以2 C放电时温升分别为26.9、25.1、23.7、21.1 ℃。即随着环境温度的升高,电池的温升不断降低。这是由于电池在低温条件下放电时电解液黏度的增加导致锂离子在电解液中的扩散系数降低,极化内阻增加产生的极化热增加,在对流换热系数不变的情况下,低温环境下的温升更高。
2.1.3 对流换热系数对锂离子电池温升特性的影响


图9 不同对流换热系数下电池温升变化Fig.9 Temperature rise of battery with different convective heat transfer coefficient
从图9可以看出,绝热情况下电池温升近似线性增长,放电结束末期电池温升为24.7 ℃。自然对流、强制风冷、强制液冷工况下电池温度变化趋势基本呈现一致,放电结束电池温升分别15.8、6.4、3.6 ℃。此外,随着对流换热系数的增大,整个放电过程电池的温升越慢,放电结束阶段电池的温度越低。这是因为绝热情况下电池与外界散热为零,电池温升较大。而随着对流换热系数的提高,电池与环境的换热量增大,从而使电池的温度降低。
2.2 电池内部产热机理及特性分析
2.2.1 不同性质产热沿电极厚度分布曲线
锂离子电池是由多层重复结构层叠或卷绕而形成因而使得内部产热较为复杂,所研究的不同性质的产热包括总产热、可逆熵热、不可逆极化热、不可逆欧姆热是基于锂离子电池内部发生的电化学反应给出的具体的产热计算公式见上。为了研究锂离子电池在放电过程中的不同性质产热沿电极厚度方向的分布趋势,通过设定模型环境温度为20 ℃,分别考察1 C 放电下不同时刻(t=10、900、1800、2700、3600 s)时电极的总产热率、可逆熵热、极化热和欧姆热沿负极、隔膜、正极分布情况。
从图10 可以看出,不同放电时刻下电极总产热曲线沿负极、隔膜、正极区域的分布趋于一致。负极区域总产热率分布较为平缓、正极区域总产热率呈非线性增长并随着放电的进行产热量逐渐增大。主要原因是,随着反应的进行锂离子浓度发生变化,放电期间在正极活性区域内产生较大的欧姆热梯度,加之沿厚度方向导热系数较小易产生一定的温度梯度。相较于电极区域产热,由于隔膜区域仅存在液相欧姆热且总产热率较小同时无显著变化,表明隔膜区域总产热较小可以忽略。负极与隔膜交界处相比正极与隔膜交界处总产热率高,这主要是因为负极与隔膜交界处的反应较为剧烈。此外,对比图10(a)和图10(b)可以看出1 C 放电下,电极不同区域欧姆热与电极不同区域总产热分布趋势较为相似且正极区域欧姆产热量比负极区域欧姆热量大并且接近总产热量。这主要是由于电极材料的自身特性,即石墨负极材料的热阻率远低于正极三元材料的热阻率[25]。

图10 1 C放电下电极总产热、欧姆热沿电极厚度分布曲线Fig.10 Distribution curve of total heat production and ohmic heat along electrode thickness under 1 C discharge
从图11(a)可以看出电极可逆熵热仅存在正负极区域,负极区域的可逆熵热变化较为平缓,放电初期其值为负,伴随着放电的进行其值增大并在放电末期达到最大值。而正极区域的可逆熵热放电初期沿厚度方向一直增加伴随着放电的进行逐渐减小,产生上述的现象主要是由于正负极熵热系数具有较大的差异性。另外,由图2可知负极材料熵热系数dUn·dT 变化范围为-0.16~0.3 mV/K,正极材料熵热系数dUp/dT 变化范围为0.008~0.202 mV/K,最终导致负熵变化比正熵变化更显著从而产生较大的差异性[26]。从图11(b)可以发现电极厚度方向不同位置处存在极化差异,隔膜中心处由于未进行电化学动力学反应因此极化产热为零,负极区域内产生的极化热远大于正极域内产生的极化热,这主要是因为电池放电过程,负极在发生脱锂反应过程中产生的极化热远大于正极发生嵌锂反应过程中所产生的极化热[27]。

图11 1 C放电下电极可逆熵热、极化热沿电极厚度分布曲线Fig.11 Distribution curve of reversible entropy heat and polarization heat along electrode thickness under 1 C discharge

图12 1 C、2 C放电下不同区域产热随放电时间分布曲线Fig.12 Distribution curve of heat production in different areas with discharge time under 1 C and 2 C discharge
2.2.2 不同区域产热随放电时间分布曲线
通常情况下,可逆和不可逆热产生对内部总热量产生的贡献随放电倍率的变化而变化。为明确不同放电倍率下电极的不同区域产热随放电时间变化的产热规律。基于产热模型得到了环境温度为20 ℃、放电倍率1 C、2 C下的电池正负极区域产热随放电时间分布的曲线,如图12所示。
从图12 可以看出,不同倍率放电时正负极产热曲线差异较大。其中放电初期,负极区域总产热较为平缓,正极区域总产热较为迅速,且正极总产热占主导位置导致电池整体温度迅速升高。放电中期,正负极总产热速率均较为平缓,对应的电池温度缓慢上升。放电末期,正负极总产热曲线快速上升电池温度达到最高。此外,随着放电倍率的增大,正极区域欧姆热占比也有较大的提升,负极的极化热相对于负极占比较高。这主要是因为极化热是由电化学极化和浓差极化产生的,放电倍率较大时电子不能及时地转移,极化内阻迅速增大,导致极化热增加。
3 结 论
本文以富镍方形三元锂离子电池为研究对象,建立了动态参数响应的电化学热耦合模型,从宏观角度对电池产热进行了定性分析,从微观角度对生热来源速率进行了定量分析,并深入探讨了放电过程的热特性变化规律及产热机制,主要得到以下结论与建议。
(1)放电倍率的增大使得电池温升近似线性增长并增大了内部的温差,环境温度和对流换热系数的增大使得温升下降。建议提前预估电池的产热量级并采取合适的冷却方案进行及时散热。
(2)负极区域总产热分布较为平缓,隔膜区域总产热较小可以忽略,正极区域总产热率接近电极总产热量。放电过程中应重点关注正极区域的产热,并给予有效的散热措施改善电池的均温性。
(3)增大放电倍率使得正极区域欧姆热急速增加,负极区域极化热显著提高。放电初期,正极总产热占主导,放电中期,正负极总产热较为平缓。放电末期,正负极总产热迅速。可考虑在电池使用过程中不完全放电来减小电池热量大幅上升,避免产生热安全问题。

