石榴石型Li7La3Zr2O12固态锂金属电池的界面问题研究进展
张赛赛,赵海雷
(1北京科技大学材料科学与工程学院;2新能源材料与技术北京市重点实验室,北京100083)
作为目前应用最广泛的二次储能装置之一,锂离子电池具备高电压、高能量密度、自放电程度低、无记忆效应等优点。然而,基于目前的锂离子电池材料体系和结构形式,锂离子电池的能量密度已经接近其理论值上限300 W·h/kg,要实现下一代电池500 W·h/kg能量密度目标,必须发展新的电池材料体系。此时,具有最低电化学电位(-3.04 V)和最高质量比容量的金属锂(3860 mA·h/g)重新受到研究者的关注。早在20世纪70~80年代,锂金属作为负极匹配无锂的TiS2、MoS2或MnO2等正极材料和有机电解液,构建了二次电池[1]。但是此类电池在循环过程中库仑效率低,容易形成锂枝晶,造成电池内部短路,引发燃烧甚至爆炸的安全事故。因此,锂金属电池的应用一直面临巨大挑战。而利用固态电解质取代有机电解液构建的固态锂电池,可以有效阻挡锂枝晶、实现电池更高的安全性,同时由于省去隔膜的使用,有望实现更高的电池能量密度。
锂离子固态电解质主要包括无机陶瓷类、聚合物和复合物三类。无机陶瓷类固态电解质因其具有较高的机械强度,被认为能够较好地抑制锂枝晶的生长。同时这类固态电解质通常具有更宽的电化学窗口和较高的室温锂离子电导率。石榴石结构Li7La3Zr2O12(LLZO)作为典型的氧化物锂离子固态电解质,具有10-4~10-3S/cm 的离子电导率,接近1的锂离子迁移数,较宽的电化学窗口、良好的对锂稳定性和热稳定性[2]。由于LLZO 的离子电导率仍不及有机电解液,早期开展的研究内容主要集中于LLZO 锂离子电导率的提高,包括:在Li、La、Zr等不同位置掺杂异价元素,稳定高离子电导立方相;掺杂大半径离子优化晶胞参数,掺杂异价离子调整载流子浓度;优化材料致密化工艺,包括添加助烧剂,改善烧结气氛和坩埚材质,利用先进烧结技术等提高材料的离子电导率。LLZO 材料性能不断提高的同时,针对固态电解质的研究重点也逐渐从材料设计与开发转移到电池应用。
LLZO 固态锂金属电池最主要的问题之一是电解质/电极界面问题。由于LLZO具有陶瓷固体的刚性特点,无法像有机电解液一样充分接触固态电极材料,因此电池具有较大的电解质/电极界面电阻。LLZO 和目前常用正极材料在高温下互反应限制了电极的制备方式,同时,二者在电池循环过程的元素互扩散等材料兼容性问题,复合正极内部以及正极与电解质之间电荷转移受阻等问题,会导致正极界面电阻过大;锂金属负极对LLZO浸润性差导致的物理接触问题,也会产生较大界面电阻,影响电池充放电性能。因此,基于石榴石型锂离子固态电解质的全固态电池技术,还面临很大的挑战。
本文围绕石榴石结构LLZO 锂离子固态电解质在固态锂金属电池中的应用,综述了包括LLZO电解质的电化学窗口,LLZO 与正负极界面的主要问题以及相应的解决思路和技术手段。作为氧化物无机陶瓷电解质的典型代表,LLZO/正负极界面的研究策略和经验能够为不同类型的陶瓷固态电解质的研究和应用所借鉴,进而促进无机陶瓷固态电池的技术进步和实际应用。
1 LLZO电化学窗口
早先的研究提出用已占有电子的最高能级轨道(highest occupied molecular orbital,HOMO)和未占有电子的最低能级轨道(lowest unoccupied molecular orbital,LUMO)描述电解质溶剂分子的电化学窗口。但是HOMO 和LUMO 适用于描述孤立分子的电子性质,其数值并不等同于物质参与氧化还原反应的能量状态,不能用于限定电解液或固态电解质的电化学窗口[3]。锂离子电池的开路电压在数值上等于正负极电化学势之差,即VOC=μC-μA。电解质的电化学窗口等于其在负电位下的还原电位和在正电位下的氧化电位所限定的电压范围。固态电解质的电化学窗口越大,意味着其抵抗负极还原和正极氧化的能力越强,能够匹配μC更大μA更小的电极材料,从而有望实现更高的电池能量密度。固态电解质电化学窗口对应的氧化还原电位,可由相应氧化还原反应的吉布斯自由能变化确定[3]。
此前的研究普遍采用循环伏安法,组装Li|LLZO|阻塞电极构型的电池测试LLZO 固态电解质的电化学窗口。实验结果表明这类电解质能够达到0~6 V,甚至更高电压的电化学窗口。但是,第一性原理计算LLZO电解质热力学稳定的电化学窗口远小于文献中报道的数值,为0.05~2.91 V[4]或0.07~3.2 V[5]。为了研究LLZO 在高电位下的抗氧化性能,混合质量比为40:60 的C 包覆的LLZO 和石墨,用于改善LLZO和半阻塞电极的接触,制备Li|LLZO|LLZO-C 电池进行CV 测试,4 V 左右就出现了氧化峰[6]。类似的工作利用Ta 掺杂的LLZO(LLZTO)组装Li|LLZTO|(LLZTO+C)电池进行CV测试,发现了2.9 V 左右的氧化峰,结合计算结果认为是电解质材料和C 反应生成CO2或者Li2CO3所致[7]。因此LLZO的氧化电压还有待进一步的确认,引入非碳材料的金属粉体作为复合正极的导电剂有望提供实验论证。
计算发现低电位下LLZO 还原反应的反应自由能绝对值非常小,因此很有可能在动力学上无法实现,同时反应产物Li2O、Zr3O 和La2O3也可能会形成中间层阻碍反应持续进行。利用磁控溅射、电子束气相沉积和电化学沉积三种方式在Al掺杂LLZO表面沉积锂,制备过程中的XPS 检测到了Zr2+和Zr0的存在,说明LLZO会被锂负极还原,并且发现这一过程的确存在动力学障碍[8]。实际过程中存在的动力学因素可能是实验结果显示LLZO对锂稳定的主要原因。
动力学过程缓慢,导致电极电解质界面形成较高的过电势,或者是由于生成的氧化还原产物,物理阻隔了电解质和电极接触,界面产物拓展了固态电解质的氧化还原电位,如图1所示,使固态电解质的表观电化学窗口变宽[4]。固态电解质的电化学稳定窗口,除了与材料本征性质决定的热力学因素有关外,还与电极反应的动力学因素有关。借鉴电解质电极界面反应中间相拓宽电解质电化学窗口的思路,人为设计电解质-电极中间层,可稳定电极/电解质界面,拓宽电解质电化学稳定窗口,同时降低界面电阻,实现全固态电池的长效工作特性。

图1 全固态锂离子电池的电化学窗口原理图[4]Fig.1 Schematic diagram about electrochemical window in all-solid-state Li-ion battery[4]
2 LLZO/正极界面
如图2所示,固态电解质和正极之间主要存在两种界面:第一种是在复合正极中固态电解质和正极材料之间的界面;第二种是复合正极和固态电解质之间的界面。由于锂金属负极本身具有良好的电子电导,固态电解质-锂金属负极界面通过良好物理接触就能够实现电极反应所需的锂离子和电子传导,而固态电解质-正极界面需要添加导电剂以同时满足锂离子和电子传导,这使得正极界面的结构更为复杂,相应的界面电阻远大于负极界面,对固态电池性能的提高也更为关键。在复合正极内部,固态电解质和固态正极活性物质之间离子传输势垒较大,界面电阻高,使得电池的放电比容量较低。因此复合正极中不仅要添加离子、电子导电相,还需要提高材料的致密度,以形成正极材料中锂离子和电子的渗流通道;与此同时,还需要提供一定的缓冲空间,应对活性物质脱嵌锂过程出现的体积变化,维持内部界面良好结合。
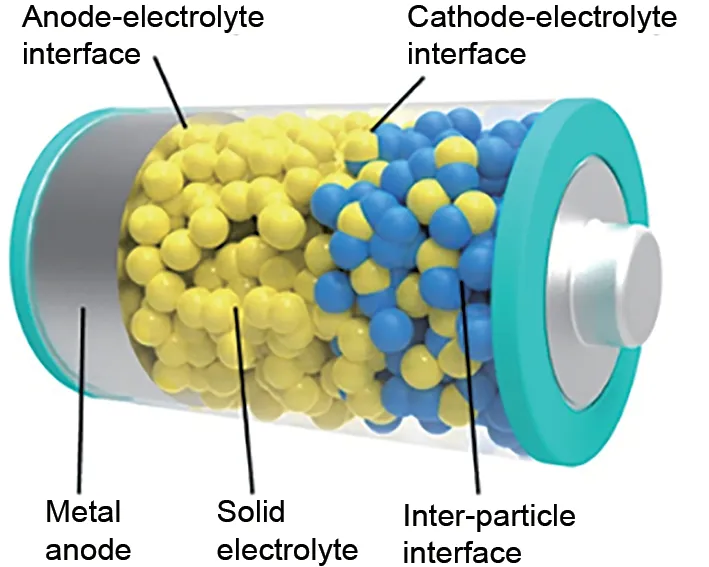
图2 固态锂电池的不同界面[9]Fig.2 Schematic of different interfaces in solid-state batteries[9]
正极/LLZO 固态电解质界面的主要问题包括:①材料兼容性,涉及到正极材料的匹配问题,包括制备过程和电池循环过程可能出现的副反应等;②界面电荷转移电阻大,主要原因包括:界面副反应生成的产物;电解质电极有效物理接触少;电池充放电过程正极脱嵌锂,体积反复变化造成界面破坏等等。
2.1 正极界面兼容性
为特定的固态电解质例如LLZO 匹配正极材料,首先需要考虑材料的兼容性问题,这一问题在复合正极制备和电池循环过程中都会出现。正极和电解质反应产生的界面副产物通常具有较差的电子和离子传导能力,阻碍电极反应的发生,增大界面电阻;同时也消耗了活性物质,破坏电池结构,进一步影响电池性能。由于氧化物固态电解质的陶瓷刚性,需要通过高温热处理的方式实现电解质与复合正极的结合。但是,热处理促进烧结、加强正极界面连结的同时,也易造成LLZO和正极材料界面发生元素互扩散[10],导致LLZO 发生相变[11],或一系列绝缘产物的形成[12]。第一性原理计算显示,LLZO和不同正极材料(LiFePO4、LiCoO2、LiMnO2)在接近LLZO本征电化学窗口的上限值附近,最有可能发生副反应。相比于其他两种正极,LLZO 和LCO 发生副反应的驱动力最小,两者兼容性最佳[13]。
通过在电解质和正极中间引入中间层的方式,可以避免两者的直接接触,抑制副反应发生和绝缘相生成,从而降低界面电阻。中间层的引入,可以是对电解质的表面修饰[11,14],也可以通过对正极包覆[15-16]的方式实现。
2.2 电解质/正极界面电阻降低策略
正极和电解质的结合通常是将制备好的正极和固态电解质直接复合,然后涂覆于或压制于电解质表面,进行高温处理,因此结合效果会受到正极材料颗粒形貌、煅烧温度等因素的影响,高温还易引起正极与电解质间的化学相容性问题。通过在正极中加入低熔点物质,如Li3BO3[17-18],可以有效降低热处理温度,缓解界面化学反应,同时加强界面结合,降低界面电阻。直接在固态电解质和正极中间引入柔性聚合物[19]、凝胶[20]电解质薄层,可显著改善界面结合,降低界面电阻,并省去高温热处理步骤。设计三维结构固态电解质[21],可以增加电极/电解质接触面积,降低界面电阻。此外,在复合正极中引入聚合物电解质[22]、凝胶电解质[23]、离子液体[24]或液态电解质[25]等,可以提高正极内部的离子传导,同时优化电解质和正极之间的界面接触,促进电极反应动力学,降低正极界面电阻。Doef等[26]利用冷冻流延法制备了多孔LLZO电解质骨架[图3(a)],单向孔隙有利于正极浆料的渗入,有效缩短锂离子扩散路径。此外,通过填充柔性复合固态电解质连结正极和LLZO骨架,可有效避免高温烧结以及有害副反应。Han 等[27]利用低熔点的Li2.3C0.7B0.3O3(LCBO)与LLZO和LiCoO2表面的Li2CO3发生反应,700 ℃热处理后生成一种LCBO 的固溶相Li2.3-xC0.7+xB0.3-xO3。Li2.3-xC0.7+xB0.3-xO3不仅作为焊料连结了两种材料,同时也提高了界面离子电导率,该复合正极形貌和元素分布如图3(b)所示。但是这种LCBO的固溶相电子电导率较低,可以引入具备电子电导的材料进一步改善正极内部的电子传输,加快电极反应动力学。在复合正极浆料的制备中除了添加导电剂和黏结剂之外,锂盐LiTFSI 与黏结剂PVDF共同作用可作为一种聚合物锂离子导体。引入锂盐LiTFSI的黏性正极浆料能够与LLZO电解质紧密结合,在60 ℃下电池0.05 C 稳定循环100 圈后仍能保持93%的比容量为100 mA·h/g。[28]

图3 正极渗入多孔致密双层LLZO后的照片和断面SEM(a)[26],复合正极Li2.3C0.7B0.3O3+LLZO@Li2CO3+LCO@Li2CO3烧结前后SEM(b)[27]Fig.3 (a)optical and SEM images of cathode-infiltrated LLZO bilayer[26];(b)SEM images of Li2.3C0.7B0.3O3+LLZO@Li2CO3+LCO@Li2CO3 cathode composite before and after sintering[27]
此外,制备LLZO-聚合物复合电解质也能改善界面接触,这类复合电解质虽然牺牲一部分离子电导率和热稳定性,但是能够发挥聚合物柔性的优势,避免正极/电解质界面电阻过大,同时还改善了电解质的成膜加工特性。在聚合物如PEO 中加入的陶瓷颗粒,能够作为交联中心,抑制PEO 结晶,促进链段运动,从而提高聚合物电解质的锂离子电导率[29-30]。实验表明这类复合电解质中,锂离子的迁移路径倾向于穿过LLZO 陶瓷相[31],LLZO相的具体组分和形态也会对复合电解质的总离子电导产生影响。
3 LLZO/锂负极界面
金属锂对LLZO 的润湿性较差,从而引起负极侧电极界面电阻较大。同时,负极侧金属锂的不均匀沉积也会引起锂枝晶的产生,造成电池安全隐患。因而,提高金属锂对LLZO的浸润,增加电解质/负极界面的有效接触,降低界面电阻,提高界面稳定性,以及抑制充放电过程中可能形成的锂枝晶是目前负极界面研究的热点。值得注意的是,和正极界面类似,电池循环过程中负极金属锂的反复沉积和剥离,容易在界面处产生孔隙,导致界面电阻增大。因此除了在电池循环前构建良好的负极界面之外,如何在动态的电极反应过程中维持负极和电解质的均匀结合也是一个大的技术挑战。
3.1 负极界面锂枝晶问题
金属锂对LLZO 的润湿性较差,从而引起负极侧电极界面电阻较大。同时,负极侧金属锂的不均匀沉积也会引起锂枝晶的产生。由于无机固态电解质普遍具有较高的机械强度,早期的研究认为,用无机固态电解质取代有机电解液,可有效抑制锂枝晶的穿透,从而实现金属锂负极的应用。例如,基于Monroe-Newman 模 型[32],LLZO 具 有 高 达 约150 GPa 的杨氏模量[33]和约为60 GPa 的剪切模量[34],远大于抑制锂枝晶所需的锂剪切模量的两倍值9.6 GPa。但是,后来研究发现,多晶的LLZO固态电解质并不能完全抑制锂枝晶的产生,在较大电流密度下锂枝晶会在陶瓷中的孔洞、晶界等缺陷位置优先沉积和生长[20,35]。主要的原因包括相比晶粒内部,晶界剪切模量小、相对更软[36],离子电导率更低[37],存在一定的电子电导[38]等。实验发现,锂在循环后的电解质断面形成了沿晶界生长的网状形貌[39]。但是,即便是在单晶LLZO 中,在严格控制电解质表面缺陷的条件下锂枝晶依然能够产生并导致裂纹形成,说明Monroe-Newman模型用剪切模量评判电解质能否抑制锂枝晶存在局限性,缺陷尺寸对锂沉积过电位和裂纹扩展都存在一定的影响[35]。因此,制备低孔隙率高致密度的固态电解质并减少界面缺陷是抑制锂枝晶生长的必要保障。此外,优化金属锂在循环前后与电解质的界面结合,均化锂沉积,也是避免锂枝晶生成的有效途径。
3.2 负极界面优化策略
LLZO 固态电解质与金属锂浸润性有限,会导致两者之间接触不良,引起局部电流密度增大,从而造成界面局部锂枝晶的形成。反复充放电后锂枝晶渗透进入电解质内部,并且会穿透陶瓷片造成短路。改善金属锂与LLZO表面的浸润性,可以从电解质和金属锂改性两个方面来实现,主要包括:①引入中间层界面修饰;②去除LLZO 表面疏锂性Li2CO3;③调控金属锂。此外与正极界面改进类似,在负极侧设计多孔三维结构LLZO[40],一方面能够有效增大负极和电解质的界面接触,降低界面电阻,另一方面可以应对循环过程锂负极体积膨胀,保持电极结构稳定性。
3.2.1 引入中间层修饰
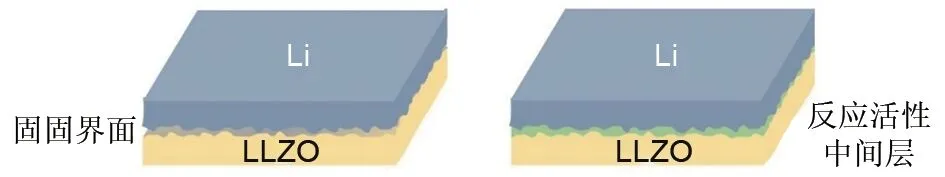
图4 反应活性中间层改善界面浸润性原理图Fig.4 Schematic of LLZO/Li interface modification using reactive interlayer
通过在LLZO 和金属锂中间引入不同的中间层,可改善界面接触,减小界面电阻。根据作用机理不同,中间层材料可分为两类:一类是对锂有反应活性,从而能够提高锂浸润性的材料,其改善机理如图4所示,金属锂能够和表面修饰后的电解质形 成 良 好 接 触[41], 如 石 墨[42]、 Al[43]、 Al2O3[44]、SnNx[45]等,这些中间层和锂的反应主要包括合金型反应和转化型反应。另一类是离子传导性柔性材料,如聚合物[19,46]和凝胶[47]。聚合物电解质得益于自身的柔性,能够减小和金属锂之间的界面阻抗。通过在LLZO 表面沉积亲锂性Au 薄层可改善负极界面接触状况,Au 和锂形成的Li-Au 合金填补了Li-LLZO 之间的空隙能够提高界面稳定性。锂沉积过程,Li+先与Au 形成合金然后在Li-Au 表面沉积锂,Li-Au作为锂离子导体能够均化锂离子传输[48]。在LLZO 表面包覆SnS2,如图5(a)所示,利用SnS2和锂的原位转化反应,提高锂的润湿性,均化负极界面的空间电荷层,并可将其作为正极材料组装获得高容量全电池,该电池0.1 C 可逆比容量可达410 mA·h/g[49]。Passerini等[50]在电极电解质界面引入离子液体电解质,促进了负极侧金属锂的均匀沉积,0.3 mA/cm2电流密度下仍可抑制锂枝晶生成,与LiFePO4组装电池能够发挥出145 mA·h/g的放电比容量和99%以上的电池效率。通过在LLZTO表面原子层沉积Li3PO4,形成具有中度离子电导和电子绝缘的人工SEI层,可填补电解质晶界和表面缺陷,诱导锂均匀沉积和剥离,有效抑制锂枝晶生长,这种改进将界面电阻降低至约1 Ω·cm2,相应的LiFePO4电池1.5 C放电比容量可达122 mA·h/g[图5(b)][51]。
长时间的充放电循环,会导致锂枝晶沿着陶瓷固态电解质孔洞和晶界等缺陷生长。为了表征电解质抵抗枝晶生长的能力,Sakamoto等[52]在2016年首次利用临界电流密度(the maximum sustainable current density or critical current density,CCD),表征不同温度下LLZO对称电池在能够维持充放电状态而不发生锂枝晶短路的最大电流密度(mA/cm2)。但是目前业界对于CCD 的测定还没有给出具体测试标准,比如电解质厚度、单次充放电时间等,这些都会对CCD产生一定影响。
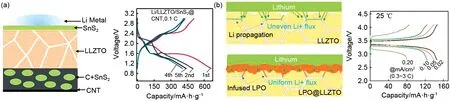
图5 Li/LLZTO@SnS2/SnS2@CNT全电池示意图和0.1C充放电曲线(a)[49],Li3PO4包覆LLZTO改善负极界面机理示意图和Li/Li3PO4@LLZTO/LiFePO4电池不同电流密度下充放电曲线(b)[51]Fig.5 (a)schematic illustration of Li/LLZTO@SnS2/SnS2@CNT all-solid-state battery and charge/discharge profiles at 0.1 C[49],(b)schematics of proposed mechanisms at the interface of Li3PO4@LLZTO and charge/discharge curves of Li/Li3PO4@LLZTO/LiFePO4 at different current densities[51]
3.2.2 去除LLZO表面疏锂性Li2CO3
研究发现LLZO 固态电解质会与空气中的二氧化碳和水反应,直接或间接生成碳酸锂,如反应式(1)~(3)所示[53]。LLZO 表面的碳酸锂不具有亲锂性,因此会显著增大LLZO和金属锂之间的界面阻抗,进而影响固态电池的容量和循环稳定性。消除疏锂的Li2CO3可显著改善LLZO 和金属锂的浸润性,降低界面电阻。消除方法包括简单的机械磨除[54]、热处理[55]或气氛热处理[54],中间层反应还原[56]、酸处理[57]等。Sun等[57]利用1 mol/L盐酸30 s快速处理LLZTO电解质,可以去除其表面Li2CO3,改善金属锂与LLZO 的接触[图6(a)],使界面电阻降低至26 Ω·cm2,其对称电池可以在0.2 mA/cm2电流密度下稳定循环700 h。


图6 LLZTO表面酸处理改善负极界面[57](a)和半液态锂负极改善负极界面(b)示意图[61]Fig.6 Schematic illustration of LLZTO/Li interface improved by acid treatment[57](a)and semiliquid lithium metal anode(b)[61]
3.2.3 调控金属锂
金属锂状态的调控也可以改善其与LLZO 固态电解质界面的结合状态,从而减小界面电阻。金属锂的调控策略包括:高温加热[58]、外加机械压力[59]、真空沉积[14]和合金化[60]。锂与其他元素合金化,可以调整熔融锂的表面能和黏度,进而改善Li 对LLZO 固态电解质的润湿性。相比于在LLZO 表面引入中间层改善界面电阻的方法,这种金属锂合金化的方法构建的界面更稳定,在长期脱嵌锂循环过程中不会产生新的锂沉积界面;在LLZO表面引入的锂反应活性中间层则有可能在初始嵌锂后体积膨胀,以及在电池循环过程脱嵌锂发生体积变化,产生和LLZO的剥离,从而破坏界面结构,增大界面电阻。Matyjaszewski 等[61]制备了一种混合电导聚合物基质中均匀分布微米锂颗粒的半液态锂负极,如图6(b)所示,将电极-电解质从固固转变为液固组成,改善了界面接触,降低了界面电阻,其对称电池在1 mA/cm2电流密度下可稳定循环400 h。
4 总结与展望
目前LLZO 基全固态锂金属电池的发展还存在诸多挑战。LLZO 本征电化学窗口的认识和电极氧化还原动力学因素的深入解析,是电极材料匹配和电极/电解质稳定界面构筑的重要理论基础。LLZO固态电解质正负极侧较高的界面电阻依然是影响全固态电池实际应用的关键问题,通过正负极组成和结构优化及界面设计,可以显著降低电极界面电阻,提高电池电化学性能,但相关措施的可应用性,还需实践验证。金属锂枝晶形成机理的正确理解和抑制策略的有效构筑,也是全固态电池实际应用前亟需解决的问题。此外,有关电池循环过程中的电极电解质界面结构演变规律、界面应力分布状态、全电池的体积变化等问题的认识,还有待进一步深化。考虑到这些科学和技术的挑战,目前利用LLZO制备无机/有机复合固态电解质可能是促进全固态电池发展的一个较好的选择。
LLZO 基固态电池微观低尺度界面物理化学性质研究还有待进一步加强。相比于电解液体系,固态电池界面的研究更为困难,不同固态部分难以分离,样品制备过程界面易被破坏,负极界面的锂金属易被氧化。因此,原位表征技术的介入十分必要。利用各类原位技术不仅能对实际工况下固态界面的结构演变、应力状态、电荷转移动力学等进行准确表征,而且能为计算模拟提供实验依据,促进以界面为中心的固态电池设计。

