超高效液相色谱法测定食品接触材料中间苯二甲酸和对苯二甲酸特定迁移量
钊,周 丛,万 富∗,谭宇诗,王 莉
(1.湖南省产商品质量监督检验研究院,长沙 410007;2.湖南农业大学资源环境学院,长沙 410128)
间苯二甲酸又称异酞酸、1,3-苯二甲酸,是一种白色结晶粉末或针状结晶,它易溶于醇和冰乙酸,微溶于沸水,但不溶于冷水。作为一种非常重要的化工中间体原料,间苯二甲酸在醇酸树脂涂料、聚酯树脂、不饱和聚酯树脂、特种纤维、热熔黏合剂、印刷油墨、聚酯纤维染色改性以及树脂增塑等方面具有广泛的用途[1-2]。GB 9685-2016《食品安全国家标准食品接触材料及制品用添加剂使用标准》中允许间苯二甲酸作为添加剂用于制作食品接触用塑料制品(聚酯、聚酰胺)、涂层涂料、黏合剂、纸和纸板等,但要求其特定迁移总量小于5.0 mg·kg-1。
对苯二甲酸又称p-苯二甲酸,是产量最大的二元羧酸,它在常温下为固体,难溶于水,主要用于制造合成聚酯树脂、合成纤维和增塑剂等,广泛用于化学纤维、轻工、电子、建筑等领域[3-5]。GB 9685-2016中允许对苯二甲酸作为添加剂用于制作食品接触用塑料制品[聚丙烯(PP)、聚对苯二甲酸乙二醇酯(PET)]、黏合剂、纸和纸板等,但要求其特定迁移总量小于7.5 mg·kg-1。GB 4806.6-2016《食品接触用塑料树脂》中明确规定需要测定聚酰胺、聚碳酸酯、聚酯树脂中间苯二甲酸和对苯二甲酸的特定迁移量。因此,建立食品接触材料及制品中对苯二甲酸和间苯二甲酸的特定迁移量的测定方法具有现实意义。
目前,对苯二甲酸和间苯二甲酸的主要测定方法有返滴定法[6]、分光光度法[7]、高效液相色谱法[8-9]、离子色谱法[10]、液相色谱-串联质谱联用法[11-12]、气相色谱法[13]。其中,在采用高效液相色谱法测定对苯二甲酸和间苯二甲酸含量时,不需要进行液液萃取分离,前处理操作比较简单;同时两种目标化合物均含有不饱和双键,在紫外光区有吸收,可以直接采用常规的二极管阵列检测器测定[14]。由于GB 31604.21-2016《食品接触材料及制品对苯二甲酸迁移量的测定》和GB 4806.6-2016中均没有间苯二甲酸的测定方法。因此,本工作建立了超高效液相色谱法(UHPLC)测定PET 材料中对苯二甲酸和间苯二甲酸的特定迁移量,以期为食品接触材料中对苯二甲酸和间苯二甲酸迁移量的监控提供技术参考。
1 试验部分
1.1 仪器与试剂
LC-30AD 型超高效液相色谱仪,配SPD-M20A光电二极管阵列检测器;MS-105DV 型电子天平;Talboys型涡旋振荡器;SHB-ⅢS型循环水式多用真空泵;雷磁p HS-3E 型pH 计;ZJ-20型超纯水制备仪;C18固相萃取柱,柱容量为200 mg/3 mL;WondaPipet型可调式移液枪,规格为0.5~10μL,10~100μL,100~1 000μL;0.45μm 有机针筒过滤器。
7.5mmo L·L-1磷酸二氢钾-磷酸缓冲溶液(pH 3.0):称取1.426 g磷酸二氢钾于烧杯中,加水950 mL,用10%磷酸溶液将其pH 调至3.0,定容至1.0 L,真空抽滤。
对苯二甲酸、间苯二甲酸混合标准储备溶液:500 mg·L-1,称取对苯二甲酸和间苯二甲酸标准品各50.0 mg,加入90 mL 甲醇,在50 ℃下加热1 h,使其充分溶解,冷却后,转移至100 mL 容量瓶中,用甲醇稀释至刻度,于4 ℃冷藏保存,有效期为6个月。
邻苯二甲酸内标储备溶液:1 000 mg·L-1,称取0.1 g(精确至0.1 mg)邻苯二甲酸标准品,用10 mL异丙醇溶解,然后将溶液转移至100 mL 容量瓶中,用异丙醇稀释至刻度,于4 ℃冷藏保存,有效期为6个月。
醇类食品模拟液为10%,20%,50%(均为体积分数,下同)乙醇溶液,酸性食品模拟液为4%(体积分数,下同)乙酸溶液。
酸性、醇类食品模拟液匹配混合标准溶液系列:分别移取0,10,20,100,200,300μL对苯二甲酸、间苯二甲酸混合标准储备溶液于6个10 mL 容量瓶中,分别加入75μL邻苯二甲酸内标储备溶液,用酸性食品模拟液稀释至刻度,配制成对苯二甲酸和间苯二甲酸的质量浓度分别为0,0.5,1.0,5.0,10.0,15.0 mg·L-1,内标质量浓度均为7.5 mg·L-1的混合标准溶液系列。以同样的方法制备另外3种醇类食品模拟液匹配混合标准溶液系列。
橄榄油食品模拟液匹配混合标准溶液:分别称取橄榄油5.0 g于6个10 mL 比色管中,分别加入0,5,10,50,100,150μL对苯二甲酸、间苯二甲酸混合标准储备溶液,混合均匀后,加入5.0 mL 异辛烷,混匀。再加入1.0 g·L-1碳酸氢钠溶液2.0 mL,振荡1 min,静置15 min,使其分层。用塑料滴管收集下层水相,以上萃取步骤重复一次。合并两次萃取所得的水相,过固相萃取小柱,将流出液收集于5.0 mL 容量瓶中,加入50%(体积分数)乙酸溶液1.0 mL,用水稀释至刻度,配制成对苯二甲酸和间苯二甲酸的质量浓度分别为0,0.5,1.0,5.0,10.0,15.0 mg·L-1,内标质量浓度均为7.5 mg·L-1的混合标准溶液系列。使用时,分取1.0~2.0 mL,用0.22μm 滤膜过滤。
邻苯二甲酸标准品的纯度为99.6%;对苯二甲酸标准品的纯度为99.8%;间苯二甲酸标准品的纯度为99.2%;乙醇、甲醇、异辛烷均为色谱纯;磷酸二氢钾为分析纯;冰乙酸、磷酸均为优级纯;橄榄油为化学纯。
1.2 仪器工作条件
ShimSen-VD C30色谱柱(250 mm×4.6 mm,3μm),柱温35 ℃;流量0.5 mL·min-1;检测波长230 nm;进样体积10μL;流动相为体积比为60∶40的7.5 mmo L·L-1磷酸二氢钾-磷酸缓冲溶液(pH 3.0)和甲醇的混合溶液;等度洗脱。
1.3 试验方法
按照GB 5009.156-2016《食品接触材料及制品迁移试验预处理方法通则》、GB/T 23296.1-2009《塑料中物质向食品及食品模拟物特定迁移试验和含量测定方法以及食品模拟物暴露条件选择的指南》,以4%乙酸溶液、10%乙醇溶液、20%乙醇溶液、50%乙醇溶液和橄榄油作为测定特定迁移量的食品模拟液进行迁移试验,迁移温度为70 ℃,迁移时间为2 h。迁移试验完成后,取1.0~2.0 mL 溶液,用0.22μm 滤膜过滤后,按照仪器工作条件测定。
2 结果与讨论
2.1 检测波长的选择
在190~800 nm 内对对苯二甲酸、间苯二甲酸和邻苯二甲酸进行光谱扫描。结果发现,对苯二甲酸、间苯二甲酸和邻苯二甲酸的最大吸收波长分别在240,230,230 nm 处。结合文献[8],试验选用的检测波长为230 nm。
2.2 色谱柱的选择
试验比较了Diamonsil C18(250 mm×4.6 mm,5μm)、Inertsil C30(250 mm×4.6 mm,3μm)、ShimSen-VD C30(250 mm×4.6 mm,5μm)等3种色谱柱对邻苯二甲酸、对苯二甲酸、间苯二甲酸的分离效果。结果发现:采用Diamonsil C18色谱柱(250 mm×4.6 mm,5μm)得到的目标化合物的拖尾现象比较严重,这与文献[8]报道的结果一致;采用Inertsil C30色谱柱(250 mm×4.6 mm,5μm)和ShimSen-VD C30色谱柱(250 mm×4.6 mm,3μm)时,3种物质都达到基线分离,但前者得到的目标化合物的色谱峰峰形不如后者的,试验选择ShimSen-VD C30色谱柱(250 mm×4.6 mm,3μm)进行后续分析。
2.3 流动相体积比的选择
通常采用缓冲溶液-甲醇体系作为流动相分离苯二甲酸的同分异构体[8-9,11],试验选择甲醇和7.5 mmol·L-1磷酸二氢钾-磷酸缓冲溶液的混合溶液(pH 3.0)作为流动相。
为使目标化合物达到基线分离,试验考察了7.5 mmol·L-1磷酸二氢钾-磷酸缓冲溶液(pH 3.0,记作流动相A)和甲醇(记作流动相B)的体积比分别为70∶30、60∶40、50∶50、40∶60时对3种苯二甲酸同分异构体分离效果的影响,所得的色谱分离结果见图1。

图1 不同流动相体积比下的色谱图Fig.1 Chromatograms at the different volume ratios of the mobile phases A and B
由图1可知:甲醇的体积分数越大,3种苯二甲酸同分异构体的保留时间越短;当甲醇的体积分数高于50%时,这3种化合物的分离度开始变差;当甲醇的质量分数达到60%时,三者不能实现基线分离;当甲醇体积分数为40%时,目标化合物的峰形及保留时间均明显好于其他体积分数下的,因此,试验选择体积比为60∶40的7.5 mmol·L-1磷酸二氢钾-磷酸缓冲溶液(pH 3.0)和甲醇的混合溶液进行等度洗脱。
2.4 流动相流量的选择
试验还考察了流动相的流量分别为0.2,0.3,0.4,0.5 mL·min-1时对3种苯二甲酸同分异构体分离效果的影响,结果见图2。
由图2可知:随着流动相流量的增加,目标化合物保留时间逐渐缩短,峰形也变得更加尖锐,但3种目标化合物均可实现基线分离。考虑到流动相流量高于0.5 mL·min-1时柱压偏大,故试验选择流动相流量为0.5 mL·min-1。
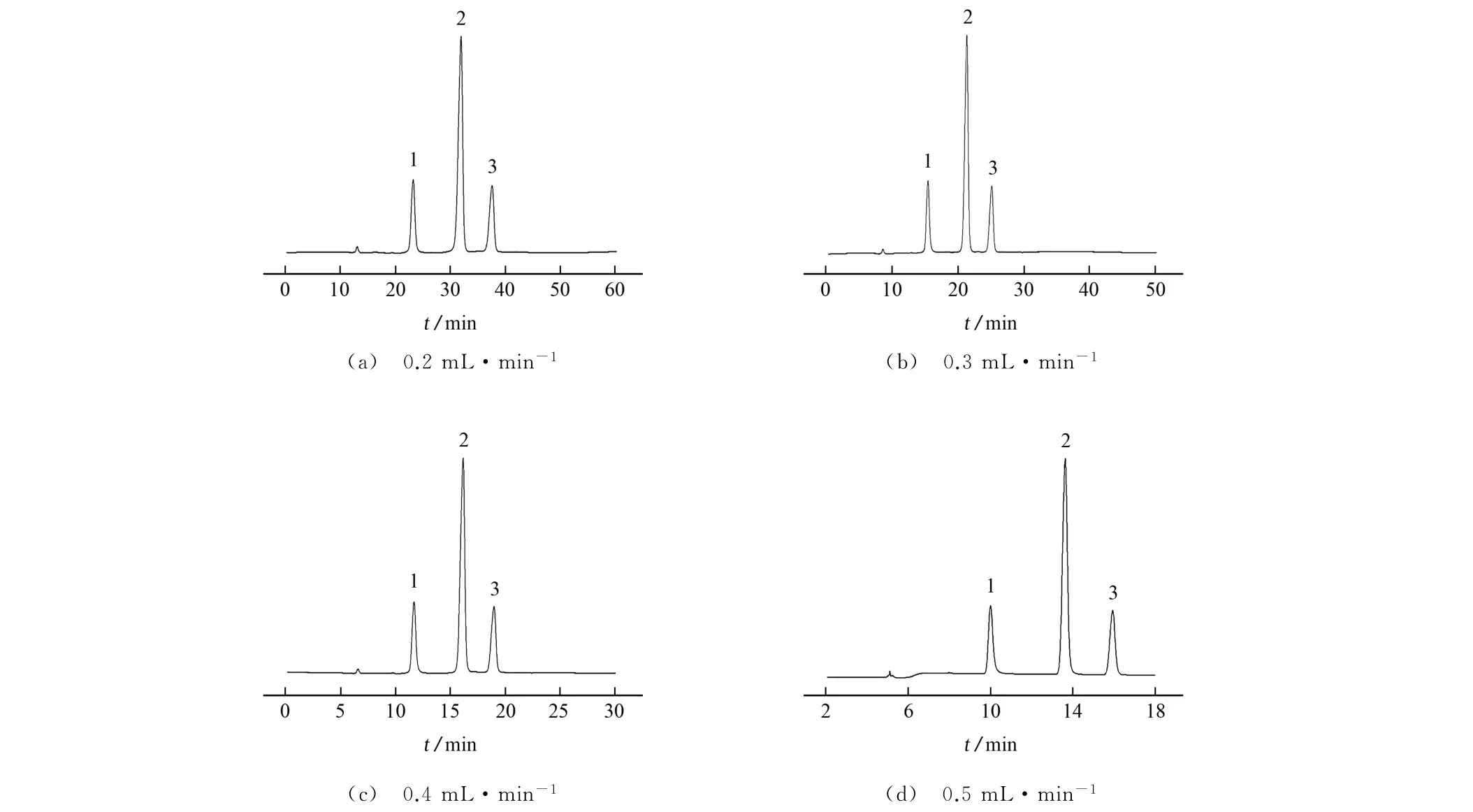
图2 不同流量下的色谱图Fig.2 Chromatograms at the different flow rates
2.5 流动相酸度的选择
由于目标化合物均为弱酸性有机物,流动相酸度对其色谱分离度和保留时间均有较大影响,因此,试验考察了7.5 mmol·L-1磷酸二氢钾-磷酸缓冲溶液的pH 分别为2.5,3.0,3.5,4.0,4.5,5.0 时对3种苯二甲酸同分异构体分离效果的影响,结果见图3。
由图3可知:随着pH 增大,3种苯二甲酸同分异构体的保留时间逐渐缩短,其中间苯二甲酸的缩短幅度最大;当pH 大于3.5时,这3种化合物的出峰顺序发生了变化,三者之间分离度变差。考虑到ShimSen-VD C30色谱柱(250 mm×4.6 mm,3μm)的酸度适用范围(pH 2.0~8.0)和使用寿命,试验选择7.5 mmol·L-1磷酸二氢钾-磷酸缓冲溶液的p H为3.0。
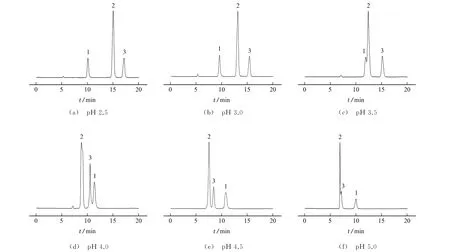
图3 不同酸度下的色谱图Fig.3 Chromatograms at different acidities
2.6 缓冲溶液中磷酸二氢钾浓度的选择
试验考察了缓冲溶液中磷酸二氢钾浓度分别为1.0,2.5,5.0,7.5,10.0 mmo L·L-1时对邻苯二甲酸、对苯二甲酸和间苯二甲酸分离效果的影响,结果见图4。
由图4可知:随着磷酸二氢钾浓度的增加,3种苯二甲酸同分异构体的保留时间逐渐缩短,其中邻苯二甲酸缩短幅度最大;但磷酸二氢钾浓度越低,邻苯二甲酸的色谱峰拖尾现象越明显;当磷酸二氢钾的浓度不低于7.5 mmo L·L-1时,这3种化合物的峰形、分离度和保留时间均较为理想。考虑到过高的盐浓度会增加色谱仪管路堵塞的风险和降低色谱柱使用寿命,试验选择缓冲溶液中磷酸二氢钾的浓度为7.5 mmo L·L-1。

图4 不同磷酸二氢钾浓度下的色谱图Fig.4 Chromatograms at different concentrations of KH2PO4
2.7 标准曲线、检出限与测定下限
按照仪器工作条件对酸性、醇类和橄榄油食品模拟液匹配混合标准溶液系列进行测定,以间苯二甲酸、对苯二甲酸与邻苯二甲酸的质量浓度之比为横坐标,其对应的响应值之比为纵坐标绘制标准曲线,这2种化合物的标准曲线的线性范围均为0.5~15.0 mg·L-1,其他线性参数见表1。
以3倍、10倍信噪比(S/N)计算方法的检出限(3S/N)和测定下限(10S/N),结果见表1。
由表1可知:2种目标化合物检出限和测定下限分别为0.03~0.07 mg·L-1与0.10~0.23 mg·L-1。

表1 线性参数、检出限与测定下限Tab.1 Linearity parameters,detection limits and lower limits of determination
2.8 精密度和回收试验
按照试验方法对PET 样品进行3个浓度水平的加标回收试验,每个浓度水平平行测定6次,回收率及相对标准偏差(RSD)结果见表2。
由表2可知:对苯二甲酸的回收率为92.4%~106%,RSD 为0.19%~4.6%;间苯二甲酸的回收率为92.4%~105%,RSD 为0.17%~5.0%。说明该方法具有良好的准确度和精密度,可用于食品接触材料中间苯二甲酸、对苯二甲酸的日常分析测定。

表2 精密度和回收试验结果(n=6)Tab.2 Results of tests for precision and recovery(n=6)
2.9 样品分析
按照试验方法分析了5个PET 材质样品,均未检出对苯二甲酸和间苯二甲酸迁移。
本工作建立了超高效液相色谱法测定5种食品模拟液中对苯二甲酸与间苯二甲酸的特定迁移量的方法。该方法精密度和准确度均较好,具有一定的实际应用价值,可为我国相关部门的监管工作提供技术支持和方法依据。

