早期肠内营养治疗神经重症患者的临床疗效分析
陈国瑜
(柳州市人民医院重症医学科 广西 柳州 545006)
神经系统重症大多为脑血管疾病或颅脑外伤,患者大多存在昏迷或吞咽功能障碍,自主摄入食物的能力明显下降甚至消失,且此时机体处于高分解代谢状态,对糖、脂肪、蛋白质的消耗明显增加,因此患者容易发生营养不良、免疫状态低下等问题,影响临床治疗及预后[1]。营养支持是改善机体营养状态的主要手段,临床虽可提供足量的代谢底物,但无法抑制蛋白质分解代谢和逆转负氮平衡,而肠外营养虽能避免食物对胃肠道的刺激,使胃肠吸收功能减弱,但会增加呼吸和循环系统负担,机体对营养物质的代谢较慢,容易引发感染以及其他并发症[2]。早期肠内营养支持治疗通过直接鼻饲营养物质进入胃肠道,能够刺激胃肠黏膜,维持或促进黏膜屏障功能的恢复,增加营养成分的吸收和利用,维持足够营养供给,达到改善机体营养状态、促进康复的作用[3]。基于此,本文分析肠内营养在神经重症患者中的疗效,现报道如下。
1.资料与方法
1.1 一般资料
将2018 年6 月—2020年6月在我院ICU 治疗的120 例神经系统重症患者按不同营养方式分为两组。所有患者均属于神经系统重症,入住ICU 病房,存在意识障碍或吞咽障碍,急性生理与慢性健康评分(APACHEⅡ)>16分,疼痛数字评分法(NRS)2002 评分≥3 分,格拉斯哥昏迷评分(GCS)≤12 分,洼田饮水试验≥3 级,均需给予营养支持治疗;排除深度昏迷、濒死患者、对营养剂过敏、存在严重心肝肾疾病等。两组一般资料比较差异无统计学意义(P >0.05),见表1。
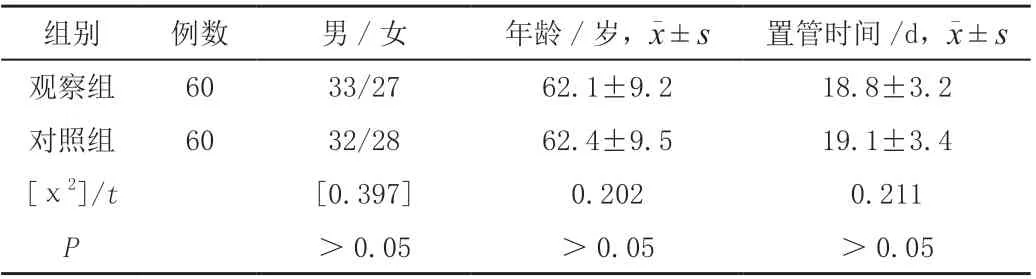
表1 两组一般资料比较
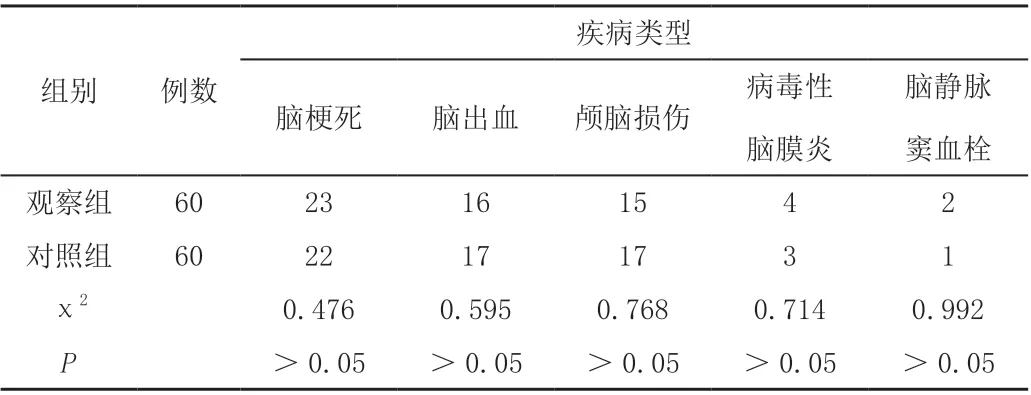
表1(续)
1.2 方法
两组均给予常规对症治疗,包括降低颅内压、改善脑循环、保护脑神经、抗感染等,维持水电解质平衡,做好生命体征监护,预防并发症。对照组使用肠外营养治疗,在入ICU 后48 h 内进行治疗,使用合一鞍全营养混合液,锁骨下静脉穿刺置管,持续24 h 泵注,计算每日所需剂量,从小剂量开始,逐步增加剂量,不足部分用25%葡萄糖溶液补足[4]。观察组行早期肠内营养治疗,入ICU后48 h内进行治疗,使用能全力混悬液,经鼻饲管泵入,持续12 h,每日热量在83.68 kJ,氮量0.2~0.24 g/(kg·d),之后可视情况逐步增加氮量至0.24 ~0.48 g/(kg·d),热量供给增加125.52 ~146.44 kJ,根据患者胃肠蠕动情况及营养液吸收情况调节剂量,每3 h 抽1 次胃残液,确保胃潴留量低于150 mL[5]。两组均治疗14 d后评价疗效。
1.3 观察指标
比较两组患者各项营养及免疫功能各指标,统计消化道出血、肠道感染、尿路感染、肺部感染等并发症发生率。
1.4 统计学方法
采用SPSS 22.0 统计软件进行数据处理。计量资料采用均数±标准差(± s)表示,行t 检验,计数资料用频数和百分比(%)表示,行χ2检验。P <0.05为差异有统计学意义。
2.结果
2.1 两组患者治疗前后营养指标比较
观察组治疗后白蛋白(Alb)、血红蛋白(Hb)、总蛋白(TP)、前血蛋白(PA)、转铁蛋白(TRF)显著高于对照组(P <0.05)。见表2。
表2 两组患者治疗前后营养指标比较(± s)
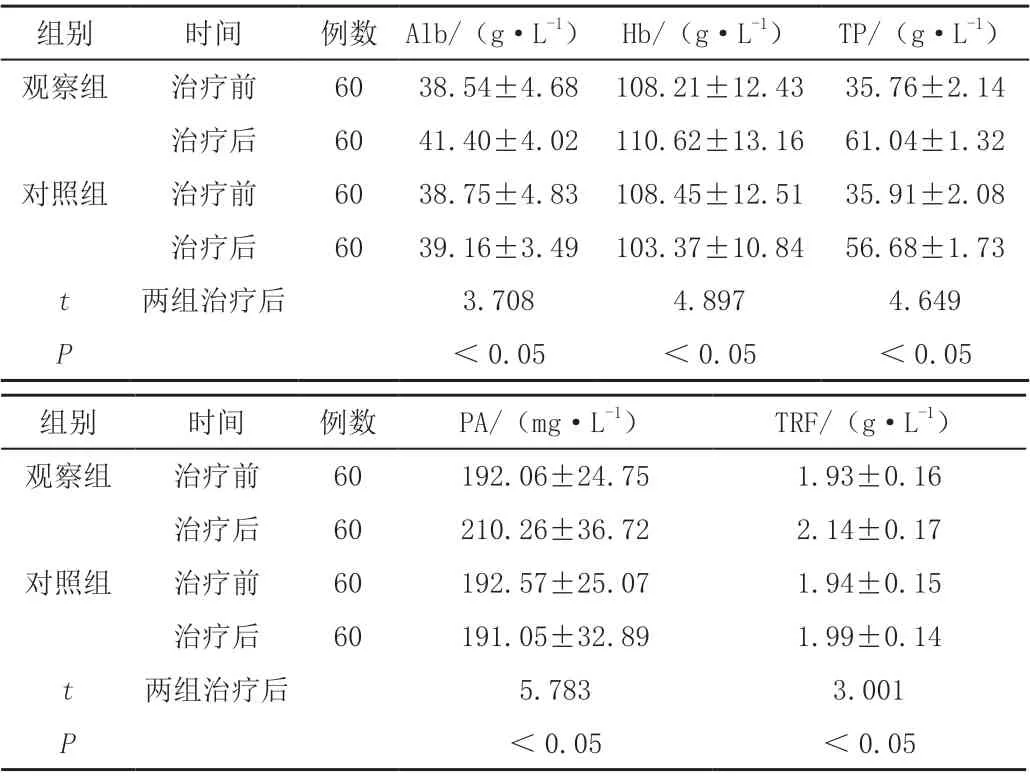
表2 两组患者治疗前后营养指标比较(± s)
组别 时间 例数 Alb/(g·L-1) Hb/(g·L-1) TP/(g·L-1)观察组 治疗前 60 38.54±4.68 108.21±12.43 35.76±2.14治疗后 60 41.40±4.02 110.62±13.16 61.04±1.32对照组 治疗前 60 38.75±4.83 108.45±12.51 35.91±2.08治疗后 60 39.16±3.49 103.37±10.84 56.68±1.73 t 两组治疗后 3.708 4.897 4.649 P<0.05 <0.05 <0.05组别 时间 例数 PA/(mg·L-1) TRF/(g·L-1)观察组 治疗前 60 192.06±24.75 1.93±0.16治疗后 60 210.26±36.72 2.14±0.17对照组 治疗前 60 192.57±25.07 1.94±0.15治疗后 60 191.05±32.89 1.99±0.14 t 两组治疗后 5.783 3.001 P<0.05 <0.05
2.2 两组患者治疗前后免疫功能各指标比较
观察组治疗后总淋巴细胞计数(TLC)、免疫球蛋白M(IgM)、免疫球蛋白G(IgG)、封闭抗体(HLA-DR)明显高于对照组(P <0.05)。见表3。
表3 两组治疗前后免疫功能各指标比较(± s)

表3 两组治疗前后免疫功能各指标比较(± s)
组别 时间 例数 TLC/×109/L IgM/(g·L-1)观察组 治疗前 60 1.02±0.03 2.06±0.03治疗后 60 1.32±0.06 1.96±0.03对照组 治疗前 60 0.99±0.02 2.07±0.02治疗后 60 1.13±0.04 1.44±0.02 t 两组治疗后 2.174 2.490 P<0.05 <0.05组别 时间 例数 IgG/g/L HLA-DR/%观察组 治疗前 60 12.87±0.76 60.94±0.83治疗后 60 10.72±1.01 70.06±1.04对照组 治疗前 60 12.93±0.79 61.07±0.88治疗后 60 9.02±0.74 66.73±1.29 t 两组治疗后 2.998 4.414 P<0.05 <0.05
2.3 两组患者并发症发生率比较
观察组消化道出血、肠道感染、尿路感染、肺部感染等并发症发生率显著低于对照组(P <0.05)。见表4。
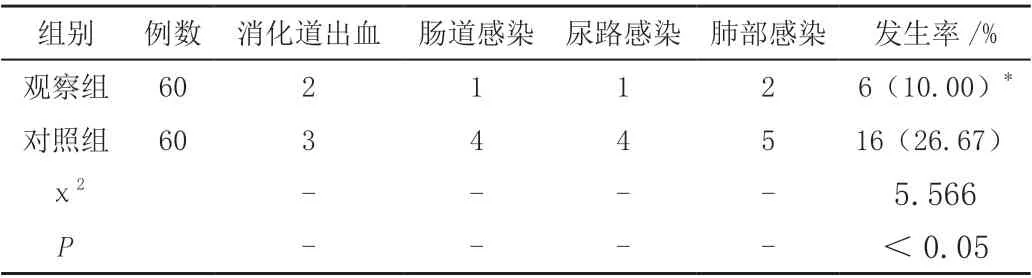
表4 两组患者并发症发生率比较(例)
3.讨论
肠内营养是经胃肠道提供代谢需要的营养物质及其他各种营养素的营养支持方式。其决定于时间长短、精神状态与胃肠道功能。肠内营养是通过胃肠道提供营养的一种营养支持方式,分为经口和经导管两种方式。神经系统重症患者的病情危重、并发症发生率高、病死率高,是ICU救治的难治性疾病。患者常处于意识障碍、昏迷状态,大部分丧失自主吞咽功能,营养摄入受阻,同时患者机体处于高分解代谢状态,对营养物质的分解代谢速度明显增快,导致营养不良、免疫功能低下等并发症发生率升高,且容易加重病情、增加感染等并发症发生率,甚至影响疗效,导致不良预后[6]。
营养支持是神经系统重症患者的重要治疗手段之一,一般分为肠内营养和肠外营养两种治疗方式,通过计算每日所需热量,制定个体化的营养补充方案,逐步增加机体营养供给[7]。肠外营养通过静脉泵注营养液进行治疗,能减少食物对胃肠道的刺激,但会减弱胃肠道吸收功能,增加循环系统及呼吸系统负担,影响机体代谢功能,增加了并发症发生风险[8]。早期肠内营养治疗直接将营养液注入胃内,刺激胃肠消化吸收功能的恢复,保护肠道屏障功能,有助于增加营养成分的吸收,减轻其他系统功能的负担,从而维持较好营养状态,降低相关并发症发生率,提升免疫力,加快病情缓解速度,改善预后[9-10]。
综上所述,肠内营养治疗用于神经重症患者效果确切,明显提升了营养及免疫功能指标,降低并发症发生率,值得使用。

