Pringle法与Glisson鞘外离断法在腹腔镜肝血管瘤切除术中的临床疗效比较
陈鹏宇,汪建初
(右江民族医学院附属医院肝胆外科,广西 百色 533000)
在肝脏肿瘤中,肝血管瘤是最常见的良性肿瘤[1],多数无症状血管瘤患者可无需干预,原则上以随访观察为主。但对于有明显临床症状、生长迅速、肿瘤直径约5 cm或不能排除肝细胞肝癌的肝血管瘤患者,应及时进行治疗,而首选的治疗方法是手术治疗[2]。由于血管瘤瘤体较大,且充满血液,手术切除过程中往往有较多的出血量。如何控制术中的出血便成为腹腔镜肝血管瘤切除术中的关键问题,因此我科根据该理论及丰富的腹腔镜肝血管瘤切除的手术经验,于2016年9月—2020年9月开展了63例腹腔镜肝血管瘤切除术,拟研究Pringle法与Glisson鞘外离断法在腹腔镜肝血管瘤肝切除术中的应用价值。
1 资料与方法
1.1 病历资料 回顾分析右江民族医学院附属医院肝胆外科2016年9月—2020年9月收治的63例行腹腔镜肝血管瘤切除术患者的临床资料,根据血流阻断方式的不同分为行Pringle阻断法的Pringle组(n=30)和行Glisson鞘外离断法的鞘外组(n=33)。其中女性34例,男性29例,年龄(55.82±10.21)岁。肿瘤分布于肝右叶37例,其中位于Ⅴ段6例,Ⅵ段11例,Ⅶ段10例,Ⅷ段6例,Ⅵ~Ⅶ段4例;肝左叶26例,其中位于Ⅰ段4例,Ⅱ~Ⅲ段8例,Ⅲ段6例,Ⅳ段8例。肿瘤平均直径(6.4±2.2) cm。纳入标准:①所有患者均行腹腔镜肝血管瘤切除术; ②吲哚氰绿15 min滞留率<14%;③Child-Pugh 肝功能分级均为A级;④既往无上腹部手术史;⑤术前经CT、MRI、腹部超声、肿瘤标记物等综合诊疗手段初诊为肝血管瘤患者,术后均经病理证实为肝血管瘤者,且一般资料比较差异无统计学意义,具有可比性。排除标准:①凝血功能异常;②经腹腔镜手术治疗但术中采取其他血流阻断方式;③未经手术治疗或选择其他非手术治疗方式;④有严重基础疾病或重要脏器功能受损不能耐受手术治疗的患者。所有患者均签署了医学临床研究知情同意书及手术知情同意书,所有病历资料均经过右江民族医学院附属医院医学伦理学委员会审查。
1.2 手术方法 患者全身麻醉,取头高足低平卧位,Trocar采用四孔法,必要时采用五孔法,建立CO2气腹,压力维持在1.60~1.86 kPa。用超声刀游离肝周围韧带,充分暴露手术视野。当胆囊同时存在病变时,可先切除胆囊,否则可保留胆囊。
1.2.1 鞘外组 将肝门板区向下方牵引,暴露Glisson鞘,将肝实质与Glisson鞘分离,预先用分离钳阻断Glisson鞘,确定缺血范围,予结扎阻断。在肝表面用超声刀沿肝脏缺血线标记切除线,切肝过程中按照由前至后,由浅入深,由下至上的顺序进行肝实质的离断。
1.2.2 Pringle组 用乳胶管扎紧肝十二指肠韧带,完全阻断入肝的肝动脉及门静脉血流,单次阻断时间15 min,对合并肝硬化者控制在10 min以内。一次阻断不能完成肝切除及断面处理时,解除阻断5 min后再次阻断。
1.2.3 两组阻断后手术步骤 所遇到的管道用可吸收夹夹闭并予阻断,肝实质断面的出血用电凝止血。逐步解剖、离断肝组织至第二肝门处,剩余肝脏及左肝静脉用直线切割闭合器一并离断。切除肝组织标本装入标本袋内。肝断面电灼止血。冲洗手术部位,检查是否有出血和胆瘘。肝创面喷洒生物胶止血或放置明胶海绵压迫止血。标本袋经延长脐孔或延长剑突下孔小切口取出。逐层关腹缝皮,腹腔常规放置引流管。
1.3 观察指标 对比两组患者手术时间、术中出血量、术后住院时间、并发症发生率和术前及术后第1天、第3天、第7天的谷丙转氨酶(ALT)、谷草转氨酶(AST)和总胆红素(TBIL)水平等相关数据。
2 结果
2.1 患者术前资料比较 两组患者的术前ALT、AST、TBIL水平等比较,差异均无统计学意义(P>0.05),见表1。
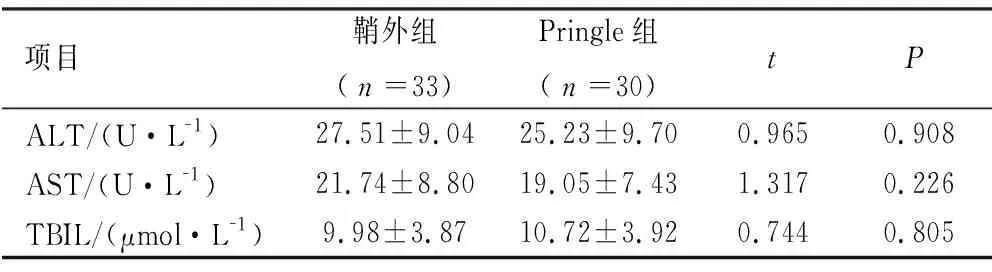
表1 鞘外组与Pringle组患者术前资料
2.2 患者手术及术后资料比较 两组患者均顺利完成了腹腔镜肝血管瘤切除术,无中转开腹。两组患者的术中出血量和术后住院时间比较,差异均有统计学意义(P<0.05)。两组患者的手术时间比较,差异无统计学意义(P>0.05)。鞘外组术后发生术后出血3例,腹腔脓肿2例,并发症发生率15.15%(5/33);Pringle组术后发生术后出血6例,胆漏1例,肝衰竭1例,并发症发生率为26.67%(8/30),两组术后并发症发生率比较,差异无统计学意义(P>0.05),见表2。两组患者术后第1天、第3天、第7天的ALT、AST、TBIL水平比较,差异均有统计学意义(P<0.05),见表3。所有标本术后病理检查结果均为肝血管瘤。两组均无围手术期死亡患者,无计划再次手术。

表2 鞘外组与Pringle组肝血管瘤切除患者手术及术后资料
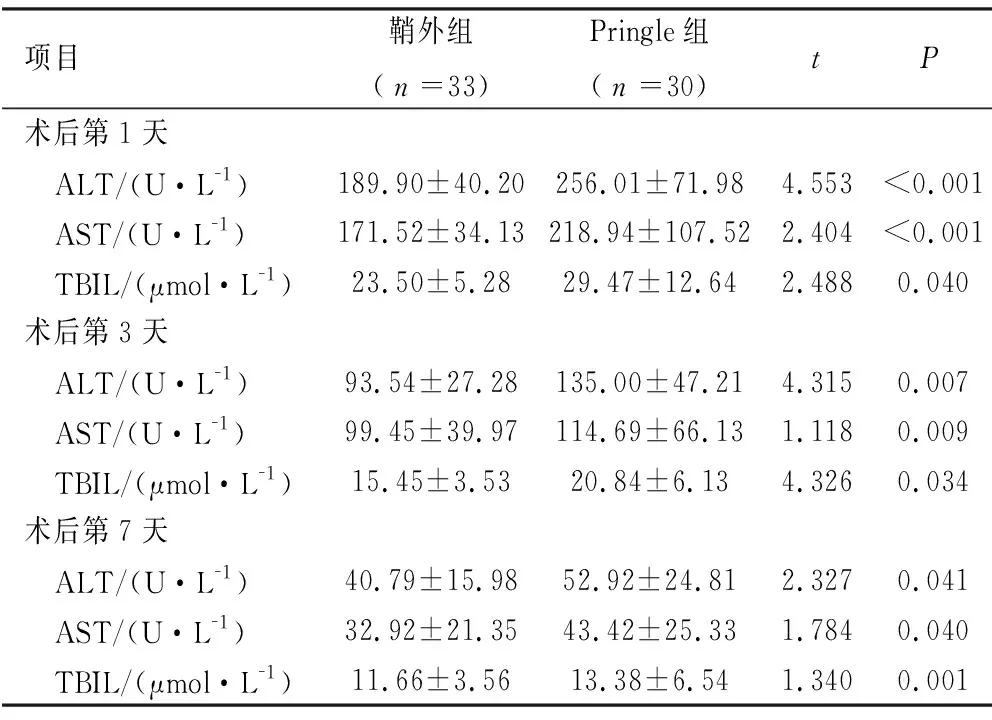
表3 鞘外组与Pringle组肝血管瘤切除患者术后肝功能资料
3 讨论
肝脏良性肿瘤中,肝血管瘤发病率最高,随着人们健康意识的提升和影像学检查手段的进步,肝血管瘤的检出率日益增加,其中约50%患者的肝血管瘤会随年龄的增大而增大[3]。对于诊断不明确、伴发症状或出现严重并发症的肝血管瘤应进行手术干预[4]。尽管外科手术技术越来越成熟,但术中最关键的步骤在于对出血的控制,因此如何有效进行肝血流阻断进而减少术中出血成为临床医师面临的主要问题[5]。
目前在腹腔镜肝切除术中常用的肝血流阻断方法有全入肝血流阻断法和选择性入肝血流阻断法[6-8]。全入肝血流阻断法即Pringle法优势在于操作简便,不需要额外的器械,且血流阻断效果明显[9],因此得以广泛应用。但其缺点也同样明显,Pringle法在阻断患侧血流的同时也阻断了健侧的血流,导致病变肝脏和正常肝脏之间无明显缺血界限,且开放血流后容易导致残留肝脏的缺血-再灌注损伤[10]。我国是肝硬化患病率大国,Pringle法对肝硬化患者术后残留肝脏再生的影响更大,甚至发生术后肝功能衰竭。由于腹腔镜手术时间往往较长,术中需多次阻断血流,全肝门阻断后,上述不足更加明显。选择性入肝血流阻断法中常用的有Glisson鞘外离断法,该方法可在肝外将Glisson鞘内的门静脉、肝动脉和胆管一并阻断,无需分别解剖鞘内结构[11-12]。阻断后可使病变肝脏和正常肝脏之间出现明显缺血线,便于手术操作。此外,该方法无需解剖第一肝门,肠系膜上静脉血流仍可回流体循环,血流动力学稳定,避免了肠道细菌的移位及肠黏膜损伤[13]。Glisson鞘外离断法的安全性和可行性得到了证实,已逐步成为临床的常规阻断法[14]。但该方法需要熟练掌握肝脏解剖学结构和腹腔镜手术技术,在术中能快速精准分离并阻断病变肝脏的Glisson鞘分支,对术者要求高。
本研究显示,Glisson鞘外组的术中出血量明显少于Pringle法。Glisson鞘外阻断法选择性阻断肝血管瘤所在肝段或肝叶的入肝血流,缺血线清晰,避免了损伤肝段之间的肝静脉主干,因此出血较少。而Pringle法在阻断的间歇期也明显增加了肝脏断面的出血[15]。在手术时间上,两组无统计学差异,因为两种阻断方法都不需要解剖第一肝门,都属于便捷的手术方式。Glisson鞘外组在肝功能损害和术后住院时间方面明显低于Pringle组,其原因主要是Glisson鞘外离断阻断法选择性阻断病侧肝组织,而正常肝脏组织供血不受影响,避免了缺血-再灌注损伤及肠道淤血,患者术后肝功能恢复较快,从而明显缩短患者术后住院时间。
综上所述,相对于Pringle法,Glisson鞘外离断法可以减少患者术中出血量、肝脏损伤和术后住院时间。因此,在腹腔镜肝血管瘤切除术中应用Glisson鞘外阻断法是安全、有效的。此外术前的影像学检查可以让我们清晰地了解Glisson系统的解剖位置,有助于指导手术医生的术中操作,减少损伤。

