耳屏软骨联合带蒂鼻腔黏骨膜瓣在修补鼻中隔大穿孔中的应用
王茂鑫,马贤,刘伟,田海月,蔺文魁,安飞
(中国人民解放军联勤保障部队第九四〇医院 耳鼻咽喉头颈外科,甘肃 兰州 730050)
鼻中隔穿孔是耳鼻咽喉科常见的疾病之一,鼻中隔穿孔后鼻腔部分功能丧失,而且会引起大出血、长期头痛、呼吸哨鸣音重、甚或呼吸困难,患者生活质量低下。鼻中隔穿孔有多种原因,临床上最常见的为医源性因素,往往合并鼻腔粘连、鼻中隔偏曲及鼻窦炎。目前对于鼻中隔穿孔的治疗多采用手术修补[1]。尽管文献报道鼻中隔穿孔有多种手术径路修补,但修补方法往往受穿孔部位、大小及鼻腔合并疾病限制。且术后再穿孔率高,手术失败者常有发生。选择什么材料进行修补才能容易存活,并可以恢复正常的鼻腔生理功能?选择怎样的手术方式可以提高手术的成功率是临床医生一直思考的问题。我科2014年8月—2018年5月于鼻内镜下采用耳屏软骨联合带蒂鼻腔黏骨膜瓣修补直径大于15 mm的鼻中隔穿孔18例,手术效果明显,穿孔愈合率高,现报道如下。
1 资料与方法
1.1 临床资料
本组鼻中隔大穿孔患者18例,其中男8例,女10例;年龄21~73岁,平均年龄40.8岁。14例为医源性穿孔(6例为外院鼻中隔偏曲矫正术后引起穿孔,2例为外院鼻窦炎鼻息肉术后引起的穿孔,2例为鼻中隔穿孔修补术后再次穿孔,4例为外院鼻出血电凝止血术后引起穿孔),1例因鼻部外伤引起穿孔,3例原因不明穿孔。穿孔直径为15~20 mm,边缘欠整齐,均需要再次手术治疗(图1)。主要症状为鼻腔干燥、头痛、间断鼻出血及呼吸时有哨鸣音,1例出现鼻腔严重阻塞。术前检查包括前鼻镜检查、鼻内镜检查和鼻腔鼻窦薄层高分辨率三维CT检查,排除其他可能伴随的病理改变,如发现慢性鼻窦炎及鼻腔肿物等疾患;术前矢状位测量穿孔缘与鼻顶、鼻底上下缘高度(图2)。根据患者鼻腔有无感染,鼻中隔穿孔创缘周围充血情况,酌情给予鼻腔药物治疗,术前1周常规生理性海水(北京宝恩科技有限公司生产)冲洗鼻腔,3次/d,术前行鼻腔内镜检查。
1.2 手术方法
1.2.1 麻醉 均采用气管插管全身麻醉,然后用含0.1%肾上腺素的2%利多卡因/生理盐水棉片在总鼻道进行贴敷3次,每次5 min,行鼻腔黏膜收缩和表面麻醉;继而用含0.1%肾上腺素的1%利多卡因/生理盐水注射液1 mL在左侧鼻腔鼻中隔穿孔周缘黏膜及右鼻腔底部黏膜做分点注射,直至穿孔周缘黏膜色泽苍白。
1.2.2 制作右侧鼻腔带蒂黏骨膜瓣 鼻内镜下彻底清理穿孔缘,用小尖刀沿穿孔边缘作环行搔刮,使其形成新鲜创面。在左侧鼻腔距离穿孔前缘0.5~0.8 cm处作纵行黏膜切口(根据术者熟练情况,也可选择鼻中隔右侧做切口),将穿孔前、上、下方黏骨膜完全剥离,分开穿孔边缘,从穿孔上下方逐步分离至穿孔后缘至少0.5 cm处。以鼻中隔穿孔下缘为轴分离鼻腔右侧鼻中隔穿孔下缘以下鼻腔底部黏骨膜,根据穿孔大小做成尽可能宽的蒂在穿孔下边缘且面积足够大的翻转黏膜瓣,向上穿过穿孔翻向左侧鼻腔,蒂部宽度应以超过穿孔前后缘1~2 mm为宜。
1.2.3 取带有软骨膜的耳屏软骨 外耳道口置一小棉球,常规皮肤消毒,用含1%利多卡因/生理盐水注射液行局部浸润麻醉,取单侧带有软骨膜的耳屏软骨于生理盐水中备用(图3)。对位缝合耳屏后取出外耳道棉球。然后根据鼻中隔穿孔的大小修剪耳屏软骨,如穿孔直径超过耳屏软骨直径,可将耳屏软骨纵行劈开扩大移植物面积。
1.2.4 修补穿孔 将修剪合适的单侧软骨膜的耳屏软骨嵌入残余鼻中隔软骨和剥开的黏骨膜之间(图4),仔细检查移植物是否位于软骨缺损的中心,穿孔完全封闭后,将右侧带蒂翻转黏膜瓣前、上、后缘分别与相对应的鼻中隔穿孔左侧前、上、后缘对位缝合固定(图5)。术后双侧鼻腔填塞止血膨胀海绵,并将(外用)重组牛成纤维细胞生长因子注入膨胀海绵。
1.2.5 术后鼻腔护理 3 d后拔除填塞膨胀海绵,此后每2 d在鼻内镜下清洁换药,并用涂有重组牛成纤维细胞生长因子的明胶海绵贴敷双侧鼻中隔黏膜,避免鼻腔过度通气导致移植物难以成活,观察移植物的成活情况。
2 结果
18例患者术后14 d复查,双侧穿孔缘黏膜与植入软骨粘附紧密,穿孔缘有血管纹沿植入软骨向中心生长,愈合后可见移植物表面黏膜上皮生长,色泽淡红。所有患者术后随访6个月至1年,17例患者术后半年复查移植物全部成活,完全修补成功;1例在术后半年复查时残留有小穿孔(直径为2 mm),门诊在局麻鼻内镜下在穿孔周缘用尖刀刮出新鲜创面后,用4-0 VICRYL贯穿对位拉合,换药2个月后完全愈合。典型患者术后鼻内镜复查图像见图6。
3 讨论
鼻中隔穿孔是耳鼻咽喉科医生的常见问题。本组18例患者中有14例患者 (77.8%)是医源性的,故不规范的鼻腔手术操作是鼻中隔穿孔的主要原因。鼻中隔成形术后穿孔率高达5%,其中黏膜下切除术后穿孔率高达25%。还有一些其他原因,包括因鼻出血而烧灼止血和填塞、强迫性挖鼻、鼻腔炎症、鼻腔感染、自身免疫状况(如结节病、韦格纳肉芽肿和修复性肉芽肿)、可卡因滥用、鼻减充血剂滥用及鼻腔内类固醇激素的长期使用等,所有这些因素均可导致特发性或不明原因的鼻中隔穿孔率增加[2-4]。另外气候干燥也会导致鼻腔结痂、阻塞和出血,患者用力地擤鼻或挖鼻可能会进一步造成出血、结痂,这些原因均可能导致鼻中隔穿孔[5]。
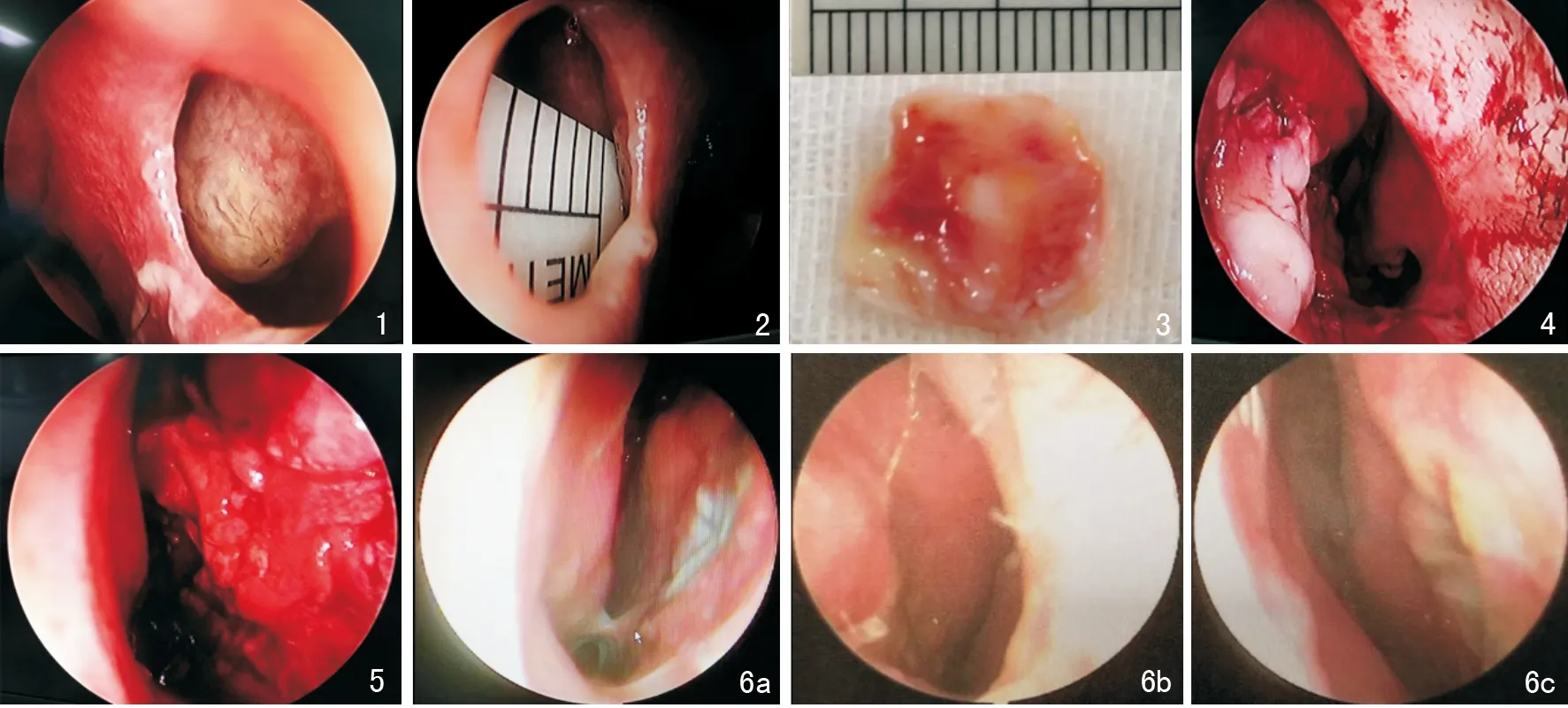
图1 右侧鼻腔显示鼻中隔穿孔 图2 测量穿孔直径大小 图3 取下的带一侧软骨膜的耳屏软骨 图4 修补后左侧鼻腔观察移植物位置和黏膜瓣位置 图5 修补后右侧鼻腔观察移植物位置和黏膜瓣位置 图6 典型患者鼻中隔穿孔修补术后复查内镜检查图像 6a:术后3个月随诊时右侧鼻腔检查移植物周边已成活,中央部分伪膜附着;6b、c:术后半年,双侧移植物全部成活,穿孔修补完好
鼻中隔穿孔修补术是很具有挑战性的鼻科手术,手术技术没有标准化,失败率较高。对于较大的穿孔,并且反复修补均失败的患者,手术难度更加大。传统方法中采用的自体骨膜[6-8]、筋膜[9-10]、双侧单侧的带蒂黏膜瓣等移植物[11]常因移植后血供不良或张力过大造成移植物缺血坏死,从而影响手术成功率。穿孔部位绝大多数位于鼻中隔软骨部,小穿孔多采用单纯转瓣缝合修补,中等以上穿孔则多采用夹层法手术修补,该手术修补成败的关键在于有无丰富的血供和合适的移植物。
2002年Hier首次报道1例27岁男性前鼻中隔穿孔(20 mm×20 mm)患者使用鼻内镜,用鼻底旋转皮瓣联合鼻中隔骨/软骨后移来修复鼻中隔穿孔,移植物被放置在两个黏膜瓣之间夹缝内,延伸到内侧脚之间以固定移植物。这项技术的缺点是在右侧鼻腔移植的骨/软骨裸露,然后用凝胶覆盖裸露的骨/软骨。作者报告裸露的骨/软骨上只有少量结皮,经过7个月的随访,移植物完全黏膜化和愈合。文中强调鼻内镜技术在没有过度创伤的情况下获得了极好的可视性和曝光性,并具有出色的教学能力[12]。2008年Lee还报道了一种鼻内镜技术,单侧推进的鼻底黏膜瓣联合颞肌筋膜修补鼻中隔大穿孔。作者强调了单侧黏膜瓣在避免术中穿孔扩大和形成新穿孔方面的优势,以及在实施一期手术时减少手术时间的优点[13]。鼻内镜技术如今可以被认为是鼻中隔穿孔修补的金标准,术中造成的创伤更小,提供了更好的手术视野,可以帮助鼻科医生修补各种大小的鼻中隔穿孔,即使是在鼻中隔的后部,成功率也很高[14-17]。
本研究利用耳屏软骨联合带蒂鼻腔黏骨膜瓣修补穿孔大于15 mm的患者18例,移植物均成活,术后14 d双侧穿孔缘黏膜即与植入软骨粘附紧密,穿孔缘有血管纹沿植入软骨向中心生长,说明带蒂鼻底黏骨膜瓣伸展性强,血管丰富,可以提供血供和足够的面积来保证移植物的成活。耳屏软骨取材方便,可塑性强,可根据穿孔的大小进行裁剪,带有软骨膜的一面,可以作为黏膜瓣的补存,防止软骨的裸露,更好地为移植软骨创造潮湿环境,而且无排异反应,经济负担小。对于手术失败的患者可以利用另一侧的鼻底黏膜瓣及耳屏软骨再次进行手术修复。本研究的缺点存在样本量太小,下一步仍需要扩大样本量进行统计分析。
总之,对于鼻中隔大穿孔的治疗,鼻内镜下应用耳屏软骨联合带蒂鼻腔黏骨膜瓣修补具有比较理想的治疗效果,值得临床推广。

