转化医学的理论演化及其发展的主要问题*
李 玲 樊春良
转化医学在国际医学研究中占据重要地位,已成为各个国家在医学领域里一项重大政策。美国最主要的医学研究机构和资助机构国立卫生研究院(National Institutes of Health,NIH)在2003年出台了NIH路线图,正式从战略层面提出发展转化医学;英国政府在2006年初发布“最佳研究,最佳健康”国家战略,推动研究成果向新的治疗方法、技术和诊断方法的转化;德国在2010年出台的“高技术战略2020”中强调了临床应用的验证研究需求,即从临床到基础研究的重要性。我国原国家卫生部、科技部、发改委和自然科学基金委员会自“十二五”起出台多项规划,提出支持转化医学研究、转化医学科技基础设施建设。
国内学者时占祥、崔志文、吴慧、荣英男、罗娟等[1-5]对我国转化医学的发展历程进行了一定的总结和概括。但这些研究大多是对转化医学的概括性描述,未系统地梳理转化医学的理论基础,对于国内外发展现状的研究主要集中在五年前的相关研究,对近年情况的分析较少,而且鲜有研究从科技管理的角度分析转化医学发展所遇到的问题。因此,本研究重点分析了转化医学的起源,在此基础上从转化医学的概念框架、过程模式、方法工具分析了其理论演化的过程,接着从转化医学机构建设、创新主体协作、经费资助、人才培养等维度提出转化医学发展面临的问题,并对未来发展进行展望,以期对我国推进转化医学发展提供借鉴。
1 转化医学的起源
转化医学理念的出现最早可追溯至20世纪60年代,McKinney等[6]从药物开发的角度提出要实现“从实验室到病床”(bench to bedside)。从半个多世纪的发展来看,转化医学的出现是“市场”需求拉动和科学发展到一定阶段的双重结果。
1.1 生物科技成果的应用需求
医药行业的投入产出比越来越低,英国近半个世纪,每十亿研发投入产出的新药数量平均每年下降8.4%[7]。Morris等[8]提出,在医学领域,从研究成果到临床应用时间差大约为17年。基因组学、蛋白质学及其相关学科产生了大量可能开发成药物的成果,但是制药公司却没有能力消化[9]。长久以来,学者们都认为生物医学研究者和患者之间存在着一个裂缝,在临床应用方面,健康领域只有很小一部分成果可以转化为有效的临床干预[10]。做基础研究的学者和临床医生都没有时间去理“死亡之谷”。
1.2 生物医学发展的推动
分子生物学、基因组学、蛋白质组学、转基因动物模型、结构生物学、生物化学、成像技术等为转化医学发现人类疾病的先进知识提供了空前的前景[11]。从历史角度来看,最早是从癌症研究开始的。Mulshine等[12]认为,对于癌症早期癌变细胞的发现、癌症生长因子的生物学机理分析等是实现对癌症有效干预的重要手段。Geraghy[13]认为,以分子生物学技术研究能够提升对基础致癌作用机制的认识。转化医学在癌症领域的影响力不断扩散,从各类癌症的转化研究扩散至其他疾病领域。
同时,分子生物学的暴发造成了基础研究与临床应用间的分离。Butler[9]认为,基础生物医学研究学者建立了通过在顶级期刊发表论文获得升迁和基金的机制,由此他们与临床医生之间的距离越来越远。这与NIH前院长Zerhouni[14]的观点一致,基础研究和临床研究之间的裂缝在越变越宽。
2 转化医学的理论演化
2.1 转化医学概念框架
当前没有获得广泛共识的“转化医学”含义,这一概念对于不同的人意味着不同的东西[15]。NIH国立转化医学中心(National Center for Advancing Translational Sciences,NCATS)主任Austin[16]把转化医学上升为一种科学,认为转化科学聚焦于应用在任何目标或疾病的一般情况,关注转化研究项目中的低效与失败,致力于阐明通用的作用机理,以此把“转化”从一个实证的现象的过程转变为预测科学。欧洲转化医学学会(European Society for Translational Medicine,EUSTM)提出转化医学经历了从“实验室至病床转化”“实验室至病床双向转化”“实验室、病床、社区双向循环转化”的不同阶段[17]。但这种认知并非是线性的,直至今日,后两种框架仍是共存的。
“从实验室到病床”是转化医学最早出现时的基本概念框架,即生物医学基础研究的成果应加速向临床、医药产业转化[6,13]。但是很快,人们就意识到实验室和病床之间应是一个双向转化的过程。Choi[18]早早提出的“实验室到病床再反馈”(bench to bedside and back)框架,认为基础研究可能有巨大的临床领域的应用前景,同时临床观察能够为基础研究提供直接证据。Marincola[19]称转化医学是一条“双向路”,临床的人体观察对于基础研究有重要的意义。之后,Nussenblatt等[20]又呼吁,当前从模型系统提出假设再进行检验的研究范式不利于开展基于临床问题的基础研究活动,应该遵循“事实驱动的研究”,从临床反向回到基础研究。《中国全科医学》期刊认为,转化医学是把生物基础研究的最新成果快速有效地转化为临床医学技术的过程,即从实验室到病床,再从病床到实验室的连续过程,简称为“B-to-B”[21]。此时,实验室与病床之间的双向转化已经被认为是连续的、可以不断迭代的过程。
在西方国家体系中,在实验室、病床之外,社区作为一个单独的利益群体也被纳入进来,由此提出了“实验室、病床、社区双向循环转化”框架。EUSTM和NCATS对于转化的理解都把社区观察包含在内。在我国,陈竺院士[22]提出,转化医学应包括基础研究、临床实践和政府决策三者之间的双向知识转化,转化医学的概念也可以拓展到公共卫生领域。同样,Lippi[15]也把公共卫生研究归入转化医学框架内,与实验室、临床三足鼎立。
基于以上分析可以看到,虽然转化医学没有共识的定义,但是开展转化医学活动的主体机构、科技期刊等基本认同“实验室、病床、社区双向循环转化”的概念框架,这可看作是转化医学的广义框架。由于社区/公共卫生与科研活动的结合相对更难,在当前的研究中,尤其是具体疾病领域的转化医学研发活动中,更多采用的是“实验室至病床双向转化”的框架,在此称之为转化医学的狭义框架。见图1。

图1 转化医学广义概念与狭义概念框架示意图
2.2 转化医学的过程模式
“转化医学就像一把伞,把基础研究、临床研究联合到了一起”[23]。在广义转化医学概念框架下,转化医学除了把基础研究、临床研究联合到一起,还把临床研究之后的临床应用,以及公众认同联合到一起。由此,转化医学是一个涵盖多个环节的长链条,许多研究者把转化医学过程进行了阶段划分。
较为概括的划分是把从基础研究成果产生的知识、机制、技术转化为疾病预防、诊断、治疗手段划分为T1阶段;把从T1阶段产生的成果促成医疗体系的重组、协调,帮助临床医生和患者改变行为习惯、进入公众认知都划分为T2阶段[24]。有的学者把过程做进一步细分,例如,从基础研究成果至第Ⅰ、Ⅱ期临床试验称为T1阶段;至第Ⅲ、Ⅳ期临床试验称为T2阶段;再至临床应用为T3阶段[25]。有部分学者强调转化医学范围应涵盖循证决策,即从医学研究到循证决策是转化医学不可分割的一部分[26]。在此基础上,把基础研究成果发展成为备选卫生实践划分为T1阶段;卫生实践发展为循证指南的价值评估为T2阶段;通过传播、扩散等研究把循证指南带到临床应用为T3阶段;“现实世界”中应用的效果评估为T4阶段[27]。
总体来看,过程模式同概念框架的扩展相一致,最终转化医学过程模式的划分涵盖从基础研究至社会全面应用或接受,本文从转化医学过程中关键环节间的“裂缝”角度进行划分,并从医疗服务(图2中实线连结部分)和医药产业(图2中虚线连结部分)两个层面提出一个全面的转化医学过程模式。见图2。
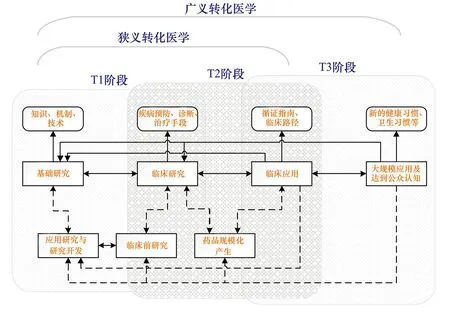
图2 转化医学过程模式示意图
基础研究跨越到临床研究为T1阶段,在医疗服务层面主要指从基础研究成果(包含知识、机制、技术等)转化为经过临床研究获得的疾病预防、诊断、治疗手段。其中包含医药产业层面基于基础研究成果进行应用研究、研究开发(如生产工艺研究、配方研究等)、临床前研究和Ⅳ期临床试验,通过临床试验的药品会纳入到疾病预防、诊断、治疗手段之中。
从临床研究跨越到临床应用为T2阶段,在医疗服务层面主要指把经过试验验证、评估的疾病预防、诊断、治疗手段进行标准化,形成指导临床应用的循证指南、临床路径等,从而使医生面对患者时治疗方案的选择更加科学化,规范医疗行为。其中包含医药产业层面在新药通过Ⅳ期临床试验后,开始规模化生产,药品的使用纳入到循证指南、临床路径内等环节。
从临床应用跨越到大规模应用及达到公众认知为T3阶段,主要指相关疾病预防、诊断、治疗的理念、知识传播至公众,促进公众形成新的健康习惯、社区卫生习惯,甚至促进整体社会医疗体系重组。T1阶段和T2阶段在狭义转化医学范畴之内;再加上T3阶段则构成了广义转化医学的范畴。
2.3 转化医学的研究方法与工具
转化医学是一门交叉学科[17,24,28]。在生物技术和医学领域的交叉基础上,还包含化学、计算机科学、数学和计算生物学以及材料科学等[4,29]。此外,Morrow等[30]认为行为科学是癌症领域转化医学效果实现的补充力量。Burgio[31]强调把社会科学干预措施转化应用至社区。
在交叉学科的基础上,转化医学在一定程度上已经形成了自己的基本研究方法,即逆向转化和迭代式的创新过程[32]。逆向转化的核心是认识到临床观察、临床信息对于生物医学基础研究的引领与辅助作用。而且,病床端关键问题的观察数据能够形成研究问题、成为研究基础,从而更快地应用于临床[33-34]。在具体医学领域中,这一点已得到了体现。例如,在肾病领域,采用逆向转化研究在临床和基础研究之间来回往复,以寻求最终的疗法,由此发现了细胞自噬方法[35]。
研究方法的实现需要工具的支撑,转化医学已经形成一定的得到广泛认可的方法工具。
(1)基因编辑工具。基因编辑工具是能够大范围应用于多个医学领域的医学工程技术,建立基因组学和转录组学测序平台能够支撑精准的、全面的疾病发病机理分析[36]。例如,CRISPR-Cas9(基因编辑工具的一种)在认识非肿瘤性血液疾病发生的基础机制中就能够发挥重要作用[37]。
(2)生物标志物。生物标志物是现代药物研发的新范式,是一项通用的加速知识转化到临床的技术[12,38]。生物标志物有很多种,如非编码RNA、蛋白酶等。以非编码RNA为例,Spizzo等[39]发现长链非编码RNA是肿瘤领域转化医学的新工具,可以在肿瘤领域的诊断、预后和治疗反应预测等各环节进行应用。
(3)干细胞。干细胞技术在多个疾病领域都可应用。例如,Maxwell等[40]通过CRISPR-Cas9对新生β细胞进行编辑,发现可实现逆转糖尿病。Soldner等[41]系统总结了多能干细胞与基因编辑技术结合对于治疗复杂疾病的重要作用,并且认为未来多能干细胞会产生更多的基础生物学和转化医学的见解。
这些研究工具在一些疾病领域、转化医学机构中已成为必须的基础设施。例如,南京鼓楼医院神经内科的范丽桢等[42]认为,卒中转化医学研究的主要工具应包含卒中发生、发展、预后判断的分子标志物,以及贴近人的动物模型等。又如,德国柏林健康研究所建有临床研究中心、健康数据平台等,提供如基因编辑CRISPR、多能干细胞等工具服务。随着生物学领域的不断发展以及多学科的不断交融,转化医学的方法工具体系将会进一步扩大。
3 转化医学发展面临的关键问题
转化医学的模式需要传统的医学研究体系进行改变,存在转化医学的支持机制、基础研究人员与临床人员间的隔阂、规章制度限制、经济效益较低等障碍[43],以及临床科学家和转化科学家队伍建设困难、工具与方法研究投入过少等挑战和问题[11]。经过近20年的发展,仍存在不少问题,从科技管理的角度可以分为以下四个方面。
3.1 转化医学机构建设问题
在转化医学理论体系逐渐成形的过程中,多个国家也在建设、调整转化医学机构。转化医学作为一个新的学科领域,如何建立适应转化医学模式的组织机构成为一项亟待解决的问题。
美国于2006年设立了临床与转化医学基金,重点资助区域性转化研究中心。之后,于2011年单独成立了NCATS,把临床与转化医学基金归入NCATS管理。从临床研究中心的建设到临床与转化医学基金设立,再到整合成立NCATS,美国对于转化医学机构的建设模式在不断调整。
英国于2006年成立英国国家健康研究所,专门资助转化医学活动,并于2007年成立健康研究战略协调办公室,以更好地协调不同机构面向转化医学的研究活动与经费分配。
德国于2009年~2012年,针对糖尿病、感染性疾病、心血管疾病、癌症、神经退行性疾病和肺病以联盟的方式成立了六个健康研究中心;2013年,又成立柏林健康研究所。柏林健康研究所从最初的内部民事合伙机构变更为公法团体(即公司),2019年又决定合并到夏里特医学院。其法人性质不断调整反映出德国仍在不断探索实体转化医学机构适宜的组织模式。
我国当前有五家国家级转化医学中心正在建设中。 “2010年~2013年,我国已建立各类临床和转化医学研究中心/平台机构等129家,分布于全国21省(市、自治区)”[44]。但据网络公开信息检索,截至2020年6月这些机构中有近一半停止了运行。
因此,对于转化医学机构建设一直存在很多争议。崔银河等[45]提出我国转化医学机构在顶层设计、体制机制等方面存在诸多问题。而且转化医学机构建设缺乏明确的标准和模式。我国当前在推进国家临床医学中心、国家医学中心的建设,通过对北京医管中心、部分医院的科研管理部门的访谈发现,此两者与转化医学中心(尤其是国家转化医学中心)的定位、功能差异及三者如何有效合作,都是未解之题。
3.2 转化医学的创新主体及主体间的协作问题
转化医学是一个生态系统,从人员个体角度来看,创新主体包括患者、学术界研发人员、产业界研发人员、商业化团队、投资资本、管理机构[46]。从机构个体角度来看,转化医学涉及的创新主体包括高校、研究院所、医院、社区医疗中心、科技管理部门、卫生行政部门、食品药品监督管理部门、社会学术团体、产业企业和科技中介等[47]。
转化医学的相关创新主体多样而复杂,不同个体间合作机制还未建立起来,如何使这些主体实现有效的协作是一个至关重要的问题。
3.3 转化医学的经费资助与分配问题
资金是转化医学活动开展的基础。面对转化医学这一新兴的科学领域,无论是资助范围还是经费分配、资助模式等都是需要研究的问题。Zerhouni[11]提出资助对象包括设施、机构、个人、生物样本存储库、分子筛选库等,NIH的确按此思想进行经费分配调整。在研究领域的分配上,Burgio[31]认为与对生物医学研究的资助总额相比,转化医学获得的经费资助很少;而且在转化医学领域内部,分配也并不均匀。Woolf[24]指出美国更倾向于投入到转化医学链条的前半阶段,即前面所述的T1阶段,但对于T2阶段和T3阶段投入的经费较少,事实上后者在拯救生命方面效益更高,应获得更多的经费。
转化医学领域应获得的经费规模,经费在转化医学领域内于上述过程模式中各阶段应如何分配,以及应采取怎样的资助模式都未有定论,这是转化医学政策领域的一项重要议题,需要引起更高的关注度。
3.4 转化医学的人才培养与评价问题
人才是转化医学发展的核心,转化医学专业人才的培养已受到学界关注。一类路径是对临床医学、基础医学等课程内容进行重塑,培养复合型人才,如以转化医学模式引导八年制医学生的基础研究、临床科研能力的共同培养[48];把转化医学理念融入基础医学课程[49]。还有一类路径是提升临床医师的作用,如以转化医学重构继续医学教育,提升卓越医师的转化医学综合素质[50];将转化医学的理念引进到医师职业精神中,指导医师行为[51];通过设立基础研究与临床实践合作基金、建立合作交流平台、基础与临床医师工作互换等方式使临床医师在转化医学中发挥更大的作用[52]。
在人才培养的同时,还涉及到转化医学人才评价的问题。代表性的研究如Van Dijk等[53]提出应在人才评价体系、个人事业发展空间等方面进行改革,为转化医学领域的人员构建职业认同和学术发展路径。但人才评价及人才职业体系构建是一个系统的问题,现在有一些机构进行了一定的尝试。例如,柏林健康研究所不再对个人成果进行评价,因为转化医学是多人协作的过程,所以对转化医学链条中的各个阶段成果进行综合评价。
我国对医学人才的评价也在做改革尝试,尤其近年一直在推进职务科技成果权属改革和科研人员评价改革,对于医学领域科研人员,包括医生,进入到转化医学进程中起到了一定的积极作用。例如,北京市在2019年出台了《北京市促进科技成果转化条例》,在其解读中特意提出有关高校院所的规定也适用于政府设立的医疗卫生机构;又如,我国出台的《关于深化项目评审、人才评价、机构评估改革的意见》和《关于优化科研管理提升科研绩效若干措施的通知》,要改进人才评价方式,实施分类评价。但当前,转化医学领域的人才评价标准还未建立。
4 展望
转化医学对于推进各类疾病的预防、诊断、治疗都是非常有效的一种模式,虽然对其概念没有形成一致的认知,但转化医学无论从学术上还是在政策议程上都在快速向前推进。转化医学在各类疾病领域都将发挥更大的作用,为提升人类健康水平贡献力量。
在转化医学理论层面,一方面,转化医学链条会进一步完善,公共卫生领域受重视程度将上升。另一方面,转化医学的方法工具体系将不断得到补充,基于此对于转化医学基础设施的需求会更加明确。
从科技管理角度看如何支持转化医学发展,交叉学科、多主体合作的特征对于其组织机构建设、人才评价机制等提出了很复杂的要求,这对于科技管理体制是一种挑战。第一,转化医学机构建设将会加速推进,但我国的国家转化医学重大基础设施、国家临床医学研究中心、国家医学中心及各地、各机构自行建设的转化医学中心应进行一定的统筹,以提升资源的利用率。第二,应从机构内部和外部构建新的机制促进不同创新主体进行合作,以此建设更有活力的转化医学创新体系。第三,转化医学应获得专项经费资助,这样才能保证转化医学的可持续发展。第四,在我国科研人才评价改革和成果转化机制不断完善的背景下,应针对转化医学各阶段的人才建立更为公平、更具激励性的评价体系。

