医疗器械评估中的不确定性特征及未来研究需求的确定
马兴华 岳立 孙尹晏

摘 要:关于采取医疗干预措施的决定是根据其成本和效果的证据作出的。由于各种原因,与医疗器械有关的证据可能受到限制。在设备生命周期早期,当设备基础最不成熟时,采用设备的决定可能会影响获得进一步证据以减少不确定性的前景。同样,拒绝一个设备将导致在实践中没有吸收,因此没有机会了解性能。决策选项,如“仅在研究中(OIR)”或“通过研究获得批准(AWR)”,可以通过允许患者尽早获得有希望的新技术来克服这些问题,同时在建立更多证据或学习之前,限制与错误决策相关的风险。本文阐述了与不确定性有关的问题和特定于设备的研究价值:学习曲线效应、增量设备创新、投资和不可恢复成本以及动态定价。我们展示了在何种情况下,只有在研究或批准的研究计划可能是一个适当的政策选择。我们还考虑如何在制造商和卫生部门之间分享额外研究的价值,以帮助告知合理预期谁将进行所需的研究。
关键词:医疗器械;医疗技术;不确定性;卫生技术评估
中图分类号:TH789 文献标识码:A 文章编号:1001-5922(2021)07-0159-04
Uncertainty Characteristics in Medical Device Evaluation and Determination of Future Research Needs
Ma Xinghua,Yue Li, Sun Yinyan
(3201 Hospital, Hanzhong 723000, China)
Abstract:The decision to take medical interventions is based on evidence of their costs and effects. For a range of reasons, evidence relating to medical devices may be limited. The decision to adopt a device early in its life cycle when the evidence base is least mature may iMPact on the prospects of acquiring further evidence to reduce uncertainties. Equally, rejecting a device will result in no uptake in practice and hence no chance to learn about performance. Decision options such as‘only in research(OIR) or ‘approval with research(AWR) can overcome these issues by allowing patients early access to promising new technologies while limiting the risks associated with making incorrect decisions until more evidence or learning is established. In this paper, we set out the issues relating to uncertainty and the value of research specific to devices: learning curve effects, incremental device innovation, investment and irrecoverable costs, and dynamic pricing. We show the circumstances under which an only in research or approval with research scheme may be an appropriate policy choice. We also consider how the value of additional research might be shared between the manufacturer and health sector to help inform who might reasonably be expected to conduct the research needed.
Key words:medical devices; medical technology; uncertainty; health technology assessment
0 引言
建立醫疗器械的临床有效性和成本有效性依赖于证据,这种证据通常比许多药品的证据更不广泛和数量更低。与制药公司不同的是,在获得上市许可之前,医疗器械通常只需要证明性能和安全性。设备的早期可用性可能看起来很有吸引力,因为它可以导致快速的临床应用;然而,当临床有效性和成本有效性不足时,医疗设备的投入使用就会具有很大的风险。对器械功效的不确定性以及实现预期功效所需的学习或培训可能会对患者的结果产生不利影响,并导致医疗资源的无效使用。因此,无论政策背景如何,都应考虑医疗器械评估中不确定性的特征,并确定未来的研究需求。
与医疗设备相关的独特特征,如快速的渐进式创新、学习效果和前期不可收回的成本,都对决策的时机和等待额外证据支持该技术的价值提出了挑战。与医疗器械评估相关的复杂性之一是,任何关于采用该器械的决定也将与收集更多与之有效性的证据。明确医疗设备的价值、研究降低医疗设备投入不确定性有着密切的联系。这些环节可以激励制造商进行相应的定价,并决定进一步的评估研究是否有足够的价值。制造商还需要一种方法,在产品开发开始时快速做出决定,并考虑在开发周期的不同阶段继续开发和研究的决定。
本文的目的是建立一个在医疗器械评估中描述不确定性和未来研究需求的框架。该框架基于所有技术所需的一些共同原则以及特定于医疗设备的一些额外原则。首先概述了共同原则。随后详细地描述评估不确定性所面临的额外原则,以及设备进一步研究的价值。
1 不确定性表征框架
1.1 技术的价值
一项技术,无论是医疗器械还是药品,如果其额外的健康效益预计将超过为适应技术的额外成本而削减其他活动所放弃的健康效益,则被认为是一种价值。这在两种预算约束的医疗保健系统中都适用,其中存在一个成本效益阈值,表示医疗支出的机会成本,以及没有固定预算约束但机会成本表现为其他形式支出的系统。这依赖于有关技术的有效性、对健康的长期影响(包括潜在的不良后果)、额外成本和对健康的机会成本的评估等等。
1.2 附加证据的价值
一项技术在其预期成本效益方面的价值是基于现有证据的平衡。然而,现有证据中的不确定性是不可避免的。这种不确定性来源于许多方面,这种证据上的不确定性最终导致采用该技术的决定的不确定性。额外的证据可以减少这种不确定性,从而降低对技术的使用做出错误决定的风险。需要对不确定性进行评估,评估不确定性对错误决策造成的健康损失的影响,以及进一步研究的必要性。还需要对进行研究的可能性、报告研究的时间长度和进行研究的费用进行一些评估。
1.3 激励研究
对额外证据价值的评估激励医疗体系确保所需的研究类型在不产生重大不可收回成本的情况下进行。然而,只有当一项技术被拒绝使用,但制造商认为有其他好处但没有证据时,制造商才可以保留进行研究的动机。对技术的价值和额外研究的价值如何在制造商和医疗系统之间共享的一些考虑可能会告知制造商是否可以合理地期望进行研究。如果技术对两个部门都有价值。确定社会和商业价值不匹配的情况,以及各部门之间如何分担成本和收益,是一个重要的考虑因素。
1.4 未来的变化
进一步的研究不太可能解决所有的不确定性。一些无法通过进一步研究减少的不确定性来源可能会随着时间的推移而发生其他变化。研究所产生的信息不会无限期地有价值,因为新的和更有效的干预措施可能变得可用,并且使信息不再与未来的临床实践相关。因此,新的或渐进式的创新也会改变一项技术的价值和未来的研究价值。
2 医疗器械特性及不确定度
2.1 学习曲线
当医疗器械被广泛应用于临床实践时,通常会出现一个与用户技能和技术培训相关的学习曲线。这种学习曲线可以对设备的效能和性能产生重要影响。设备评估面临的挑战是很难将技术的“真实”功效与使用该技术的有效性和临床经验之间的相互作用所产生的功效区分开来。由于用户重复任务的表现预计会随着时间的推移而随着经验的变化,因此对该技术的早期评估可能会偏向于新技术。学习曲线效应可以取决于许多基本机制,例如用户体验、社区体验/系统学习和特定中心患者的病例组合。这些机制不仅会改變对有效性的估计,而且还会随着时间的推移影响不确定性的规模,在学习的早期阶段预计会有更大的不确定性。
与学习相关的投资风险概况对于覆盖率决策非常重要,因为技术的批准可能会带来不可恢复的负净收益的机会成本。例如,如果该技术在学习的早期阶段被批准广泛使用(预期用户将变得更有经验),并且该决定随后被修订,由于更多的用户经验表明,技术不如最初预期的那样有效,或者额外的研究和/或其他变化报告了这一点,那么这些最初的损失将已经发生,不能用以后的收益来补偿。为了在学习曲线上的某一点判断最合适的覆盖率决定,新技术相对于其比较器的净效益是根据该点可用的证据估计的。还需要估计进一步研究的预期净收益。
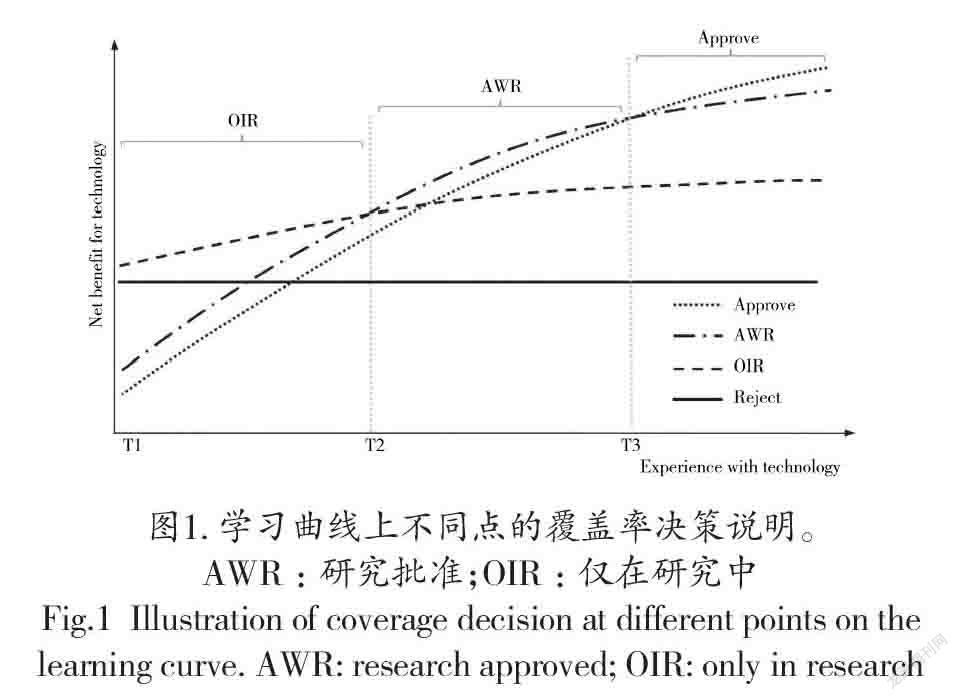
图1说明了学习曲线上不同点的覆盖决策的净收益。在这个例子中,OIR在学习曲线中最不确定的点(例如,用户体验较少的T1点)提供了最好的回报。这是因为OIR避免了负净收益的后果,直到有了进一步的经验和/或研究报告才能做出更明智的决定。在学习曲线的晚些时候(如T2)做出的决定表明,AWR提供了最佳回报,而在晚些时候(如T3),AWR的净收益不足以超过不批准该技术的机会成本。然而,在现实中,一项技术一旦被批准使用就很难在实践中移除。
2.2 增量设备创新
设备经常通过新的方法、升级和功能进行产品修改。这在一定程度上与希望尽快将设备推向市场,然后进行改进的改造有关。它还与使用设备的临床经验和设备本身之间的相互作用有关。例如,增量创新的很大一部分来自最终用户,他们建议制造商进行一些小的改进。一个很好的例子就是经导管主动脉瓣植入术。植入式设备通常与较新一代的电池容量和较低的植入失败可能性相关联,作为渐进式创新的结果,临床疗效和结果在首次评估时不太可能达到稳定状态。因此,证据的水平在很大程度上取决于技术在其生命周期中的地位。这表明,评估不可能是一次性的活动,随着时间的推移,随着更多证据的出现,可能需要迭代方法对评估进行修订。这将对覆盖范围决策产生影响,因为在技术生命周期的成熟期之前最好不要批准。 然而,由于增量开发和用户体验之间的紧密联系,所做的任何决定也将与收集额外证据的能力相互作用。
2.3 投资和不可收回成本
与其他技术相比,如果未来改变决定,与医疗设备相关的成本更有可能成为沉没成本。这尤其适用于具有与设备(例如磁共振成像机)的资本购买相关的大量前期投资成本的设备。这些前期费用通常按患者成本进行年金化和分配。如果未来的变化导致随后在设备寿命结束之前撤回技术覆盖范围,则这些成本代表无法收回的成本。例如,如果植入式装置的效果不如最初设想的那样好,那么与可以立即停止的药物相比,撤销决定就不那么简单了。在临床实践中引入设备也可能会带来更广泛的组织影响。这可能包括培训和学习成本和/或基础设施调整,如对专门房间的要求。
在通过技术或AWR批准对成本作出承诺之前,需要对这些不可收回成本的重要性进行评估。潜在的重要性取决于以下3点:①如果一项决定比预期的提前修改,成本效益的估计是否会改变;②该决定可能改变的可能性;③不可收回成本占技术总成本的比例。
圖2显示了EECP与对照组(不接受EECP治疗)相比的净健康效益,对照组目前和未来的患者的治疗选择将由决策决定。使用EECP治疗的初始成本很高,远远超过治疗初期产生负净效益的直接健康效益。这一负净收益被后期的正净收益抵消,但直到17年后,医疗体系才收回投资。如果研究报告(或其他变化)发生在17年的盈亏平衡点之前,则研究结果有可能表明该技术不具成本效益,在这种情况下,最初的损失是沉没成本,因为额外的健康收益没有在足够数量的患者身上累积,无法超过前期投资成本。
2.4 动态定价
与药品相比,医疗器械的价格随着时间的推移变化的可能性要大得多。这主要是由于新产品进入市场,随着时间的推移不断进行增量开发,设备采购更加灵活。设备和/或比较器的价格显然在确定设备是否具有成本效益方面起着关键作用。不过,这一价格也将对不确定性和附加证据的价值产生重要影响。最简单的形式是,如果降低了技术价格,提前获得技术将有更大的好处,如果技术已经被预期在原价上有价值,那么附加证据的价值将趋于下降。技术决策的结果也会直接影响定价。例如,比较器技术(即不被认为具有成本效益的技术)的价格可能会迅速下降,并且可能会比新技术的价格下降得更快,从而改变对成本效益和不确定性水平的隐含估计。
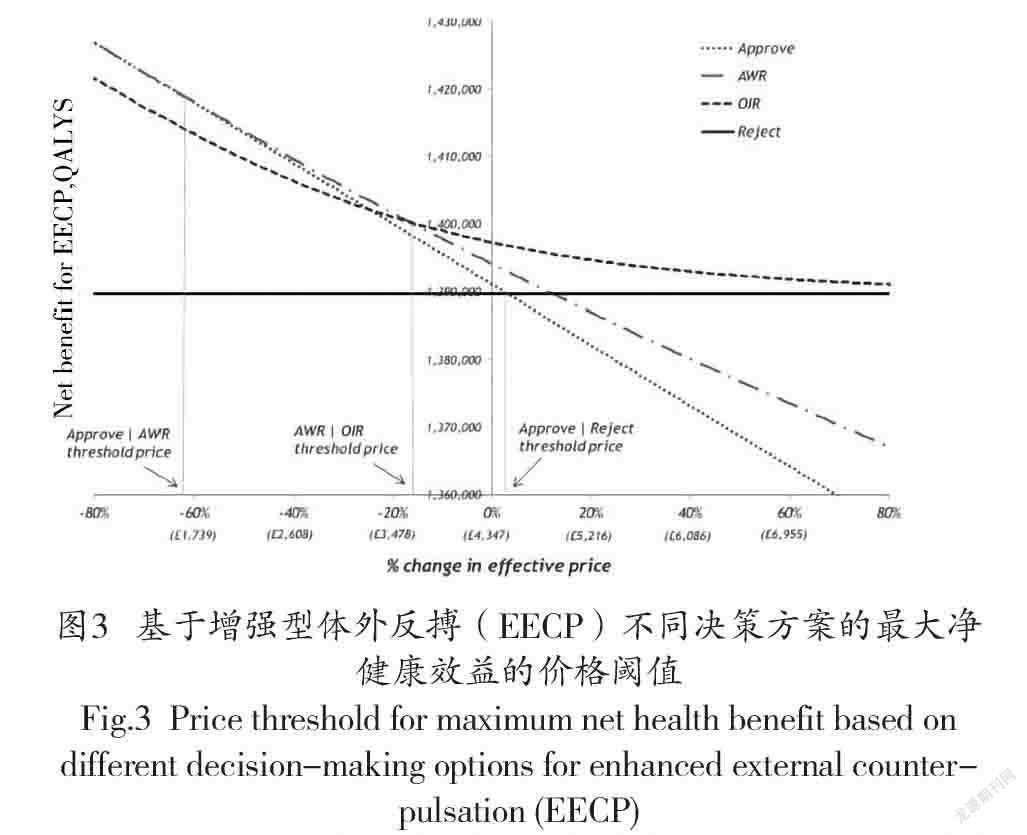
图3显示了当研究需要3年来报告时,基于不同决策选项的最大净健康效益,EECP决策发生变化的价格阈值。曲线外包络上的决策期权是在每种价格下提供最高净收益的期权。尽管根据证据,EECP在英国的当前价格为每名患者4347英镑,预计具有成本效益,但OIR在这个价格下提供了更大的预期净健康效益。这是因为它避免了重大的不可收回成本的承诺,如果研究结果表明应撤销其最初批准,则无法收回这些成本。也就是说,不限于开放源码软件,所需的价格要低得多,因为存在着巨大的不可收回的机会成本。
3 结语
文章阐述了在处理不确定性时需要考虑的概念问题,以及进一步研究医疗器械的价值。本文着重于所需的原则和评估,而不是分析方法。所需评估和分析方法之间的这种区别认识到,评估的信息方式可能在不同类型的医疗保健系统和司法管辖区之间有所不同。分析方法可能比原则本身更易于实施。即使这些概念不是通过正式的分析方法来实现的,在对一项技术作出决定时,也应将其作为审议过程的一部分加以考虑。
该框架的制定旨在提高在采用创新的临床和成本效益高的医疗技术方面发挥重要作用的考虑因素的交流透明度,并确定何时可以合理地预期赞助者提供研究。在OIR或AWR方案下进行研究的前景更加复杂,因为如果制造商有一些关于不确定性的信息,而监管者没有这些信息,就可能出现信息不对称。制造商和卫生系统之间的代理关系也将在面对各种不确定性模式时发生变化。因此,价格、不确定性、附加证据的价值与相关机构之间潜在的信息不对称之间存在着重要联系。
参考文献
[1]Claxton K,Griffin S,Koffijberg H,et al.How to estimate the health benefits of additional research and changing clinical practice[J].British Medical Journal,2015:351-398.
[2]Karl Claxton,Stephen Palmer,Louise Longworth,et al.A comprehensive algo rithm for approval of health technologies with, without, or only in research: the key principles for informing coverage decisions[J].Value in Health,2016,19(6):885-891.
[3]Alan Girling,Richard Lilford,Amanda Cole,et al.Headroom approach to device development: current and future directions[J].International Journal of Technology Assessment in Health Care, 2015,31:331-338.
[4]Claire McKenna,Marta Soares,Karl Claxton,et al.Unifying research and reimbursement decisions: case studies demonstrating the sequence of assessment and judgments required[J].Value in Health,2015,18(6):865-875.
[5]Karl Claxton,Andrew Briggs,Martin J Buxton,et al.Value based pricing for NHS drugs:an opportunity not to be missed?[J].The BMJ,2018,336.
[6]Louis P.Garrison,Adrian Towse,Andrew Briggs,et al.Performance-based risk-sharing arrangements-Good practices for design, implementation, and evaluation: report of the ISPOR good practices for performance-based risk-sharing arrangements task force[J].Value in Health 2013,16(5):703-719.
[7]Nicolas Martelli,Hélène van den Brink.Special funding schemes for innovative medical devices in French hospitals:the pros and cons of two different approaches[J].Health Policy,2014,117:1-5.
[8]Claire McKenna,Neil Hawkins,Karl Claxton,et al.Cost-effectiveness of enhanced external counterpulsation (EECP) for the treatment of stable angina in the United Kingdom [J].International Journal of Technology Assessment in Health Care,2010,26:175-182.

