超重力法脱除氮氧化物实验研究
*孙艺 于正林
(长春理工大学 吉林 130022)
氮氧化物(NOx)是大气重要污染源之一,主要危害有生成酸雨和光化学烟雾对森林植被造成巨大伤害、腐蚀建筑和设备、导致人类疾病等[1],氮氧化物的治理研究问题迫在眉睫。
目前常用的处理氮氧化物的方法主要分为:干式吸收法和湿式吸收法。干式吸收法主要包括催化还原法、催化分解法、吸附法与电子线照射法等。湿式吸收法主要包括水吸收法、酸吸收法、碱吸收法等。工业上常用的脱硝技术是选择催化还原法(SCR),但传统塔器设备体积过大,许多老式锅炉没有预留足够的安装空间[2]。
超重力技术顾名思义是超过重力场,通过旋转产生离心力来模拟一种比地球重力加速度大的环境,使得气相和液相能够充分接触。在多相流质量的传递过程中,超重力在该方面起着积极的作用,在离心力的作用下,制造更大的传质面积、更薄的液膜和更强烈的液体湍动,实现了更好的微观混合[3],以达到加速传质的目的。相对传统塔器设备,超重力设备以其体积小、能耗低、极大强化传质过程等特点被广泛应用于精馏、吸收、萃取等传质和除尘、纳米粉体制备等领域[4],秦月娇等[5]在此技术的基础上,实现了降解苯胺废水的目的。段绍君等[6]完成了超细碳酸锂粉体的制备工作。在脱硝方面,李裕等[7]在臭氧存在下用超重力机研究HNO3吸收NOx的效果。近年来,超重力设备在脱除工业气中其他气体方面也有研究。
本文中,采用湿式吸收法作为处理方法,使用自制超重力设备作为反应设备,吸收剂组成为KOH和H2O2混合溶液,考察转速、气液比、反应温度、H2O2溶液浓度、KOH溶液浓度对脱除效率的影响,制定出一套能够达到最佳脱除效率的方案。
1.实验
(1)碱液吸收法吸收机理
碱液吸收法采用KOH和H2O2混合溶液作为液体吸收剂。氮氧化物在液相中进行化学反应生成HNO2和HNO3,与KOH溶液反应生成产物为KNO2和KNO3,主要化学方程式为:
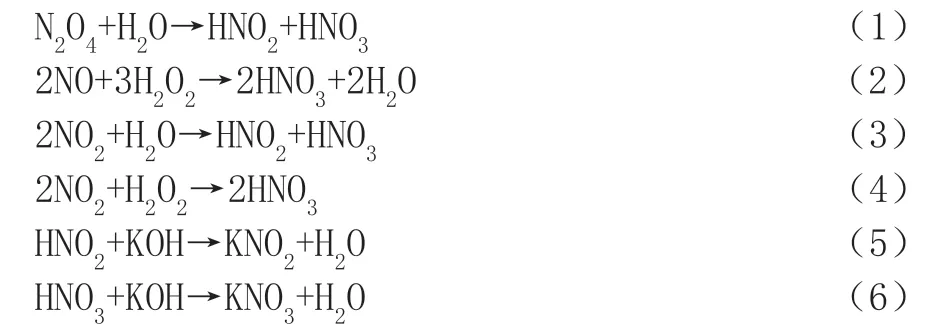
(2)实验流程
工艺流程为:气体在系统外充分混合后由风机引入沿径向进入超重力设备,碱液贮罐和过氧化氢贮罐中的KOH和H2O2溶液经过计量泵在药剂循环罐中混合作为吸收剂,通过循环泵进入超重力设备,由液体分布器喷洒在填料内腔,吸收剂在离心力的作用下沿径向流过填料,过程中与气体不断进行逆流接触充分反应。反应后超重力设备中的剩余气体由气体出口排出,然后通过旋转板式除沫器除沫后再进行尾气排放。液体吸收剂被甩到空腔中由液体出口流出,回到药剂循环罐,药剂循环罐和超重力设备之间始终在循环泵作用下不断进行循环。超重力设备转速、进气量和进液量由电机和涡街流量计进行控制,控制过程通过控制柜完成,整个工艺流程如图1。
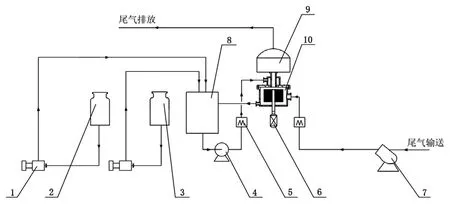
图1 工艺流程图
(3)NOx脱除效率计算
液体吸收剂对NOx的脱除效率是通过测量超重力旋转床出入口NOx气体浓度来计算,计算公式为:

式中:η-NOx脱除率;
C1-超重力旋转床入口处NOx气体浓度,单位为ppm;
C2-超重力旋转床出口处NOx气体浓度,单位为ppm。
2.实验结果分析及讨论
(1)超重力设备转速对NOx脱除效率的影响
初始条件设定为气液比10:1,反应温度为30℃,吸收剂分成四种情况进行实验:水、0.04mol/L KOH溶液、0.1mol/L H2O2溶液以及上述浓度两种溶液的混合溶液。分别取150-1500rpm十个转速,讨论并分析超重力设备转速对NOx脱除效率的影响,如图2所示。

图2 转速对脱除效率的影响
分析图2可以得出,转速的不断增加的过程中,以水为吸收剂,脱除效率波动较小,在30%-35%之间;以H2O2溶液作为吸收剂,脱除效率保持在60%左右;以KOH溶液作为吸收剂,脱除效率只能保持在50%左右;以KOH和H2O2混合溶液作为吸收剂时,脱除效率好于之前的情况。当转速达到900rpm时,脱除效率为81.96%,后续转速继续提高,脱除效率有所下降。
根据实验结果可见:相同条件下,转速较低时,气液停留时间长,随着转速增加,能够增加填料对吸收剂的切割力度和程度,液体被粉碎为液滴和液膜;在转子的转动下,气体和液体的接触面积扩大,气液充分反应,传质效率和脱除效率稳步提高。转速继续提高,超过900rpm时,离心力增大,液体还没有来得及被填料转子切割粉碎便在离心力的作用下被甩出超重力设备,因此导致NOx脱除效率大大降低。最终选用转速为900rpm。
(2)气液比对NOx脱除效率的影响
设定条件为:转速900rpm、反应温度30℃、吸收剂组成为H2O2浓度0.1mol/L和KOH浓度0.04mol/L的复合溶液,其余参数同2.1。气液比对脱除效率的影响,见图3。
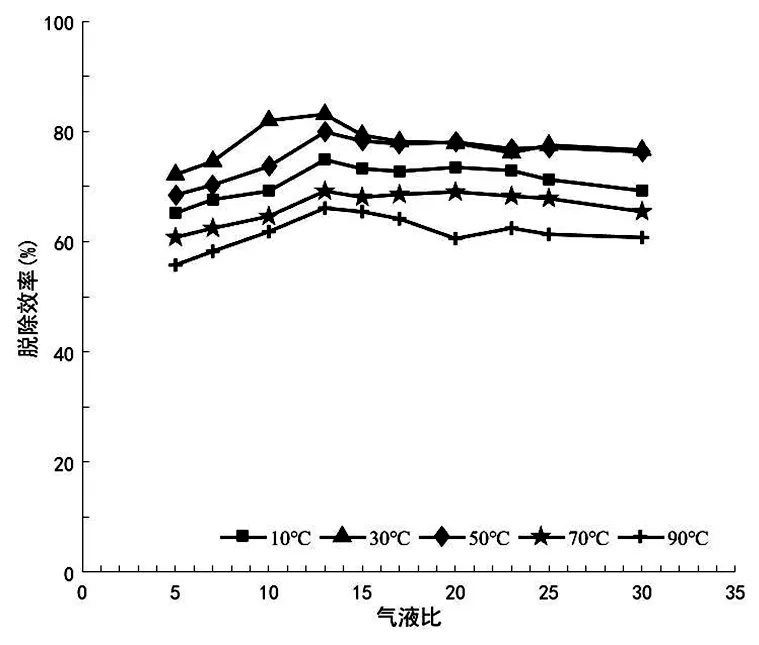
图3 气液比对脱除效率的影响
根据图3结果分析可知,适宜的气液比是13:1。在5:1到13:1这个阶段,脱除效率逐步上升,说明提高进气量确实起到了提高脱除效率的效果。但是超过13:1之后,脱除效率波动不再明显,甚至略有下降。增大进气量就是增大进气速率,在某个范围内有利于传质,会提高脱除效率。但是如果超出合适范围气体还来不及跟液体接触反应便被甩出超重力设备,达不到理想的脱除效率;若大幅减小进气量,又不符合实验目的,达不到期望的脱除效率。综合考虑经济性,气液比的合理选择为13:1。
(3)反应温度对NOx脱除效率的影响
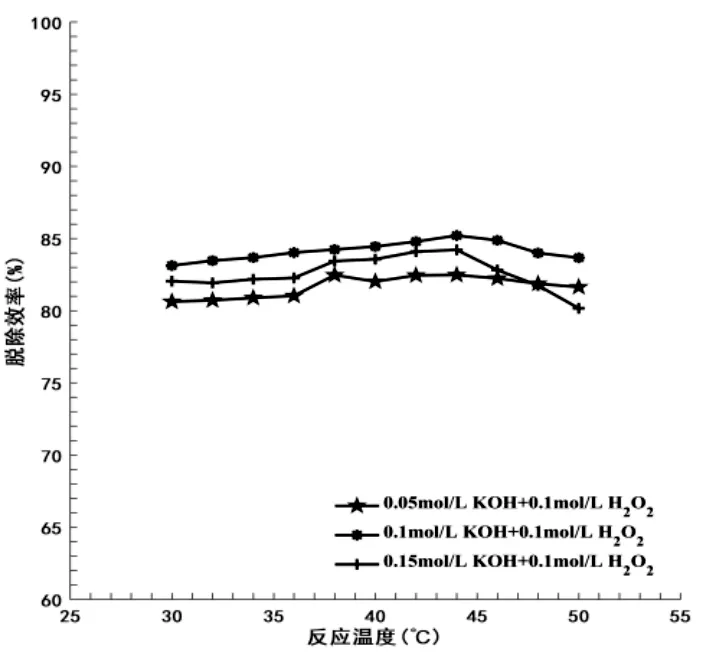
图4 反应温度和KOH对脱除效率的影响
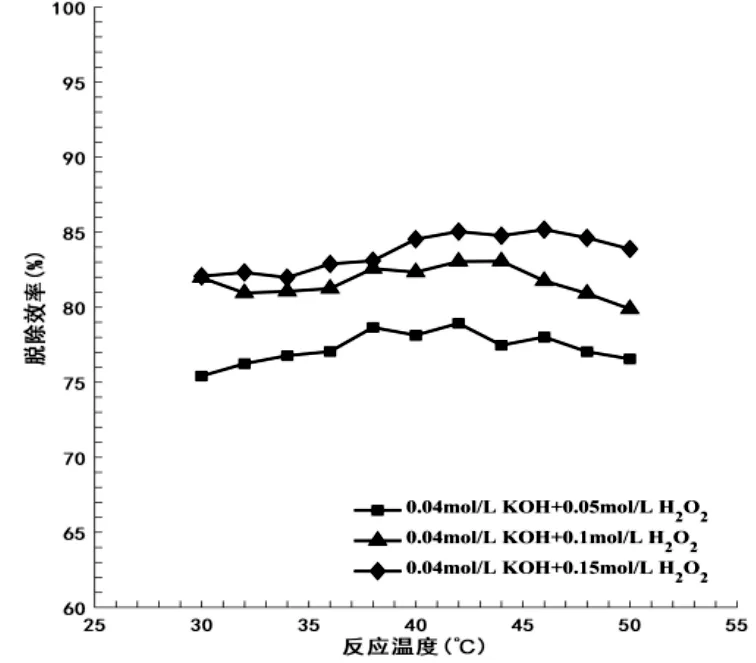
图5 反应温度H2O2对脱除效率的影响
气液比的实验中可以观察到反应温度对脱除效率有影响,大胆猜测最佳反应温度在30℃-50℃之间,在此范围内改变反应温度进行实验确定最佳反应温度。吸收剂采用两种方案:一是保持H2O2浓度0.1mol/L不变,分别改变KOH浓度为0.05mol/L、0.1mol/L、0.15mol/L;二是保持KOH浓度0.04mol/L不变,依次设定H2O2浓度为0.05mol/L、0.1mol/L、0.15mol/L。其余参数同2.2,分析反应温度对NOx脱除效率的影响。反应温度和KOH浓度对脱除效率的影响见图4,反应温度和H2O2浓度对脱除效率的影响见图5。
图4和图5可见,最佳脱除效率反应温度在42℃-44℃之间,脱除效率在整个过程中先上升后持平。随着KOH浓度增加,脱除效率均有所波动但幅度不大,此时的吸收反应在整个过程中不是关键。H2O2浓度不断增加,脱除效率有所上升,说明提高NOx的氧化程度能有效提高脱除效率。综合分析,最佳反应温度选择42℃。
(4)H2O2浓度对NOx脱除效率的影响
设定条件:转速900rpm,反应温度为42℃,H2O2溶液分别取0.05mol/L、0.1mol/L、0.15mol/L、0.2mol/L、0.025mol/L、0.3mol/L、0.35mol/L、0.4mol/L八个浓度,其余参数同2.1进行实验。图6为H2O2溶液浓度对脱除效率的影响。
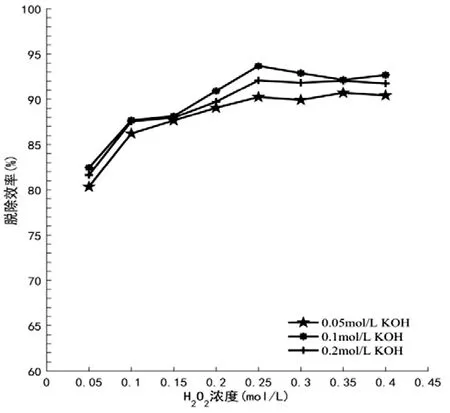
图6 H2O2溶液浓度对脱除效率的影响
由图6可知,整体趋势是:随着吸收剂H2O2浓度不断地增加,整体的脱除效率是先增加然后逐渐保持稳定。在这个阶段,随着H2O2浓度升高,NO被氧化成易溶于水的NO2和N2O3,脱除效率逐步提高,说明氧化程度直接影响脱除效率。但是继续提高H2O2浓度,脱除效率略有降低但基本保持稳定,此时吸收反应才是关键。在相同H2O2浓度下,KOH浓度大的对脱除效率更有利。尽管还存在高于现有脱除效率的情况,但是考虑经济性,0.25mol/L的H2O2溶液最为适宜。
(5)KOH溶液浓度对NOx脱除效率的影响
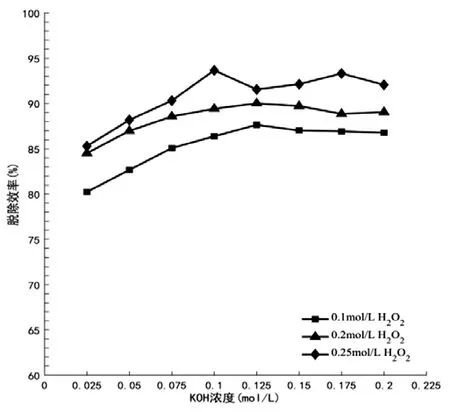
图7 KOH溶液浓度对脱除效率的影响
转速900rpm,反应温度为42℃、吸收剂为含KOH和H2O2的混合溶液,H2O2浓度选择:0.1mol/L、0.2mol/L、0.25mol/L,其余参数同2.1,讨论KOH浓度对NOx脱除效率的影响。实验分别在以下8个不同浓度进行,浓度分别为0.025mol/L、0.05mol/L、0.075mol/L、0.1mol/L、0.125mol/L、0.15mol/L、0.175mol/L、0.2mol/L。图7反应的是KOH浓度对脱除效率的影响。
由图7可知,在图示三种H2O2浓度下,KOH浓度增加,NOx的脱除效率均先增加后基本持平。当KOH溶液浓度还处在较低的时候,NOx中的氧化产物传质速率加快,脱除效率提高。脱除效率达到最佳是当0.1mol/L KOH时,此时的脱除效率为93.66%;KOH溶液浓度继续提高,传质速率受到限制,脱除效率变化不明显。KOH溶液浓度的高低,直接决定了OH-的量,直接影响了参加反应的OH-的量。高浓度的溶液OH-的量比低浓度的溶液的OH-的量要高,参加反应的OH-的量也大,脱除效率便会提高。当KOH溶液浓度足够大,OH-的量达到饱和,对整个反应过程的影响也达到了一定程度,脱除效率基本维持在相应水平。根据以上判断,KOH溶液浓度选择0.1mol/L。
3.结论
(1)实验结果表明,超重力设备转速增加,脱除效率先增加后下降;脱除效率随气液比增加先增加后基本稳定;脱除效率随反应温度升高先增加后基本持平;脱除效率随KOH溶液浓度先增加后基本持平;脱除效率随H2O2溶液浓度先增加后持平。
(2)实验结果表明,在实验过程中不能一味增大或减小因素参数,进气量过度提高会导致气体流速过快,不能与液体充分反应,降低传质效率。进液量过量增大会导致吸收剂不能得到充分剪切,降低脱除效率。合理适宜的实验条件是得到最佳脱除效率的基础。
(3)采用超重力法脱除含氮氧化物的废气。超重力设备转速为900rpm、气液比为13:1、反应温度为42℃、吸收剂使用双组分吸收剂,H2O2溶液浓度取0.25mol/L、KOH溶液浓度取0.1mol/L。该种方案可以让脱除效率达到最佳,为93.66%。

