MgO吸附剂捕集CO2的研究进展
徐运飞,李英杰,王 涛,雷文涛
(1.山东大学 能源与动力工程学院,山东 济南 250061;2.山东纳鑫电力科技有限公司,山东 济南 250101)
0 引 言
随着工业化的推进,化石燃料大量开发利用,CO2等温室气体大量排放造成的全球气候变化是21世纪以来人类面临的严峻挑战之一,世界各国对控制和减少碳排放已达成共识[1]。煤炭是我国能源消耗的主体,煤气化或煤燃烧发电技术的飞速发展已成为社会发展不可缺少的推动力,但能源消耗与CO2排放等环境问题日益突出。因此将煤气化或燃烧发电系统与CCUS技术结合,可在获得高效率的同时有效减少CO2排放,为煤发电技术提供新的发展方向[2]。CCUS技术主要是指将CO2从化石燃料、工业流程或火电厂的排放废气中分离出,运输到特定地点加以利用或封存,以实现被捕集CO2与大气的长期隔离[3]。
利用固体吸附剂捕集CO2是CCUS技术中常用的方法。固体吸附剂主要分为:低温固体吸附剂(如固体胺、沸石等[4])、中温固体吸附剂(如类水滑石衍生物(LDH)、MgO等[5])、高温固体吸附剂(如CaO基材料等[6])。MgO具有理论CO2吸附能力高、无毒性、成本低、工作温度范围宽和再生温度相对较低等优点,因而具有较大工业应用潜力。MgO可在200~400 ℃内捕集CO2,在450~500 ℃再生[7-8]。本文对MgO吸附剂捕集CO2研究进行了总结,介绍了MgO吸附CO2的性能变化,分析总结了提高MgO吸附剂捕集CO2性能的方法,并对MgO捕集CO2技术进行了总结及展望。
1 MgO基材料吸附CO2特性
MgO捕集CO2反应主要以化学吸附为主,CO2与MgO在200~400 ℃下发生化学反应,生成MgCO3。MgCO3在450~500 ℃下逆向脱附再生成MgO和CO2。具体吸附再生反应式如下:

(1)

(2)
MgO的理论CO2吸附容量达24.8 mmol/g,但纯MgO的实际CO2吸附量很低(0.5 mmol/g),因此限制了其大规模工业应用[8]。MgO吸附CO2性能大小主要取决于MgO表面氧离子的配位状态,通常位于晶格边缘、角落处的氧离子有较高碱性,为吸附CO2的活性位点[9]。MgO较低的CO2吸附量一方面是由于常规MgO比表面积较小,表面碱性位密度较低,碱性位点暴露少[10]。另一方面,MgO吸附CO2后表面形成的碳酸盐钝化层覆盖邻近碱性位点,阻碍了CO2进一步被MgO吸附[11]。由于MgO的强晶格焓和来自碳酸盐产物层的扩散阻力产生的高反应势垒,使得碳酸化反应缓慢,从而使CO2吸收量非常低[12]。因此有必要提高常规MgO对CO2的吸附能力。
用于工业捕集CO2的固体吸附材料,需研究其吸附CO2性能,另外再生能耗也是制约其大规模应用的重要因素,较高的再生温度要求输入更高热量以及更多昂贵设备与过程匹配,使成本增加[13]。MgO因其再生能耗低、材料成本低等优点,是工业CO2捕集中极具潜力的吸附剂材料。Kumar等[13]总结比较了不同固体吸附剂的CO2吸附性能,讨论了常用固体吸附剂(如锂基吸附剂Li4SiO4,钙基吸附剂CaO、MgO等)的循环吸附CO2性能。不同于锂基、钙基等较高再生温度(800 ℃以上),MgO再生通常在450 ℃时即可发生。过高的再生温度导致吸附材料严重烧结,使吸附材料活性降低,循环稳定性差。Hwang等[14]研究了压力0.1~3.0 MPa内碱金属硝酸盐改性下MgO的CO2吸附解吸特性,并利用程序升温解吸(TPD)研究了再生过程中气体组成对MgO再生性能的影响,结果表明,再生温度升高会导致能耗增加。在纯N2条件下,最佳再生温度约为430 ℃,MgO吸附CO2量能达15.4 mmol/g。MgO再生过程采用100% CO2作为再生气氛时,所需再生温度升到620 ℃。
在工业CO2捕集过程中,由于MgO粉末粒径分布不均或因磨损和破碎而产生的小粒径粉末颗粒,在应用于流化床反应器时极易逸出反应器,造成吸附剂材料的浪费及设备的损坏;此外造粒后的MgO吸附剂在循环工作后由于碰撞等原因会造成颗粒破碎[15],因此有必要研究吸附性能及机械性能高的MgO造粒工艺。张钰伟等[16]采用湿式混合法制备了NaNO3/NaNO2掺杂的MgO吸附剂,并对其进行挤压-滚圆造粒,发现该成型球粒MgO的CO2吸附性能较优异,吸附温度为340 ℃、100% CO2时,CO2吸附量最大达15 mmol/g,经10次循环后仍保持较高的CO2吸附量(8.18 mmol/g)。陈林等[17]以CMC(羧甲基纤维素钠)为黏结剂制备了柱状MgO颗粒吸附剂,结果表明,煅烧温度为500 ℃、CMC添加量为20%时,MgO颗粒具有最高比表面积和机械强度,50 ℃、常压下的CO2吸附量可达 0.57 mmol/g。Jin等[18]制备了掺杂LiNO3/KNO3/Na2CO3的MgO混合溶液,并采用油包水法合成了粒径几百微米的MgO球形颗粒,研究了造粒后的MgO吸附CO2性能,结果显示,在300 ℃、纯CO2吸附条件下,10次循环后MgO球粒具有稳定CO2吸附量,为5.2 mmol/g。
在流化床系统中,除了要提高造粒后MgO吸附剂的CO2吸附性能,还需提高造粒材料的机械强度,以更适合工业应用。Hu等[19]利用挤出-滚圆法对NaNO3或Na2CO3掺杂的复合MgO吸附剂进行造粒,研究了造粒后MgO颗粒的机械强度(如抗压强度、颗粒磨损度)和CO2吸附性能,研究结果表明,造粒后MgO颗粒具有良好的机械性能:较高抗压强度(颗粒抗压峰值大于3 MPa)以及较低磨损消耗(质量损失平均值小于4%)。此外由于加入碱金属盐掺杂剂,其造粒后MgO颗粒具有较大的比表面积,因此在循环吸附/再生过程中,造粒后MgO比粉末MgO具有更稳定CO2吸附性能,但造粒后MgO反应速率比粉末低。
MgO吸附剂可用于燃烧前CO2捕集,如整体煤气化联合循环发电系统(IGCC)。图1为MgO吸附剂用于IGCC电厂示意,该电厂的合成气温度为250~450 ℃,常用MgO吸附剂将合成气中的CO2与H2分离,剩下高浓度H2用于燃烧或燃料电池发电[20]。MgO吸附剂除了用于合成气CO2分离,还用于吸附增强水煤气变换反应(SEWGS)来提升H2产量[21]。通过MgO对CO2的吸附,打破反应平衡,使反应向正向进行的程度加大,从而H2产量增加。图2为MgO用于SEWGS反应提升H2产量的示意[22]。Abbasi等[23]在高压填充床装置中模拟了MgO吸附剂在预燃烧合成气环境中的CO2吸附性能,结果表明,MgO吸附剂在水煤气转化(WGS)反应中的CO2吸附量达2.9 mmol/g,这可使WGS反应转化率增至40%,可认为通过MgO吸收CO2显著提升了H2产量。Hu等[24]利用硝酸盐和碳酸盐掺杂的复合MgO吸附剂对WGS反应中产生的CO2进行原位脱除,掺杂碱金属的MgO吸附剂具有优异的CO2吸附性能,该吸附剂用于SEWGS反应过程中可产生纯度约99.5%的H2(反应条件为300 ℃、1.216 MPa、水蒸气与碳比值为1.5)。
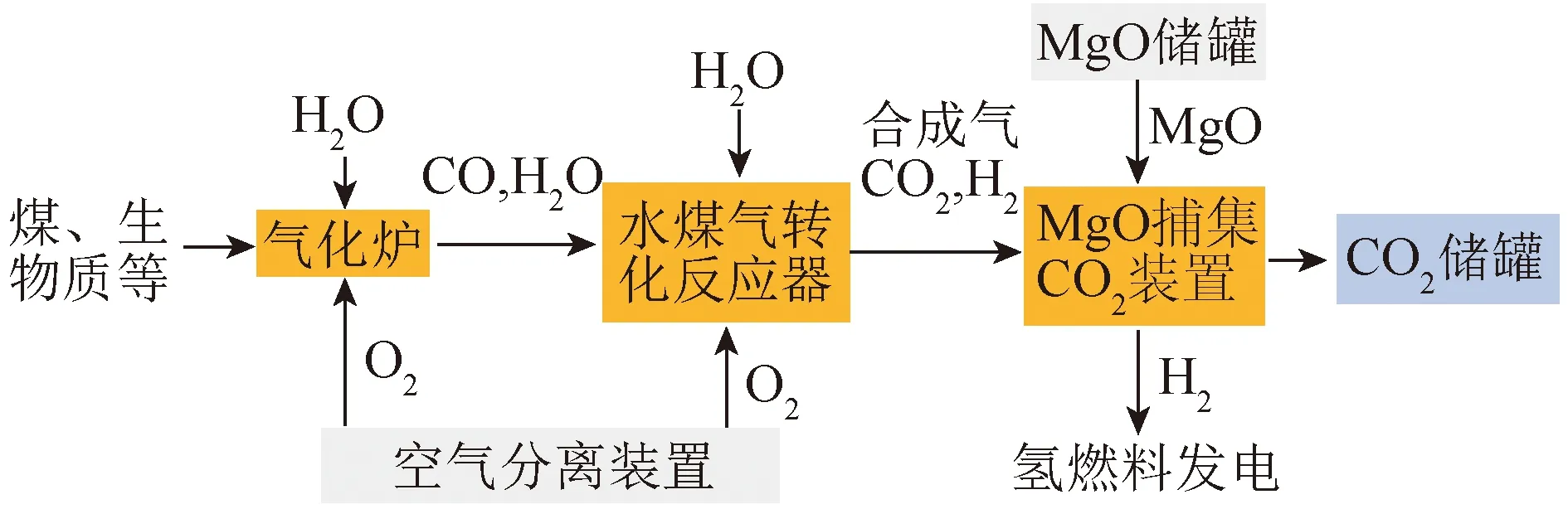
图1 IGCC发电厂的MgO捕集CO2示意[20]

图2 MgO用于SEWGS反应提升H2产量的示意[22]
MgO吸附剂除了用于燃煤电站捕集CO2,还可用于净化环境吸附CO2。Halawy等[25]为监测实验室内CO2污染水平,利用声化学法制备的纳米MgO吸附剂对学校有机化学实验室内的CO2进行吸附。将制备的纳米MgO暴露于17~19 ℃室内环境中,采用热重分析仪对吸附过程实时监测,结果表明,56 d后,MgO吸附环境CO2量为7.9 mmol/g,并在500 ℃、纯N2下对此时的MgO样品煅烧后,通入纯CO2流,发现MgO材料仍有较高CO2吸附性能。
2 微观结构优化MgO的CO2吸附性能
优化MgO微观结构,可显著提高其比表面积,获得发达的孔隙结构,使MgO表面具有丰富且暴露的碱性吸附位点。常用的通过优化MgO微观结构提高CO2吸附性能的方法有:从不同前驱体制备获得MgO;将MgO负载在多孔载体上;添加金属氧化物制备MgO复合材料。
2.1 源于多类型前驱体MgO
与纯MgO较低的CO2吸附容量相比,从天然含镁矿物(如菱镁矿、水菱镁矿、水镁石)制得MgO的CO2吸附性能更高。Guo等[26]研究了通过煅烧含镁矿物制得MgO的CO2吸附性能,发现200 ℃时,由水菱镁矿和水镁石分别煅烧制得的MgO吸附剂的CO2吸附量较高(分别为1.73 mmol/g和1.67 mmol/g),且10次循环后吸附量仅分别降低了5.65%和5.33%,这主要是由于天然含镁矿物煅烧后具有较发达孔隙结构,降低了CO2在产物层的扩散阻力,提升了CO2吸附容量。除了天然含镁矿物外,成本低廉的MgO基工业废弃物也被用作MgO前驱体来捕集CO2。菱镁矿渣是菱镁矿冶炼过程中通过硅热还原法获得金属镁的一种废料。Yang等[27]通过煅烧菱镁矿渣得到MgO吸附剂,研究了湿烟气中MgO对CO2的捕集能力,结果表明:通过煅烧废渣得到的MgO最大CO2吸附量为3.01 mmol/g,8次循环后降至2.18 mmol/g,其吸附性能明显优于菱镁矿(CO2吸附量为1.82 mmol/g)。因此利用菱镁矿渣捕集CO2不仅可减少温室气体CO2排放,还可综合利用工业废渣。
Alkadhem等[28]以硝酸镁和氢氧化铵为原料,采用溶胶-凝胶法制备了多孔MgO,其比表面积高达350 m2/g,CO2吸附量为0.68 mmol/g(常压,30 ℃)。多孔MgO与APEST(3-氨基丙基-三乙氧基硅烷)功能化后的CO2吸附量增至1.47 mmol/g。胺官能化MgO吸附剂表现出高CO2捕集性能和理想的吸附选择性,但其热稳定性和机械性能需进一步提高。Tan等[29]研究表明,在不同温度和气氛下煅烧草酸镁制得MgO的CO2吸附性能不同,研究认为草酸镁在较高或较低温度下煅烧都不利于MgO吸附CO2,草酸镁在较低温度下煅烧很难完全分解形成多孔结构,因此制备的MgO可用于CO2吸附的碱性活性位点有限;而在较高温度下煅烧草酸镁将导致MgO晶体烧结、孔隙结构堵塞和碱性活性位点损失。草酸镁在500 ℃、CO2气氛下煅烧时,制得的MgO具有最大CO2吸附量,为5.09 mmol/g。Guo等[30]以六水氯化镁为前驱体,采用不同合成方法制备MgO,研究该MgO微观结构与CO2吸附性能之间的关系,结果表明,用固态化学反应法制备的MgO材料具有发达的孔隙结构(比表面积和比孔容分别为100.03 m2/g和0.67 cm3/g)、较好表面形态(具有较低的层扩散阻力的片状结构)和较高CO2吸附能力(2.39 mmol/g),这是由于固态化学反应法赋予MgO丰富的表面碱性活性位,强化了CO2吸附。
表1为通过多种前驱体类型制备MgO的CO2吸附性能。通过不同前驱体制备MgO的CO2吸附性能均有所提高。Guo等[31]研究认为,通过前驱体改性方法能提高MgO的CO2吸附性能,主要是因为前驱体在煅烧制备MgO过程中会释放气相产物,在吸附剂内部形成疏松多孔结构,从而有效改善MgO吸附剂微观结构、表观形貌以及活性位点。
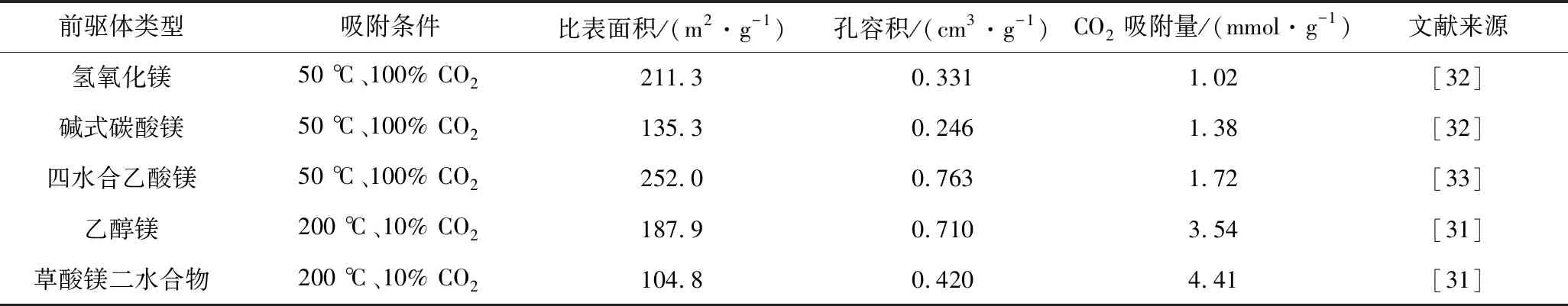
表1 多种前驱体制备MgO的CO2吸附性能
2.2 MgO负载多孔载体
常用的多孔载体材料通常具有发达孔隙和较大比表面积,可使MgO较好地分散,使MgO表面暴露更多的碱性吸附位点。Burri等[34]通过浸渍法将MgO负载在介孔碳上,结果表明,MgO负载量为10%时,在25 ℃、常压条件下,MgO/介孔碳复合材料的CO2吸附量达1.68 mmol/g。Chen等[35]通过固相分散法将MgO负载在多孔活性炭上,制备的多孔复合材料MgO/C具有大比表面积(1 450 m2/g)和优异的CO2吸附容量(3.1 mmol/g)。Guo等[36]研究了将MgO负载在蔗渣、咖啡渣、稻壳和锯末等生物质废料上的CO2吸附性能,结果表明,稻壳灰负载的样品具有最高的CO2吸附能力,MgO负载量为20%时,在10% CO2、200 ℃吸附条件下,CO2吸附量为4.56 mmol/g,且10次循环后的吸附量仅下降7.68%。该研究为制备高性能MgO吸附剂节约了成本,实现了废弃资源的价值化。
Li等[37]通过含镁金属-有机络合物的简单热解,制备了具有分级结构的MgO/C多孔纳米复合材料,在27 ℃和0.1 MPa CO2下的CO2吸附能力为0.67 mmo/g。图3为利用透射电子显微镜(TEM,图3(a)~(c))、高分辨率透射电子显微镜(HRTEM,图3(d))和能量色散X射线荧光光谱仪(EDX,图3(e))得到的MgO/C复合材料的微观结构图像。发现该复合材料具有由超薄纳米片结构单元构成的花瓣形分级结构,此结构单元上具有高度分散的超细MgO纳米粒子,使其具有较大比表面积、较高比孔容和较小的MgO纳米晶体,因此可提供更多的活性吸附位点,促进CO2气体扩散,增加CO2吸附量。

图3 MgO/C复合材料的微观结构[37]
Lugai等[38]制备了一种MgO/C纳米纤维-陶瓷多孔复合材料,先将碳纳米纤维涂覆在宏观陶瓷基载体上,再将MgO纳米粒子高度分散在多孔复合材料上。多孔陶瓷提供了一种高比表面积的负载基底,碳纳米纤维起到结构促进剂作用,稳定了MgO纳米颗粒的分散性,复合材料在0.1 MPa、94 ℃下具有较高CO2吸附量,为4.9 mmol/g。将MgO负载在金属氧化物上也是一种提高MgO吸附CO2性能的方法。Hanif等[39]将MgO分别负载在有序介孔SiO2和纳米纤维状SiO2上,在0.1 MPa、200 ℃下,由于纳米纤维SiO2具有非常高的热稳定性和结构完整性,复合材料在7次循环后保持稳定CO2吸附能力(达1.7 mmol/g)。
2.3 添加金属氧化物制备的MgO复合材料
Jin等[40]采用溶胶-凝胶燃烧法制备MgO-CeO2复合材料,研究20次循环的吸附性能,结果表明,添加5% CeO2时,MgO-CeO2复合材料具有较高的比表面积,达330 m2/g,CO2吸附容量达0.24 mmol/g;此外,该MgO-CeO2复合材料也显示了较高吸附速率,3 min内达到CO2最大吸附量的70%。Chen等[41]采用醋酸镁和醋酸亚铁合成了FeO-MgO复合材料,FeO添加量为3%时,复合材料为7 nm的纳米颗粒,具有较大的比表面积(176 m2/g),FeO-MgO复合材料的CO2吸附容量达0.875 mmol/g(吸附条件:200 ℃、100% CO2),这归因于FeO使复合材料具有较大的比表面积,增加了吸附材料表面碱性位点,使CO2吸附容量增加。
Kwak等[42]通过在Na2CO3-MgO上添加金属氧化物分散剂ZrO2,促进了MgO复合材料的CO2吸附性能,并提高了循环稳定性,K∶Mg∶Zr=0.3∶1∶0.6时,在330 ℃、纯CO2吸附条件下,MgO复合材料吸附CO2的转化率能达到理论CO2吸附值的73%;10次循环后CO2吸附量仅下降了4%。这主要是因为ZrO2使MgO复合材料的比表面积显著增加,Na2CO3在该表面上分布广泛且均匀,使大多数MgO与Na2CO3促进剂接触,活性吸附位点增加,进而提高了CO2吸附能力及循环稳定性。
Al2O3常作惰性支撑载体来提高MgO的CO2吸附性能,因其具有较高的塔曼温度,在多次循环吸附解吸CO2时可有效改善MgO烧结现象,另外,Al2O3材料具有发达的孔隙结构和较大比表面积,使混合Al2O3后MgO更易暴露出较多的CO2吸附位点[21]。
表2为Al2O3/MgO复合材料的最大CO2吸附量。可以发现,相比于纯MgO吸附剂,掺杂Al2O3后MgO复合材料表现出相对较高CO2吸附量。此外吸附条件(如温度、反应气氛等)对Al2O3/MgO复合材料也有重要影响,吸附温度升高及加入水蒸气均有利于提高Al2O3/MgO复合材料的CO2吸收量。Han等[43]利用共沉淀法制备的Al2O3-MgO复合吸附剂在Al/Mg摩尔比为1时,比表面积为177 m2/g,孔容约为0.45 cm3/g;在200 ℃、10% CO2和10% H2O条件下,该复合材料的CO2吸附量为3.02 mmol/g。Li等[44]采用湿法浸渍法将K2CO3负载在Al2O3/MgO复合材料上制备一系列新型KMgAl吸附剂,30次循环后该吸附剂仍具有稳定的CO2吸附性能,为2.4 mmol/g(吸附条件:60 ℃、10% CO2和12% H2O;再生条件:480 ℃)。Jeon等[45]研究了添加Al2O3和共晶碱金属盐制备的MgO复合材料(EM-MgO-Al2O3)的CO2吸附性能,结果表明,Mg/Al=5时,在300 ℃、纯CO2吸附条件下,MgO复合材料达到较高的CO2吸附容量,为2.95 mmol/g,这主要是因为Al2O3作为惰性支撑载体,使MgO的孔隙结构更发达,减少了MgCO3层团聚,从而增加了CO2吸附容量。

表2 掺杂Al2O3的MgO复合材料CO2吸附量
Li等[51]添加Cu制备了MgO复合材料,200 ℃时,MgO-Cu复合材料的CO2吸附量达0.78 mmol/g。这主要是因为在合成复合材料过程中CuO还原为Cu伴随着纳米粒子的体积收缩,使更多MgO活性位点暴露出与CO2接触,从而提高MgO的CO2吸附性能。Hiremath等[52]研究了添加TiO2制备的MgO复合物的CO2吸附性能,发现TiO2引入到MgO中可产生Mg-O-Ti离子对,形成不同价态Ti离子的钛酸镁相,使MgO复合材料除了具有较高的比表面积和孔容,还使材料表面产生更多的高强度碱性位点,在200 ℃、纯CO2时,TiO2-MgO复合材料(Mg/Ti摩尔比为3)的CO2吸附量为1 mmol/g。
3 熔盐改性的MgO
Harada等[53]研究了通过添加硝酸盐/亚硝酸盐改性的MgO吸附剂的CO2吸附性能,其CO2吸附容量高达15.7 mmol/g,因此通过熔盐改性可显著提高MgO吸附CO2的性能。
3.1 单一熔盐改性的MgO
Vu等[54]采用四步煅烧法合成KNO3改性MgO复合吸附剂,结果表明,该复合材料在325 ℃下表现出3.16 mmol/g的高CO2吸附能力,认为较高的CO2吸附能力是因为在该吸附温度下,碱金属盐KNO3处于熔融态覆盖在MgO吸附表面,在MgO吸附CO2的过程中为CO2的快速扩散提供了一个液体“通道”。Gao等[55]研究了碱金属硝酸/亚硝酸盐改性MgO的CO2吸附性能,发现NaNO3改性MgO在350 ℃时取得最高的CO2吸附性能,达17.0 mmol/g。Liu等[56]添加碱金属碳酸盐Cs2CO3制备了MgO复合材料,发现Cs2CO3添加量为15%时,MgO复合材料的CO2吸附量为1.9 mmol/g(吸附条件:300 ℃、常压、纯CO2),认为碱金属盐Cs2CO3的作用有:① Cs2CO3在一定温度下达到熔融态,覆盖在MgO表面产生了更多的镁离子与氧离子;② 部分Cs2CO3作为反应物参与到MgO吸附CO2的反应中,产生Mg-Cs碳酸盐中间相,该反应活化能相比于MgO吸附CO2活化能低,因此促进了MgO复合材料对CO2的吸附。
3.2 混合熔盐改性的MgO
Pozzo等[57]研究了多种硝酸盐(LiNO3、KNO3、NaNO3)改性MgO的CO2吸附性能及循环稳定性,揭示了混合硝酸盐增强MgO吸附性能的作用机制。图4为混合熔融硝酸盐在MgO吸附CO2中的作用机理。混合硝酸盐在一定温度下会形成熔融态覆盖在MgO表面,使大部分MgO溶解以自由离子对(Mg2+-O2-)形式存在,降低了MgO的晶格能,进而与CO2反应形成MgCO3,在脱附温度下MgCO3会脱附再生MgO,随着循环次数的增加覆盖在MgO表面的碱金属盐分离分散开,且MgO表面有烧结现象,从而导致CO2吸附量下降。共晶混合熔融盐的熔点温度比单一熔盐熔点温度低,有利于进一步提高MgO的CO2吸附性能。
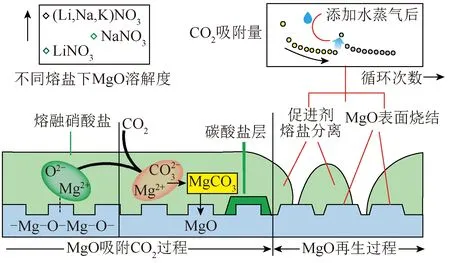
图4 混合硝酸盐改性下的MgO吸附CO2的机理[57]
Ding等[58]通过沉积混合碱金属硝酸盐和碳酸盐合成了一系列MgO基吸附剂,结果表明,按一定比例添加KNO3、LiNO3、Na2CO3、K2CO3时,MgO复合吸附剂的最大CO2吸附量达19.06 mmol/g,经30次循环后,CO2吸附量仅降到15.7 mmol/g,具有良好的长期吸附/解吸稳定性。Wang等[59]采用不同的前驱体和沉淀剂,通过不同方法制备出不同形貌的MgO样品,再采用湿法浸渍方法,用三元硝酸盐(LiNO3、KNO3、NaNO3)对MgO进行改性。结果表明,当前驱体为六水硝酸镁、碳酸钾为沉淀剂时,制备的MgO呈比表面积最大的棒状形貌,在30 min内CO2吸附性量达10.48 mmol/g,最大CO2吸附量为13.45 mmol/g。
尽管碱金属盐改性MgO的CO2吸附容量显著提高,但其吸附动力学缓慢且循环稳定性差,因此需制备高吸附速率及循环稳定性优异的MgO材料。柳春杰等[60]研究了添加CaCO3对碱金属盐改性MgO吸附CO2性能的影响,CaCO3添加量为3%时,MgO复合材料的初次CO2吸附量达14.3 mmol/g(吸附条件:40% CO2、350 ℃),20次循环后,CO2吸附量仍可达11.3 mmol/g。这是因为CaCO3在一定程度上限制了碱金属盐在高温下的流动,使碱金属盐有效分散在MgO表面,进而提高了MgO吸附剂的循环稳定性。Cui等[61]将碱土金属碳酸盐(CaCO3、BaCO3或SrCO3)加入混合碱金属盐(AMS)改性MgO复合材料,可以改善MgO吸附剂在多次吸附/解吸循环中的CO2捕集性能,明显提高CO2吸附速率。碱土金属碳酸盐添加量为10%时,在350 ℃、纯CO2下吸附,400 ℃、纯N2下解吸,20次循环后,CaCO3-AMS-MgO、BaCO3-AMS-MgO和SrCO3-AMS-MgO三种复合吸附材料的CO2吸附量分别为10.9、9.5、11.1 mmol/g,具有优异的循环稳定性(初次CO2吸附量分别为11.5、9.8、11.1 mmol/g)。认为部分CaCO3或BaCO3、MgO在熔融AMS中溶解,引入CO2后快速反应生成CaMg(CO3)2或BaMg(CO3)2,吸附速率增加。SrCO3不参与反应,作为惰性稳定剂可缓解MgO烧结,因此添加SrCO3的MgO复合材料比其他2种材料具有更高的循环稳定性。
反应条件对混合熔盐改性MgO的CO2吸附性能有一定影响。王磊等[62]研究了吸附温度和CO2分压力对混合碱金属硝酸盐和碳酸盐改性MgO的CO2吸附性能的影响。发现温度相同时,MgO的CO2吸附量随着CO2分压增加而提高;CO2分压相同时,随着吸附温度的增加,CO2吸附量先升高后降低。CO2分压为81.06 kPa、吸附温度为360 ℃时,改性MgO的CO2吸附量最大为11.8 mmol/g。Qiao等[63]研究了煅烧温度(300~600 ℃)对混合硝酸盐改性MgO吸附CO2性能的影响。结果表明,当碱金属硝酸盐添加量为10%、吸附温度为300 ℃,随煅烧温度升高,CO2吸附性能先提高后下降,煅烧温度为450 ℃时,吸附量最高为16.75 mmol/g。
表3为熔盐改性MgO的CO2吸附量。可以看出,在反应条件、熔盐种类等不同条件下,混合熔盐改性并不一定比单一熔盐改性下的MgO吸附CO2性能差,混合硝酸盐和碳酸盐比混合多种硝酸盐改性MgO的CO2吸附效果要好。尽管通过不同碱金属盐改性MgO的CO2吸附容量都有所提高,但不同的熔盐改性效果不同,且作用机理不同,目前对熔盐改性MgO的作用机理没有唯一确定的解释。相比优化MgO微观结构、提升其比表面积的方法,熔盐改性能显著提高MgO吸附CO2的性能。

表3 熔盐改性下MgO的CO2吸附性能
4 结语与展望
CO2捕集、利用与储存技术(CCUS)被认为是一种能有效减少碳排放的技术。MgO吸附剂以其较高的理论CO2吸附容量及优越的物理化学特性被认为是具有良好应用前景的CO2吸附材料。本文综述了近年来 MgO的成型造粒研究及提高MgO吸附CO2性能方法。虽然前期大量研究证明MgO在捕集CO2方面具备巨大优势,但仍存在一些问题,另外研究MgO最终目的是将其用于实际工业应用解决CO2排放问题。基于此未来MgO吸附剂捕集CO2的研究重点关注:
1)目前CO2吸附剂仍停留在实验室研发阶段,尚未大规模工业应用,未来研究需要在实际应用中所遇到的测试条件下评估MgO捕集CO2的性能,如有的电厂排放烟气中CO2浓度低和含有多种杂质气体,这些实际条件与目前实验室研究的温和测试条件不同;另外目前应用于MgO吸附CO2性能测试的循环周期数不多,在实际设备和条件下需对MgO进行长周期循环测试。未来研究仍需重点关注MgO成型造粒技术,其中要以制备具有优异机械性能及化学吸附性能的MgO吸附剂为目标。
2)对于MgO捕集CO2技术,应重点关注针对不同工业应用设计不同循环系统,并将这些系统与现有工业过程集成。此外除考虑设计最优系统外,还应考虑原料成本、制造工艺成本、优化工艺成本、能源消耗等经济环境因素。因此未来研究应该以简易高效、低成本、绿色环保为路线开发MgO吸附剂。

