Ag/TiO2纳米粒子的制备及其光催化降解苯酚的性能研究*
魏永春
(北京理工大学 珠海学院材料与环境学院,广东 珠海 519085)
0 引 言
过去20年间,人们对生存环境中水和空气中的化学污染物关注度逐渐增加。大量研究表明,采用半导体氧化物可光催化分解这类化学污染物,其中纳米结构的半导体氧化物光催化分解效率更高[1-2]。TiO2粒子是其中一种半导体氧化物粉体材料,由于其稳定的化学和物理性质而被广泛研究[3-5]。它无毒、不溶且成本低廉,在紫外光照射下具有高度的活性。因此,TiO2一直是光催化降解技术研究的热点材料[6-9],主要用于含有有机污染物的废水处理修复等[10-12]。
一些学者对TiO2粒子的光催化活性进行了研究,发现TiO2粒子的缺点是它的宽禁带中只有一小部分电磁光谱处于可用于光催化过程的紫外线区域[13-15]。然而有研究表明,可以通过负载或掺杂一些金属或者非金属等具有宽或窄带隙的半导体材料在TiO2粒子中,来提高TiO2粒子的光催化性能[16-18]。例如将Fe3+或Ce3+掺杂到TiO2粒子中[19],或者将P-N掺杂到TiO2中[20]等。此外,通过Ag等贵金属单质,对TiO2粒子进行表面修饰,也可增强TiO2粒子的光催化性能[21]。与Ag等金属粒子结合,可以导致TiO2粒子的带隙变窄或在表面产生一些等离子体,这两者都能增强TiO2粒子的反应活性[22]。众所众知,有机化合物(污染物)的光降解速率主要取决于以下几个因素:污染物类型、污染物初始浓度、催化剂类型、催化剂浓度、其它有机物的存在及温度等[23]。除了TiO2粒子,Girija K等[24]开发了纳米b-Ga2O3微球,用于有机污染物的光催化降解。
苯酚是化工工业废水中常见的主要污染物之一,由于其具有化学毒性,世界卫生组织国际癌症研究机构将其列为致癌物。因此,工业废水中苯酚的光催化降解受到了科研工作者的广泛关注[25-27]。Ag纳米粒子具有高的化学活性和强的还原性,可作为杀菌剂和抗菌剂使用,且通过Ag改性TiO2纳米粒子可以提高其光催化活性[28]。目前,对TiO2纳米粒子的光催化活性研究报道较多[29-30],而Ag改性TiO2纳米粒子对苯酚光催化降解的研究报道很少,且大多数研究都是基于污染溶液中分散的TiO2纳米粒子悬浮液。然而,从实际的应用角度来看,考虑到纳米TiO2粒子的过滤难题,在浆料光反应器中可能无法使用催化剂悬浮液。因此,本文采用溶胶-凝胶法,首先制备了TiO2和Ag/TiO2纳米粒子;然后制备了纳米TiO2和Ag/TiO2纳米粒子光催化剂,使用XRD、SEM和拉曼光谱等对试样进行了材料结构、表面形貌和光稳定性能分析;最后用涂覆法将光催化剂涂覆在陶瓷板载体上,制备了TiO2和Ag/TiO2纳米粒子光催化剂基板样品,并对含苯酚废水进行了光催化降解研究。
1 实 验
1.1 TiO2纳米粒子的制备
采用溶胶-凝胶法制备TiO2纳米粒子,过程如下:首先,在三口烧瓶中,将9.3 mL异丙醇滴加至3.2 mL的异丙醇钛中,充分摇匀;然后,将反应混合物在60 ℃下加热10 min,密闭搅拌;接着,倒入10.3 mL乙酸,匀速搅拌15 min;最后,加入24 mL甲醇,匀速搅拌2 h。
1.2 Ag/TiO2纳米粒子的制备
采用溶胶-凝胶法制备 Ag/TiO2纳米粒子,过程如下:首先,将室温下的1 mol异丙醇钛、2 mol冰醋酸和2 mol异丙醇按顺序加入三口烧瓶中,搅拌均匀,制备出溶液A;其次,将超纯光谱级的硝酸银(3%(质量分数))溶于2 mol去离子水、2 mol冰醋酸和2 mol异丙醇中,搅拌均匀,制备出溶液B;最后,通过剧烈搅拌将溶液A和B混合在一起。
1.3 光催化剂样品的制备
首先,在热洗涤液、丙酮、甲醇和去离子水中超声清洗玻璃板基板(20 mm×100 mm),随后把基板擦干;其次,采用浸涂技术,以2.5 mm/s的恒定速度,从TiO2纳米粒子的溶胶-凝胶中提取基片,涂覆的表面积为2 cm×3 cm;然后,在500 ℃的空气中退火1 h,退火过程如下:设定升温速率为5 ℃/min,在500 ℃处保持恒温并保温1 h,之后以5 ℃/min的降温速率降至室温;最后,将制备的光催化剂样品保存在一个干净、干燥且黑暗的容器中,用于苯酚溶液的光催化降解实验。
1.4 苯酚溶液的光催化降解
在室温下,采用光催化剂TiO2和Ag/ TiO2涂覆基板,对浓度为0.0002和0.001 mol/L的苯酚溶液进行光辐照。所使用的光催化反应器系统包括一个有效体积为250 mL的圆柱形玻璃反应器容器和作为UV-A光源的两个放置在反应器核心容器外的8-W紫外灯(UVP,美国,型号UVL-26p),主要发射波长为365 nm。在反应器底部放置一种通过缓慢流速的氧气扩散器的特殊玻璃碎屑,以均匀地将氧气分散到溶液中。降解反应后,每1 h测量紫外吸收光谱。
1.5 样品表征与性能测试
采用FI532W型激光拉曼光谱仪对TiO2和Ag/TiO2纳米粒子的拉曼光谱进行测试;采用日立SU8010型扫描电子显微镜(SEM)观察TiO2和Ag/TiO2纳米粒子的表面形貌;采用岛津6100型XRD衍射分析仪(Cu Kα辐射,40 kV,40 mA,扫描角度为20~80°,扫描速率为5 °/min)对合成的纳米TiO2和Ag/TiO2纳米粒子光催化剂进行物相结构分析;采用岛津SPD-20A/20AV UV-Vis检测器(线性范围为2.5AU,波长范围为190~700 nm)分析了样品的光稳定性。
2 结果与讨论
2.1 纯TiO2和Ag/TiO2纳米粒子的物性表征
图1为纯TiO2和Ag/TiO2纳米粒子的XRD图谱和拉曼光谱。其中,图1(a)为纯TiO2和Ag/TiO2纳米粒子的XRD图谱。从图1(a)可以看出,纯TiO2和Ag/TiO2纳米粒子均为纯净的金红石相,在27.1,37.8和55°处存在(110)、(101)和(211)峰;单质Ag粒子的衍射峰在38.1,44.5和64.4°处,分别为(111)、(200)和(220),部分Ag粒子的衍射峰峰与TiO2衍射峰并不能明显区分。图1(b)纯TiO2和Ag/TiO2纳米粒子的拉曼光谱。由图1(b)可知,纯TiO2和Ag/TiO2纳米粒子均在145,400,510和640 cm-1处出现了拉曼峰,Ag/TiO2纳米粒子的拉曼光谱强度比纯TiO2更高,峰更尖锐,且峰位发生了偏移。这可能是因为Ag单质的吸附,改变了TiO2纳米粒子之间的电场强度,提高了分子极化率,增强了拉曼光谱的散射效应,说明Ag单质粒子成功负载在TiO2纳米材料上。
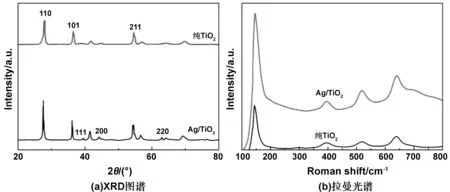
图1 纯TiO2和Ag/TiO2纳米粒子的XRD图谱和拉曼光谱Fig 1 XRD patterns and Raman spectra of pure TiO2 and Ag/TiO2 nanomaterials
2.2 SEM分析
图2为纯TiO2和Ag/TiO2纳米粒子的SEM图。由图2可知,纯TiO2和Ag/TiO2纳米粒子的尺寸均在10~20 nm之间,颗粒均匀,分散性较好,二者表面形貌并没有明显区别。说明Ag单质附着在TiO2纳米材料上并未改变TiO2纳米粒子的表面形貌,只是直观上来看,Ag/TiO2纳米粒子的尺寸稍微增大了一些。

图2 纯TiO2和Ag/TiO2纳米粒子的SEM图Fig 2 SEM images of pure TiO2 and Ag/TiO2 nanomaterials
2.3 光稳定性分析
图3为纯TiO2和Ag/TiO2溶胶-凝胶薄膜的紫外-可见光吸收光谱。从图3可以看出,Ag单质的负载明显增强了TiO2纳米粒子对可见光的吸收,并且Ag改性TiO2薄膜吸收光谱表现出明显的红移。特征峰的位置主要取决于纳米粒子的大小和形貌,Ag/TiO2薄膜特征峰的红移,可能是Ag/TiO2纳米粒子的制备过程中,粒子团聚或纳米粒子尺寸大于纯TiO2引起的。由图3可知,Ag/TiO2薄膜在450 nm左右出现吸收峰,这与Ag单质相关的表面等离子体共振峰有关,可能是单质Ag的存在引起了TiO2带隙之间的电子跃迁造成的。
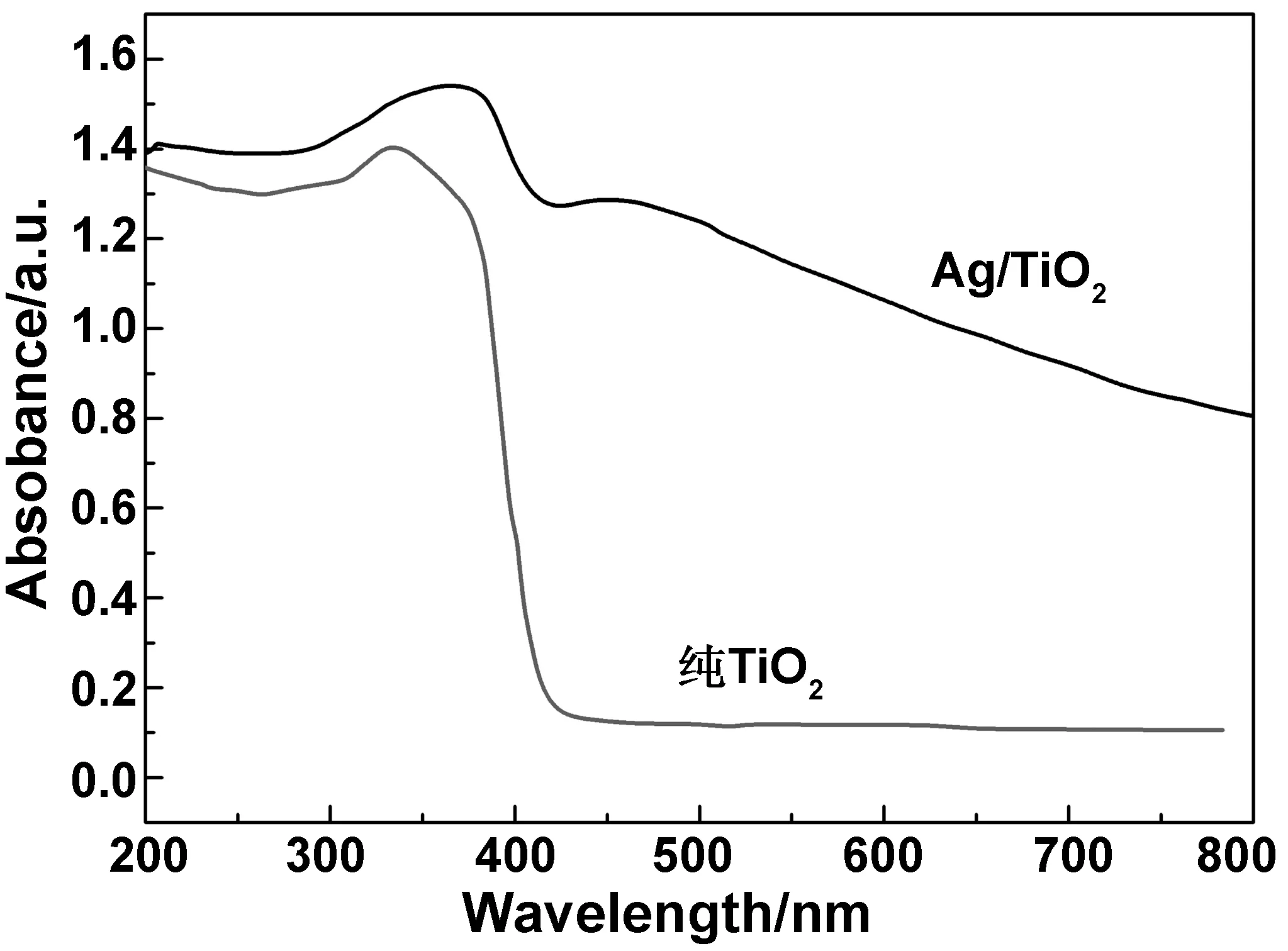
图3 纯TiO2和Ag/TiO2溶胶-凝胶薄膜的紫外-可见光吸收光谱Fig 3 UV-Vis absorption spectra of pure TiO2 and Ag/TiO2 sol-gel thin films
2.4 光催化降解性能分析
图4为在不同辐照时间下纯TiO2和Ag/TiO2纳米粒子对苯酚的光学吸收光谱。图5为纯TiO2和Ag/TiO2纳米粒子对苯酚的光催化降解性能,图5中不同降解时间下苯酚的浓度,通过图4中光学吸收光谱计算得到。图4(a)中,苯酚的初始浓度为0.0002 mol/L,光催化降解催化剂为纯TiO2纳米粒子薄膜;图4(b)中,苯酚的初始浓度为0.001 mol/L,光催化降解催化剂为Ag/TiO2纳米粒子薄膜。由图4(a)和5可知,当降解时间1 h时,纯TiO2纳米粒子薄膜的光催化降解实验中降解了约30%(质量分数)的苯酚;当降解时间>1 h时,苯酚的浓度达到0.00014 mol/L左右,光降解过程出现饱和趋势。由图4(b)和5可知,与纯TiO2纳米粒子薄膜不同,Ag/TiO2纳米粒子薄膜的降解反应速率显著增加,且在3 h内没有观察到饱和趋势的出现。在光降解1 h后,Ag/TiO2纳米粒子薄膜的吸光度从开始的1.435(0.099 g/L)明显下降到0.678(0.041 g/L),表明超过50%(质量分数)的苯酚已经降解;在光降解3h后,苯酚被降解了80%(质量分数),浓度从开始的0.099 g/L降至0.019 g/L,此时光降解过程仍未出现饱和趋势。
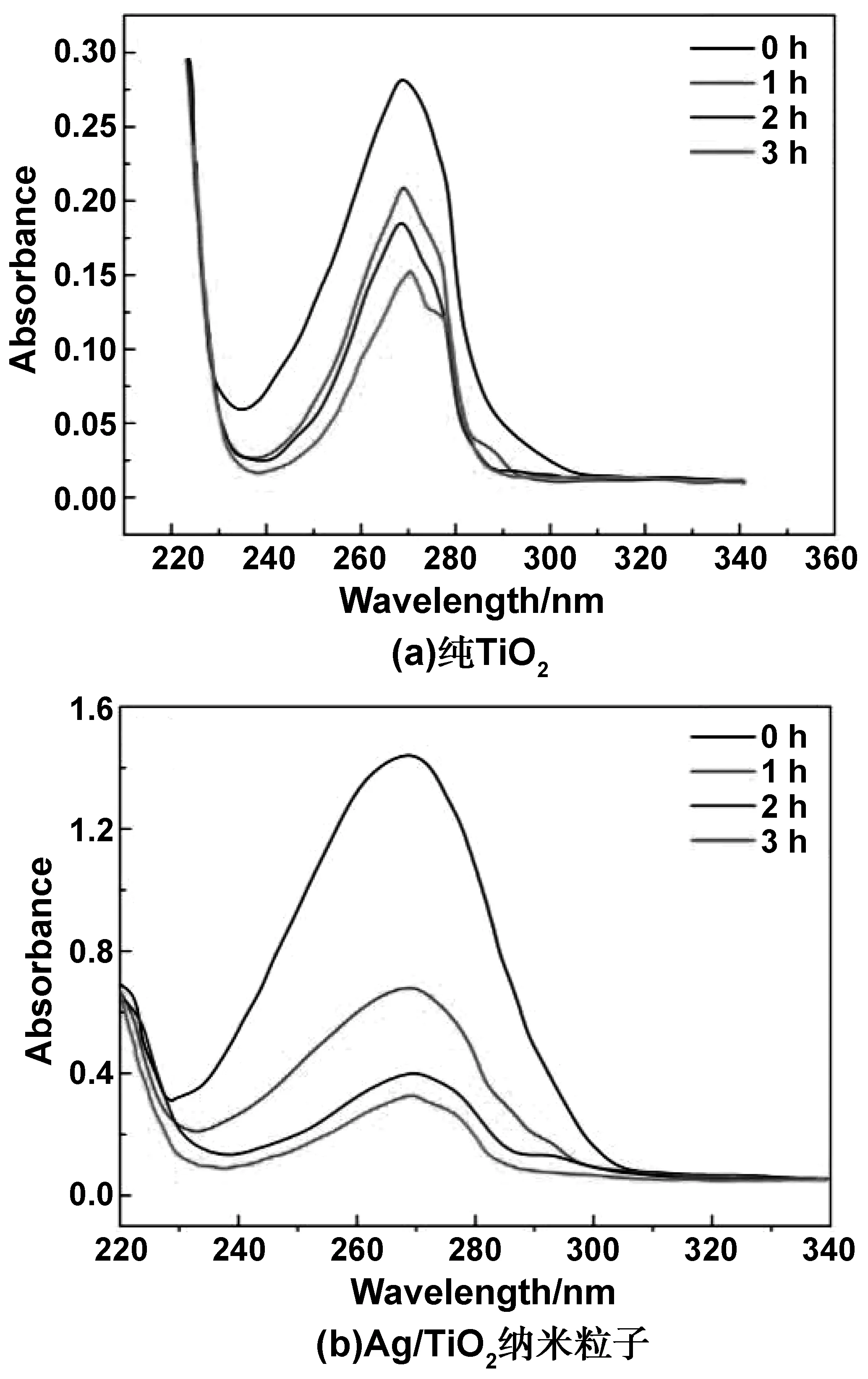
图4 在不同辐照时间下纯TiO2和Ag/TiO2纳米粒子对苯酚的光学吸收光谱Fig 4 Optical absorption spectra of phenol by pure TiO2 and Ag/TiO2 nanoparticles at different irradiation times
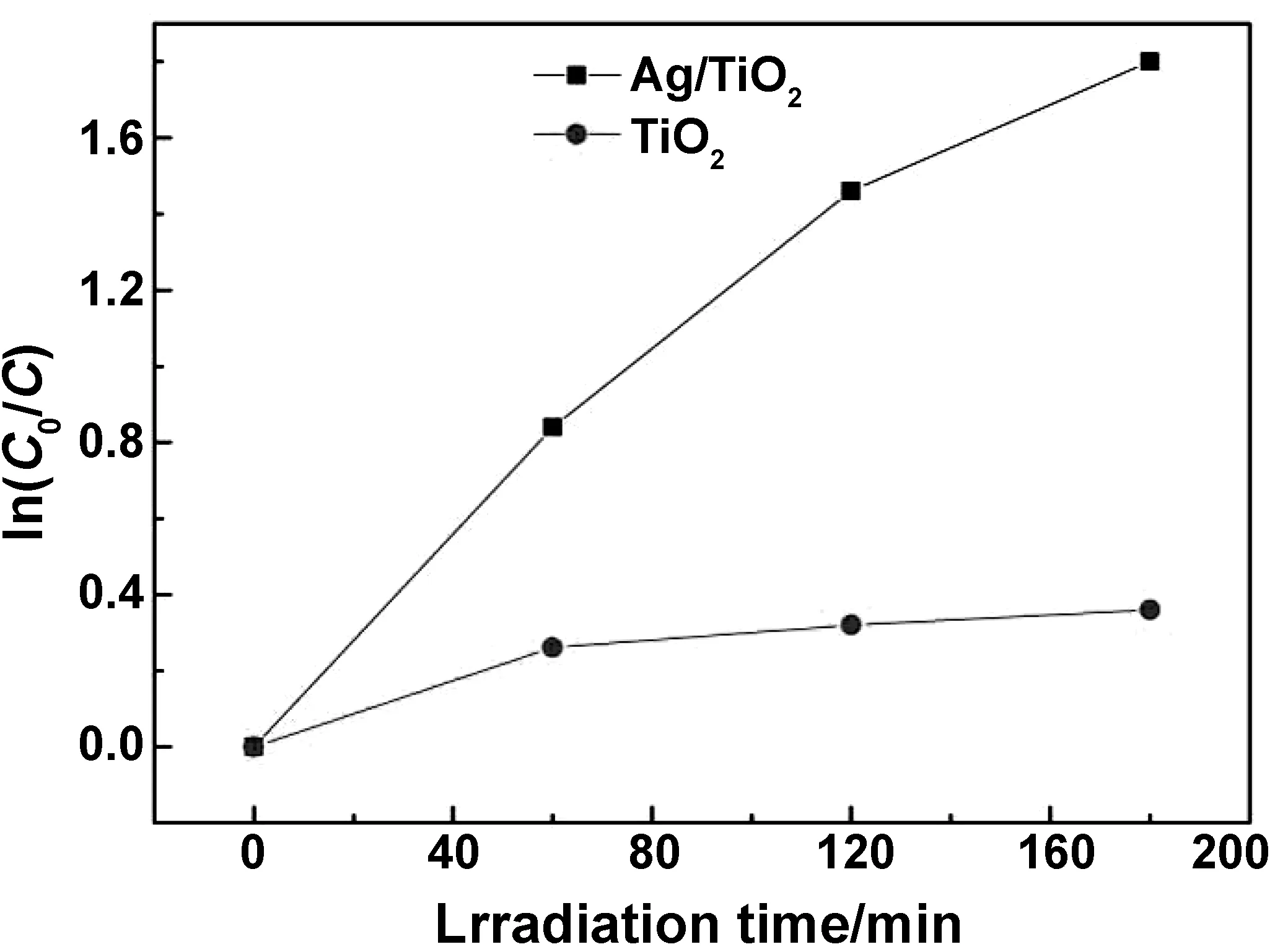
图5 纯TiO2和Ag/TiO2纳米粒子对苯酚的光催化降解性能Fig 5 Photocatalytic degradation performance of pure TiO2 and Ag/TiO2 nanoparticles on phenol
3 结 论
采用溶胶-凝胶法制备了纳米TiO2和Ag/TiO2纳米粒子光催化剂,再用涂覆法将光催化剂涂覆在陶瓷板载体上,制备了TiO2和Ag/TiO2纳米粒子光催化剂基板样品,对试样进行了材料结构、表面形貌、光稳定分析,并对含苯酚废水进行了光催化降解研究,结论如下:
(1)制备的TiO2和Ag/TiO2纳米粒子均为纯净的金红石相,Ag单质粒子成功负载在TiO2纳米材料上;
(2)纯TiO2和Ag/TiO2纳米粒子的尺寸均在10~20 nm之间,颗粒均匀,分散性较好,二者表面形貌并没有明显区别;
(3)Ag改性TiO2薄膜相比纯TiO2薄膜,紫外-可见光吸收光谱表现出明显的红移,且对可见光的吸收明显增强;
(4)Ag/TiO2纳米粒子薄膜对苯酚的光催化降解性能明显优于TiO2纳米粒子薄膜,在光催化降解1 h后,TiO2纳米粒子薄膜仅催化降解了溶液中30%(质量分数)的苯酚,且光催化降解出现了饱和趋势,而Ag/TiO2纳米粒子薄膜可催化降解溶液中50%(质量分数)的苯酚,且在光催化降解3 h后,仍未出现饱和趋势。

