植物乳杆菌LV02 抑菌特性及发酵培养基优化研究
杨 悦,滑婉月,陈志迪,张 瑶,易欣欣,高秀芝
(食品质量安全北京实验室/农产品有害微生物及农残安全检测与控制北京市重点实验室/微生态制剂关键技术开发北京市工程实验室/北京农学院食品科学与工程学院,北京 102206)
0 引 言
【研究意义】植物乳杆菌属于革兰氏阳性杆菌,兼性厌氧[1]。在人体的胃肠道内,植物乳杆菌属于优势菌群,可以通过代谢产生有机酸及细菌素等有益物质,有效抑制腐败菌[2]。乳酸菌素是具有类似抗生素的杀菌功效,但不会产生抗药性及毒性的多肽或蛋白质[3−4]。大部分乳酸菌素只有效抑制G+或G−,而均具有抗菌效果的则较少[5]。菌株产抗菌物质能力的大小与菌株特性有很大关系。有研究表明发酵培养基中的营养成分也对菌株所产抗菌物质的抑菌能力有所影响[6]。另外,乳酸菌素在食品中应用广泛,为使之发挥最大作用,了解抑菌活性的适宜pH 环境及温度也十分重要[7]。因此,开展植物乳杆菌发酵培养基的优化及其抑菌特性的研究,对替代抗生素类防腐剂的开发具有重要意义。【前人研究进展】近年来,为研究植物乳杆菌抑菌特性及生物量OD600的优化,学者们进行了大量探索[8]。王瑶等[9−10]研究的植物乳杆菌LPL-1 对单增李斯特氏菌具有抑制作用。优化培养基发现,葡萄糖对发酵产物影响最大,优化后细菌素可提高1.62 倍;在100 ℃,30 min 条件下LPL-1 的细菌素仍具有热稳定性;徐珑倩等[11]研究的植物乳杆菌P158 对藤黄微球菌、铜绿假单胞杆菌具有抑制作用。在对培养基的氮源及吐温80 成分进行优化后,细菌素明显提高了218%。Zhao 等[12]研究植物乳杆菌素JLA-9 的生化特性时,发现该乳杆菌素具有耐高温的特性。而许女等[13]对植物乳杆菌素KF1 进行pH 2.0~12.0 处理时发现,只有pH 为2.0~6.0 时该乳杆菌素具有较好的抑菌性,中性及碱性环境便失去了抑菌活性。Yoo 等[14]研究优化植物乳杆菌JNU 2116 的发酵培养基,发现酵母提取物对其生长影响最大。【本研究切入点】目前的研究成果中,对于可同时抑制G+及G−的植物乳杆菌报道较少。植物乳杆菌LV02 可抑制部分革兰氏阳性及阴性菌[15]。对大肠杆菌YS 有一定的抑菌效果,大肠杆菌YS 分离于生菜,为植物乳杆菌LV02后续开发抗菌保鲜类产品提供技术参考。采用响应面法优化发酵培养基,可以克服正交法筛选范围宽泛的缺点,经爬坡与最陡爬坡试验对水平范围进行缩减,使最终结果更具说服力[16]。【拟解决的关键问题】植物乳杆菌LV02 分离于发酵蔬菜,前期发现其可抑制部分革兰氏阴性及阳性菌[15]。本研究以植物乳杆菌LV02 为研究对象,对其抑菌特性进行探讨。并基于单因素、爬坡试验及最陡爬坡试验,以抑菌圈直径及生物量OD600为响应值,利用CCD 试验进行数据分析,通过优化植物乳杆菌LV02 的发酵培养基,提高对大肠杆菌YS 的抑菌性及生物量OD600,以期为植物乳杆菌LV02 的进一步开发利用奠定基础。
1 材料与方法
1.1 菌种与主要试剂
植物乳杆菌LV02(Lactobacillus plantarum,NCBI登录号:MH885507),分离源于发酵蔬菜;大肠杆菌YS(Escherichia coli,NCBI 登录号:MN153456.1),分离源于生菜。以上菌种均保存于北京农学院食品学院菌种保藏室。营养琼脂(nutrient agar,NA)、营养肉汤(nutrient broth,NB)、酵母浸粉,酪蛋白胨均购于北京陆桥技术股份有限公司;葡萄糖及蔗糖均购于国药集团化学试剂有限公司。MRS 肉汤(MRS):葡萄糖20 g·L−1、蛋白胨10 g·L−1、牛肉粉5 g·L−1、酵母菌4 g·L−1、乙酸钠5 g·L−1、磷酸氢二钾2 g·L−1、硫酸镁0.2 g·L−1、柠檬酸三铵2 g·L−1、硫酸锰0.05 g·L−1、吐温80 1 mL·L−1、蒸 馏水1 L。pH6.2 ± 0.1,121 ℃高压灭菌15 min 备用。
1.2 主要仪器设备
WS-01 型恒温恒湿箱,湖北黄石恒丰医疗器械有限公司;BSA2202S 型分析天平,赛多利斯科学仪器有限公司;DL-CJ-1N 型超级洁净工作台,北京东联哈尔仪器制造有限公司;MLS-3750 型高压蒸汽灭菌锅,Sanyo ELectric Co.Ltd;T6 型新世纪紫外可见分光光度计,北京普析通用仪器有限责任公司。
1.3 试验方法
1.3.1 植物乳杆菌LV02 发酵上清滤液的制备 从植物乳杆菌LV02 的甘油保藏管中以2%的接种量置于10 mL 的MRS 液体培养基中,37 ℃静置培养12 h。蘸取一环菌液进行两代平板划线,每代培养24 h,得到二代活化板。从中挑取2 环单菌落转接到50 mL的MRS 液体培养基中37 ℃静置培养12 h,再用同样的温度以5%的接种量转培静置24 h,得到LV02发酵培养液。4 ℃,15 min,8 000 r·min−1离心,再用0.22 μm 的无菌滤膜过滤,得到LV02 发酵上清过滤液。
1.3.2 指示菌的培养 从经二代活化的大肠杆菌YS 平板上挑取一环单菌落,置于已高压灭菌的LB肉汤中进行12 h、150 r·min−1、37 ℃的恒温培养。
1.3.3 抑菌试验 向60 ℃左右的150 mL 营养琼脂内注入107CFU·mL−1的大肠杆菌菌液150 μL,在超净台上左右混匀,倒入一次性平板内。琼脂凝固后,放上牛津杯,向每个牛津杯内注入100 μL 的LV02 发酵上清过滤液,三组平行,37 ℃培养12 h观察抑菌圈直径。
1.3.4 植物乳杆菌LV02 抑菌特性
1.3.4.1 硫酸铵沉淀法初步分离LV02 的细菌素 取LV02 发酵上清过滤液,分别以40%、50%、60%、70%、80%及90%的饱和度硫酸铵进行12 h 沉淀。将硫酸铵沉淀液进行15 min、8 000 r·min−1的4 ℃低温离心,将得到的离心沉淀,用去离子水(体积为发酵上清液的1/10)进行混匀复溶。采用0.22 μm 的无菌滤膜过滤复溶液,采用牛津杯法,筛选硫酸沉淀LV02 的细菌素最佳饱和度。
1.3.4.2 植物乳杆菌LV02 热稳定性试验 将pH 6.3 的LV02 发酵上清滤液,分别置于60 、80、100 ℃的恒温水浴锅中处理60、90 、120 min。经0.22 μm 的无菌滤膜过滤后进行牛津杯试验。
1.3.4.3 pH 对植物乳杆菌 LV02 抑菌活性的影响用1 mol·L−1的NaOH 溶液及盐酸将LV02 发酵上清滤液的pH 分别调至3.0、3.5、4.0、4.5、5.0、5.5、6.0、6.5、7.0、7.5。以未经处理的LV02 发酵上清滤液作为对照,采用牛津杯法观察对大肠杆菌YS 的抑制效果。
1.3.4.4 植物乳杆菌LV02 对不同指示菌的抑菌效果取5%的LV02 种子液,转置MRS 肉汤培养24 h,得到LV02 发酵培养液。以4 ℃,15 min,8 000 r·min−1离心,再用0.22 μm 的无菌滤膜过滤,得到LV02 发酵上清过滤液。向60 ℃左右的150 mL 营养琼脂内分别注入107CFU·mL−1的大肠杆菌YS、单增李斯特菌及猪霍乱沙门氏菌150 μL。在超净台上左右混匀,倒入一次性平板内。琼脂凝固后,放上牛津杯,在每个牛津杯内放入100 μL 的LV02 发酵上清过滤液,每次重复3 次,37 ℃培养12 h 观察抑菌圈直径。
1.3.5 单因素试验
1.3.5.1 优化氮源、碳源 以MRS 肉汤配方为 基础,将氮源(19 g·L−1)等量替换为大豆蛋白胨、酪蛋白胨、酵母浸粉、蛋白胨及酵母浸粉+蛋白胨(1∶1)。确定氮源后,再将碳源(20 g·L−1)等量替换为葡萄糖、蔗糖、果糖、D-果糖、乳糖、葡萄糖+乳糖(1∶1)及葡萄糖+蔗糖(1∶1),其他成分及含量和MRS 肉汤一致,用50 mL 去离子水搅拌加热溶解,121 ℃、15 min 高压灭菌。以体积分数为5%的量进行发酵接种,37 ℃培养24 h,以牛津杯法测定抑菌圈直径,选出最佳碳源。
1.3.5.2 优化矿物质组合 固定氮源、碳源,对矿物质进行优化。组合因子有磷酸氢二钾(0、2、4、6、8 g·L−1)、硫酸镁(0、0.1、0.2、0.3、0.4 g·L−1)、乙酸钠(0、2.5、5.0、7.5、10 g·L−1)及硫酸锰(0、0.1、0.2、0.3、0.4 g·L−1)。首先选取其中一种考察因子,按照所设计的不同添加量来逐一筛选。其他因子以此类推。最终得到一组无机盐组合,其他成分及含量和MRS 肉汤一致,用50 mL 去离子水搅拌加热溶解,121 ℃高压灭菌15 min。以体积分数为5%的量进行发酵接种,37 ℃培养24 h,以牛津杯法[17]测定抑菌圈直径,选出最佳矿物质组合。
1.3.5.3 优化吐温80、生长因子组合 以0、1、2、3、4 mL·L−1对吐温80 进行单因素筛选。确定吐温80 添加量后,分别加入胡萝卜汁、黄瓜汁、西红柿汁、胡萝卜汁+西红柿汁(1∶1)、黄瓜汁+西红柿汁(1∶1),各50 mL·L−1。其他成分及含量和MRS 肉汤一致。用50 mL 去离子水搅拌加热溶解,采用121 ℃、15 min 高压灭菌。以体积分数为5%的量发酵接种,37 ℃培养24 h 后取出,以牛津杯法测定抑菌圈直径,选出最佳生长因子。
1.3.6 爬坡试验 在单因素试验结果的基础上,采用PB 试验初步设计出每个因子的高低水平(高低水平的差值要适合,否则会出现效应不明显的结果)。对葡萄糖、酵母浸粉、硫酸锰、硫酸镁、乙酸钠、吐温80 及胡萝卜汁,这7 种因子进行PB 试验(n=12)。以抑菌圈直径为响应值,分析影响LV02抑菌效果的显著影响因子,Plackett-Burman 设计因子水平见表1。
1.3.7 最陡爬坡试验根据PB 试验结果中的排列图,可确定因子的步长及方向[18],正效应则添加量以最低水平往上增加步长,负效应则将添加量以最高水平往下减步长[16]。取对LV02 抑菌影响贡献率最高的前三种因子,其余因子添加量则以单因素结果为准,进行最陡爬坡试验得到CCD 试验中心点。
1.3.8 CCD 试验 将最陡爬坡试验结果作为CCD 试验的中心点,其他非关键因子固定,以抑菌圈直径及OD600作为响应值,进行3 因子5 水平的CCD 优化试验[19]。CCD 优化试验对考察因子设定的水平范围大,可使预期值和实际结果更相符。试验因子与水平设计见表2。
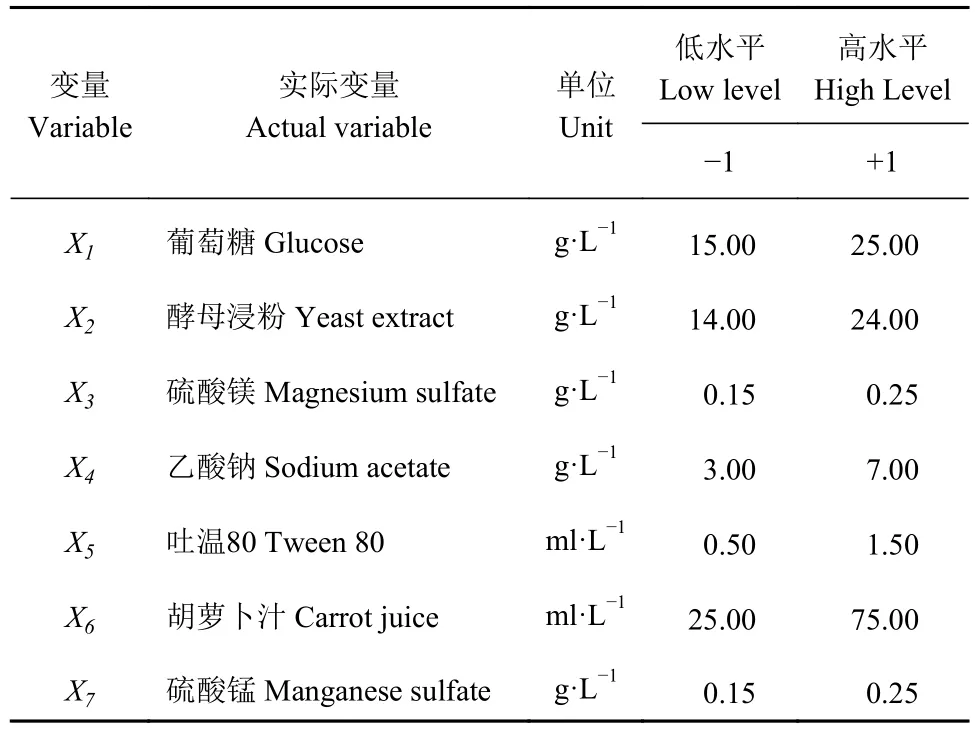
表 1 Plackett-Burman 设计因子水平及编码Table 1 Factors, levels, and codes of Plackett-Burman experimental design
2 结果与分析
2.1 不同饱和度硫酸铵溶液的细菌素测定
不同饱和度硫酸铵溶液的细菌素测定结果见图1,所有考察的饱和浓度经沉淀后,其复溶液均有抑菌效果。其中在硫酸铵溶液饱和度为80%时,抑菌圈直径可达到最大,为15.50 ± 0.50 mm,证明80%饱和度的硫酸铵沉淀植物乳杆菌LV02 的细菌素能力明显优于其他饱和度(P<0.05)。
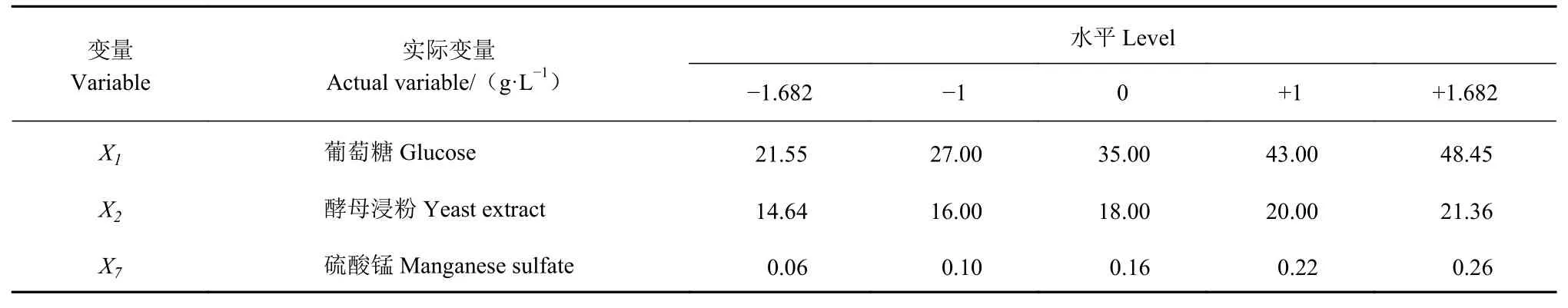
表 2 CCD 试验各因子水平数Table 2 Levels for each factor on CCD experiment
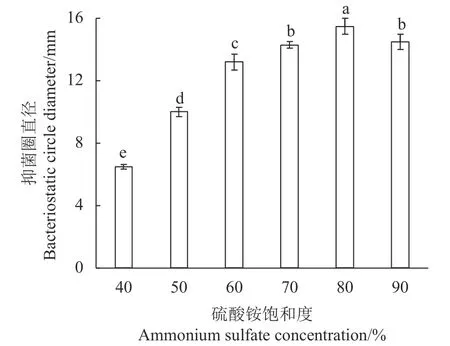
图 1 不同饱和度的硫酸铵溶液沉淀细菌素的效果Fig. 1 Effect of saturation degree of ammonium sulfate solution on bacteriocin precipitation

图 2 热处理对植物乳杆菌LV02 抑菌效果的影响Fig. 2 Effect of heat treatment on bacteriostatic property of LV02 bacteriocin
2.2 植物乳杆菌LV02 热稳定性试验
植物乳杆菌LV02 热稳定性试验结果见图2,pH 6.3 的LV02 发酵上清滤液经不同温度、时间处理后抗菌活性逐渐降低。在处理60 min 内,LV02 对3 种温度不敏感,结果之间差异不显著(P>0.05)。而在这之后,开始呈现明显的下降趋势。直到处理90 min,3 条温度线出现平缓态,LV02 的抗菌活性处于稳定状态。60 ℃处理60 min,抑菌结果比初始值高,这可能是有该温度处理下使抑菌物质得到分解产生了活性肽[20]。100 ℃处理120 min,抑菌圈直径为14.30 ± 0.14 mm,保留了约80%的抑菌活性,说明植物乳杆菌LV02 对高温不敏感,可以在高温环境内保持活性。
2.3 pH 对LV02 抗菌活性的影响
pH 对LV02 抗菌活性的影响结果见图3,植物乳杆菌LV02 在pH 为 3.0~7.5 均具有抗菌活性。pH 为3.0 时抗菌活性最强,抗菌圈直径为21.58 ± 0.34 mm。pH 3.0~6.0 时,LV02 的抑菌活性是缓慢下降的趋势,直到pH 在6.0 以上时,抗菌活性下降的幅度开始增大,且pH 6.0、6.5、7.0、7.5 之间差异显著(P<0.05),pH 为7.0 时保留了近80%的抗菌活性,说明LV02 在酸性及中性环境下pH 稳定性较好。这与姜晶等[21]在研究植物乳杆菌DMS20174 对pH 的耐受情况相似,并指出这可能与大肠杆菌在该环境下竞争性不强有关。
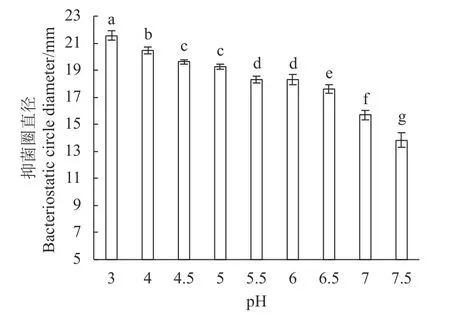
图 3 不同pH 对植物乳杆菌LV02 抑菌性的影响Fig. 3 Antibacterial effect of LV02 bacteriocin under pH in large intestines
2.4 LV02 对3 种指示菌的抑菌情况
植物乳杆菌LV02 对不同指示菌的抑菌效果如表3所示。LV02 对大肠杆菌YS、单增李斯特氏菌以及猪霍乱沙门氏菌这3 种指示菌均具有抑制作用。其中,对猪霍乱沙门氏菌的抑菌效果最佳,抑菌圈直径可达到24.74 ± 0.51 mm。其次是单增李斯特氏菌、大肠杆菌。虽然从3 种指示菌比较来看,大肠杆菌对LV02 所产抑菌物质的敏感度不高,但是从先前研究人员在植物乳杆菌对大肠杆菌抑菌作用方面的研究结果来看[22],抑菌圈直径仅为5~10 mm,与LV02 抑制大肠杆菌的作用结果差异显著。并且与对革兰氏阴性菌没有杀菌效果的同科菌株(Nisin)相比,LV02 具有明显的优势[23]。因此,LV02 植物乳杆菌可对部分革兰氏阴性及阳性菌产生抑制作用,未来可将其应用于抑菌产品类开发。

表 3 LV02 对3 种指示菌的抑菌结果Table 3 Antibacterial results of LV02 against three kinds of ndicator bacteria
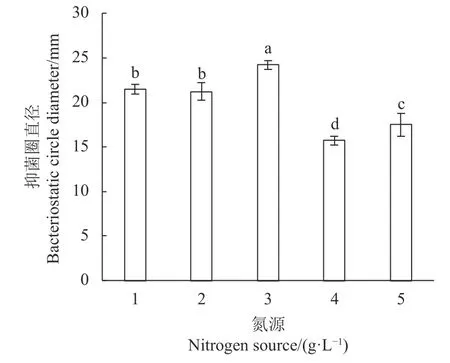
图 4 不同氮源对LV02 的细菌素抗菌性的影响Fig. 4 Effect of culture nitrogen sources on antibacterial activity of LV02 bacteriocin
2.5 单因素优化结果
2.5.1 氮源、碳源的优化 氮源的优化结果如图4 所示,不同氮源对植物乳杆菌LV02 的细菌素抗菌性均具有显著性影响(P<0.05),可被LV02 所利用。在以酵母浸粉为唯一氮源时,细菌素抗菌性最好,抑菌圈直径可达24.25 ± 0.29 mm。添加蛋白胨时,抗菌性最低,抑菌圈直径仅为15.75 ± 0.50 mm。将蛋白胨与酵母浸粉1∶1 添加,抗菌效果也次于单一氮源酵母浸粉(P<0.05),与大豆蛋白胨之间差异不显著(P<0.05),本试验与章检明[24]在优化Lactobacillus plantarumLac-B23 发酵培养基氮源时的结论一致,其以蛋白胨作为氮源时细菌素效价仅为40 AU·mL−1,而氮源为酵母浸粉时效价则为560 AU·mL−1。故本试验以酵母浸粉作为LV02 优化培养基的最佳氮源。不同碳源对LV02 的细菌素抗菌性的作用效果如图5可知,葡萄糖的影响作用最大,抑菌圈直径可达24.28 ± 0.32 mm,与其他碳源相比具有显著性影响(P<0.05)。其次为果糖、葡萄糖+蔗糖(1∶1)。D-果糖、乳糖、蔗糖及葡萄糖+蔗糖(1∶1)之间差异不显著(P>0.05)。不同碳源的结构是不同的。蔗糖及乳糖属于双糖,果糖及D-果糖虽为单糖,但也需要分解才能被利用,因此利用率偏低。生物对糖类物质的摄入,主要以葡萄糖的形式进行吸收[25]。故本试验以葡萄糖为LV02 优化培养基的最佳碳源。
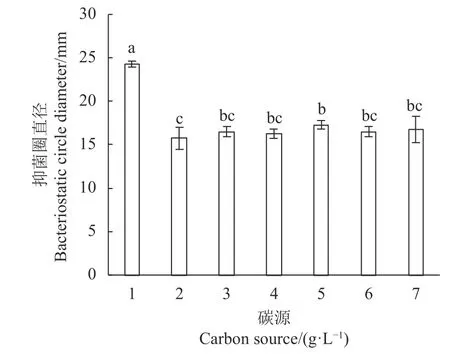
图 5 不同碳源对LV02 的细菌素抗菌性的影响Fig. 5 Effect of culture carbon sources on antibacterial activity of LV02 bacteriocin
2.5.2 矿物质组合的优化 物质优化的结果见图6~9。图6 中,K2HPO4质量浓度为2 g·L−1时,对LV02的细菌素抗菌影响最大,与未添加效果相比差异显著(P<0.05)。而低于或高于此质量浓度时对抗菌效果均有影响,故以2 g·L−1作为K2HPO4的添加量。乙酸钠的质量浓度为5 g·L−1时(图7),对LV02 抑菌效果最好,与未添加相比两者具有显著差异(P<0.05)。质量浓度为5 、10 g·L−1时,两者差异不显著(P>0.05),但考虑成本,故选5 g·L−1作为乙酸钠的添加量。图8 中,随着硫酸镁质量浓度的增加,抑菌圈直径呈现先增大后降低的趋势,质量浓度为0.2 g·L−1时,对大肠杆菌YS 的抗菌效果最佳。高玉荣等[26]研究结果表明向植物乳杆菌G1-28 发酵培养基中添加0.3%的硫酸镁时活菌数可达到最高,低于或高于此剂量都会使活菌数的优化不利。故以0.2 g·L−1进行硫酸镁的添加。由图9 可知,硫酸锰对LV02 的抑菌效果影响较大,与其他各处理组差异明显(P<0.05),随着质量浓度的增加抑菌圈直径呈现先增大后降低的趋势。0.2 g·L−1时抗菌效果最佳,抑菌圈直径为23.50 ± 0.50 mm,与其他各处理量呈显著性差异(P<0.05)。王帅[27]研究影响植物乳杆菌L69 发酵液OD 值的影响因子时,发现硫酸锰相较硫酸镁及吐温80,对L69 的OD 值具有显著影响。因此本实验对硫酸锰以0.2 g·L−1进行添加。
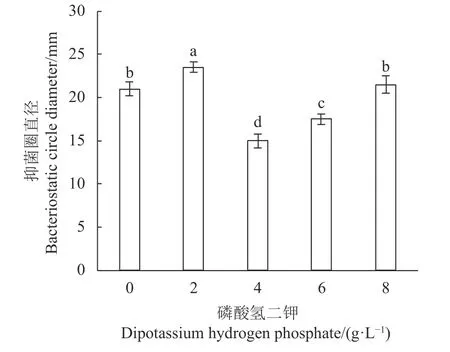
图 6 磷酸氢二钾对LV02 的细菌素抗菌效果的影响Fig. 6 Effect of dipotassium hydrogen phosphate in medium on antibacterial activity of LV02 bacteriocin
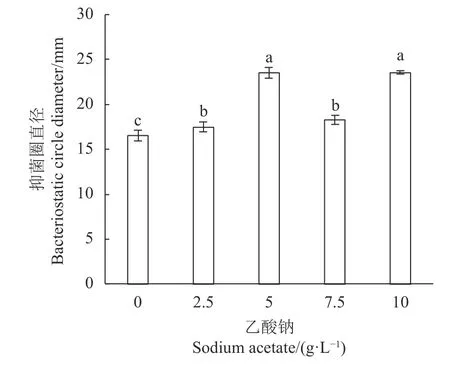
图 7 乙酸钠对LV02 的细菌素抑菌效果的影响Fig. 7 Effect of sodium acetate in medium on antibacterial activity of LV02 bacteriocin
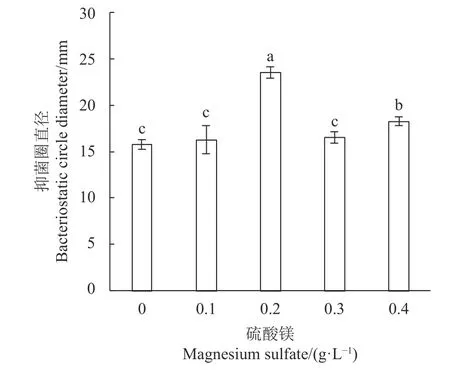
图 8 硫酸镁对LV02 的细菌素抗菌效果的影响Fig. 8 Effect of magnesium sulfate in medium on antibacterial activity of LV02 bacteriocin
2.5.3 吐温 80、生长因子的优化 吐温 80 的优化结果见图10,不同含量的吐温80 对LV02 的细菌素抗菌作用影响不同。在1 mL·L−1时,LV02 的细菌素抗菌效果最佳。而在此含量以上添加量越大会出现抗菌效果下降的趋势。因此以1 ml·L−1作为吐温80 的添加量。生长因子的优化结果如图11,5 种生长因子均可提高LV02 的细菌素抗菌能力,其中胡萝卜汁所作用的抗菌效果最佳(P<0.05),其次为西红柿汁、黄瓜汁。这可能是3 种蔬菜均含有大量B 族维生素及多种矿物质[27−28],而胡萝卜还含有胡萝卜素及多种维生素,可刺激LV02 的菌体产出更多的细菌素,增强抑菌效果。而这些是黄瓜和西红柿所不可替代的,故以50 mL·L−1的胡萝卜汁作为单一生长因子进行添加。
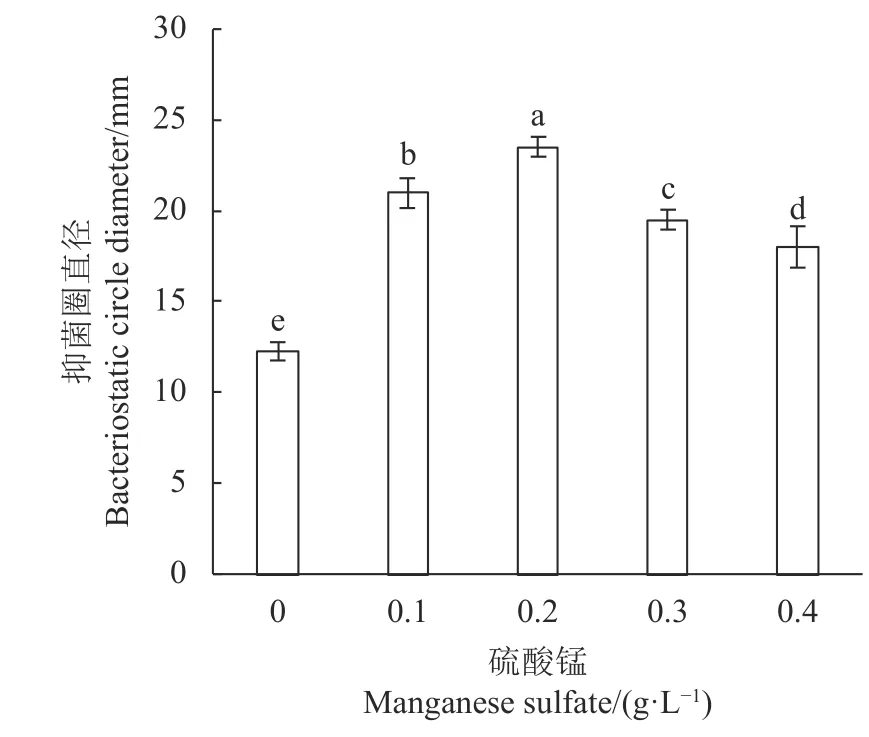
图 9 硫酸锰对LV02 的细菌素抗菌效果的影响Fig. 9 Effect of manganese sulfate in medium on antibacterial activity of LV02 bacteriocin
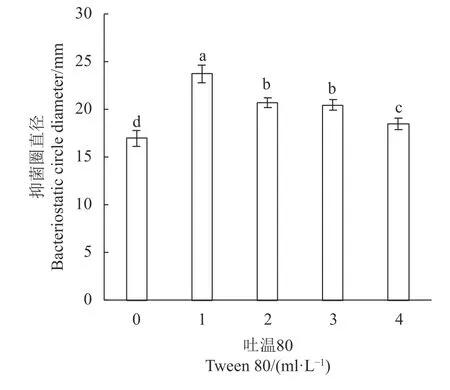
图 10 吐温对LV02 的细菌素抗菌效果的影响Fig. 10 Effect of Tween-80 in medium on antibacterial activity of LV02 bacteriocin
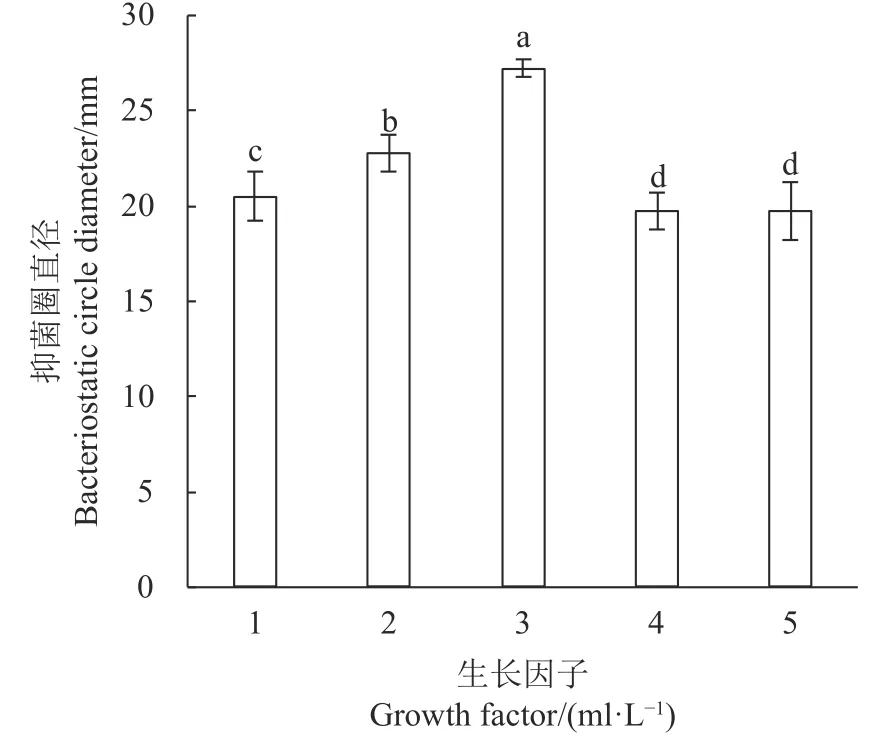
图 11 不同生长因子对LV02 细菌素抗菌效果的影响Fig. 11 Effect of growth factors in medium on antibacterial activity of LV02 bacteriocin
2.6 爬坡试验结果
Plackett-Burman 试验结果及各因子贡献率及效应值见表4、5。表5 中,葡萄糖(X1)、硫酸锰(X7)及酵母浸粉(X2)这3 种因子对LV02 抑菌能力的贡献率最高其中葡萄糖可达到41.39%。其次为硫酸锰、酵母浸粉,分别为19.61%和15.41%。根据各组分的效应值结果可知,葡萄糖为正效应,设计最陡爬坡试验的取值范围应以低水平往上增。酵母浸粉与硫酸锰为负效应,取值应以高水平往下减。3 种组分相对于其他4 种具有显著性差异(P<0.05)。因此,以葡萄糖、酵母浸粉及硫酸锰进行最陡爬坡试验,其余因素按照单因素结果比例进行添加。
2.7 最陡爬坡试验结果
最陡爬坡试验的设计方案及结果见表6。5 组试验中,4 号试验组的抑菌圈直径最大。故将4 号试验组,即葡萄糖(35.00g·L−1)、硫酸锰(0.16 g·L−1)及酵母浸粉(18.00 g·L−1),作为CCD 试验中心点。
2.7.1 CCD 试验结果 采用Design Expert 12 做方程拟合与显著性分析,CCD 试验设计及结果见表7。得到了植物乳杆菌LV02 抑制杆菌LV02 抑制大肠杆菌YS 的抑菌圈直径及OD600相对于葡萄糖(X1)、硫酸锰(X7)及酵母杆菌LV02 抑制大肠杆菌YS 的抑菌圈直径及OD600相对于葡萄糖(X1)、硫酸锰(X7)及酵母浸粉(X2)的回归方程:

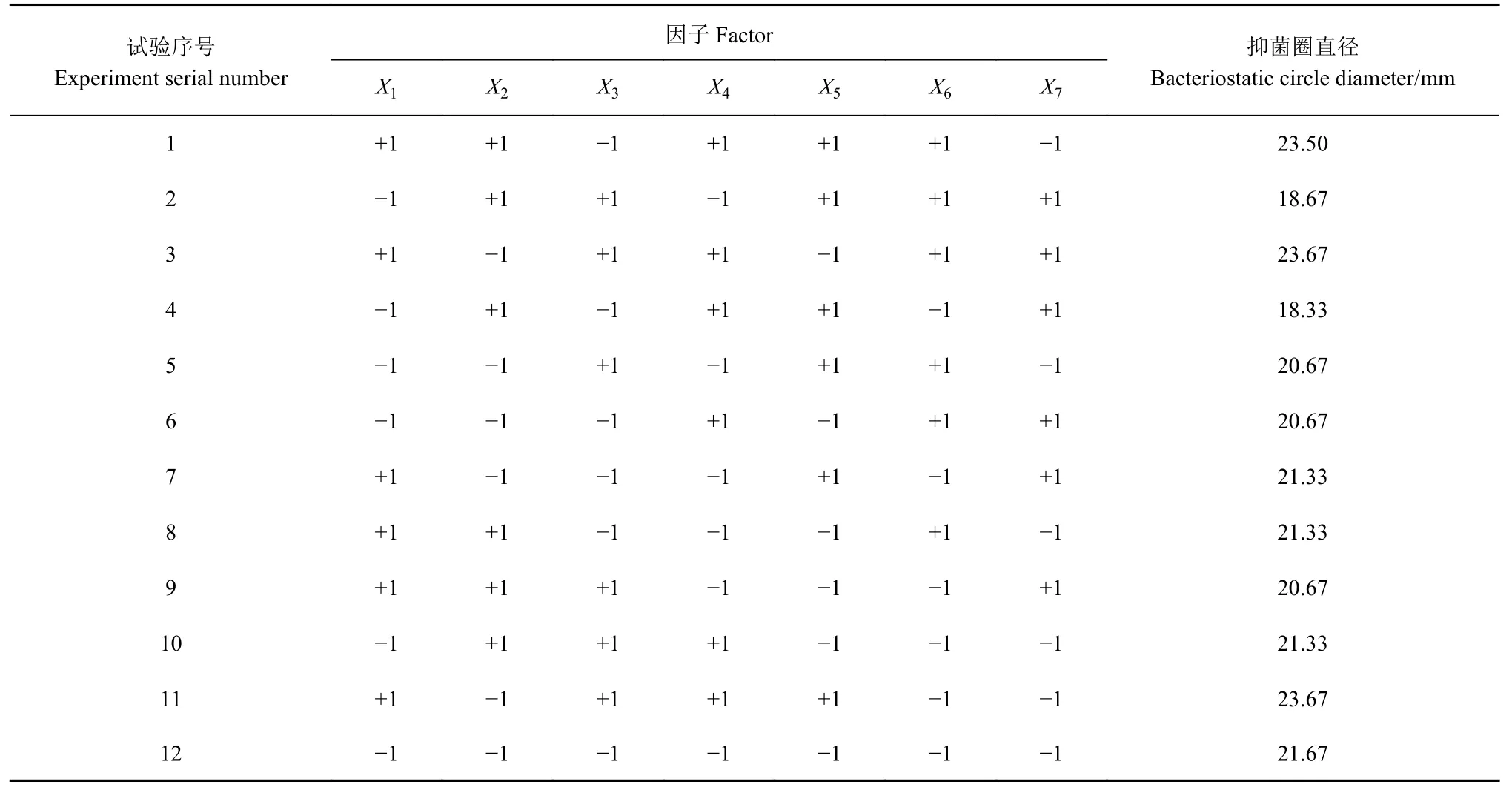
表 4 Plackett-Burman 试验结果Table 4 Results of Plackett-Burman experiment
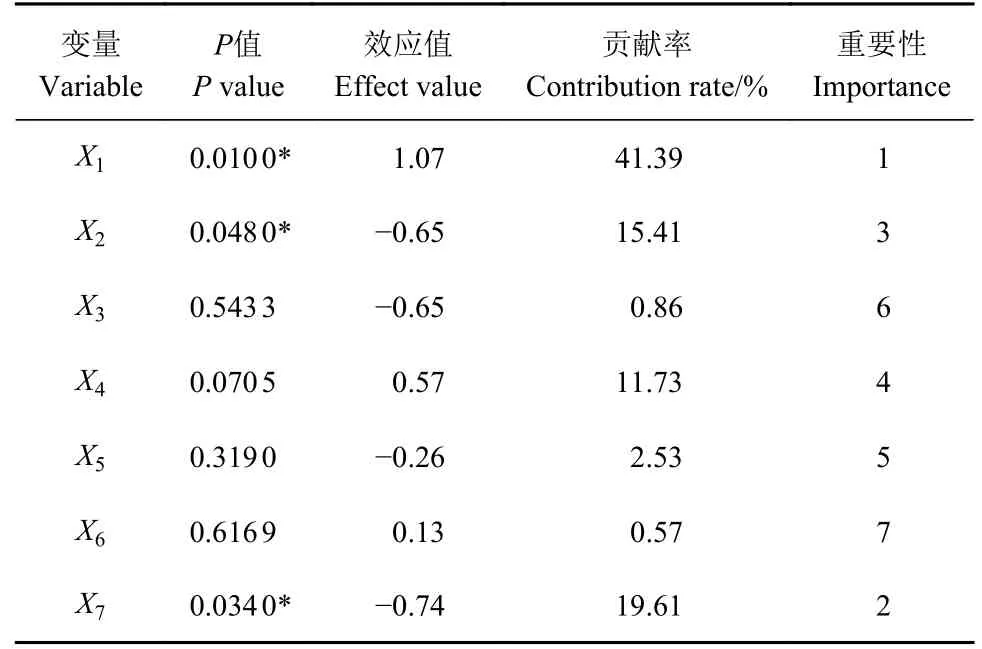
表 5 各因子贡献率及效应值Table 5 Contribution rates and effect values of individual factors

表 6 最陡爬坡试验结果Table 6 Results of steepest ascent experiment
对Y抑菌圈直径及YOD600这2 个回归方程进行方差分析,由表8,9 可知,模型均为P<0.0001,说明模型均可行且可达到极显著水平(P<0.01)。2 组模型的失拟项均P>0.05,说明实验结果与模型高度匹配。另外,2 组模型的R2分别为0.9263 和0.9408,均>0.9,说明2 组模型能够分别反应LV02 的细菌素抑菌圈直径及OD600与葡萄糖、硫酸锰及酵母浸粉之间的关系,可描述90%以上的试验值。2 组模型的R2
abj分别86.01%与88.76%,表明培养基配方对抑菌圈直径和OD600的影响达到了85%以上。变异系数(C·V)均<5%,表明该模型的重现性高。并且由Prob 值分析可知,Y抑菌圈直径模型中二次项X12、为极显著,X22为显著,一次项及交互项均不显著。YOD600模型中交互项X1X2为显著,说明葡萄糖与酵母浸粉对OD600菌体量有促进作用。X12、X72及为极显著,其余一次项及交互项均为不显著。2 组回归方程中的二次项系数均为负值,说明该方程具有最大值。另外根据Y抑菌圈直径及YOD600的方差分析结果,得到影响LV02 的细菌素抗菌能力及OD600的因素大小顺序为:X1>X2>X7,即葡萄糖>酵母浸粉>硫酸锰。

表 7 中心组合设计及结果Table 7 CCD design and response values
影响因子葡萄糖、硫酸锰及酵母浸粉两两与响应值抑菌圈直径及OD600之间的响应曲面图及等高线结果如图12~15 所示。图12(a)及图13(i)反映了酵母浸粉不变的条件下,硫酸锰和葡萄糖对抑菌圈直径的交互影响。葡萄糖的质量浓度为27 ~35 g·L−1内抑菌圈直径有所提高,随后出现降低。等高线图形近圆形,说明硫酸锰和葡萄糖之间的交互影响较显著。图12(b)及图13(h)可以看出,在葡萄糖质量浓度不变的情况下,随着硫酸锰的增加、酵母浸粉的降低,抑菌圈直径呈上升趋势。当硫酸锰达到0.16 g·L−1左右、葡萄糖降低至16 g·L−1之后抑菌圈直径呈减小趋势。硫酸锰的响应面坡度比酵母浸粉的坡度大,说明硫酸锰对抑菌圈直径的影响较大。等高线呈现椭圆形,表明酵母浸粉和硫酸锰之间交互作用明显。从图12(c)及图13(d)可知,在硫酸锰一定的条件下随着葡萄糖的增加与酵母浸粉的降低,抑菌圈直径呈上升趋势。当葡萄糖添加量达到35 g·L−1时,酵母浸粉降至18 g·L−1之后抑菌圈直径逐渐降低。等高线呈椭圆形,表明酵母浸粉和葡萄糖之间的交互作用显著。图14、图15中关于酵母浸粉、硫酸锰及葡萄糖之间与OD600的作用效果与抑菌圈直径的结果相同。
2.7.2 验 证 试 验 结 果 为 了 验 证CCD 模 型 的 可 靠性,以葡萄糖34.07 g·L−1、硫酸锰0.16 g·L−1、酵母浸粉18.12 g·L−1,其他因素固定不变,进行3 次验证试验。如表10 所示,抑菌圈直径实际值为24.50 ± 0.31 mm,预测值为24.58 mm,与预测值相差近0.022%;OD600实际值为2.877 ± 0.23,预测值为2.877,与预测值相差近0.023%。表明2 个拟合方程优化结果可靠性大。同时,优化后的两种响应值相比未优化前分别提高了近26%与12%,说明试验所确定的优化方式合理有效,LV02 的抑菌能力及OD600的增加程度达到了预期目的。
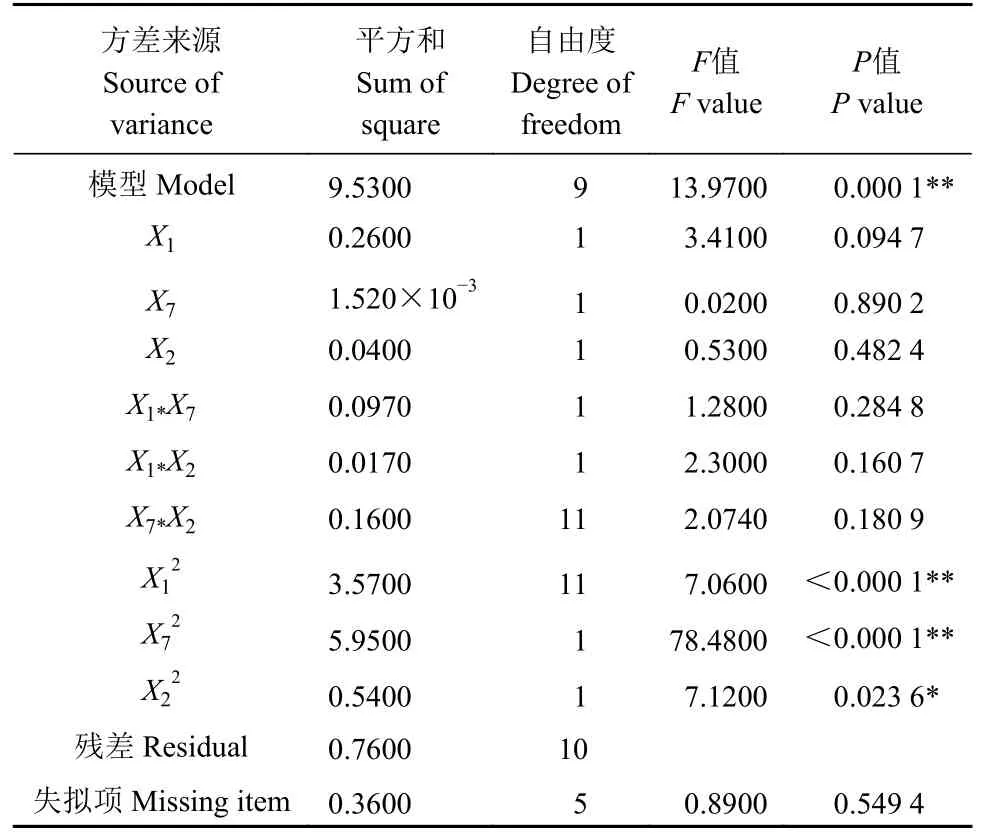
表 8 以抑菌圈直径为响应值的回归方程方差分析Table 8 Analysis of variance for regression model based on bacteriostatic zone diameter as response value
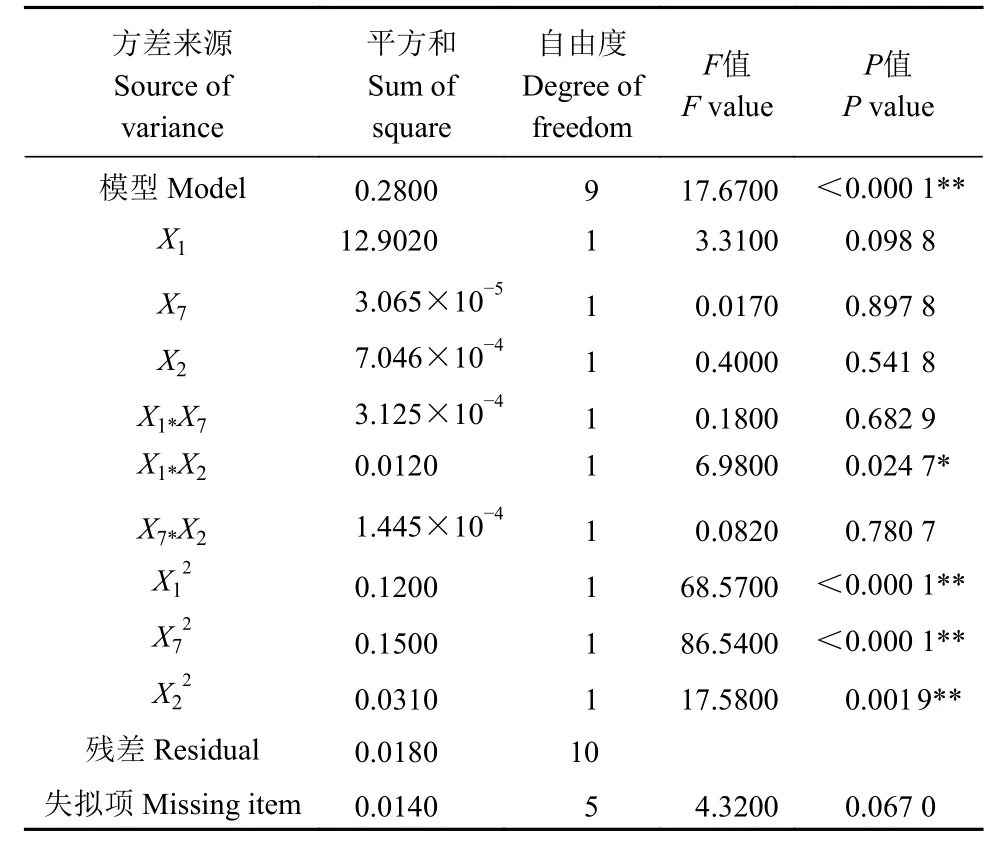
表 9 以OD600 为响应值的回归方程方差分析Table 9 Analysis of variance for regression model based on OD600 as response value
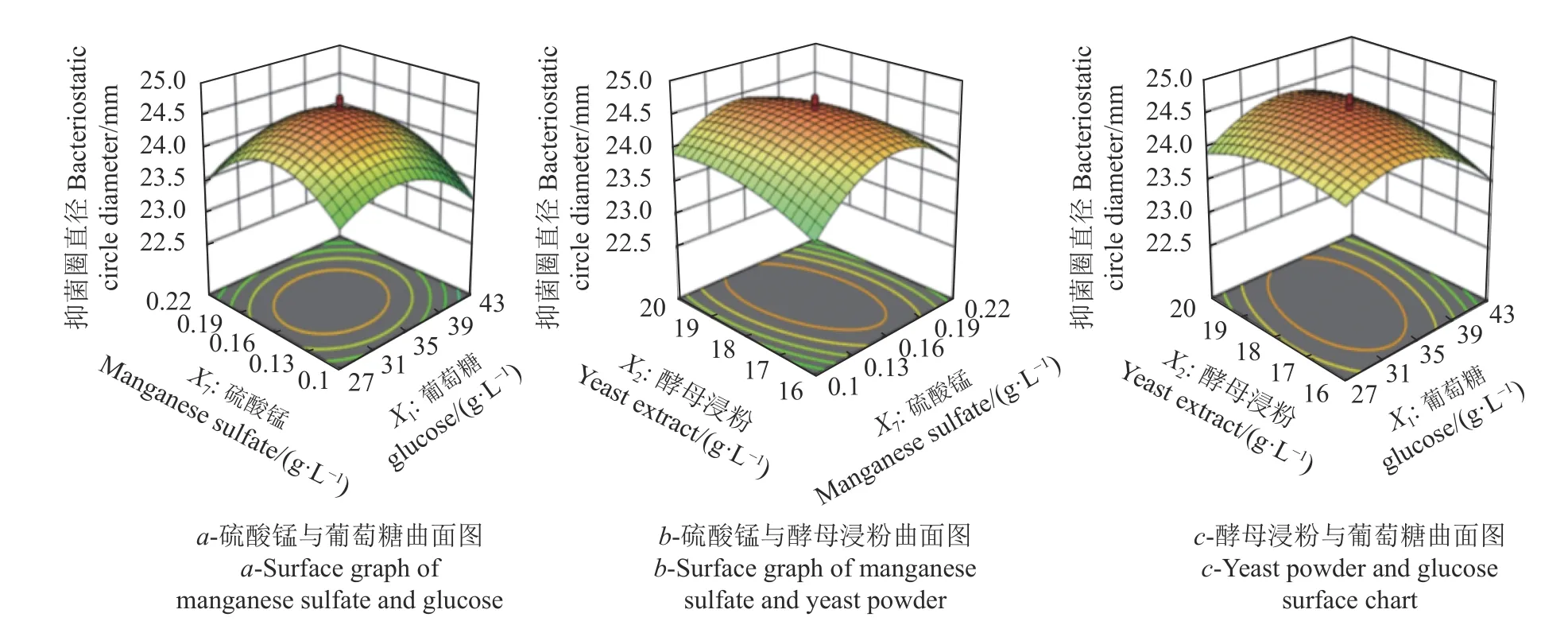
图 12 葡萄糖、硫酸锰和酵母浸粉两两交互影响LV02 抑菌圈直径的曲面图Fig. 12 Curved view on effects of glucose, manganese sulfate, and yeast extract in medium on LV02 inhibition zone diameter
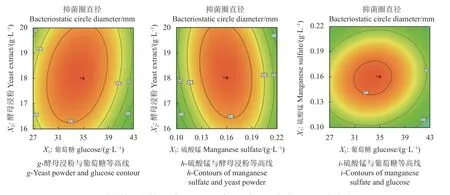
图 13 葡萄糖、硫酸锰和酵母浸粉两两交互影响LV02 抑菌圈直径的等高线图Fig. 13 Contour lines on effects of glucose, manganese sulfate, and yeast extract in medium on LV02 inhibition zone diameter
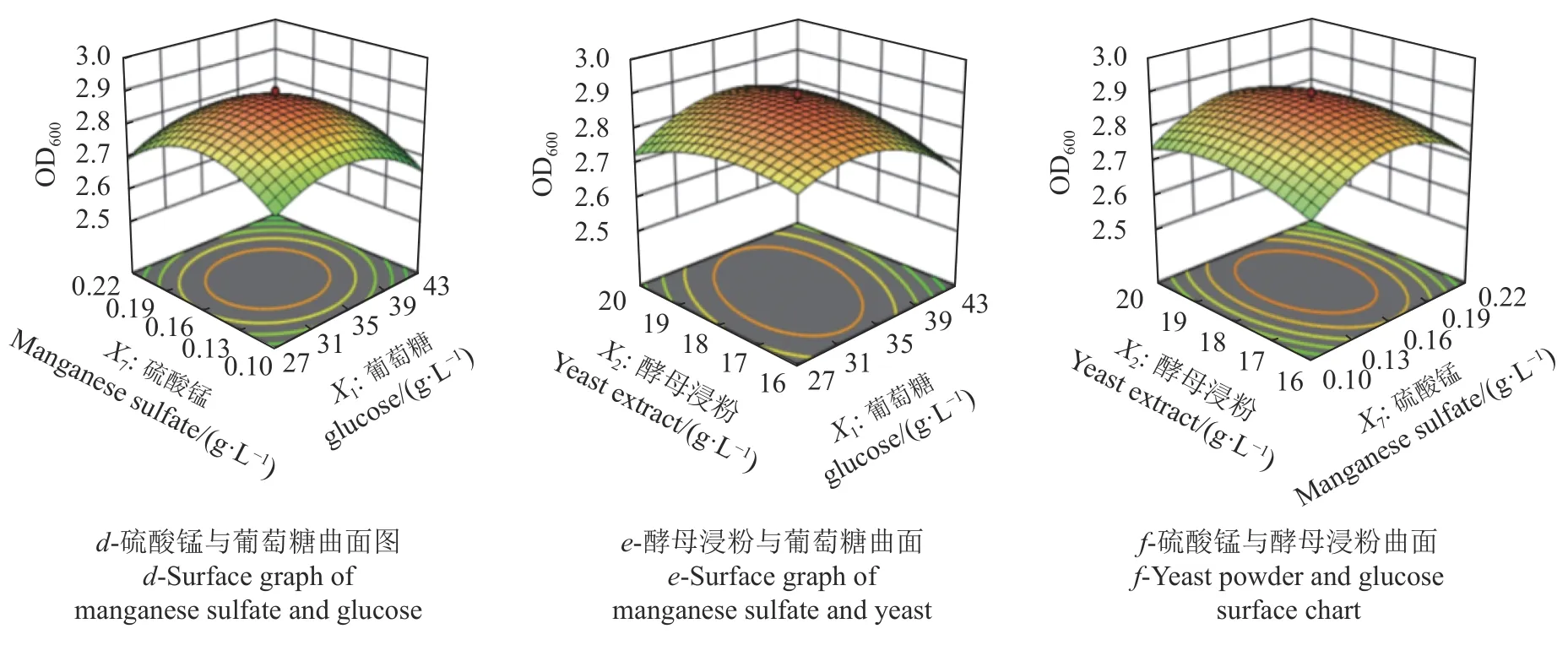
图 14 葡萄糖、硫酸锰和酵母浸粉两两交互影响LV02 OD600 的曲面图Fig. 14 Curved view on effects of glucose, manganese sulfate, and yeast extract in medium on LV02 OD600
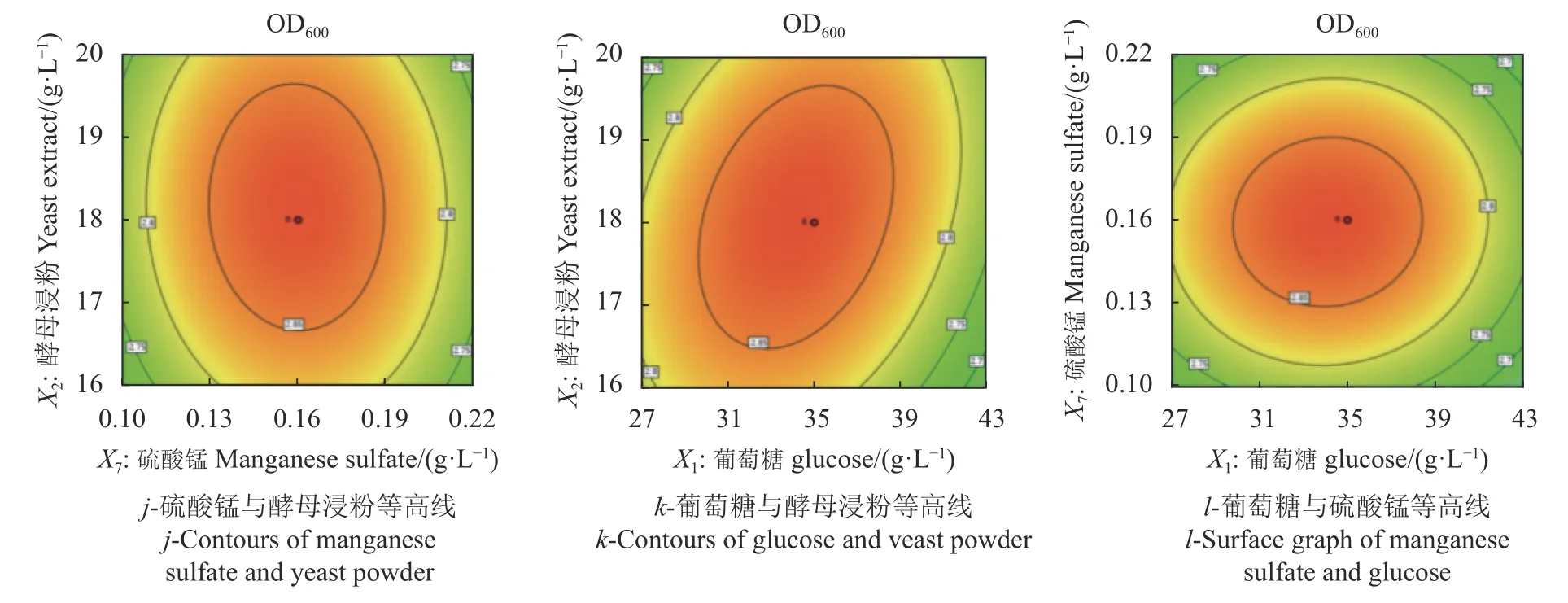
图 15 葡萄糖、硫酸锰和酵母浸粉两两交互影响LV02 OD600 的等高线图Fig. 15 Contour lines on effects of glucose, manganese sulfate, and yeast extract in medium on LV02 OD600
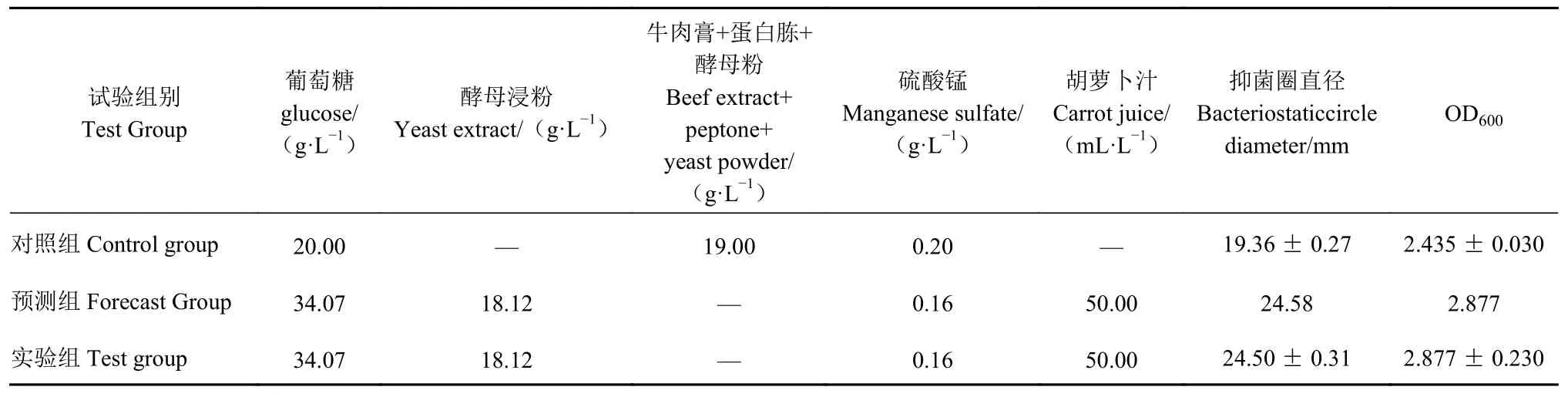
表 10 LV02 发酵培养基验证试验结果Table 10 Verification of LV02 fermentation medium
3 讨论与结论
植物乳杆菌LV02 发酵培养基对其抑菌能力及OD600有着重要影响,这决定着LV02 对腐败菌的抗菌效果与活菌数。有研究表明,经优化后的发酵培养基可明显提高抗菌能力,细菌素是原先的1.62倍[9],具有较高的研究与利用价值。研究者曾发现酵母提取物对植物乳杆菌的生物量影响最大[14]。本研究选用以大肠杆菌YS 为指示菌,抑菌圈直径及生物量OD600为评价指标。在单因素试验的基础上,采用PB 试验及最陡爬坡试验使影响因子的步长及方向接近最大产值,确定CCD 试验中心点。采用CCD设计试验,确定关键影响因子的最佳水平。并通过牛津杯法研究LV02 的抑菌特性,来确定LV02 对温度及pH 的稳定性。试验结果显示,酵母浸粉、葡萄糖及硫酸锰这3 种因子对LV02 发酵培养基抑菌功效影响较大,这与章检明[24]、王莉[25]和王帅[26]等的研究结果一致,可能是酵母浸粉中含有利于抗菌物质合成的氨基酸、生长因子;葡萄糖是最基础的单糖,可以使植物乳杆菌LV02 得到直接的碳源吸收;而硫酸锰可能是其Mn2+可促进合成植物乳杆菌LV02 的抗菌物质;PB 试验结果表明,胡萝卜汁可促进植物乳杆菌LV02 分泌抑菌物质,但其不属于关键因子,优化后的培养基配方中除了胡萝卜汁用量无变化之外,其余多种组分含量有变更,分析可能不同培养基成分之间存在相互作用[16,29],降低了胡萝卜汁的正效应。
pH 在偏酸性环境下更利于发挥LV02 的抑菌性,可能是在该环境下更有利于LV02 抑菌物质的合成;LV02 在100 ℃处理120 min 后可保留抗菌活性,可能是LV02 菌株自身可耐高温;LV02 可以抑制大肠杆菌YS,可能是其产生的细菌素可以抑制大肠杆菌形成生物膜[30]。本文最终得到LV02 发酵培养基的优化配方为:葡萄糖34.07 g·L−1、酵母浸粉18.12 g·L−1、磷酸氢二钾2 g·L−1、硫酸锰0.16 g·L−1、乙酸钠5 g·L−1、硫酸镁0.2 g·L−1、柠檬酸铵1 g·L−1、吐温80 1 mL·L−1、胡萝卜汁50 mL·L−1,蒸馏水1 L。用该配方培养LV02,使对大肠杆菌YS 的抑菌圈直径比未优化前提高了近26%,OD600提高了12%,说明优化方式合理有效。通过抑菌特性分析,确定了粗提植物乳杆菌LV02 的细菌素所需硫酸铵饱和度为80%,证明了植物乳杆菌LV02 具有热稳定性(100 ℃,120 min)、酸碱稳定性(pH 3.0~7.5)与抑菌性。本试验可为植物乳杆菌LV02 开发抗菌保鲜类产品提供技术参考。

