溶胶-凝胶法构筑介孔二氧化硅纳微结构
韩延东,韩明勇,杨文胜,2
(1.天津大学分子+研究院,天津300072;2.吉林大学化学学院,长春130012)
二氧化硅(SiO2)是自然界最为丰富的物质之一[1]. 1864年Graham[2]采用溶胶-凝胶技术首次获得凝胶状SiO2,迄今,利用此方法制备的各种SiO2材料已被大量生产并得到了广泛的应用. 尤其是在催化[3,4]、吸附[5,6]、分离[7,8]和生物医药[9~11]等领域的重要应用前景,有序介孔结构的SiO2材料一直备受关注. 1992年Kresge 等[12]首先发现以表面活性剂十六烷基三甲基溴化铵(CTAB)为介孔导向剂,硅酸酯在醇/水混合体系中经水解/缩合过程形成均匀的孔径为3~4 nm 的六角形介孔SiO2. 随后以CTAB 为介孔导向剂的溶胶-凝胶策略被扩展应用于合成不同种类的有序介孔材料,包括金属氧化物[13]、有机聚合物[14]、过渡金属[15]等. 该溶胶-凝胶法制备介孔SiO2分为如下过程:(1)硅酸酯水解;(2)介孔导向剂与硅酸脂水解物种间的自组装;(3)水解物种间的缩合[16,17]. 反应体系的pH、温度、凝胶化时间、表面活性剂浓度及抗衡离子种类等对这3个过程较为敏感,通过改变这些变量可以对介孔SiO2的孔径和结构进行有效调控[18].

Fig.1 Schematic representation of various mesoporous silica nanomicrostructures prepared by the sol-gel approach[22~27]
此后研究者也尝试使用其它表面活性剂,如嵌段共聚物或非离子型表面活性剂等调控介孔SiO2的孔道尺寸及形状[19],但以CTAB 为介孔导向剂的溶胶-凝胶法仍是迄今为止制备介孔SiO2材料最为常见的方法[20,21]. 为了改善和提高介孔SiO2材料的性能以拓展其应用范围,近年来研究者构筑了各种复杂的介孔SiO2纳微结构,包括单壳层空心、多壳层空心、蛋黄壳层、双面神、纳米管状、薄膜等不同类型的纳微结构(见图1)[22~27]. 本文综述了利用溶胶-凝胶法构筑介孔SiO2纳微结构的研究进展及其在生物、医药、催化、吸附等领域的应用研究,并对这一领域所面临的问题和未来发展方向进行了展望.
1 介孔SiO2纳微结构的构筑
1.1 球形介孔SiO2纳微结构
1.1.1 实心介孔SiO2由于操作简单、条件温和、变量多样,如CTAB浓度、温度、溶剂极性或其它助模板剂等,以CTAB为介孔导向剂的溶胶-凝胶法可以更有效地调控实心介孔SiO2粒子的尺寸、尺寸分布及孔径的均一性,已成为介孔SiO2粒子制备的重要方法[20]. 其优点在于可以在较低温度下在溶液中形成介孔结构,而且通过对CTAB 分子浓度进行调控或化学修饰,就可以较容易地调控介孔SiO2粒子的尺寸和孔径[12,16]. 至今,利用CTAB为模板的溶胶-凝胶法改善介孔SiO2的尺寸、结构、性能及其应用仍然是介孔SiO2材料领域的研究热点和难点.
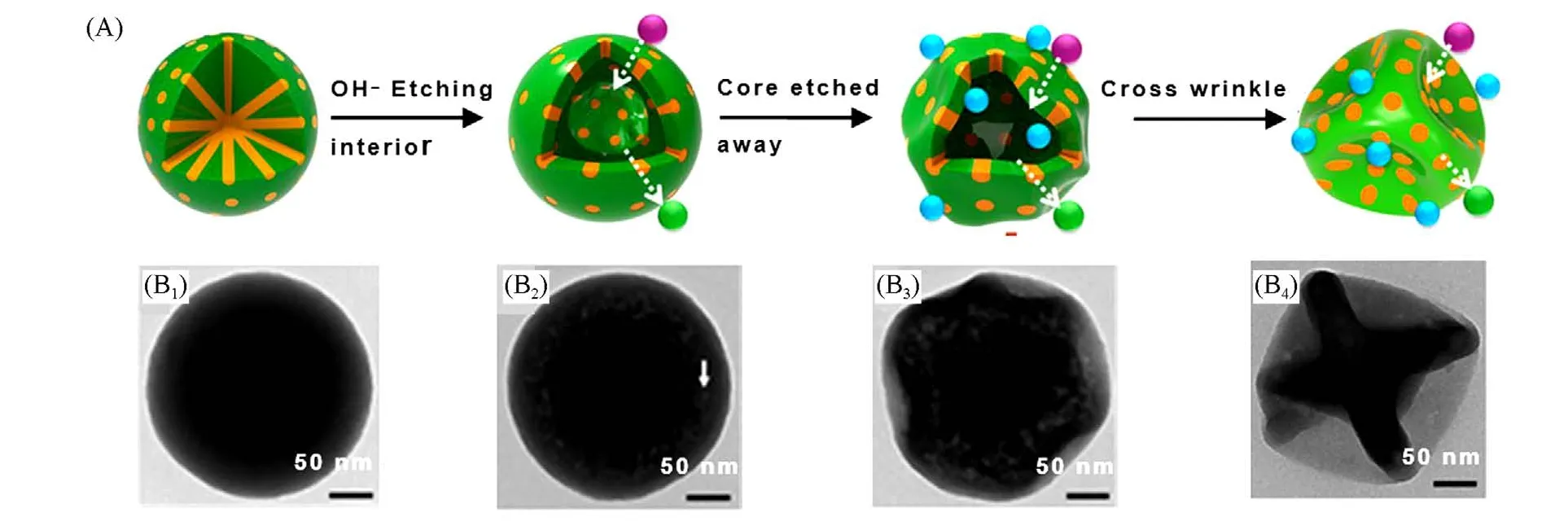
Fig.2 Illustration of the formation mechanism of the defrmable hollow mesoporous silica spheres(A),TEMimages of deformable hollow mesoporous silica via the preferential etching approach for the thioether-bridged mesostructured silica spheres incubated in NaOH aqueous solution(0.48 mol/L)for 1(B1),3(B2),5(B3)and 20 min(B4). The arrow in(B2)indicates the voids[22]
1.1.2 单壳层空心介孔SiO2由于具有较大的内部空腔和较高的比表面积,单壳层空心介孔SiO2微球备受关注,在药物存储/释放、催化、吸附、分离等领域有广阔的应用前景[28~33]. 1996年,Stucky等[34]在乳液体系中利用阳离子表面活性剂为介孔导向剂进行硅酸脂水解/缩合形成空心介孔SiO2. 随后,Wang等[35]在非离子表面活性剂稳定的水/油乳液中,也能够得到空心介孔SiO2微球. 除油包水体系外,其它水包油体系[36~39]、水-油-水体系[40]或油-水-油体系[41]等,都可以控制硅酸脂前体在油-水界面的水解/缩合得到空心介孔SiO2微球. 虽然乳液体系的稳定性较差,但在以CTAB为介孔导向剂的溶胶-凝胶法中通过优化醇/水比和CTAB 的使用浓度,可以调控正硅酸乙酯(TEOS)的水解/缩合速率,形成相对稳定的微乳液油滴(水包油),再经缓慢的水解/缩合过程不但可以得到粒径均一的空心介孔SiO2微球,还可实现对微球尺寸(210~720 nm)和壳层厚度(40~140 nm)的有效调控[42]. 近年来的研究还发现,在空心SiO2的骨架中引入键长和键角易于改变的有机组份,可以使空心SiO2粒子壳层具有一定的柔性,从而赋予粒子结构形变的能力[43,44]. 如Lu等[22]采用CTAB为介孔导向剂的溶胶-凝胶法,在醇/水溶液中加入双硅源前体,TEOS和双[3-(三乙氧基甲硅烷基)丙基]四硫化物(TESPTS),可形成有机/无机杂化的介孔SiO2粒子. 该粒子刻蚀后,缩合度较低的内核部分会被选择性刻蚀掉,形成空心介孔结构[图2(A)]. 当壳层厚度降低到20~38 nm之间时,粒子的柔性明显增加,烘干后会形成清晰的皱褶形状[图2(B1)~(B4)]. 研究结果表明,该空心介孔粒子的杨氏模量可以降低到3.95~47.7 MPa. 这种柔性的空心介孔SiO2胶囊加载抗癌药物后,表现出更高的细胞摄取效率和对癌细胞的杀伤作用. 除此之外,也有研究报道以聚合物[45]或其它胶体粒子[46]作为硬模板制备空心介孔SiO2,该类硬模板在对空心介孔粒子的尺寸和壳层厚度等结构参数调控方面更具优势,但需要更为苛刻的煅烧或刻蚀去除模板获得空心介孔结构.
1.1.3 多壳层空心介孔SiO2与单壳层空心介孔SiO2相比,多壳层空心介孔SiO2具有多腔室的内环境、可调的质量传输通道、以及更大的面积/体积比[47,48],可以进一步拓展空心介孔SiO2在异相催化[49]、多级药物释放[50]、高性能锂离子电池[51]、光子学器件[52,53]等领域的应用. 在多壳层空心介孔SiO2的制备方法中,常见的是软模板的方法[54~58]. 如Zhang等[54]以1,2-双(三乙氧基甲硅烷基)乙烷(BTSE)为硅源和非离子表面活性剂聚环氧乙烷-b-聚环氧丙烷-b-聚环氧乙烷三嵌段共聚物(P85)为介孔导向剂,在酸催化条件下经溶胶-凝胶过程,制备了壳层数为2~7层的海绵状多壳层空心介孔SiO2微球. 此外也有众多研究者为调控多壳层空心SiO2微球的壳层厚度和壳层间距等结构参数,采用硬模板的方法[48,49].如Li 等[59]以TEOS 作为硅源,聚甲基丙烯酸(PMAA)为硬模板,经溶胶-凝胶过程层/层组装生长形成SiO2@PMAA@SiO2@PMAA@SiO2多壳层夹心结构,高温煅烧除去PMAA 模板层后,得到多壳层空心介孔SiO2微球. 但这种硬模板的制备方法需要反复离心纯化和多次的投料后再生长,实验步骤较为繁琐,且容易产生自成核[48],随后的高温煅烧也会在一定程度上导致多壳层结构的损坏[49,59]. 近年来,研究者开始尝试利用无模板法制备多壳层空心介孔SiO2微球. 2011年,Chen等[60]在研究中发现,SiO2微球在水中加热孵化时,其壳层会因为水解而发生软化(—Si—O—Si—缩合度降低);在醇相中加热孵化时其壳层会进一步缩合而发生硬化(—Si—O—Si—缩合度升高). 通过在醇或水中交替处理后多次生长的SiO2微球,可以得到界面结构具有明显差异性的多壳层SiO2微球. 经水中加热进行选择性刻蚀后,软壳层部分会被水溶解掉,而硬壳层部分会被保留,从而形成多壳层空心多孔SiO2微球. 2015 年,Zhao 等[61]以CTAB 为介孔导向剂,以TEOS 和BTSE 为双硅源进行共水解/缩合,得到了内部缩合度较低,而外部缩合度较高的SiO2微球. 通过多次注入2种硅源分子进行再生长,也可以形成界面结构具有明显差异性的多壳层SiO2微球. 这种微球经水热处理并高温煅烧去除CTAB后,可以转化成多壳层空心介孔(约3.2 nm)SiO2. 本课题组[62]在对Stöber法中SiO2粒子的生长过程研究中发现,TEOS的水解/缩合速率会随反应体系碱浓度的升高而加快,并且改变所使用碱催化剂的种类可以调节水解和缩合速率的相对速度. 据此,以强碱性四甲基氢氧化铵(TMAH)作为催化剂,使反应初期TEOS 水解更有优势,形成缩合度较低的SiO2粒子;而在反应后期由于催化剂的消耗,TEOS 水解/缩合速率趋于相对平衡,所沉积的SiO2壳层具有较高的缩合度. 此外,定量的TEOS滴定实验证实TEOS的消耗量与TMAH的消耗呈线性关系,因此可以通过改变TMAH的使用量实现对层/层组装生长过程中SiO2粒子低缩合度和高缩合度壳层厚度的精准调控[图3(A)],从而实现对多壳层空心介孔二氧化硅粒子的壳层数目、壳层厚度以及壳层间距等结构参数的精准调控[图3(B1)~(B3)])[23],为复杂多孔金属氧化物纳微结构的构筑提供了新的设计思路.
1.1.4 蛋黄壳层结构介孔SiO2由于具有可移动核并且与外部介孔壳层之间具有较大的空腔,蛋黄壳层介孔结构具有密度低、比表面积大、渗透性好、负载能力强等特点,并且其内核与外壳层还可具备不同的功能[63~66],可应用于药物可控释放[67,68]、催化[69,70]、能量存储[71,72]等领域. 硬模板层/层组装生长是构筑蛋黄壳层介孔结构的常规方法. 如可以首先制备出内核粒子,然后在内核粒子表面层/层组装生长2层不同材质的壳层,其中内侧的壳层可以通过刻蚀或煅烧选择性去除,而外侧壳层和内核粒子得以保留[73~75]. 这种硬模板法可以较好地控制蛋黄壳介孔微球的内核尺寸、空腔大小、外壳层厚度等结构参数. 利用软模板法如乳液途径[76,77]也可以构筑出复杂的蛋黄壳层介孔结构,其特点是操作相对简单,但对微纳结构调控的精准度尚有所不足. 此外,也有课题组利用柯肯达尔效应(Kirkendall effect)制备蛋黄壳层介孔结构[78,79]. 该方法利用刻蚀过程中溶质在粒子内部不同壳层部位扩散速率的差异,实现对微球内核尺寸和外壳层厚度等结构参数的调控. 2008年,Yin等[80]研究发现,利用溶胶-凝胶法制备的无定形SiO2粒子在NaBH4碱溶液中孵化时,粒子内部更容易受到刻蚀,然后再生长形成新的多孔外壳. 通过改变孵化时间和孵化温度可以得到不同尺寸的蛋黄壳层多孔的SiO2. 2009年,Tang等[81]在研究中也发现,通过调控硅酸酯的水解/缩合过程,可以使SiO2粒子形成内核与外壳层缩合度较高,而中间夹层缩合度较低的夹心结构,此时通过选择性刻蚀就可以去除缩合度较低的中间夹层,得到具有蛋黄壳层多孔结构的SiO2微球. 由于在溶胶-凝胶过程中没有引入介孔导向剂,上述研究中所得到的SiO2微球外壳层都是无序的多孔结构. 2014年,Teng 等[24]以TEOS和BTSE为双硅源,以CTAB 为介孔导向剂,通过双硅源共水解/缩合制备了具有介孔结构的有机-无机杂化的SiO2微球. 由于BTSE的水解/缩合速率低于TEOS,导致微球从内至外缩合度和化学成分存在差异,水中加热孵化后,缩合度相对较低的中间夹层部分发生溶解,从而形成尺寸较为均一的蛋黄壳层介孔SiO2微球. 通过改变2种硅酸酯前体的摩尔比和CTAB 的用量,可以实现对微球尺寸的有效调控(110~380 nm),微球的最大比表面积可达到975 m2/g. 由于使用CTAB 作为介孔导向剂,制备微球的孔径均为3.2 nm 左右. 又由于使用BTSE作为硅源与TEOS共水解/缩合,孵化处理后微球内部仍会残留大量的有机基团(乙基),与使用单一TEOS硅源制备的介孔SiO2相比,这种有机-无机杂化的介孔SiO2在高浓度条件下仍呈现良好的非溶血活性(图4).
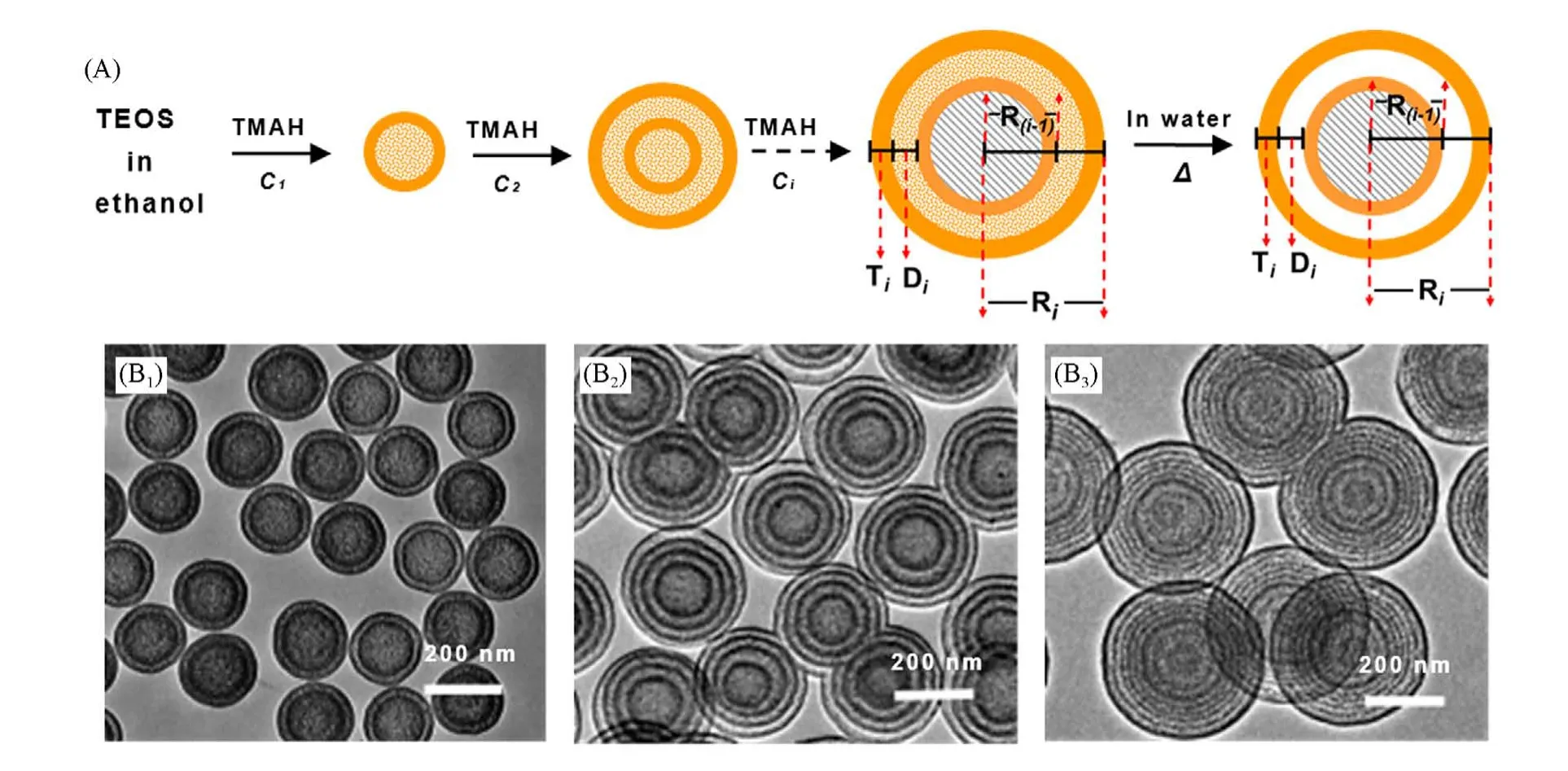
Fig.3 Schematic representation for fabrication of the multi-shelled hollow mesoporous silica spheres via the in situ seed growth(A), TEM images of multishelled hollow silica spheres after incubating solid spheres prepared by two(B1),four(B2),and eight(B3)successive injections of TMAH into 500 mmol/L ethanol solution of TEOS[23]
1.2 非球形介孔SiO2纳微结构
1.2.1 管状介孔SiO2除了上述的空心、多壳层、蛋黄壳层等球形介孔SiO2纳微结构以外,研究者也尝试了其它非球形介孔SiO2纳微结构的设计与构筑. 如一维管状的介孔SiO2,由于其内壁和外壁表面均可实现功能化,在生物分离、催化等领域有潜在的应用前景[82,83]. 2010年,Huang等[84]研究发现,新型组氨酸衍生的表面活性剂N-十二烷酰基-L-组氨酸(DHis)在水溶液中存在聚集行为. 将其与阳离子表面活性剂适量混合后,溶液会逐渐从透明均相变成果冻状溶胶,并逐渐演变成表面带有正电荷的纤维状凝胶. 基于此过程,可以复制构筑管状介孔SiO2纳微结构,其内径为约10 nm,外径为约30 nm. 当改变反应温度时,内径和外径尺寸会有适当变化(8~10 nm 和26~30 nm),但管壁厚度基本保持不变. 近期研究还发现,有机/无机杂化的手性SiO2纳米管表现出独特的光学和传感特性[85,86]. 2019 年,Yang等[25]研究发现,以有机硅源1,2-二苯基-1,2-双[4-(三乙氧基甲硅烷基)苯基]乙烯(BTSTPE)为前驱体,以手性阳离子凝胶剂L-ValPyBr(由L-缬氨酸组成)或D-ValPyBr(由D-缬氨酸组成)的自组装体作为模板,在碱性条件下经溶胶-凝胶过程,可分别得到含四苯乙烯(TPE)的左旋(Silica-M)或右旋(Silica-P)的SiO2介孔纳米管(图5),由此得到的管状介孔SiO2具有独特的圆偏振发光特性.
1.2.2 薄膜型介孔SiO2以金属、玻璃、石墨或光纤等为基底或支撑物沉积的二维薄膜型介孔SiO2纳微结构,由于其具有较高的比表面积以及有序的介孔结构,在光学、传感、分离等领域的应用价值一直备受关注[87~89]. 在早期研究中,通常是通过硅酸酯前体在两相界面通过溶胶-凝胶过程构筑有序的介孔SiO2薄膜,此时由于沉积物与基材平行时,表面能更低,导致构筑的介孔SiO2薄膜中孔道取向总是平行于薄膜表面[90,91]. 从应用角度看,垂直于薄膜表面的孔道其性能可能更为优越[92]. 近期有课题组尝试使用热解的石墨[93]或改性玻璃[94]为基底,通过π-π或亲水-疏水相互作用改变介孔的取向,得到平行或垂直取向的介孔薄膜结构. 如Zhao等[26]以CTAC为介孔导向剂,基于双相分层生长策略,将玻璃基底浸入含有CTAC 和TEOS 的油水混合的两相体系中. 通过调控TEOS 在CTAC 胶束表面的水解/缩合速率,经缓慢的溶胶-凝胶过程,可最终形成孔道取向垂直于基底的薄膜型介孔SiO2纳微结构,该介孔SiO2薄膜具有约50 nm的超薄厚度,以及约1420 m2/g的超高表面积(图6).
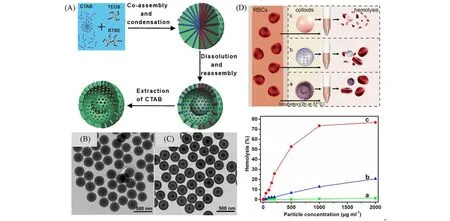
Fig.4 Schematic illustration for the sol-gel formation of yolk-shell mesoporous hybrid silica spheres with ordered radial mesochannels(A), TEM image of the as-made mesostructured inorganic-organic hybrid spheres(B),TEM image of the yolk-shell mesoporous hybrid spheres with ordered radial mesochannels prepared by incubating the as-made hybrid spheres in water at 70 ℃for 12 h(C),schematic representation for hemolysis experiments(top panel) and percentages of hemolysis of red blood cells(lower panel)incubated with the yolk-shell mesoporous hybrid silica spheres(a), mesoporous silica spheres prepared by using TEOS as precursor and CTAB as pore directing agent(b) and commercial Stöber amorphous silica spheres prepared by using TEOS as precursor at different concentrations(c)(D)[24]
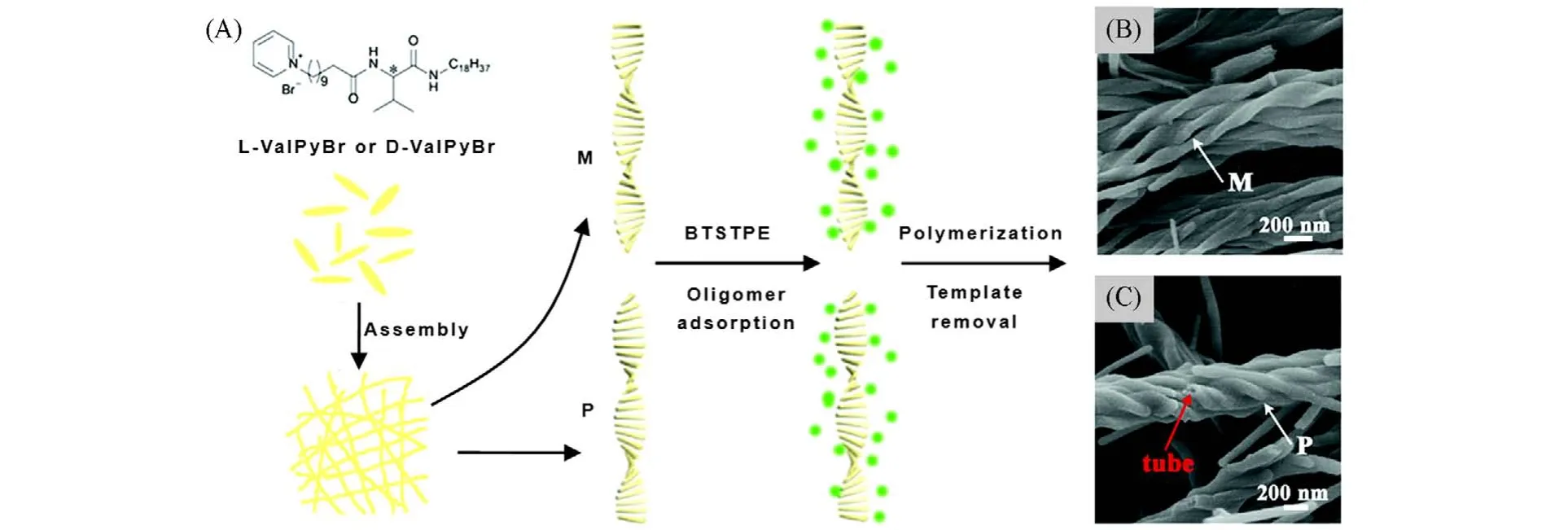
Fig.5 Chemical structures of the chiral L-ValPyBr and D-ValPyBr and schematic illustration for formation of the single-handed helical TPE-containing silica nanotubes(A), FESEM images of TPE-containing silica-M(B)and silica-P(C)nanotubes[25]

Fig.6 Schematic illustration for the formation of membranous mesoporous silica via the simple biphase stratification growth strategy(A), SEM(B) and TEM(C) images of the membranous mesoporous silica[26]
1.2.3 双面神结构介孔SiO2除一维纳米管、二维薄膜外,近年来在三维非球形介孔SiO2粒子制备方面也取得了突破. 如双面神结构介孔SiO2,由于其具有双重的表面结构和两个相对独立的空间,有利于双客体分子的负载或不同材料的复合,从而赋予介孔SiO2粒子多功能特性[27,95~97]. 2014年,Li等[97]利用溶胶-凝胶法以CTAB为介孔导向剂制备了表面带有大量的亲水基团(—Si—OH)的介孔SiO2微球,以此为种子,通过不断滴加亲油的BTSE硅源,在CTAB导向剂作用下通过异相成核/生长,在亲水微球表面形成亲油的介孔SiO2方块. 这种具有“球@方块”结构的双面神型介孔SiO2不仅具备双重浸润性,还具有双重介孔孔道(2.1 和4.5 nm). 2018 年,Zhao 等[27]也基于溶胶-凝胶法,通过表面电荷介导(Surface-charge-mediated)的策略成功合成出了具有疏水性碳和亲水性SiO2空间隔离的双介孔Fe3O4@mC@mSiO2双面神纳微结构(图7). 其中亲水性介孔SiO2棒部分具有可调的长度(50~400 nm)和均一的孔道尺寸(约2.7 nm);而疏水性介孔碳球部分也具有可调的体积(其直径约为150 nm)和均一的孔径(约10 nm). 通过改变SiO2棒和碳球之间的体积比可以精确调控其亲水/疏水比. 由于兼具两亲性和磁性,这种材料具有类似表面活性剂的乳液稳定能力以及在外加磁场下的可回收能力.
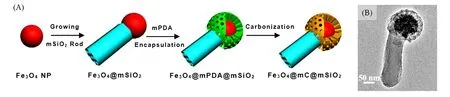
Fig.7 Schematic illustration for the formation of Janus mesoporous Fe3O4@mC@mSiO2 via the surface-chargecontrolled selective encapsulation(A),TEM image of the Janus mesoporous Fe3O4@mC@mSiO2(B)[27]
2 介孔SiO2纳微结构的应用
由于具有均一介孔孔径、较高的比表面积、较大的孔容、差异性界面结构等特点,复杂的介孔SiO2纳微结构在生物医用、催化、吸附、分离等领域拥有广泛的应用前景,受到学术界和工业界的广泛关注.
2.1 生物医学
由于单壳层或多壳层空心介孔SiO2纳微结构具有优异的药物负载能力以及良好的生物相容性和生物降解能力,其在生物医学领域的应用一直备受期待[98~102]. 如Shi 等[102]报道,通过水热刻蚀的途径可将溶胶-凝胶法制备的有机/无机杂化的空心介孔SiO2粒子进一步刻蚀成具有更大孔径的空心介孔结构. 该粒子可以负载更大尺寸的客体分子,如可将抗癌药盐酸阿霉素(DOX)和P-糖蛋白(P-gp)调节的小干扰核糖核酸(siRNA)同时封装到聚β-氨基酯-修饰的空心介孔SiO2粒子中. 这种载药控释体系具有更强的细胞穿透性和滞留作用,可以积聚在肿瘤中并被进一步内吞,从而有效杀死耐药性的癌细胞[图8(A1)~(A3)]. 此外,近期也有研究发现,通过设计空心介孔SiO2的壳层数目和构建有机/无机的杂化结构,可以更好地促使溶酶体逃逸和提高抗原的递送功效,从而提升癌细胞的免疫效果[103~106]. 如Yu等[106]报道,将卵清蛋白或肿瘤细胞片段负载在双壳层有机空心介孔SiO2上,与单壳层空心无机SiO2粒子相比,其肿瘤细胞碎片的释放得到了明显延长[图8(B1)~(B3)]. 皮下接种实验表明,有机硅的组成和双壳层结构可共同提高小鼠体内的免疫刺激,皮下接种疫苗后可显著延长35 d 后50%小鼠的存活率,并抑制了肿瘤接种后的黑色素瘤. 从生物成像角度看,介孔SiO2独特的纳微结构和良好的生物相容性有利于各类荧光探针的负载,并可应用于生物成像[107,108]. 2012年,Xiong等[108]报道,ZnO纳米晶经过三乙氧基硅烷、四乙氧基硅烷和氨丙基三乙氧基硅烷3种硅氧烷前体的层/层包覆,可得到单分散的ZnO@SiO2核-壳型粒子,在水、磷酸盐缓冲液和细胞培养基中均表现出良好的稳定性. 通过改变ZnO纳米晶的尺寸,可以得到蓝色、绿色和黄色的ZnO@SiO2复合粒子,其荧光量子产率可分别达到53.8%,48.7%和33.5%[图8(C1)~(C5)]. 细胞毒性和细胞吸收动力学实验结果证实,不同颜色的ZnO@SiO2复合粒子均表现出低细胞毒性,是一类有潜在应用价值的生物成像材料.
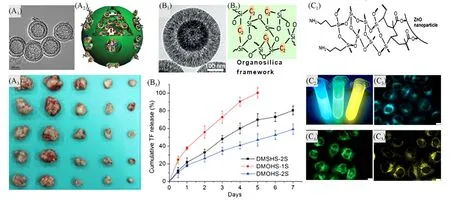
Fig.8 TEM image(A1)of the large-pore hollow mesoporous organosilica nanoparticles(HMONs),and schematic structures of P-gp modulator siRNA and DOX co-loaded in HMONs(A2),photographic images of tumors after different immunotherapy(A3)[102],TEM image(B1)and schematic(B2)of the wall structure of double-shelled mesoporous organosilica hollow silica(DMOHS-2S),tumor cell fragments(TF)release profile from various nanoparticles in PBS solution(B3)[106], schematic structures of ZnO@silica nanoparticles(C1), photograph(C2) and confocal luminescence images of Hela cells incubated with 50 μg/mL of 2.5 nm-ZnO@silica(C3),3.5 nm-ZnO@silica(C4)and 4.2 nm-ZnO@silica(C5)particles at 37 ℃under 365 nm UV light[108]
2.2 异相催化
空心或蛋黄-壳介孔SiO2粒子由于具有较高的比表面积、较大的孔容、良好的稳定性及易功能化的表面,是一类较为理想的异相催化剂或催化剂载体[109~114]. Liu等[114]通过将手性N-磺酰化二胺基有机铑的络合物固定在乙烯桥连的有机硅酸盐中,可制备出手性有机铑官能化的空心介孔纳米球. 该非均相催化剂在手性邻苯二甲酸酯的合成中具有高催化活性和对映选择性,且可方便地回收并多次重复使用. 此外,蛋黄-壳介孔结构的SiO2在作为催化剂时,由于其外壳层可以较好地保护活性粒子的浸出和聚集,其内核与外壳层又可具有协同作用,因此可更高效地促进催化反应进行[115,116]. 2012 年,Yang等[116]通过选择性刻蚀的方法制备出氨基-核/巯基-壳的空心介孔SiO2,该粒子的壳层厚度约为20 nm,核与壳之间的空隙间距约为24 nm. 在这种蛋黄-壳介孔结构中,核上碱性催化位点(氨基)和壳上的酸性催化位点(巯基)由于在空间上既相对独立,又彼此关联,因此可以有效催化亨利-脱缩醛串联反应(Deacetalization-Henry cascade reaction),其催化活性要明显优于简单物理混合的酸性和碱性催化剂.Qiao等[117]利用囊泡软模板的方法可制备出一种蛋黄-壳有机/无机杂化的空心介孔SiO2. 该粒子的空隙间距约为4 nm,壳层厚度约为16 nm[图9(A)],而且通过浸渍和还原的方法可将各种金属纳米粒子(如Au,Pt和Pd等)封装并限域在核与壳层之间的空间内[图9(B1)~(B3)],从而改善和提高金属粒子的催化活性. 如包裹了Pd 纳米粒子的蛋黄-壳型粒子,在醇氧化成醛的反应中,其催化转化率可接近100%,选择性可高达约99%[图9(C)].
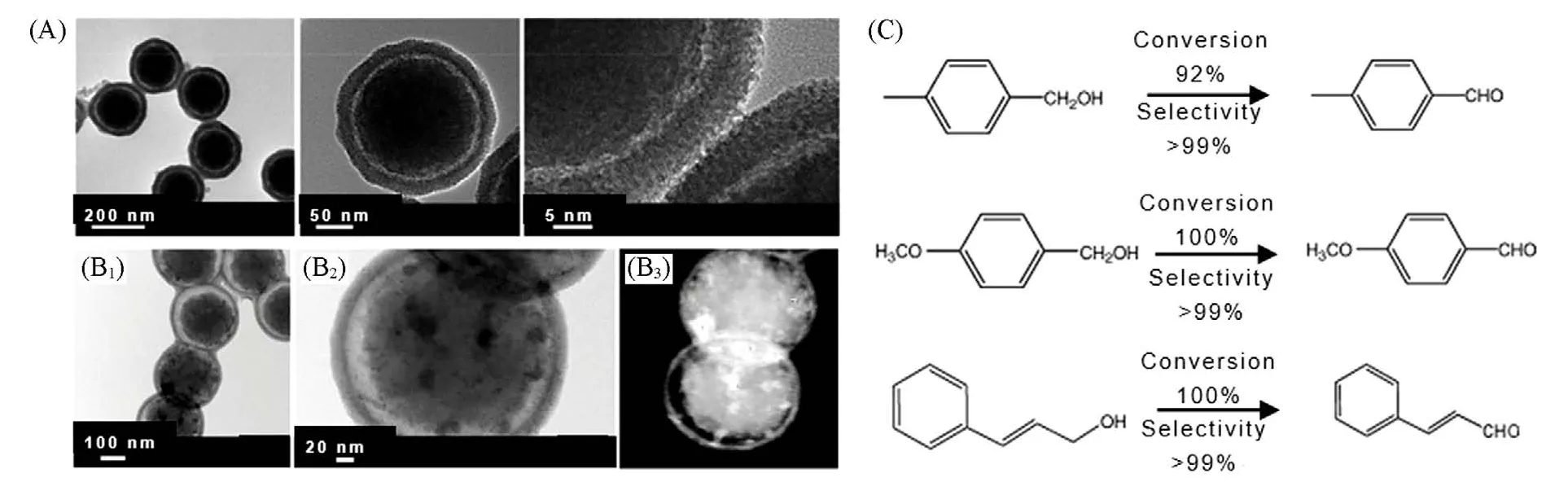
Fig.9 TEM images of the yolk-shell hybrid silica nanoparticles at different magnifications(A),TEM image(B1), HRTEM image(B2), and HAADF-STEM image(B3) of Pd-containing yolk-shell hybrid silica nanoparticles,selective oxidation of various alcohols into aldehyde over Pd-containing yolk-shell hybrid silica nanoreactors(C)[117]
2.3 吸附和分离
由于出色的分离选择性,分子印迹材料已经在吸附分离领域得到了广泛应用[118~122]. 通过聚合物合成过程引入与目标分子结构和形状互补的模板分子,除掉模板后可以得到大小和形状与模板分子互补的特异性结合位点[123~125]. 利用无机硅前体水解/缩合得到的介孔SiO2材料,其具有较大的比表面积和孔体积、明确且可调节的介孔通道、以及快速的吸附速率和易于功能化的表面,是一类较为理想的分子印迹基质材料[126,127]. 然而,在介孔SiO2的表面印记虽然很容易实现,但由于无机SiO2材料中—Si—O—Si—键刚性的化学特征,在吸附分离的应用中很容易受到磨损而破坏印迹的结合位点[128].进一步,通过无机和有机硅前体的共水解/缩合的溶胶-凝胶过程,形成有机/无机杂化的韧性孔壁结构可以克服这些缺陷[129]. Ozin等[130]首先将双酚A(BPA)印迹分子连接至功能性硅烷氧基单体上,生成共价结合的印迹前体,再以三嵌段共聚物为模板经酸催化溶胶-凝胶过程,将该前体掺入到交联的周期性介孔二氧化硅基质中,并在介孔SiO2的孔壁中形成清晰的印迹位点,可以从水中选择性地去除超过90%的双酚. 近期,Liang等[131]也设计了一种功能性的双酚A印迹单体[图10(A)],可通过溶胶-凝胶化学反应将分子印迹引入到有机/无机杂化的介孔SiO2膜中[图10(B)]. 这种双酚A印迹的介孔SiO2具有高度有序的周期性六边形介孔结构,比表面积为944.28 m2/g,在pH=6.5 时对双酚A 的饱和吸附容量可达到16.8 mg/g[图10(C)],相对选择性系数为1.06~3.20. 经过5个萃取/洗脱循环后,双酚A印迹介孔SiO2的吸附效率仍高达97.96%. 与未印迹的介孔SiO2相比,在从废水中选择性去除双酚A 的实验中,印迹后的介孔SiO2体现出明显的优势[图10(D)].
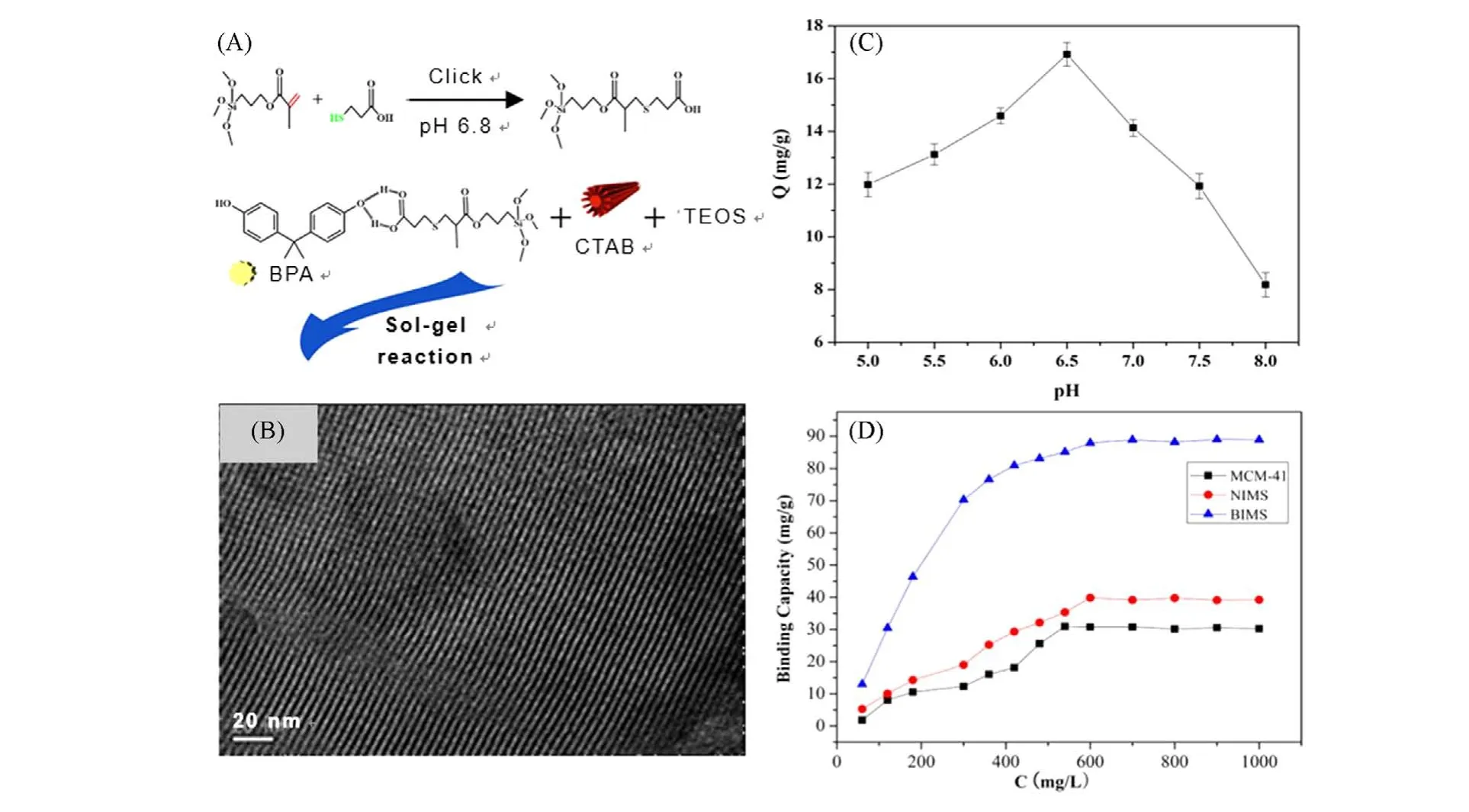
Fig.10 Schematic illustration for the synthesis of the functional monomer(A) and TEM image of the BPA(bisphenol A)imprinted mesoporous silica(BIMS)membrane(B),effect of pH on the binding capacity of the BIMS(C), binding capacity of the BIMS, non-imprinted mesoporous silica(NIMS), and bare mesoporous silica(MCM-41)(D)[131]
3 总结与展望
利用溶胶-凝胶法构筑介孔SiO2纳微结构的研究不但丰富和推动了硅化学领域自身的发展,同时也促进了纳米硅化学与生物医学、催化、吸附与分离等学科的交叉与融合. 然而从溶胶-凝胶法出发构筑的介孔SiO2纳微结构,目前对于尺寸、形貌、孔径、孔容、比表面积、缩合度、化学组分等调控更多地是依靠经验方法,对这些结构参数的调控还远未达到理性设计和构筑的层面. 这是因为硅酸酯类型及硅酸酯分子水解/缩合的速率与CTAB间的相互作用对结构参数的控制密切相关. 特别是在碱催化下溶胶-凝胶反应中,常规的硅烷试剂(如TEOS)与其它有机硅烷试剂在含有介孔导向剂的醇/水混合溶液中进行水解/缩合反应时,由于TEOS和其它硅烷试剂的水解/缩合速率不同,难以实现对于所形成的介孔SiO2纳微结构的精准调控. 在介孔导向剂的作用下,系统研究和深入理解双硅源或多硅源前体的水解/缩合的反应机制,并探究水解/缩合速率与纳微结构之间的相关性是实现介孔SiO2纳微结构理性设计与精准构筑的前提.
此外,能否实现介孔SiO2材料通过人体肾脏等组织的有效清除及其在人体肿瘤组织中特异性积累的平衡是介孔SiO2粒子在生物医药应用中所面临的一个重要挑战. 同时,载药后的介孔SiO2材料对肿瘤组织的靶向能力也至关重要,在肿瘤上的有效富集及剩余的部分通过肾脏等组织的快速清除对减少药物的副作用是有益的. 通过调控溶胶-凝胶过程,精准调控介孔SiO2纳微结构内部的活性位点(—Si—OH等)与—Si—O—Si—键的缩合度等结构参数,实现载药控释体系在体内靶向和生物降解/肾脏清除之间的相对平衡,是介孔SiO2在生物医药领域应用中必须解决的一个关键问题. 如果能够调控基于介孔SiO2载药体系在体内靶向和肾脏清除之间的平衡,这将有助于进一步提高和改善肿瘤的检测与治疗效果.
作为催化剂或催化剂载体使用时,介孔SiO2相对有限的热稳定性和化学稳定性是其进一步应用推广所必须解决的问题. 利用水热或溶剂热方法合成的介孔SiO2材料具有较好的稳定性,但目前还难于规模化制备. 深入理解溶胶-凝胶过程中不同反应阶段水解/缩合速率及其平衡关系,设计具有更高活性的有机硅酸酯前驱体,进一步提高介孔SiO2的缩合度及有序程度,是提高其稳定性的一个可能途径. 此外,一般手性催化反应的反应条件都比较温和,以手性的有机分子作为连接基团,设计合成具有手性的有机硅酸酯前驱体,通过溶胶-凝胶反应获得具有对映选择性的手性催化剂,是一个值得关注的研究领域.
在作为吸附剂时,通过溶胶-凝胶法制备的介孔SiO2通常是非晶态的,孔壁中—Si—O—Si—难以形成长程有序的网络结构,孔的机械强度较差,在吸附或脱附过程中易发生结构塌陷. 在溶胶-凝胶过程中引入有机硅源,形成无机-有机杂化结构,是提升介孔SiO2孔壁的韧性,改善其机械强度的一个可行途径. 这类无机-有机杂化SiO2构筑通常涉及双硅源的反应,与单硅源前驱体相比,双硅源或多硅源前驱体的共水解/缩合反应更为复杂,其尺寸/尺寸分布调控机制尚不够清晰. 系统研究和深入探索在介孔模板剂存在条件下,双硅源或多硅源的水解/缩合速率及其平衡机制,实现对无机-有机杂化介孔SiO2微纳结构以及尺寸/尺寸均一性的有效调控,在保证其吸附性能及机械强度的同时,提高其过滤回收效率,也是一个很有研究价值和重要应用背景的研究课题.
总之,通过有效调控溶胶-凝胶过程中多种硅酸酯分子的水解/缩合,精准调控其纳微结构,更为清晰地推测出构-效关系,是实现介孔SiO2纳微结构理性设计与构筑的重要前提,也是其进一步走向应用推广的必经之路.

