杂质铁对钛白性能的影响及机理分析
张 云,王 勇,杨 波
(1.河北奇正环境科技有限公司,河北 石家庄 050018;2.中国科学院过程工程研究所,北京 100190;3.河北煜泰热能科技有限公司,河北 辛集 052300;4.中国科学院过程工程研究所 南京绿色制造产业研究院,江苏 南京 211100)
0 引 言
二氧化钛(TiO2) 是一种重要的无机化工原料,对人体无毒、无害。当二氧化钛作为白色颜料时,被称为钛白。钛白是一种重要的白色颜料,占全部白色颜料使用量的80%。
TiO2作为白色颜料,具有极高的不透明度、优良的光学性能和颜料性质。因此,被广泛应用于涂料、油墨、塑料、橡胶、造纸、化纤和日用化妆品等领域。
目前,制备TiO2的原料主要为钛铁矿或富钛料(含高钛渣)。由于钛对氧元素的亲和力很强,使得铁、钒、镁、铝、铬、铅、铜、钴、铌、锆、锰、钙、硅、稀土等形成的物质均成为了这些矿物的伴生矿。
TiO2作为白色颜料,其中的杂质尤其是显色元素对其质量影响很大。因此,研究各种微量显色杂质元素对钛白产品性能的影响,以及制备高质量颜料级的TiO2产品都是十分必要的。
TiO2生产过程中常见的显色元素金属氧化物主要包括 Fe2O3、Cr2O3、MnO2、CuO、CoO。本文主要研究了重要杂质氧化物Fe2O3对钛白粉中TiO2的形貌、晶型转化和色度等方面的影响。
1 实验部分
1.1 实验材料
(1) 硫酸法偏钛酸:未盐处理,山东东佳集团生产。
(2) FeSO4·7H2O:分析纯,国药集团化学试剂有限公司生产。
1.2 实验仪器
(1)X射线衍射仪:XRD,X’Pert PRO MPD,Cu-Kα辐射,λ=1.542 A,工作电压为40 kV,工作电流为30 mA,扫描速率为2o/min ,扫描角度为10°~90°。
(2) 冷场发射扫描电子显微镜:FESEM,Hitachi S4800。
(3)X荧光光谱仪:XRF,Simultix12,日本理学。
(4) 色度计:WSD-3C 型,北京康光仪器厂生产。
1.3 实验方法
将不同量的金属氧化物Fe2O3掺杂于TiO2中,并进行煅烧,具体实验过程如下:
(1) 首先,将偏钛酸湿滤饼进行称重,按照湿滤饼中TiO2的含量(45%) 计算出滤饼中TiO2的质量。
(2) 将FeSO4·7H2O 配制成一定浓度的溶液。掺杂时,移取一定体积的上述溶液加入到偏钛酸中,再加入一定体积的蒸馏水,最终配制成浓度为300 g/L(以 TiO2计) 的浆液。
(3) 将浆液充分搅拌混合,20 min 后放入蒸发皿中,在105 ℃温度下进行干燥。
(4) 将干燥后的滤饼研磨,再置于瓷坩埚中,放入马弗炉,以10 ℃/min 的升温速度升至指定温度,并在恒定温度下煅烧一定时间。
(5) 煅烧结束后,打开马弗炉的炉门,使产品缓慢降温,待冷却后取出坩埚。
(6) 将得到的TiO2粉末混合、研磨,即可进行微观结构及性能分析。
1.4 分析方法
(1) 使用X射线衍射仪对钛白粉末晶型进行分析。
(2) 使用冷场发射扫描电子显微镜表征TiO2涂层的形貌。
(3) 使用X荧光光谱仪对钛白粉中含有的杂质元素的含量进行分析。
(4) 使用色度计对掺杂钛白粉色度进行测定。
2 结果与讨论
Fe2O3是TiO2颜料中重要的显色元素之一,既使含量很低的Fe2O3,也能使钛白粉的白度明显下降。通常要求金红石型TiO2颜料产品中Fe2O3的含量 <30 mg/L。
本文选取FeSO4作为Fe2O3的来源,将不同量的FeSO4加入到偏钛酸中,并在980 ℃下煅烧2 h后得到产品。
分别使用XRF、XRD 和色度计对产品进行分析,即可得到不同样品的Fe2O3含量、色度以及晶型组成,其结果见表1。

表1 Fe2O3 掺杂TiO2 产品的色度和金红石含量Table 1 Chroma and rutile content of Fe2O3 doped TiO2 products
由表1 可以得出以下结论。
(1) 随着Fe2O3加入量的逐渐增加,TiO2产品的明度指数L有小幅的升高。
(2) 黄相指数b随Fe2O3加入量的增加有非常显著的增大,这说明样品中的Fe2+在高温加热过程中生成了棕黄色的Fe3+,严重影响了产品的色相,导致产品发黄,使得其白度降低。
(3) 同时,由于Fe2O3的加入,也促进了产品晶型的转化。
Fe 掺杂 TiO2产品的 UV-vis-NIR 图谱如图 1所示。

图1 Fe 掺杂TiO2 样品的紫外可见漫反射光谱Fig.1 UV-Vis diffuse reflectance spectra of Fe doped TiO2 samples
由图1 中可以看出:随着Fe 掺杂量的增加,产品在可见光区的吸收增加,尤其是在近紫外的蓝光区(400~500 nm) 的吸收增加,所得产品表现出吸收光的补色,即产品黄相增强。
Fe 掺杂 TiO2过程可以用Kroger-Vink 符号方程表达为:
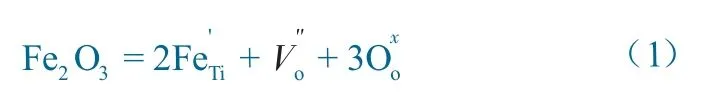
由式(1) 可以得出以下结论。
(1) Fe2O3可以增加TiO2晶格的氧空位数量,而TiO2表面形成的氧空位可以迅速迁移到TiO2内部,这种氧空位的流动性有利于金红石晶型在TiO2表面和内部的成核。
(2) 同时,在较高煅烧温度下产生了更多的氧空位,这些氧空位又增加了Fe3+在TiO2中的扩散,因此,Fe3+在TiO2中的溶解和扩散也促进了相的转化。
掺杂了Fe2O3的样品Fe-3 的XRD 图谱如图2所示。

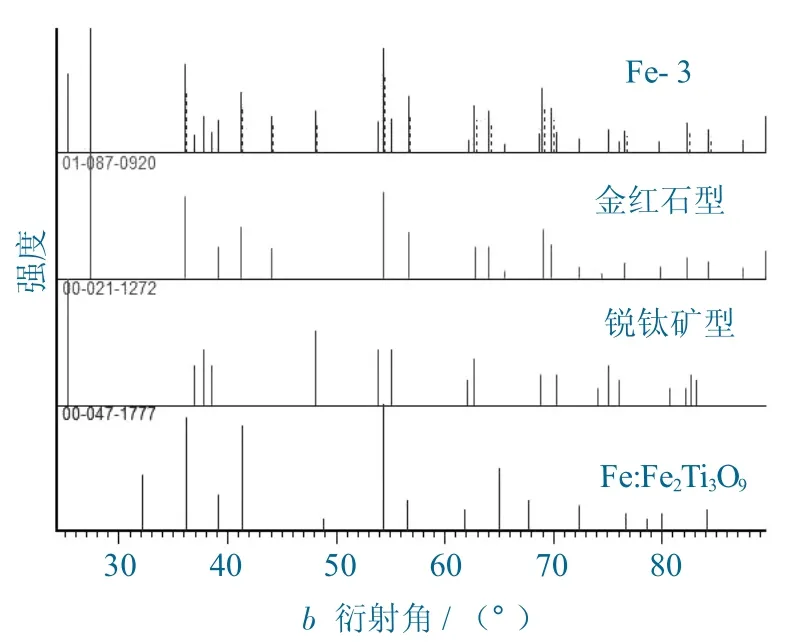
图 2 掺杂 Fe2O3 样品 Fe-3 的 XRD 光谱Fig.2 XRD spectra of Fe2O3 doped sample Fe-3
由图2(a) 中可以看出,产品Fe-3 是由金红石型(R,JSPD 01-087-0920) 和锐钛矿型(A,JSPD 00-021-1272) 2 种晶型的TiO2组成的,没有明显的钛酸铁的特征峰出现,这个结果和Gennari使用FeCl3掺杂得到的结果相同,XRD 谱图中也没有出现明显的钛酸铁晶体峰。
将钛酸铁的XRD 谱线图与图2(b) 样品谱线图进行对比,可以看出:钛酸铁(Fe2Ti3O9,JSPD 00-047-1777) 的标准谱线中在低角度的最强3 个峰 (衍射角=36.2o、41.5o和54.2 )o分别和金红石的峰重合或非常相近。
由此判断,当较多量的Fe2O3掺杂进入TiO2中时,一部分的Fe3+可以通过固相扩散进入到TiO2晶格内,而其他的Fe 可以和TiO2反应生成新相Fe2Ti3O9。
Fe 的掺杂可能会对钛白中TiO2的形貌产生影响。Iida 研究认为,Fe2O3的加入可以强烈的促进TiO2颗粒的生长,相反,Gennari 则认为Fe2O3的加入,对于TiO2的生长促进作用较弱。
Fe2O3的加入对于TiO2颗粒生长的影响如图3所示。


图3 样品Fe- 3 的SEMFig.3 SEMdiagram of sample Fe-3
由图中3 可以看出:Fe2O3的加入促进了颗粒间的烧结,从而促使颗粒长大,但仍有些较小的颗粒存在,样品的粒度分布不均匀。
3 结 语
本文系统研究了显色杂质Fe2O3对钛白粉中TiO2的晶型、形貌和色度的影响,得到以下结论。
(1) Fe3+的存在,增加了TiO2表面氧空位的数量,促进了锐钛矿型相金红石型的转化,当Fe掺杂量为1.8%时,煅烧后产生了新相Fe2Ti3O9。
(2) Fe 杂质的存在,促进了TiO2颗粒的烧结和长大,使产品粒度分布变宽。同时,Fe 杂质的存在,明显地升高了钛白粉的黄相指数,降低了钛白粉产品的白度。
——以金红石为例

