基于网络药理学分析门氏保元汤治疗过敏性紫癜的作用机制
程生辉,刘逸轩,姚帅君,门九章
(山西中医药大学,山西 晋中 030619)
过敏性紫癜是系统性IgA 免疫复合物介导的白细胞破碎性血管炎,临床特征主要为皮肤非血小板减少性紫癜、关节炎、胃肠道出血及肾炎等。发病机制为毛细血管变态反应和血管的自体免疫损伤[1]。门氏保元汤是门九章教授治疗过敏性疾病和自身免疫性疾病的常用方主方,由当归、金银花、元参、黄芪、炙甘草5 味药组成,以“扶正培元,标本兼顾”组方,针对过敏性紫气阴两虚、热瘀互结的病机特点,具有清热解毒、益气活血等功效,有着良好的临床效果[2-3]。
整合药理学是融合了中药学、药理学、计算机科学等多个学科的交叉学科,用以研究药物与机体的相互作用及作用原理[4]。通过中医药整合药理学平台(TCMIP,http:www.tcmip.cn),本研究对门氏保元汤治疗过敏性紫癜的机制进行了探究与分析,为阐释本方分子机制以及临床新药研发提供依据。
1 材料与方法
1.1 化学成分来源
在整合药理学平台(http://www.tcmip.cn/)中的中药材数据库,收集中药材当归、金银花、元参、黄芪、甘草所含有的化学成分,建立门氏保元汤的化学成分数据库。
1.2 候选靶基因预测
通过整合药理学平台“整合药理学分析工具”采取化学成分二维结构相似性搜索,即采用MACCS 分子指纹特征提取方法和Tani-moto 系数定义的相似度计量方法,针对中药化学成分和美国食品药品监督管理局上市药物进行相似性打分,从而获取高可信度(相似度>0.8)的中药候选靶点谱,在平台“中药成分数据库”版块分别输入当归、金银花、元参、黄芪、炙甘草,即可获得不同的药物的化学成分信息,并可提取不同成分对应靶点信息。
整合药理学平台TCMIP 平台依托“人类表型本体数据库(HPO)”“Drugbank 数据库”“基因相关性数据库(DisGeNET)”“治疗靶点数据库(TTD)”等资源,构建疾病和常见临床表型相关基因数据库。在平台“疾病相关分子集及其功能挖掘”板块以“allergic purpura”为疾病或症状进行检索,提取检索出来的所有治疗靶点。
1.3 关联网络挖掘与分析
TCMIP 平台整合了蛋白互作数据库(Database of Interacting Protein,DIP)、分子交互数据库(molecular interaction Database,MINT)人类蛋白质参考数据库(Human Protein Reference Database,HPRD)、反应途径数据库(Reactome Pathway Database,Reactome)等8 个现有的蛋白相互作用网络数据库的信息,通过整合药理学平台的蛋白相互作用网络构建门氏保元汤的潜在作用靶点-过敏性紫癜疾病靶点的蛋白相互作用网络。通过整合药理学平台网络分析模块,计算靶点之间的PPI 网络特征值,以“节点连接度(degree)”的2 倍中位数为卡值,选取中药靶点-疾病基因网络的核心节点(hubs);并且在此基础上,以“节点连接度(degree)”“节点紧密度(closeness)”和“节点介度(betweenness)”的中位数为卡值,选取满足3 个卡值的节点为关键靶点网络,而后对关键靶点网络进行富集分析,选取P 值前20 的通路,构建“中药-成分-靶点-通路”的多维关系网络,并对其进行可视化分析。
TCMIP 基于基因本体数据库(gene ontology,GO)和京都基因和基因组数据库(kyoto Encyclopedia of genes and genomes,KEGG),确定药物靶点所参与的生物学反应和通路。结合富集计算,获得门氏保元汤及其治疗过敏性紫癜关键网络靶点的生物学功能及其所参与的网络通路。按P 值大小取前20 个GO 及KEGG 分析结果。
2 结果
2.1 门氏保元汤的化学成分分析及靶标预测
门氏保元汤共收集化学成分301 个,化合物主要为黄酮类、三萜类和有机酸类等。当归收集到的成分有66 个,主要为有机酸类和挥发油化合物;元参收集到的成分有30 个,主要为环烯醚萜苷、苯丙素苷类化合物;金银花共收集化学成分47 个,主要为有机酸类、黄酮类、挥发油类化合物;黄芪共收集化学成分27 个,主要为三萜皂苷类、黄酮类化合物;甘草共收集化学成分131 个,主要为三萜类、黄酮类化合物。当归的60 个化学成分共预测出251 个靶标,元参中30 个化学成分共预测出73 个靶标,金银花中47 个化学成分共预测出133 个靶标,黄芪中27 个成分共预测出249 个靶标,甘草中131 个化学成分共预测出184个靶标。
对中药方剂候选靶标进行功能分析(表1),可见候选靶标基因功能涉及辅因子代谢、四氢叶酸互变、一氧化氮合酶合成、肽基-丝氨酸磷酸化调节等条目。对中药方剂候选靶标进行通路富集分析(表2),可见涉及通路有四氢蝶呤合成、叶酸和嘌呤代谢、细胞内受体的类泛素化、核受体转录途径等通路。
2.2 门氏保元汤治疗过敏性紫癜的核心靶标网络、基因功能和通路富集分析
通过整合药理学平台的网络分析模块,构建了门氏保元汤潜在靶点与疾病靶点相互作用网络。根据上述条件共获得62 个靶点并筛选出25个关键靶点(表5),采用PPI 模块构建了“药物-疾病核心靶点”网络(图1),图中节点的大小与degree 呈正比。
GO 和KEGG 富集分析结果显示,门氏保元汤对过敏性紫癜的干预机制涉及B 细胞增殖、一氧化氮生物合成过程、辅因子代谢过程、血小板聚集、细胞因子介导的信号通路等多个条目(表3)。通路富集分析结果显示主要集中在NF-κB 信号通路异常导致免疫缺陷、血小板聚集、四氢蝶呤合成、内皮型一氧化氮合酶激活、BRAF 的异常转导以及BRAF 对RAF 激酶的异常激活等通路(表4)。
2.3 门氏保元汤治疗过敏性紫癜的“中药-成分-靶标-通路”多维网络分析

表1 门氏保元汤候选靶点功能信息

表2 门氏保元汤候选靶点参与的通路信息

表3 门氏保元汤治疗过敏性紫癜靶点生物过程富集分析
涉及到的通路主要有NF-κB 信号通路、血小板聚集、四氢蝶呤合成、内皮型一氧化氮合酶激活、BRAF 编码RAF 激酶等通路。从候选靶标网络与“药物-化学成分-靶标-通路”网络图(图2),认为门氏保元汤对过敏性紫癜的干预作用与血小板代谢、NF-κB 信号通路以及BRAF 编码RAF 激酶等有关。

表4 门氏保元汤治疗过敏性紫癜靶点通路富集分析

表5 门氏保元汤治疗过敏性紫癜关键靶点
3 讨论
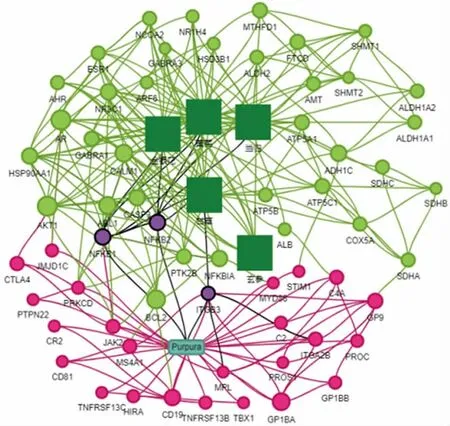
图1 门氏保元汤治疗过敏性紫癜靶点网络
门氏保元汤由当归、金银花、元参、黄芪、炙甘草组成,黄芪多糖可以显著增加胸腺和脾内T 细胞的数量,进而促进IgG 的生成,从而提高机体的免疫功能;抑制血小板相关抗体,减少血小板的损伤与破坏[5]。黄芪甲苷、黄芪黄酮等能使血管的通透性得到改善,使毛细血管对损伤的抵抗力增强,使出血的风险得到降低[6]。当归有机酸具有抑制抗血小板凝聚的作用,当归多糖具有升高血小板和刺激骨髓造血的功能[7]。元参苯丙素苷能减少血管炎症,元参环烯醚萜苷能有效抑制血小板聚集[8]。金银花有机酸类化合物有抗血小板凝聚和保护内皮细胞过氧化损伤的作用[9]。甘草中的甘草皂苷和甘草黄酮类能抑制致炎性因子,有明显的抗变态反应作用[10]。

图2 门氏保元汤治疗过敏性紫癜“中药-成分-核心靶点-通路”多维网络关系
经过富集分析得出,门氏保元汤治疗过敏性紫癜与NF-κB 信号通路、内皮型一氧化氮合酶激活、血小板代谢以及BRAF 编码RAF 激酶有着密切的关系。研究发现NF-κB 是一种由两个亚单位(P50 和P65)组成的二聚体[11]。由于NF-κB 参与多种蛋白基因转录,且与T 细胞的活化密切相关[12]。T 细胞过度激活是过敏性紫癜发病的机制之一,有研究认为黄芪能抑制NF-κB 的活性,从而减少T 细胞的过度活化[13]。NO 是具有免疫调节作用的小分子,可调节血管张力及血流速度,防止血小板黏附和血栓形成[14]。研究表明,黄芪多糖能激活被抑制的AMPK-eNOS 通路,进而保护血管内皮细胞[15]。当归能够对血小板聚集产生明显的抑制作用,也可以提高已聚集血小板的解聚率[16],从而对过敏性紫癜起到一定的治疗作用。血小板膜糖蛋白(ITGA2B)是一类与血小板凝聚有关的蛋白,这类蛋白主要参与出血与凝血过程,并发挥着重要的作用。对于HSP 患儿来说,其自身的血小板聚集功能加强,因而存在血液的高凝状态甚至会形成微血栓。ITGA2B 含量的增加是导致血小板凝聚、微血栓形成的关键原因[17]。而当归有机酸、金银花有机酸、元参环烯醚萜苷有抗血小板凝聚的作用,能降低细胞内ITGA2B 的水平,从而对过敏性紫癜起到治疗作用。有研究报道,BRAF 基因编码RAF 家族蛋白激酶,该蛋白在调节MAPK-ErK 信号通路中起重要作用,影响细胞分裂,分化和分泌;并且影响着肿瘤的产生及进展,有着生长、增殖甚至是凋亡细胞的作用[18-19]。有研究发现可通过活化MAPK/Erk 信号通路,对糖尿病血管病变中起到抑制作用[20],另有研究发现白芷提取物可能通过增加NO 和TNF-α 产物,激活MAPK 通路发挥免疫调节作用,进而抑制大肠癌瘤体的增长[21]。潘耀谦等[22]研究发现Erk 信号转导通路通过强大的级联反应参与了家兔脑炎原虫性脑肉芽肿的形成,在脑肉芽肿形成过程中促进星形胶质细胞、血管内皮细胞和成纤维细胞增殖。
综上所述,本研究借助整合药理学这一新兴学科理念及技术,对门氏保元汤治疗过敏性紫癜的作用机制及药效物质基础进行分析,既为该方未来的进一步研究提供理论依据,也为过敏性紫癜的临床治疗提供更加开阔的思路。

