新型杀螨剂丁氟螨酯的特性及在柑橘上的应用
姚周麟 吴韶辉 平新亮 林媚
(浙江省柑橘研究所台州 318026)
丁氟螨酯(cyflumetofen),化学名 2-methoxyethyl(RS)- 2-( 4-tert-butylphenyl)- 2-cyano- 3-oxo- 3-( 2-trifluor omethylphenyl)propanoate,是由日本大冢化学公司开发的新型酰基乙腈类手性杀螨剂,2007年首次在日本获准登记并销售,用于果树、蔬菜、茶树等农作物和花卉主要螨类[1]的防治。丁氟螨酯可抑制害螨的线粒体复合体II,其去酯化代谢产物(螨的主要代谢产物AB- 1)能以极低的浓度抑制线粒体复合物II[2],对螨类具有长效的持久控制能力[3],其对若螨的活性更高,对昆虫、甲壳类动物或脊椎动物则比较安全[2],与现有的多数杀螨剂无交互抗性[4]。丁氟螨酯不能与碱性农药混合使用,无内吸性,主要通过触杀起效,药剂处理的成虫在24 h内瘫痪[5],同时具有一定的杀卵活性。
1 丁氟螨酯的合成及结构确证
丁氟螨酯的合成工艺研究报道,有以下对叔丁基苯乙腈为原料,经酯化、酯交换得到中间体 2-( 4-叔丁基苯基)-氰基乙酸( 2-甲氧基)乙基酯( I);邻三氟甲基氯苯发生格氏反应后,通入二氧化碳得到邻三氟甲基苯甲酸,经氯化亚砜氯化得到中间体邻三氟甲基苯甲酰氯(II)。中间体 2-( 4-叔丁基苯基)-氰基乙酸( 2-甲氧基)乙基酯( I)在碳酸钠催化下与中间体邻三氟甲基苯甲酰氯(II)在相转移催化下得到目的产物丁氟螨酯,总收率43.1%(以对叔丁基苯乙腈计)。何丽英等[7]以对叔丁基苯乙腈为起始原料,经亲核取代和酯交换反应得到丁氟螨酯,其结构经气相色谱/质谱(LC/MS)、核磁共振(1HNMR)确证。在优化条件下,合成总收率达50%。李爱军等[8]以对叔丁基氯苄为原料经氰化、缩合、酯交换、酰化反应合成丁氟螨酯。在优化的反应条件下,反应总收率60.3%(以对叔丁基氯苄计),含量98.2%。收率高、操作简便、产品纯度高,该方法适合工业化生产。
丁氟螨酯的化学结构如图1,何丽英等经液-质联用、1HNMR对其结构进行确证[7]。张一鸣等[9]对其红外吸收光谱(IR)、紫外吸收光谱(UV)、质谱(MS)及核磁共振波谱(包括1HNMR、13C NMRDEPT、1H-1HCOSY、1H-13CHSQC、1H-13CHMBC)进行了测定,明确了其UV和IR谱图特征吸收峰对应的基团,并对其1H和13CNMR信号进行了归属,确证了丁氟螨酯的结构。
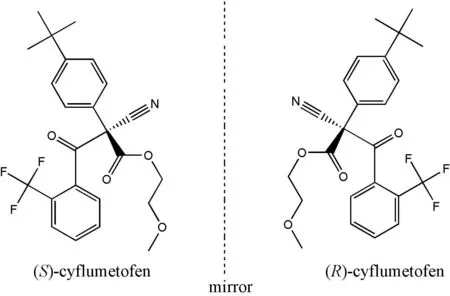
图1 丁氟螨酯(对映体)结构
2 丁氟螨酯的检测方法
2.1 丁氟螨酯的外消旋检测方法
丁氟螨酯的外消旋检测方法有液相色谱法(HPLC)、液-质联用法(HPLC-MS)和气-质联用法等。陈建波等[5]采用高效液相色谱法测定20%丁氟螨酯悬浮剂中有效成分质量分数,Kromasil C18色谱柱(200mm× 4.6mm,粒径 5μ m),流动相为乙腈+水,检测波长220nm。在20~500mg/L范围内,线性相关系数达 0.9999,方法相对标准偏差为 0.82%,平均添加回收率为99.8%。李敏敏等[10]建立了农产品、水及土壤中丁氟螨酯及其代谢产物的超高效液相色谱串联质谱(UPLC-MS)残留分析方法。前处理样品经乙腈:水( 9: 1)提取、10mg多壁碳纳米管净化,m/z448>173、m/z189>145、m/z190>173定量。在0.005~ 1.0mg/kg的浓度范围内,相关系数在 0.9977以上。LODs范围是 0.2~ 3.0mg/kg,LOQs范围是 0.7~ 9.8mg/kg。赵来成[11]和王磊[12]均建立了超高效液相色谱-质谱/质谱法(UPLC-MS/MS)检测草莓中丁氟螨酯残留分析方法。前处理样品采用乙腈提取,QuEChERS净化,在 2~100μg/L浓度范围内,线性 R2= 0.9999,回收率在82%~102%,相对标准偏差<10%,方法的检出限为 1μ g/kg。Minmin Li等[13]建立了气相色谱质谱联用法测定水、土壤和水果中的丁氟螨酯残留,用乙腈萃取,基质匹配标准在三个浓度水平( 0.05、 0.5和 1.0mg/kg)下,总体平均回收率在76.3%~101.5%之间,相对标准偏差在1.2%~11.8%之间(n= 5),计算得出的检出限和定量限低于 0.005和 0.015g/kg。MinminLi等[14]开发了将多壁碳纳米管用于分散固相萃取结合超高效液相色谱-串联质谱同时测定动植物来源样品中丁氟螨酯及其主要代谢产物残留方法,采用正负离子切换模式, 4min即可完成检测。平均回收率为79.3%~117.6%,相对标准偏差低于 7.6%,LOQs范围是 0.7~ 9.8μ g/kg。
2.2 丁氟螨酯的手性检测方法
丁氟螨酯的手性检测方法研究较少,Xiu Chen等[15]用高效液相色谱法在黄瓜,番茄和苹果中手性测定了丁氟螨酯对映体。在25℃的Chiralpak AD-H色谱柱上,以正己烷和 2-丙醇(95: 5,v/v)的混合物作为流动相,在 1.0mL/min的流速下检测到出色的分离234nm。对映体的拆分度高达 5.5。对映体的LOQ在黄瓜和番茄中为 0.5mg/kg,在苹果中为 0.33mg/kg,回收率在71.4%~102.0%,RSD值均低于14.8%。对映体的洗脱顺序由在线OR-2090检测器在相同的色谱条件下确定,第一个洗脱的是(-)-丁氟螨酯,第二个洗脱的为(+)-丁氟螨酯。Na Liu等[16]和Guo等[17]均建立了一种超高效合相色谱串联三重四极杆质谱(UPC 2–MS/MS)对土壤中丁氟螨酯对映异构体手性拆分的方法 。 色谱 柱 AMY 1(150mm× 2.1mmi.d.,2.5μ m)即直链淀粉-三( 3, 5-二甲基苯基氨基甲酸酯),背压2000psi,柱温40℃,流动相组成CO2/异丙醇(96.5: 3.5,v/v),两个对映体在土壤中的LOQs分别为 9.45和15.79μ g/kg。各对映体的回收率在78.3%~119.9%之间,相对标准偏差低于14.0%。
3 丁氟螨酯在柑橘上的应用效果
丁氟螨酯具有较好的速效性和持效性,同时对柑橘安全。柑橘全爪螨是重要的柑橘害虫之一,对多种化学农药已产生抗性,王彦博等[18]采用改进浸叶法对柑橘全爪螨雌成螨进行了室内毒力测定,并开展了田间药效试验,表明丁氟螨酯对柑橘全爪螨( 4.645mg/L)具有速效性好且持效期长,曹相余等[19]也得出同样结果。
丁氟螨酯对多数杀螨剂无交互抗性。丁氟螨酯对叶螨属和全爪螨具有很高的活性,但对鳞翅目、同翅目和缨翅目害虫几乎无活性。该药剂对叶螨各发育阶段的螨均有较好的活性,且对幼螨的防效远高于成螨。蒲占湑[1]和杨国璋[20]均发现,该药剂与其他杀螨剂无交互抗性,对已产生抗性的螨类防治效果显著,可与现有杀螨发现剂轮换使用,更经济有效地防治柑橘全爪螨。
丁氟螨酯与结构类似的药剂可产生交互耐药风险。Wang等[21]研究朱砂叶螨对丁氟螨酯的敏感性和耐药性,发现其最终耐药率达到21.33%。Khalighi[22]研究指出,丁氟螨酯和腈吡螨酯对一系列特征明确的耐弧菌Tetranychus urticae 有交叉耐药风险,协同实验也表明 P450单加氧酶与耐药有关。Feng等[23]选择了两个对丁氟螨酯具有抗药性的螨虫种群(CyR和YN-CyR)持续进行了104和12代的研究,分别产生了104.7倍和25.6倍的耐药性。同时,交叉抗药性研究表明,丁氟螨酯与其他四种杀螨剂(阿维菌素,甲氰菊酯,克螨特和联苯肼酯)之间没有交叉抗性,但对哒螨灵的交叉抗性达到了63.8倍的高水平。Zhang等[23]发现一个microRNA- 1基因片段tci-miR-1- 3 p通过朱砂叶螨中靶向谷胱甘肽 S-转移酶参与了螨对丁氟螨酯的抗药性,其中TCGSTM 4是负责螨对丁氟螨酯抵抗的功能基因。
丁氟螨酯可与其他药剂复配,产生更好的防治效果。田亚等[24]采用共毒因子法、共毒系数法对丁氟螨酯和伊维菌素复配的最佳配比进行筛选,并进行田间防效试验。当伊维茵素:丁氟螨酯为 1: 1时,防效最佳。
4 丁氟螨酯的代谢及环境行为
丁氟螨酯在环境中的主要代谢物为 2-(三氟甲基)苯甲酸(B- 1)和 2-(三氟甲基)苯甲酰胺(B- 3)。不同环境条件和土壤类型对丁氟螨酯半衰期有显著影响。在有氧环境下,丁氟螨酯在四种类型的土壤(黑土、灰钙土、红壤和潮土)的半衰期分别为11.2、10.3、12.4和11.4 d;在无氧条件下,这四类土壤半衰期分别为13.1、10.8、13.9和12.8d。丁氟螨酯在水中的半衰期与pH值之间有很强的相关性。在有氧环境下,丁氟螨酯在三种类型的水(东北湖,湖南稻田和北京上庄水库)中的半衰期分别为15.4、16.9和15.1 d,厌 氧条件 下为16.5、17.3和16.1 d[25]。20%丁氟螨酯SC以最高推荐使用量和 1.5倍最高推荐使用量对草莓各施药 1次和 2次。草莓果实上原始沉积量为0.5882mg/kg,半衰期为 9.364 d[26]。采用风险商方法进行评估,不同施药浓度、施药次数下丁氟螨酯用药后 1~21 d的草莓对 2~ 4岁、18~30岁和60~70岁人群的风险均较低(风险商为 0.001~ 0.020)。
不同的环境条件对于丁氟螨酯对映体的代谢反应不同。Liu等[16]研究了温室条件下丁氟螨酯两个对映在土壤中的半衰期分别为12.2和13.6 d,具有选择性。而Sun等[27]认为露地条件下,(-)-丁氟螨酯和(+)-丁氟螨酯在土壤中的半衰期分别为 6.37 d和6.99 d,两对映体几乎无选择性。同时Sun等[27]研究表明,(-)-丁氟螨酯和(+)-丁氟螨酯在柑橘中的半衰期分别为16.5 d和19.8d ,发生了选择性降解。郭静等[17]在 5倍施用剂量下,(-)-丁氟螨酯和(+)-丁氟螨酯在苹果中的半衰期分别为22.13 d和22.23 d, 1.5倍的剂量,各对映体的半衰期分别为22.42 d和23.64 d。在高浓度、低浓度丁氟螨酯悬浮液喷施条件下,苹果中丁氟螨酯两个对映体的降解趋势基本保持一致[4],无选择性。
5 丁氟螨酯的安全性
丁氟螨酯[28]可作为线粒体电子传输链复合物II的抑制剂,其去酯化代谢产物抑制力更强,可抑制包括对大多数农药产生抗性的二斑叶螨。丁氟螨酯及其去酯化代谢物都是TuGSTd 05结合的潜在底物,同时 Y107和N 103等几种氨基酸参与了相互作用。丁氟螨酯可通过氧化损伤、激活 P38蛋白和JNK蛋白诱导人经神经母细胞瘤细胞SH-SY 5 Y细胞 G 1期阻滞和凋亡[29]。Toshinori Yoshi-da 1等[30]通过在10只雄性和10只雌性大鼠饲料中按10、10、300、1000和3000ppm丁氟螨酯的剂量水平90 d重复口服毒性研究,根据实验结果,丁氟螨酯的无可见有害作用水平(NOAEL)判定为雄性和雌性大鼠均口服300ppm的添加剂量(雄性为16.5mg/kg· d,雌性为 19.0mg/kg· d)。使用 MTT,LDH,ROS,MDA,SOD和CAT的指标评估丁氟螨酯对映异构体对HepG2细胞的对映选择性细胞毒性和氧化应激,观察到剂量和结构形式依赖性现象,毒性顺序为(-)-丁氟螨酯>rac-丁氟螨酯>(+)-丁氟螨酯。尽管有相似的环境降解行为,CYF对映异构体的毒性仍显示出很大差异,基于安全考虑,(+)-丁氟螨酯可被开发为rac-丁氟螨酯的潜在替代品[27]。

