PD-1/PD-L1免疫检查点抑制剂联合化疗治疗非小细胞肺癌的临床观察
蒋轶 王志 左宏波

【摘要】 目的:探討程序性死亡因子(PD-1)/程序性死亡因子配体1(PD-L1)免疫检查点抑制剂联合化疗治疗非小细胞肺癌(non-small cell lung cancer,NSCLC)的临床效果。方法:选取2015年6月-2017年6月本院收治的84例NSCLC患者,根据随机数字表法将其分为观察组和对照组,每组42例。对照组采用顺铂联合吉西他滨治疗,观察组在对照组的基础上加用帕博利珠单抗。比较两组治疗效果、生存情况及毒副反应发生情况。结果:观察组治疗总有效率为85.71%,高于对照组的59.52%,差异有统计学意义(P<0.05)。观察组随访1、2、3年的生存率分别为90.48%、66.67%、47.62%,均高于对照组的57.14%、42.86%、16.67%,差异均有统计学意义(P<0.05)。观察组毒副反应发生率为9.52%,低于对照组28.57%,差异有统计学意义(P<0.05)。结论:NSCLC患者治疗方案采用PD-1/PD-L1免疫检查点抑制剂联合化疗能够增强治疗效果,生存率高,不良反应较少,预后更好。
【关键词】 非小细胞肺癌 程序性死亡因子 程序性死亡因子配体1 免疫检查点抑制剂 化疗
Clinical Observation of PD-1/PD-L1 Immune Checkpoint Inhibitor Combined with Chemotherapy in the Treatment of Non-Small Cell Lung Cancer/JIANG Yi, WANG Zhi, ZUO Hongbo. //Medical Innovation of China, 2021, 18(24): 051-054
[Abstract] Objective: To investigate the clinical application effect of programmed death factor (PD-1)/programmed death factor ligand 1 (PD-L1) immune checkpoint inhibitor combined with chemotherapy in the treatment of non-small cell lung cancer (NSCLC). Method: A total of 84 NSCLC patients admitted to our hospital from June 2015 to June 2017 were selected, and they were divided into observation group and control group according to the random number table method, 42 cases in each group. The control group was treated with Cisplatin combined with Gemcitabine, and the observation group was treated with Pembrolizumab on the basis of the control group. The therapeutic effect, survival situation and the occurrence of toxic reactions were compared between two groups. Result: The total effective rate of the observation group was 85.71%, which was higher than 59.52% of the control group, the difference was statistically significant (P<0.05). The survival rates of the observation group after 1, 2 and 3 years of follow-up were 90.48%, 66.67% and 47.62%, respectively, which were higher than 57.14%, 42.86% and 16.67% of the control group, the differences were statistically significant (P<0.05). The occurrence of toxic reactions of the observation group was 9.52%, which was lower than 28.57% of the control group, the difference was statistically significant (P<0.05). Conclusion: The treatment of NSCLC patients with PD-1/PD-L1 immune checkpoint inhibitor combined with chemotherapy can enhance the therapeutic effect, with a high survival rate, fewer adverse reactions and better prognosis.
[Key words] Non-small cell lung cancer Programmed death factor Programmed death factor ligand 1 Immune checkpoint inhibitor Chemotherapy
First-author’s address: The First People’s Hospital of Jiujiang City, Jiujiang 332000, China
doi:10.3969/j.issn.1674-4985.2021.24.013
癌症是威胁人类生命的重要疾病,肺癌占所有癌症的30%,且随着诊断技术发展,肺癌的检出率越来越高,其发病率、病死率均位居首位,预后较差[1]。肺部恶性病变中80%以上为非小细胞肺癌(NSCLC),虽然临床对该疾病有了更深认识,但其病死率仍居首位,对于早期确诊患者手术治疗效果较好,通过切除病灶,避免癌细胞扩散,延长生存时间为治疗目标[2-3]。NSCLC患者错失手术机会后,若治疗不及时或治疗方法不当,易导致病情快速进展,使得患者预后较差,为患者及其家庭带来沉重负担。NSCLC治疗多选择放化疗,治疗后患者病情有所改善,但因病情进展快速,整体效果不佳,因此急需寻找更为有效的治疗方案。近些年临床对该疾病已有新的认识,新型药物也逐渐用于临床,使得治疗效果得到提高,但放化疗对延长患者生存时间无明显作用[4]。免疫治疗的出现使得NSCLC获得了新的治疗方向,尤其以程序性死亡因子(PD-1)/程序性死亡因子配体1
(PD-L1)免疫检查点抑制剂效果突出[5]。鉴于此,本研究进一步分析PD-1/PD-L1免疫检查点抑制剂联合化疗治疗NSCLC的临床效果,现报道如下。
1 资料与方法
1.1 一般资料 选取2015年6月-2017年6月本院收治的84例NSCLC患者。纳入标准:(1)均经病理学、影像学、临床表现体征等确诊;(2)首次发病;(3)无自身免疫性疾病;(4)依从性较好。排除标准:(1)合并全身感染;(2)已出现脑转移;(3)预计生存期<6个月;(4)合并其他恶性肿瘤;(5)合并其他脏器衰竭。根据随机数字表法分为对照组和观察组,每组42例。本研究已经医院伦理学委员会批准,患者均知情同意。
1.2 方法 对照组行顺铂(生产厂家:江苏豪森药业集团有限公司,批准文号:国药准字H20040813,规格:6 mL︰30 mg)+吉西他滨(生产厂家:江苏豪森药业集团有限公司,批准文号:国药准字H20030104,规格:0.2 g)化疗,第1天予以75 mg/m2
顺铂+0.9%氯化钠溶液500 mL,静脉滴注;第1、8天予以1 250 mg/m2吉西他滨+0.9%氯化钠溶液100 mL,静脉滴注。基于此,观察组加用PD-1/PD-L1免疫检查点抑制剂[帕博利珠单抗,生产厂家:Merck Sharp & Dohme Corp., a subsidiary of Merck & Co., Inc.,批准文号:S20180019,规格:100 mg/4 mL)治疗,帕博利珠单抗2 mg/kg,静脉输注,每3周给药一次。两组均21 d为一个周期,连续治疗,若病情进展或出现无法忍受的毒副反应时停止。
1.3 观察指标与判定标准 (1)比较两组疗效。治疗3个周期后评估疗效,疗效参照实体瘤疗效标准划分:病灶完全消失为完全缓解;病灶最大径减少≥30%为部分缓解;病灶减少<30%,或增加≤20%为稳定;病灶增加>20%为进展[6]。总有效=完全缓解+部分缓解+稳定。(2)比较两组生存情况。通过电话、门诊复查等方法对所有患者进行随访,统计1、2、3年生存率。(3)比较两组毒副反应发生情况。记录两组治疗期间白细胞减少、呕吐、皮疹、血小板减少等发生情况。
1.4 统计学处理 采用SPSS 22.0软件对所得数据进行统计分析,计量资料用(x±s)表示,比较采用t检验;计数资料以率(%)表示,比较采用字2检验。以P<0.05为差异有统计学意义。
2 结果
2.1 两组一般资料比较 观察组男25例,女17例;年龄58~81岁,平均(68.47±5.54)岁;体重45~84 kg,平均(64.19±5.49)kg;病理分型:腺癌27例,鳞癌15例。对照组男24例,女18例;年龄57~82岁,平均(68.94±5.76)岁;体重45~82 kg,平均(64.76±5.89)kg;病理分型:腺癌26例,鳞癌16例。两组一般资料比较,差异均无统计学意义(P>0.05),具有可比性。
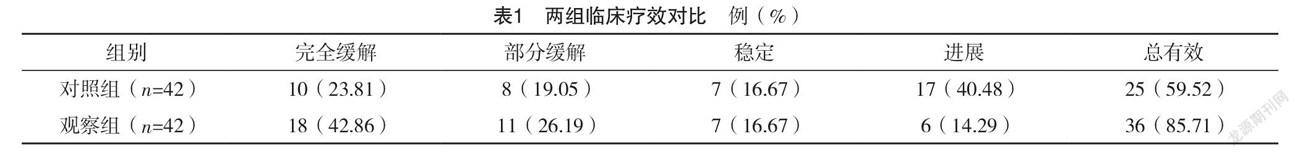
2.2 两组临床疗效比较 观察组治疗总有效率为85.71%,高于对照组的59.52%,差异有统计学意义(字2=7.245,P<0.05),见表1。
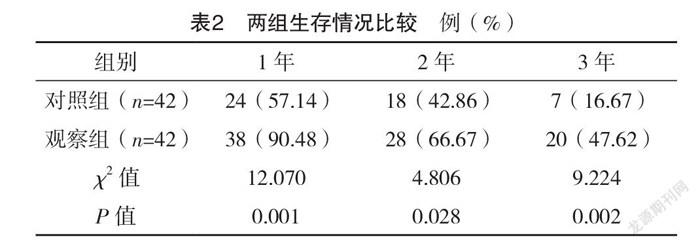
2.3 两组生存情况比较 观察组随访1、2、3年的生存率分别为90.48%、66.67%、47.62%,均高于对照组的57.14%、42.86%、16.67%,差异均有统计学意义(P<0.05),见表2。
2.4 两组毒副反应发生情况比较 观察组毒副反应发生率为9.52%,低于对照组的28.57%,差异有统计学意义(字2=4.941,P<0.05),見表3。
3 讨论
NSCLC是一种常见的肺部恶性病变,发病机制较为复杂,具体原因至今未明,肿瘤发生发展、转移等受多方因素影响,临床认为可能与环境、遗传、营养状况、免疫等相关[7-8]。临床控制疾病的关键在于抑制癌细胞分裂与增殖,但NSCLC发病初期缺乏特异性表现,个别患者常常忽视,往往确诊时已处于中晚期,无法进行手术治疗,对于错失手术的患者,治疗多选择放化疗,对患者症状进行缓解,缩小病灶,达到较好的治疗效果[9-10]。NSCLC患者常规化疗所需周期长,毒副反应多,而该病本身极易反复、转移,导致治疗效果不理想,化疗引发的毒副反应较为严重,加重患者心理负担,产生抵触情绪,甚至因无法耐受毒副反应而终止治疗,导致预后极差。
顺铂+长春瑞滨为临床化疗的常见方案,在各肿瘤治疗中均获得较好效果,短期疗效已获得认可,但NSCLC疗程较长,长期使用顺铂+长春瑞滨治疗,弊端逐渐显现[11-12]。因化疗药物毒性较大,在杀伤肿瘤细胞的同时,还会对机体正常细胞造成影响,诱导癌细胞免疫原性死亡,释放肿瘤相关抗原及损伤相关分子模式,使树突状细胞活化,改变机体免疫环境,使免疫抑制性细胞生成减少;另外还会诱发严重的毒副反应,部分患者因无法耐受不得不终止治疗,对患者身心均造成重创,预后较差[13-14]。刘克元[15]研究显示,肺癌根治术后应用以铂类为主的不同化疗方案均有一定效果,但不良反应均较多,临床可根据患者体质选择更为适合的应用方案,以保证治疗效果与安全性,由此可见以铂类为主的化疗方案安全性并不理想。目前临床治疗NSCLC在含铂类药物化疗基础上已成为巨大变化,临床正在积极寻找更加安全、高效的治疗方法。PD-1/PD-L1抗体已被临床广泛应用,在多种恶性疾病中均发挥出较好的治疗作用,已成为临床重要的辅助手段[16-17]。本研究结果显示,观察组随访1、2、3年的生存率分别为90.48%、66.67%、47.62%,均高于对照组的57.14%、42.86%、16.67%,差异均有统计学意义(P<0.05)。观察组毒副反应发生率为9.52%,低于对照组的28.57%,差异有统计学意义(P<0.05)。表明与单纯化疗方案相比,PD-1/PD-L1免疫检查点抑制剂联合化疗治疗NSCLC效果更好,不良反应少,且短中期生存率较高,利于改善患者预后。吕厚宽等[18]研究显示,PD-1/PD-L1抑制剂治疗效果确切,安全性较好,可使一线化疗方案失败或复发的晚期NSCLC患者获益,进一步佐证PD-1/PD-L1抑制剂的有效性与安全性,具有较为广阔的应用前景。
分析其原因为,PD-1为人免疫球蛋白,能够特异性结合人体PD-1,使PD-1与PD-L1、PD-L2配体相互作用,是一种新的治疗癌症的靶制剂,临床治疗优势突出,已取得较为理想的治疗效果[19]。PD-1/PD-L1是目前临床免疫检查点抑制剂应用最为广泛的一个,为治疗NSCLC提供了新的方向,已成为二线治疗方案,并将PD-L1作为判断疗效的标志物,且PD-1/PD-L1抑制剂不会引起明显的不良反应,即使出现不良反应,使用糖皮质激素治疗能够较好控制,临床处理毒副反应应遵循早发现、早治疗,尽快控制不良反应,避免影响治疗进程,使得用药安全性得到保障,具有较好的应用前景[20]。但本研究因随访时间短、纳入样本少使其仍存在一定局限性,未来需扩大样本量、延长随访时间,观察对患者长期生存率的影响。
综上所述,NSCLC患者治疗方案采用PD-1/PD-L1免疫检查点抑制剂联合化疗能够增强治疗效果,生存率高,不良反应较少,预后更好,可作为患者优先选择方案。
参考文献
[1]陈丽娥,王识华,洪湘,等.非小细胞肺癌患者PD-L1表达水平与临床病理特征及细胞免疫的关系[J].中国医师杂志,2020,22(8):1266-1268.
[2]易军,万保林,张芳芳.同步加量调强放疗联合化疗治疗局部晚期非小细胞肺癌的临床效果[J].中国医学创新,2017,14(27):27-30.
[3]史芳.康莱特注射液联合化疗治疗NSCLC的效果及对癌因性疲乏、血清肿瘤标记物和预后的影响[J].中国医学创新,2019,16(36):40-44.
[4]郭志强,钱正宇,米小芳,等.PD-L1在非小细胞肺癌中的表达及意义[J].山西医科大学学报,2018,49(6):17-20.
[5]李婷,刘金燕,刘朝俊,等.PD-1在非小细胞肺癌肿瘤细胞表达水平及预后的临床意义[J].郑州大学学报(医学版),2020,55(3):343-347.
[6]杨学宁,吴一龙.实体瘤治疗疗效评价标准-RECIST[J].循证医学,2004,4(2):85-90.
[7]王淑冰,伍全概,郭予武,等.西妥昔单抗联合NP方案治疗晚期非小细胞肺癌的疗效及其对患者免疫功能的影响[J].海南医学,2019,30(9):21-24.
[8]朱蓓,方亮,王营营.非小细胞肺癌患者血清HMGB1和PD-L1检测的临床分析[J].临床输血与检验,2020,22(1):60-62.
[9]张盼.晚期非小细胞肺癌PD-1/PD-L1单抗治疗临床转化现状[J].中国肿瘤生物治疗杂志,2018,25(4):426-430.
[10]周建英,刘敏知,黄晖,等.PD-L1及TGF-β在非小细胞肺癌中的表达及其临床意义[J].实用癌症杂志,2017,32(12):1922-1927.
[11]王自全,王保庆,李庆妍.替吉奥联合长春瑞滨治疗进展期非小细胞肺癌的疗效以及对COX-2和MMP-9水平的影响[J].实用癌症杂志,2018,33(11):41-44.
[12]闫小龙,夏津.厄洛替尼对比长春瑞滨联合顺铂辅助治疗ⅢA期EGFR突变阳性非小细胞肺癌患者的疗效[J].循证医学,2019,19(1):44-46.
[13]韩文杰,刘军,孙永臣.红参发酵产物联合长春瑞滨及顺铂化疗方案治疗晚期非小细胞肺癌患者的疗效[J].癌症进展,2020,18(7):694-698.
[14]李超,陈俊花,吴静.康莱特注射液联合NP方案化疗对晚期NSCLC患者免疫状态、炎症因子及生命质量的影响[J].国际肿瘤学杂志,2018,45(9):535-538.
[15]刘克元.顺铂联合长春瑞滨辅助化疗对行肺癌根治术后患者的临床疗效及毒副反应[J].中国医师杂志,2020,22(3):428-431.
[16]李小霞,孙艳,曲荣锋,等.PD-1/PD-L1信号通路阻滞剂在晚期非小细胞肺癌的临床应用[J].國际老年医学杂志,2018,39(4):193-198.
[17]万秋,杨扬,黎友伦.PD-1单抗/PD-L1单抗与多西他赛治疗进展期非小细胞肺癌疗效与安全性的荟萃分析[J].中国新药杂志,2018,27(2):229-235.
[18]吕厚宽,庄文辉,黄一桂,等.PD-1/PD-L1抑制剂治疗非小细胞肺癌的疗效及预后观察[J].癌症进展,2020,18(3):279-281.
[19]邢玉斐,潘雪,钱斌,等.晚期非小细胞肺癌患者外周血PD-1和PD-L1分子的表达及其意义[J].中华医学杂志,2019,99(2):111-114.
[20]郁华晴,施敏骅.非小细胞肺癌PD-1/PD-L1信号通路及其与EGFR突变的相关性[J].国际呼吸杂志,2018,38(8):602-605.
(收稿日期:2020-11-16) (本文编辑:张明澜)

