儿童静脉输液治疗临床实践循证指南
儿童静脉输液治疗临床实践循证指南工作组
目次
1 前言 2
2 应用人群 2
3 适用人群 2
4 制定时间 2
5 文献检索数据库和起止时间 2
6 利益关系声明 2
7 指南制作经费来源 2
8 证据质量和推荐强度说明 2
8.1 基于系统评价的证据质量 2
8.2 基于专家共识的证据质量 2
8.3 推荐强度 2
9 版本说明 2
10 相关定义 2
10.1 外周静脉装置 2
10.1.1 外周静脉短导管 2
10.1.2 中长导管 2
10.2 中心静脉输液装置 3
10.2.1 脐静脉导管 3
10.2.2 经外周静脉置入中心静脉导管 3
10.2.3 中心静脉导管 3
10.2.4 隧道式中心静脉装置 3
10.2.5 完全置入式静脉输液港 3
10.3 非外周输疗药物 3
10.4 外周输注药物 3
10.5 导管相关性血流感染 3
10.6 中心静脉导管相关血流感染计算公式 3
10.7 中心静脉导管相关性血栓 3
11 静脉治疗团队 3
11.1 静脉治疗团队定义 3
11.2 静脉穿刺困难 3
11.3 高风险静脉治疗 3
11.4 静脉治疗护士 4
11.5 静脉治疗团队建制 4
11.6 静脉治疗团队职责体系 4
11.6.1 临床操作职责 4
11.6.2 质量控制职责 5
11.6.3 培训教育职责 5
11.6.3.1 培训方案 6
11.6.3.2 规范化操作流程 6
11.6.3.3 住院和居家患儿静脉治疗教育清单 6
11.6.3.4 知情同意 6
12 静脉治疗装置的选择 7
12.1 儿童主要血管通路的局部解剖 7
12.2 输液装置 7
12.3 静脉输液装置的选择原则 7
13 感染的预防 10
13.1 安全配置药物的环境准备 10
13.2 静脉输液治疗中对手卫生的基本要求 10
13.3 消毒液的选择 10
13.4 输液治疗中的标准预防措施 11
14 血管通路的置入和拔除 11
14.1 血管通路的置入 11
14.1.1 置管环境准备 11
14.1.2 手卫生 11
14.1.3 置管部位消毒 11
14.1.4 最大无菌屏障 11
14.1.5 置管过程相关技术 11
14.1.5.1 导管类型 11
14.1.5.2 置管方法 13
14.1.5.3 镇痛 15
14.1.6 血管通路装置穿刺部位 16
14.2 血管通路拔除 17
14.3 拔管过程中的相关技术 18
15 血管通路使用和维护 18
15.1 有效冲管和封管 18
15.2 无菌操作技术(接头) 23
15.3 导管敷料 24
15.4 导管有效固定 25
16 输液治疗中的特殊预防措施和有害药物、废弃物的处理 26
17 导管并发症 27
17.1 中心静脉导管血流感染 27
17.2 导管相关性血栓 30
17.3 其他并发症 33
18 指南工作组及其职责 33
19 文献筛选结果 33
20 GRADE评价工具 34
21 更新计划 34
22 指南制定主要事件时间表 34
23 指南工作组 34
24 附表 34
24.1 置管操作流程(附表1~9) 34
24.2 置管宣教要点(附表10~14) 37
24.3 置管知情同意要点(附表15~20) 38
参考文献 39
1 前言
输液治疗被广泛应用于临床实践。静脉通路是临床最常应用的治疗性操作,具有操作相对便捷、患儿痛苦少、可以迅速给药及药物起效快等优势,在诊疗过程中发挥着积极的作用。但是,由于儿童年龄跨度较大,发育认知水平的不同、患儿家庭照顾能力的差异、护士置管技术和维护水平等原因,均会导致相关并发症的发生,为患儿及家庭带来痛苦。因此,需要临床实践者对静脉输液治疗具有完整的知识体系,通过开展科学研究和应用已有科学证据,确保患儿静脉治疗的安全性和有效性,并促进静脉治疗质量和护理学科体系发展。
儿童静脉输液治疗临床实践循证指南(简称指南)选题共有8个维度,①相关定义维度(7个条目,7个子条目),②静脉治疗团队维度(6个条目,7个子条目),③静脉输液装置的选择维度(3个条目),④感染的预防维度(4个条目),⑤血管通路的置入和拔除维度(3个条目,9个子条目),⑥血管通路的使用和维护维度(4个条目),⑦输液治疗中化疗药物使用及废弃物处理维度,⑧导管并发症维度(3个条目)。指南的推荐意见来自于系统评价,蓝色字体标识;来自于中国22家儿童专科医院、妇幼保健院、综合医院儿科的护理专家的专家共识,绿色字体标识。
2 应用人群
儿科护士,护理管理工作者,护理教学工作者,患儿及其家长或监护人。
3 适用人群
临床需要通过静脉输液治疗的新生儿至青少年。
4 制定时间
2017年12月19日至2021年2月20日。
5 文献检索数据库和起止时间
中文数据库:SinoMed(中国生物医学文献服务系统)和CNKI(中国知网)数据库,检索起止时间:2000年1月1日至2019年8月16日;英文数据库:PubMed、Cochrane 图书馆和EMBASE数据库,检索起止时间:2000年1月1日至2018年10月12日。英文文献委托复旦大学上海医学院图书馆检索,中文文献由指南核心专家组检索,部分选题检索至2020年11月16日。
6 利益关系声明
指南制作过程中,核心专家组、共识专家组、审稿专家组、文献筛选和评价护士,均保证与任何药商和器械商无利益关系,亦无学术冲突关系。
7 指南制作经费来源
指南制作核心组工作会议、专家共识会、指南终审会得到《中国循证儿科杂志》编辑部和复旦大学附属儿科医院指南制作和评价中心的资助。
8 证据质量和推荐强度说明
8.1 基于系统评价的证据质量 采用GRADE证据质量定义,分别用A、B、C和D代表高、中、低和极低质量证据。
8.2 基于专家共识的证据质量 采用共识面对面会议法,对专家共识维度及其条目逐条讨论、修改和表决,给予表决中的少数专家意见充分的表述时间,再次讨论、修改和表决,取得≥95%专家赞同的维度及其条目和内容为专家共识,均为低质量证据,用D来表示。
8.3 推荐强度 无论是基于系统评价还是专家共识均以1为推荐和反对,2为建议和不建议。
9 版本说明
指南共有3个版本。①电子版:由指南全部内容组成。②书籍版:由指南主要内容组成。③杂志版:由指南核心内容组成。
10 相关定义
10.1 外周静脉输液装置(peripheral venous access device) 经外周静脉置管、导管头端未到达腔静脉的输液装置。
10.1.1 外周静脉短导管(peripheral intravenous catheter,PIVC) 经外周静脉置入、长度为2~6 cm的输液装置,导管头端位于外周静脉。
10.1.2 中长导管(midline catheter,Midline) 经外周静脉置入,导管头端未达到腔静脉。
10.2 中心静脉输液装置(central venous access device,CVAD) 经不同部位置入、导管头端到达腔静脉的输液装置。
10.2.1 脐静脉导管(umbilical catheter,UVC) 经脐静脉置入,导管头端位于上腔静脉中下1/3与右心房交界处。
10.2.2 经外周静脉置入中心静脉导管(peripherally inserted central catheter,PICC) 经外周静脉(上肢为贵要静脉、肘正中静脉和头静脉等,下肢为大隐静脉、小隐静脉或股静脉等,新生儿还可通过头部颞静脉、耳后静脉)置入,导管头端位于上腔静脉中下1/3与右心房交界处或位于下腔静脉横膈膜水平。
10.2.3 中心静脉导管(central venous catheter, CVC)或非隧道式中心静脉装置(nontunneled central venous access device, NTCVAD) 经皮肤穿刺进入颈静脉、锁骨下静脉或股静脉等,导管头端位于上腔静脉中下1/3与右心房交界处。
10.2.4 隧道式中心静脉装置(tunneled central venous access device,TcCVAD) 将带有“袖套”(cuff)的导管经胸前皮下隧道置入上腔静脉中下1/3与右心房交界处的输液装置。
10.2.5 完全置入式静脉输液港(totally implanted venous device,TIVD) 经手术置入皮下、长期留置在体内的静脉输液装置,由可穿刺的港体和静脉导管系统组成。导管头端位于上腔静脉中下1/3与右心房交界处。
10.3 非外周输注药物 不能通过短期或长期外周静脉给予刺激药物(可引起炎症、压痛、发热或沿静脉发红的药物)或发疱剂(引起起泡或发红的药物)治疗,包含持续输注发疱剂化疗、肠外营养,pH值<5或>9,渗透浓度为600 mOsm·L-1。
10.4 外周输注药物 可通过外周静脉给药,不含刺激性或发疱属性的药物。
10.5 导管相关性血流感染[2]
10.5.1 中心静脉导管相关血流感染(central line associated bloodstream infection,CLABSI) CVAD置管48 h后,满足以下2项之一:①1组或多组血培养阳性,病原菌包括肠杆菌科或其他革兰阴性杆菌、金黄色葡萄球菌和真菌,且血培养阳性结果不能用其他部位的感染解释;②至少2组血培养阳性,病原菌为常见的皮肤污染菌,包括凝固酶阴性葡萄球菌、草绿色链球菌、丙酸杆菌属、芽孢杆菌属或微球菌属等,以及临床征象满足体温>38℃、寒战和/或低血压。
10.5.2 导管相关血流感染(catheter related bloodstream infection,CRBSI) 需同时满足以下3项:①CVAD装置和外周静脉抽血培养获得≥1种阳性结果,并有感染的临床表现(如发热、寒战和/或低血压);②除CVAD外没有明显的血流感染源;③实验室检查支持:半定量(每导管段15 cfu/导管片段或皿)或定量(每导管段10 cfu·mL-1)导管培养阳性,即从导管段和外周血培养中分离出相同种类的菌群;同时定量培养血液,导管∶外周血比值>5∶1 (cfu·mL-1);或报告血培养阳性的时间不同(通过CVAD 的血液培养阳性比同时抽取的外周血培养早2 h)。
10.5.3 血液感染(bloodstream infection,BSI) 外周和/或中心静脉血培养阳性,有或无可识别的主要感染部位。
本指南中所涉及的导管相关血流感染均以1 000个导管日内发生事件数进行计算。
10.6 CLABSI发生率计算公式 (CLABSI发生事件数/CVAD总日数)×1 000‰。
10.7 CVAD相关性血栓[3]由静脉造影或血管静脉超声诊断的因CVAD置入导致的至少1条血管中出现堵塞性或非堵塞性血栓。根据有无特异症状(CVAD置管同侧肢体出现肿胀、疼痛、发红或变色,或无法从CVAD持续或反复回抽血液或推注液体)分为症状性血栓和无症状性血栓。
10.8 儿童年龄划分 新生儿:0~30 d(国内新生儿年龄界定为0~28 d),婴儿:~1岁,儿童:~12岁,青少年:~24岁。
11 静脉治疗团队
11.1 静脉治疗团队定义
推荐意见(1) 静脉治疗团队应由置管经验丰富且经过培训的护士组成,组织架构清晰,覆盖全院范围的专业团队及其成员,利用自身的知识和技能协同合作,在完成临床输液实践、控制临床输液质量的基础上,实现对临床护士的静脉治疗的专业培训,着力于推进最佳静脉治疗实践的开展(1D)。
11.2 静脉穿刺困难
推荐意见(2) 接受临床护士2人各2次静脉穿刺失败为静脉穿刺困难(2D)。
静脉穿刺困难后给予安抚及止痛措施,再寻求静脉治疗团队给出处理方案(1D)。
推荐说明 来自美国东南部2所三级儿童专科医院的病例系列报告[4],在相似的患儿人群中,有社工安慰和止痛措施的保障下,由经过培训的非静脉治疗团队的护士(工作1年占37%,工作>5年占36%)对539例患儿(排除了新生儿、病情危重的患儿、手术后8 h以内的患儿)行1 135例次静脉穿刺,基于第三方(非操作者)评价静脉穿刺成功率(有血液回流和通畅)和尝试率(刺破皮肤记为1次尝试),1次穿刺成功率46%,累计2次成功率89%,累计4次成功率93%,最多穿刺15次。60%患儿1个护士穿刺成功,24%患儿1~2个护士穿刺成功,16%患儿3~7个护士穿刺成功。
在美国俄亥俄州东北部1家综合性医院(儿科床位数120张),基于时间序列前后对照研究,前时间序列无特别干预下最大限度的静脉穿刺成功,后时间序列实施患儿舒适计划+2人2次静脉穿刺失败由更高级护士评估选择方案;穿刺护士自我评估穿刺成功率并记录静脉穿刺次数;78个护士完成了721例次穿刺,前时间序列第1次穿刺成功率51%,总成功率92%,穿刺护士为1~6人次;后时间序列第1次穿刺成功率52%,总成功率89%,穿刺护士为1~4人次;仅穿刺护士人次后时间序列较前时间序列差异有统计学意义(P=0.019);需要说明的是,穿刺患儿年龄为0~27(8.3±7.0)岁[5]。
综合外周静脉穿刺困难判断标准的2项研究[4,5],也考虑到开通静脉通路对疾病诊断或治疗是必需的,专家共识认为,接受2人各2次静脉穿刺失败作为外周静脉穿刺困难的标准虽然显得保守,但尽早寻求静脉治疗团队给出方案,对疾病诊断或治疗、对患儿及其家长的负面影响、对操作护士的保护都利大于弊。特别是在不具备有社工安慰和止痛措施保障的静脉穿刺操作时。

问题: 静脉穿刺困难[推荐意见2]患儿或人群: 儿科人群;场所:病房和门诊结局、患儿数量 (研究数量)穿刺例次对照组干预组证据质量证据质量降级说明1次穿刺成功率[4]患儿数量:539例(1项病例系列报告)1 3151次穿刺成功率46%,累计2次成功率89%,累计4次成功率93%,最多穿刺15次。60%患儿1个护士穿刺成功,24%患儿1~2个护士穿刺成功,16%患儿3~7个护士穿刺成功极低不评价1次穿刺成功率[5]患儿数量:未报告(1项非RCT)721前时间序列第1次穿刺成功率51%,总成功率92%,穿刺护士为1~6人次后时间序列第1次穿刺成功率52%,总成功率89%,穿刺护士为1~4人次极低未实施(-1);病例纳入非连续病例(-1);基线数据均衡性不确定(-1);混杂因素无恰当鉴定和分析(-1)
11.3 高风险静脉治疗
推荐意见(3) 高风险静脉治疗涉及高风险患儿、药物和通路。高风险患儿:如血流动力学不稳定,极低出生体重,3或4级手术后等;高风险药物:如化疗药物、胃肠外营养、高浓度电解质、血液和血制品等;高风险静脉通路:如PIVC、TIVD和UVC等(1D)。
11.4 静脉治疗护士
推荐意见(4) 静脉治疗护士定义:接受过静脉治疗专科培训并通过结业考试的专职或兼职从事静脉治疗的护士,不仅能独立从事临床静脉治疗操作,还能承担临床护士静脉治疗教育和顾问的角色,参与静脉治疗质量控制、结果监测和规范制定等相关工作(1D)。
11.5 静脉治疗团队建制
推荐意见(5) 在儿童专科医院,可建立儿科静脉治疗团队;在有儿科专业的综合医院中,至少要有儿科护士在静脉治疗团队中发挥作用;综合医院儿科规模较大(100张床位),也可考虑单独建立儿科静脉治疗团队(2D)。
推荐说明 建立静脉治疗团队的必要性主要体现在:①促进静脉输液专业化的发展;②推广静脉治疗相关标准化循证实践方案的建立和实施;③为静脉治疗相关政策的制定,提供专业化建议;④提供静脉治疗相关资讯及获取渠道;⑤降低静脉治疗相关并发症,改善患儿结局;⑥合理控制静脉治疗费用。
静脉治疗团队成员,可根据医院实际情况由专职或兼职人员担任。完善的静脉治疗团队建制可考虑分为专业组专员和核心组专员。
专业组专员为院内静脉输液骨干护士,熟练掌握PIVC、Midline、PICC、CVC和 TIVD的操作,以及常见问题的处理,亦可承担对院内参与静脉治疗护士的培训和静脉治疗会诊。
核心组专员负责各种院级静脉治疗制度和标准的制定,对全院静脉治疗护理质量进行监督和考核,针对全院参与静脉治疗的护士进行教育培训计划的制定,主持与静脉治疗相关的科研活动。
此外,双休日、节假日和夜间可建立静脉治疗护士值班制,全方位解决全院24 h的各种静脉通路问题。
静脉治疗已经从一项单纯的临床护理操作技能发展为涉及多学科、多领域的复合型技能。其涉及血管通路装置的置入、维护和管理,同时还要求临床工作人员就装置和血管通路的选择进行临床决策。因此,推广静脉治疗相关标准化循证实践方案的建立并上升为行业标准,是十分必要的,而且这一工作责无旁贷是由静脉治疗团队的专业人士来推动和实现。
对于静脉治疗团队是否能合理控制静脉治疗费用,少数专家提出如下担忧:①静脉治疗费用与医院一次性耗材采购、医嘱开具和患儿自身血管条件等多种因素有关,控制静脉治疗费用不完全取决于静脉治疗团队的操作;②对于较为复杂和有难度的血管通路装置的置入、维护和管理,应综合考虑置管利弊,以免影响治疗过程的顺利完成。
11.6 静脉治疗团队职责体系
推荐意见(6) 建议从临床操作、质量控制和培训教育3个方面构建静脉治疗团队完整职责体系(2D)。
11.6.1 临床操作职责
推荐意见(7) 建议临床操作职责包括:①进行静脉治疗相关评估;②接受静脉治疗会诊;③应静脉穿刺困难和高风险静脉治疗要求行PIVC及CVC的置入和拔除;④指导或参与CVC的维护(1D)。
推荐说明 静脉治疗团队的成员执行中华人民共和国国家卫生和健康委员会颁布的《静脉治疗护理技术操作规范(WS/T 433-2013)》[6],获得静脉输液团队成员资质评估和认证,基于此,本指南专家共识认为,静脉治疗相关评估,除了血管通路及其装置的评估外,还包括置管患儿及其家长状况的评估、置管后导管状况的评估等;对临床评估为外周静脉穿刺困难、高风险静脉治疗的患儿进行会诊,必要时行经PICC的置入和拔除操作,对静脉治疗相关并发症会诊并制定处理方案;CVC的维护包括导管评估、紧急情况处理(如敷贴卷边、潮湿、污染或穿刺点出血等)以及常规敷贴更换[7],当出现不能解决的并发症、终止输液治疗时需拔除血管通路装置[8]。
11.6.2 质量控制职责
推荐意见(8) 从建立静脉治疗评价指标体系、监督体系、考核体系和改进体系4个方面完善质量控制职责(2D)。
推荐意见(9) 建议静脉治疗评价一级指标3个(要素、过程、结局),二级指标3个(制度及操作规范、置管维护、护理结局),三级指标14个,见表1(2D)。

表1 静脉治疗评价指标体系
推荐说明 关于整体的静脉治疗评价指标体系的文献仅检索到1篇2018年发表的中文文献[9],基于三维质量结构管理模式,以静脉治疗护理技术操作规范[6]的静脉输液条目为基础,结合文献、专家小组讨论和德尔菲函询,采用界值法进行指标筛选,百分比权重法确定指标权重。指南共识专家组认为文献[9]中静脉治疗评价三级指标42项,不适宜在临床推广应用。借鉴和参考了文献[9]指标权重系数较大的三级指标,提出了基于有完整静脉治疗团队的医院应具备的重要静脉治疗质量评价指标体系,指南共识专家组等1轮表决后,文献[9]中的三级指标中的13条(表1)得到了87%~100%的专家认同,医源性皮肤损伤有56%、疼痛有15%、安全注射工具的配置率有2%、导管维护有2%、一次性穿刺成功率有5%、感控标准有2%的专家认为应当增加到三级指标中。专家共识组讨论后,第2轮表决,表1中14条作为三级指标。
推荐意见(10) 建议监督体系应当至少包括:每月对静脉治疗操作规范进行抽查,每季度对静脉治疗出现的不良事件进行分析汇总,并制定相应的护理策略(2D)。
推荐意见(11) 建议考核体系的重点是静脉治疗评价指标体系中的护理结局指标(2D)。
推荐意见(12) 建议改进体系采用恰当的质量管理方法,如PDCA(计划、执行、检查、行动)原则和QCC(品管圈)等进行临床持续质量改进(2D)。
11.6.3 培训教育职责
推荐意见(13) 建议培训教育职责包括:①静脉治疗团队的培训应当基于医院实际,参考相关标准或指南;②建议制定儿科静脉治疗规范,并适时更新;③静脉治疗团队成员应当取得省级、市级、至少是院级的资质评估和认证,静脉治疗团队成员至少2年做1次能力确认;④静脉治疗团队成员应当对患儿及其家长进行静脉治疗相关教育(2D)。
推荐说明 静脉治疗团队的培训不应当基于一种固定的模式,应当结合不同等级的医院、综合医院和专科医院、不同护理团队的能力和素养等特点,参考相关标准或指南做出符合自身阶段性特点的培训方案并不断加以改进。
11.6.3.1 培训方案
推荐意见(14) 建议采用系统教学安排的儿科静脉治疗护士培训方案(表2和3)(1D)。
11.6.3.2 规范化操作流程
推荐意见(15) 建议采用基于表单流程的置管及维护操作(1D)。
推荐说明 不同医院都应建立儿科静脉治疗规范,本指南借鉴复旦大学附属儿科医院建立的儿科静脉治疗规范,在此基础上通过共识专家组讨论进行了调整和修改供参考(附表1~9),在表单流程中共同要求:①执行手卫生,②标准防护(戴帽子、口罩),③操作前按置入导管类型、操作地点做好物品准备和工作,④除非特殊要求,尽可能选择上肢静脉置管,⑤操作前应采取2种标识(建议采用住院号和姓名)核对患儿身份,未放置在附表表单中,但这些基本要求是必须具备的,特此说明。
推荐意见(16) 建议不论是学会、省级、市级和院级资质评估和认证,静脉治疗团队成员资质评估和认证至少要完成如下内容:在护理学会等学术机构或在具有成熟静脉治疗团队经验的医院完成基础理论课程,笔试通过理论知识掌握情况的考核,在具有成熟静脉治疗团队经验的医院中至少要观摩静脉治疗操作2周(高级)至2个月(初级),期间从由指导老师的带教下完成静脉治疗操作10例到独立完成静脉治疗操作2例,对指导老师设计的静脉治疗操作临床情景,做出恰当的评价和给出解决方案(1D)。
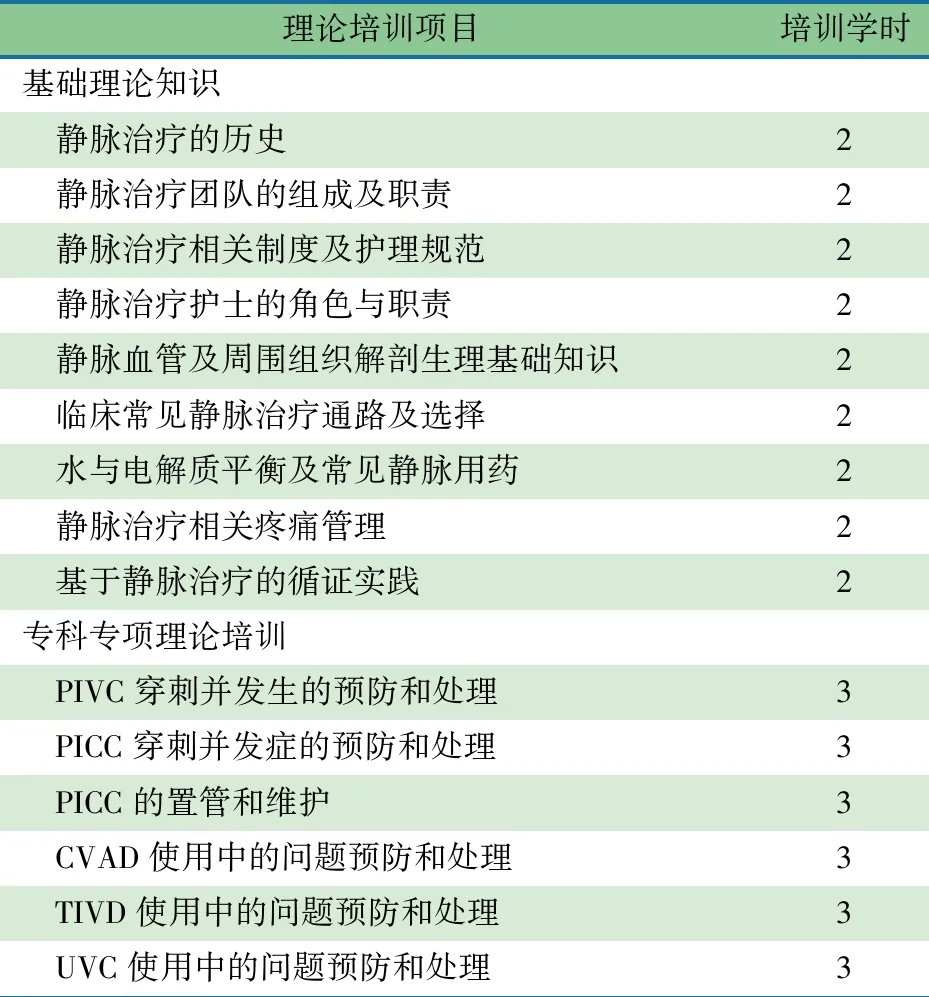
表2 静脉治疗护士理论培训项目
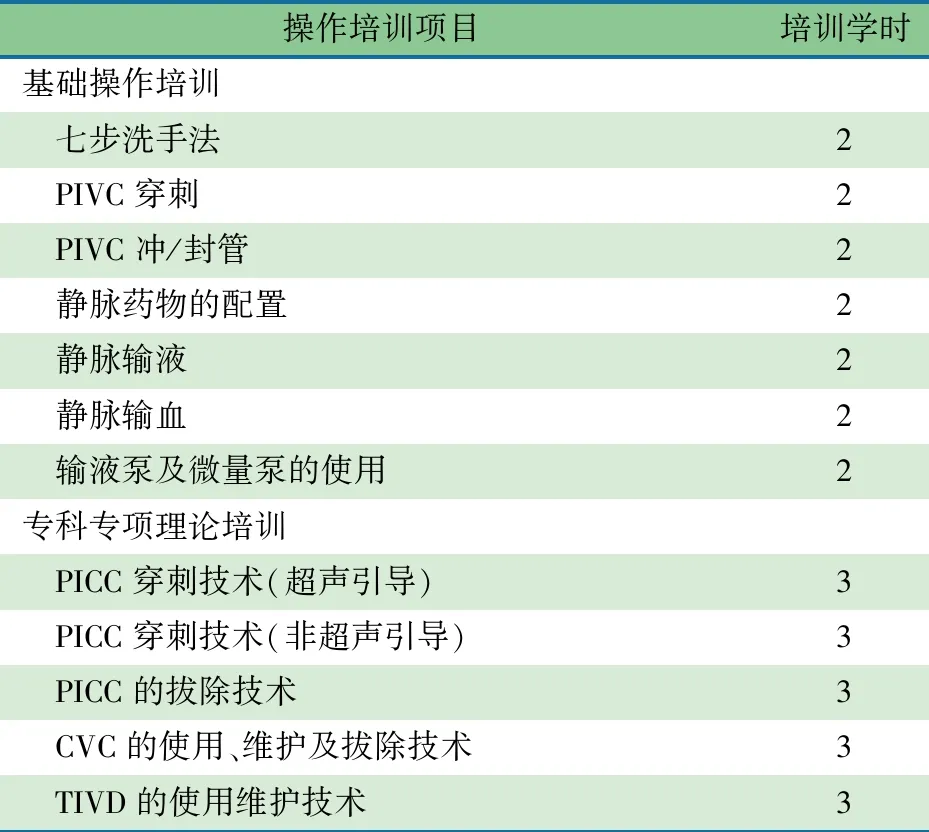
表3 静脉治疗护士操作培训项目
11.6.3.3 住院和居家患儿静脉治疗教育清单
推荐意见(17) 建议采用基于患儿及其家长住院期间和居家静脉治疗相关教育清单的健康教育(2D)。
推荐说明 本指南提供了患儿及其家长住院期间和居家静脉治疗相关教育清单供参考(附表10~14)。住院和居家清单由4部分组成,①患儿一般情况(姓名、年龄、体重);②主要照顾者(教育水平、学习意愿、宗教信仰、语言交流顺畅程度);③宣教方式(口头、书面、多媒体、示教、其他);④宣教内容。其中①~③为格式化内容,未放置在清单中,特此说明,④为不同静脉治疗的具体宣教内容(优势、注意事项),本指南重点展示第4部分。
11.6.3.4 知情同意
推荐意见(18) 建议根据不同的静脉置管行针对性的知情同意面谈和签字(2D)。
推荐说明 无论何种静脉治疗手段都是有创操作,医生和护士选择静脉治疗一定是基于疾病治疗的必需,同时有创操作也一定存在风险,告知患儿及其家长静脉治疗操作中和维护时的利弊与风险的医疗文书,不仅具有法律效应,也应照顾到患儿及其家长的心情和知情权利,尽可能用患儿及其家长能理解的语言和形式进行解释。
本指南提供了PIVC、PICC、CVC、UVC、Midline、TIVD知情同意要点,包括置管指征、优势、潜在风险和替代方案(附表15~20)供使用者参考。置管中潜在风险主要指置管并发症,在附表中并发症会多次重复出现,故对其做统一定义和表述,附表15~20中只体现不同并发症名称。
(1)非导管相关并发症
静脉麻醉并发症:在非隧道式导管穿刺过程中会造成疼痛,导致患儿不配合以及病情变化,因此要在静脉麻醉下完成。静脉麻醉剂注入患儿体内可能会出现静脉麻醉相关并发症,如呼吸抑制、休克、心跳呼吸暂停等。在穿刺过程中,医护人员会严密监视患儿的生命体征,避免上述情况的发生。
麻醉意外:因TIVD置入需在常规手术下进行,将对患儿实施全身麻醉,由于麻醉药物的特殊性,可能会导致麻醉相关并发症,严重者可能导致患儿休克或死亡。在患儿手术期间,由专业的麻醉科医生全程监测患儿的生命体征,当出现意外时会启动相应措施来处理。
手术过程并发症:TIVD是在手术下进行,由于患儿个体差异性,在导管送入心脏时可能刺激心脏导致心律不齐,甚至心跳骤停;在置管过程中可能会损伤相关血管、胸膜、肺尖等邻近组织等;如出现上述情况,应采取相应措施进行处理。
手术伤口并发症:手术切口部位出现出血、血肿形成和疼痛等情况。
(2)导管相关并发症
置管过程并发症:在置管过程中,由于操作人员的熟练程度、患儿个体差异、病情等原因,出现穿刺血管破裂、心房或心室穿孔、导管刺激瓣膜等,导致心律失常等。
PIVC置管失败:由于患儿的血管状况差、疾病因素,导致多次置管不成功,需要替代置管方案。
PICC/CVC置管失败:由于不可预知的静脉瓣、血管变异等因素,在送管时可能会出现局部神经和动脉损伤、送管困难、拔除导丝困难、穿刺失败等情况发生。
穿刺部位并发症:穿刺成功后,穿刺部位可能会有红肿、渗血和渗液现象,患儿主诉有疼痛。
静脉炎:是最常见的PIVC的潜在风险,主要表现为穿刺部位的红、肿、热、痛,沿静脉走向出现硬肿,穿刺点可能有脓性分泌物。
CLABSI、CRBSI和BSI:见本文10.5部分。
血栓及导管纤维包裹形成:在导管使用过程中,因留置时间过长、药物之间发生相互作用等原因,使导管内出现血栓及导管纤维包裹形成。
药物外渗:由于敷料固定不牢固、输液时间长及导管在血管内移动等原因,出现药物外渗情况的发生。
导管移位:中心静脉导管尖端不处于腔静脉内。
导管断裂:分为体内断裂和体外断裂。体内断裂包括完全断裂和不完全断裂。如发生导管断裂,可能会引起血管内栓塞等严重并发症。
非计划性拔管:因患儿自身原因(如挣扎或因医护人员操作不当)导致导管脱落,或未经医护人员同意自行拔除导管。
导管相关性血栓:见本文10.7部分。
医用粘胶相关性皮肤损伤:在揭除医用粘胶后,局部皮肤出现持续30 min或更长时间的红斑、水泡糜烂、撕脱伤等。主要类型有皮炎、机械性皮肤损伤、潮湿皮囊炎等。
导管材质过敏:尽管导管供应商在导管材质说明书中都有描述可能会发生导管材质过敏,但并无文献报告过敏症状和体征。
固定材料过敏:固定导管的材料(胶布、敷贴等)过敏,出现过敏的症状和体征。
(3)特殊并发症
脐血管穿破:置管时出现不可预知的脐血管走向,导致脐血管穿破。
脐出血:在切断脐残端或者荷包缝合后出现伤口出血。
UVC相关腹胀:仅在UVC置管时因不可预知的脐血管走向,导致导管误入静脉导管和肝脏。
泵体损伤:TIVD使用不规范及某些药物之间的原因导致泵体损伤。
导管夹闭综合征:导管经过第1肋骨和锁骨之间的狭窄间隙进入锁骨下静脉时,受第1肋骨和锁骨挤压发生狭窄或夹闭而影响输液,严重时可导致损伤或断裂,主要表现为回抽、冲洗及注射困难。
12 静脉治疗装置的选择
推荐意见(19) 推荐2020年在PEDIATRICS发表的“儿科血管通路标准”中的血管通路的局部解剖、输液装置和静脉输液装置的选择原则(1D)。
推荐说明 本指南静脉治疗装置的选择维度有3个条目:儿童主要血管通路的局部解剖、输液装置和静脉输液装置的选择原则,鉴于2020年在PEDIATRICS发表的由澳大利亚和美国等国家的13家医院参与的专家共识对这3个条目进行了充分的报告[10],共识专家组讨论认为,可全面接受文章的观点,并从PEDIATRICS购买了图表使用版权。本文对图的标注做了汉化。
12.1 儿童主要血管通路的局部解剖 如图1。
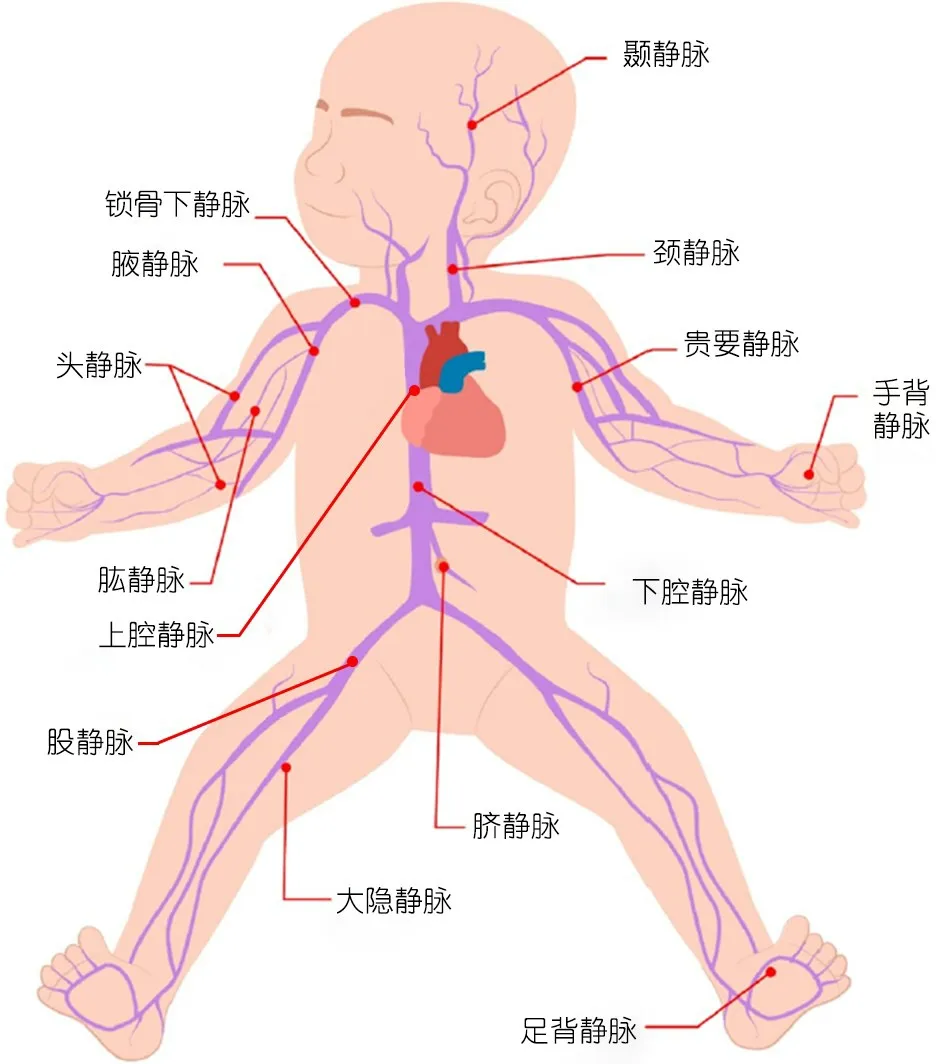
图1 儿童静脉输液主要血管通路的局部解剖示意图
12.2 输液装置 如图2。
12.3 静脉输液装置的选择原则 应根据患儿年龄、药物理化性质、静脉条件、治疗时长及疾病状况选择合适的静脉治疗输入装置(表4)。
药物的理化性质。①药物的酸碱性:血液的pH值7.35~7.45,<7.0为酸性,<4.1为强酸性,>9.0为强碱性。②药物的渗透浓度(mOsm·L-1):以人血浆的渗透浓度为标准来衡量,人体正常渗透浓度为280~295,低渗溶液<250,等渗溶液~375,高渗溶液>375;渗透浓度越高,对静脉刺激越大;<400为低危风险渗透浓度,~600为中危风险渗透浓度,>600为高危风险渗透浓度。
治疗时长:根据目前医疗水平及文献回顾,静脉治疗时长可分为1周(7 d)、~2周、~4周和~1年。
患儿疾病状况:分为普通儿科、血液肿瘤、危重症(分为生命体征平稳和生命体征不稳定)和先天性心脏病。
图3~10[1]为不同年龄段在不同治疗疗程以及不同疾病状态下进行静脉输液装置[PIVC、IO(骨髓腔穿刺)、Midline、UVC、PICC、TcCVAD、NTCVAD和TIVD]的选择示意图。
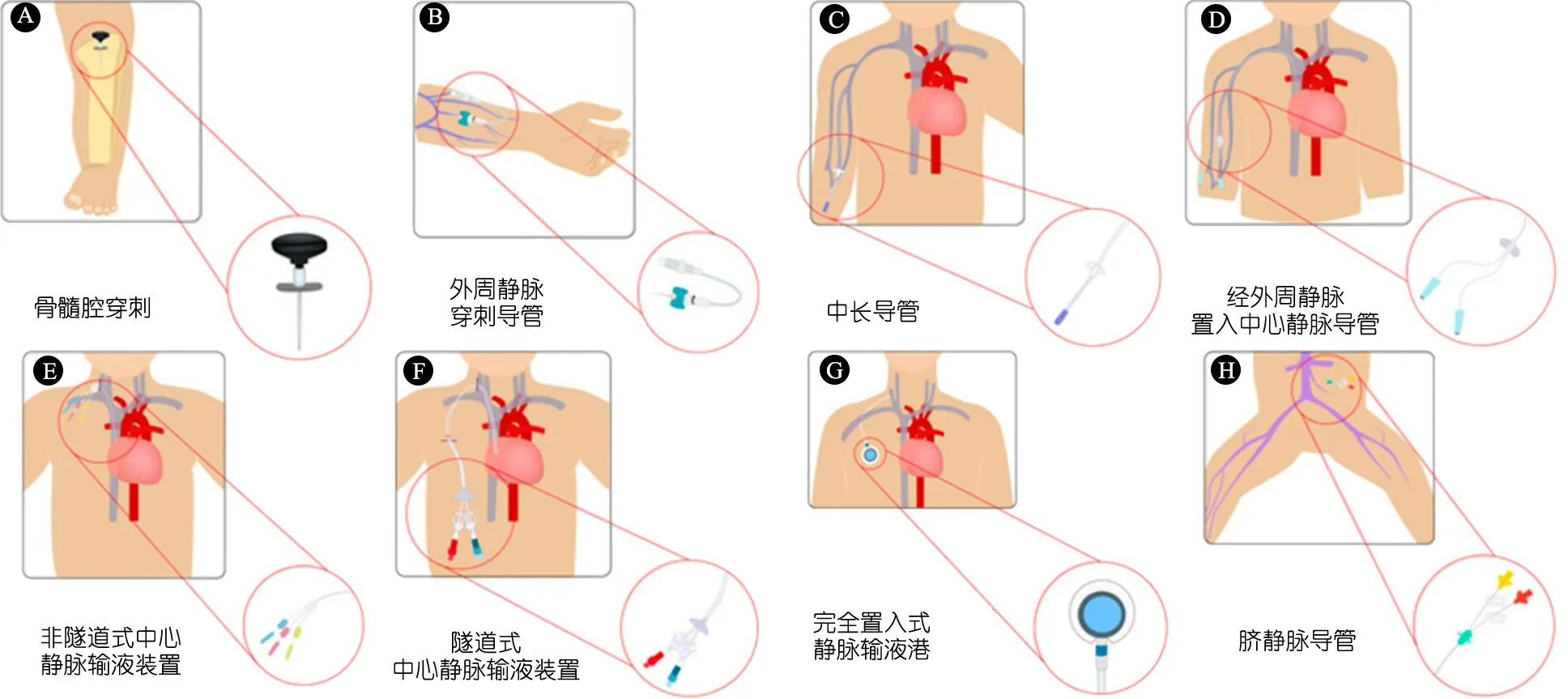
图2 儿童不同体表部位静脉输液装置示意图
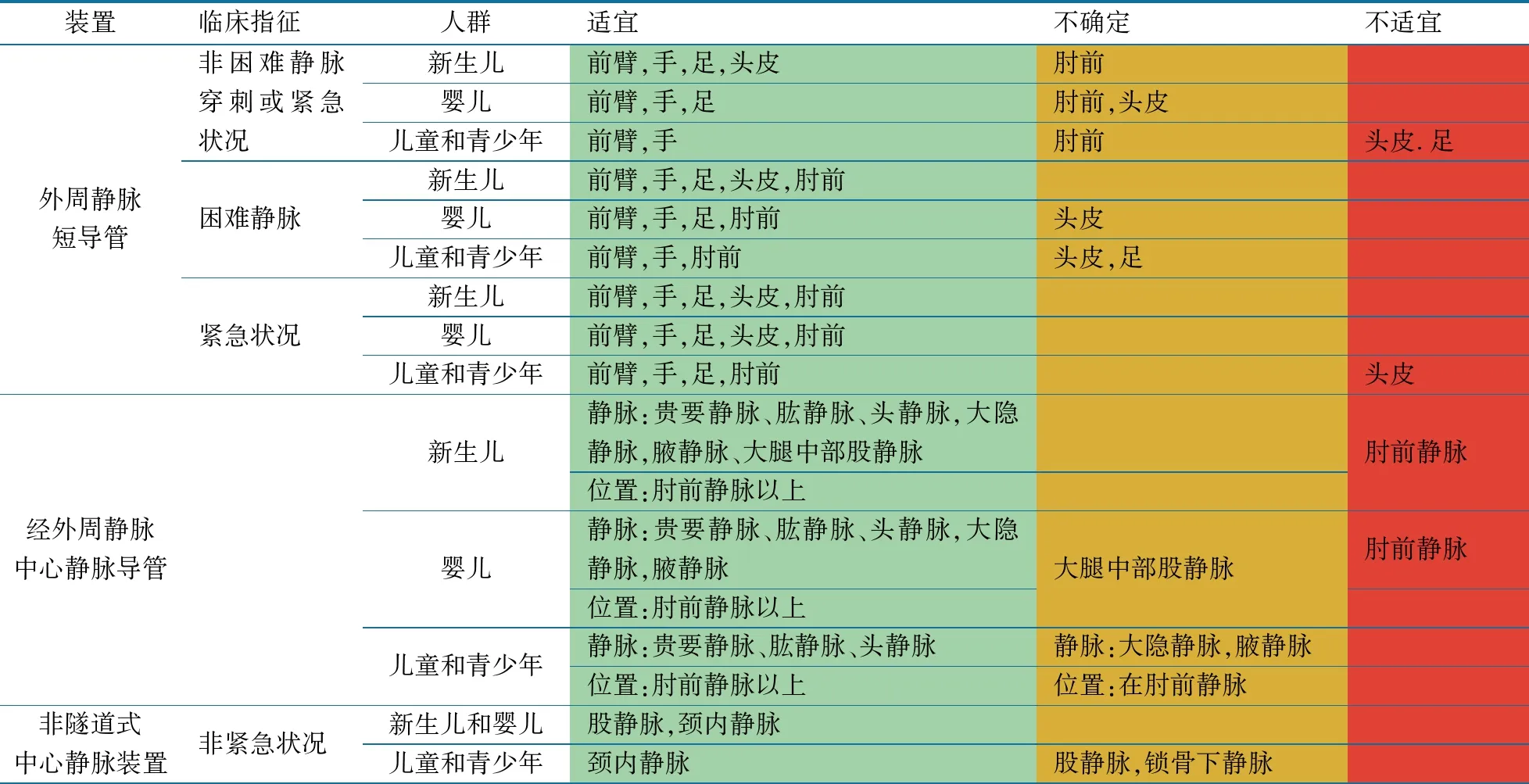
表4 不同儿科人群静脉输液装置临床使用指征和适宜性
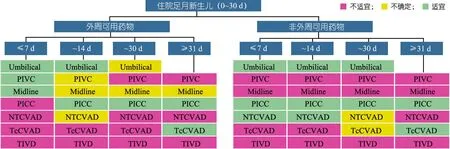
图3 新生儿外周可用和不可用药物不同治疗疗程状态下静脉输液装置的选择
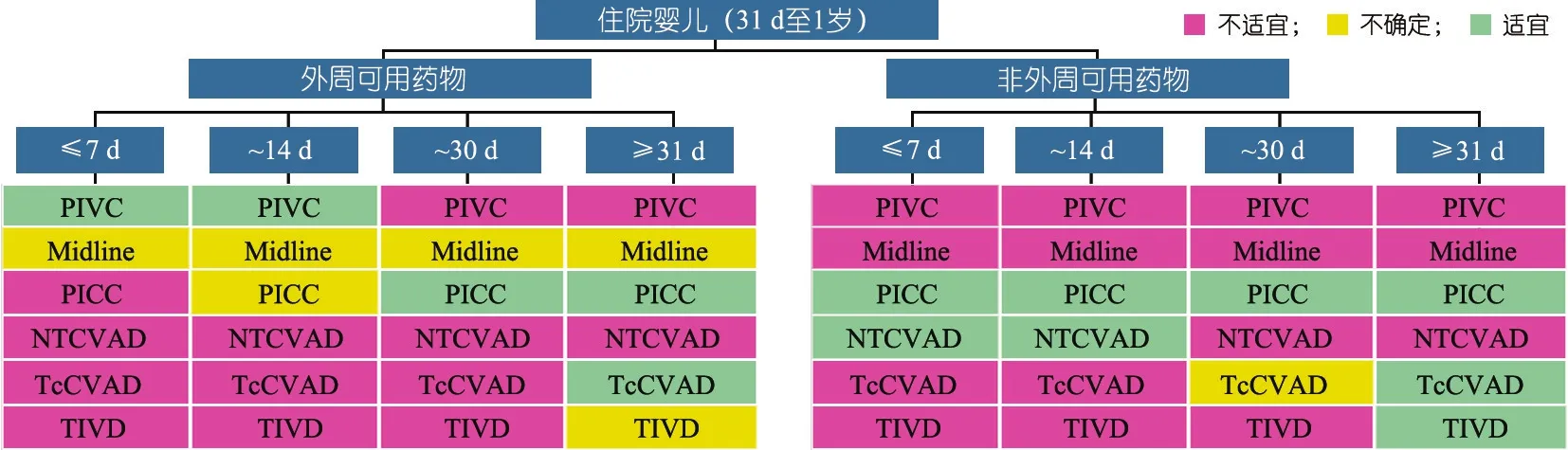
图4 婴儿外周可用和不可用药物不同治疗疗程状态下静脉输液装置的选择
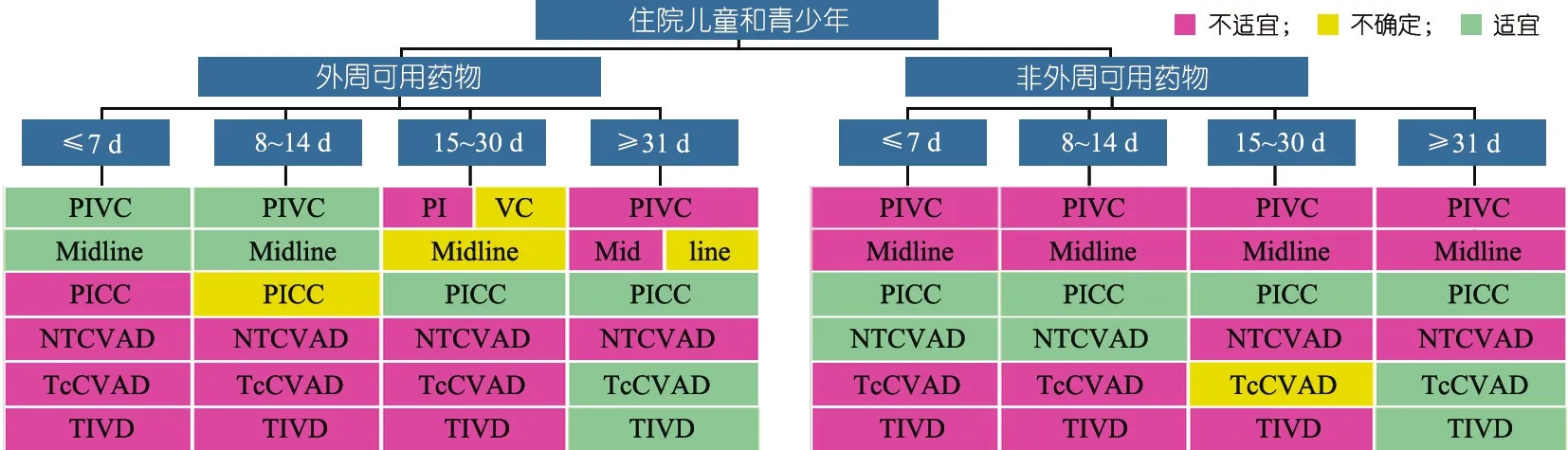
图5 儿童和青少年外周可用和不可用药物不同治疗疗程状态下静脉输液装置的选择
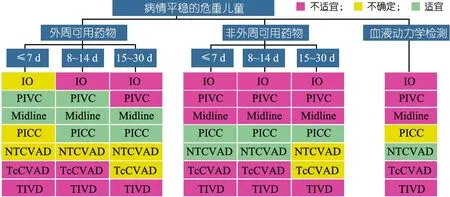
图6 病情平稳的危重儿童外周可用和不可用药物不同治疗疗程状态下静脉输液装置的选择
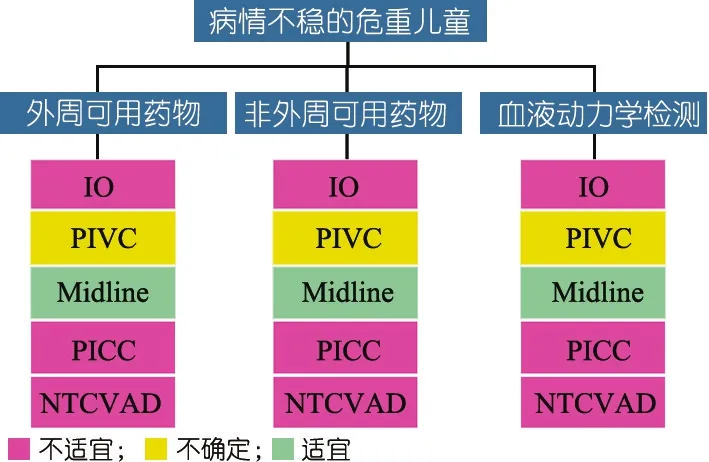
图7 病情不平稳的危重儿童外周可用和不可用药物不同治疗疗程状态下静脉输液装置的选择
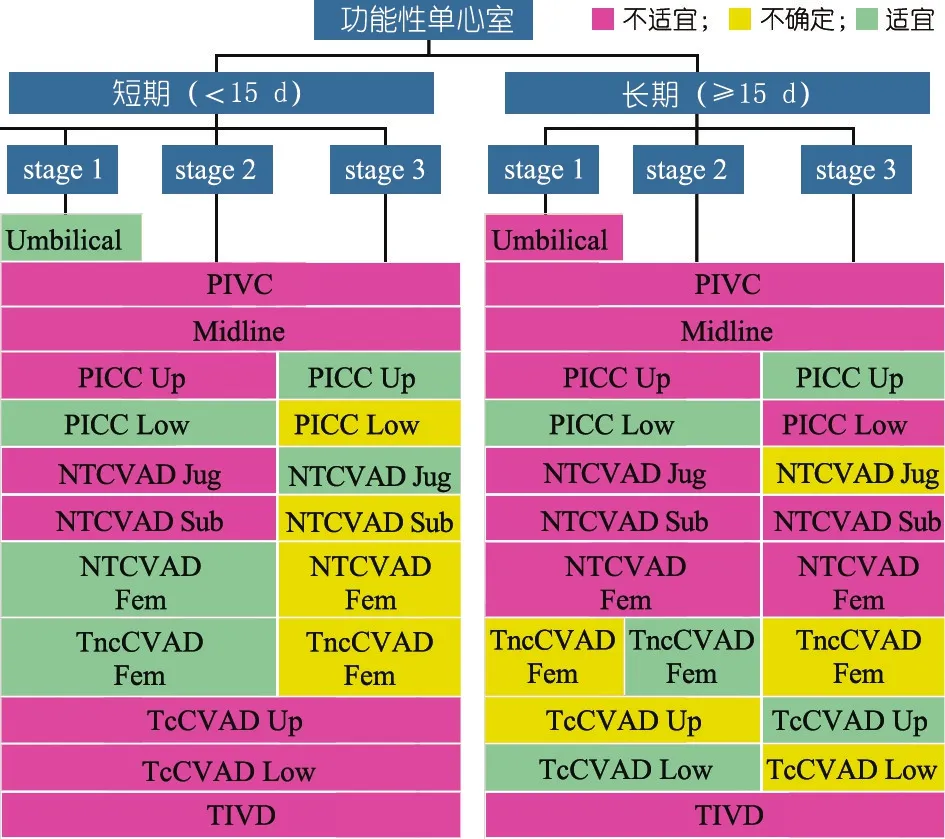
图8 功能性单心室儿童不同留置时间状态下静脉输液装置的选择
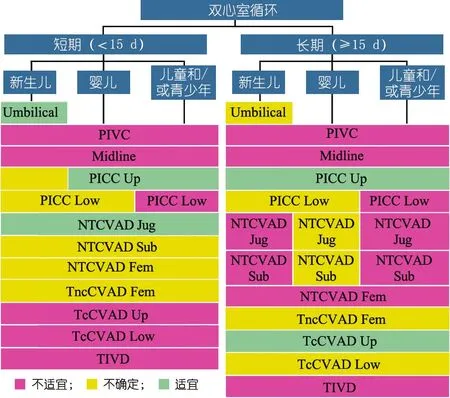
图9 双心室循环儿童不同留置时间状态下静脉输液装置的选择
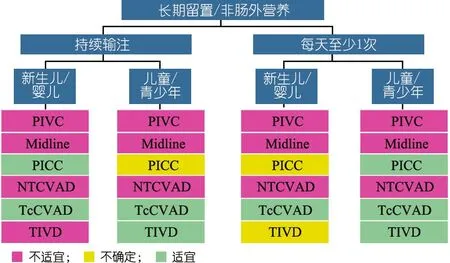
图10 长期留置或非肠外营养儿童不同持续和间断状态下静脉输液装置的选择
13 感染的预防
13.1 安全配置药物的环境准备
推荐意见(20) 推荐中华人民共和国国家标准-静脉用药集中调配质量管理规范[11](1D)。
静脉用药调配总体区域应保证洁净区、辅助工作区和生活区的划分,不同区域之间人流和物流走向合理,不同洁净级别区域间应当有防交叉污染的相应设施。
静脉用药调配中心(室)应当设置于人员流动少的安静区域,且便于与医护人员沟通和成品的运送。设置地点应远离各种污染源,禁止设置于地下室或半地下室,周围的环境、路面、植被等不会对静脉用药调配过程造成污染。洁净区采风口应当设置在周围30 m内环境清洁、无污染地区,离地面高度不低于3 m。
静脉用药调配中心(室)室内应当有足够的照明度,墙壁颜色应当适合人的视觉;顶棚、墙壁、地面应当平整、光洁、防滑,便于清洁,不得有脱落物;洁净区房间内顶棚、墙壁、地面不得有裂缝,能耐受清洗和消毒,交界处应当呈弧形,接口严密;所使用的建筑材料应当符合环保要求。
静脉用药调配中心(室)洁净区应当设有温度、湿度、气压等监测设备和通风换气设施,保持静脉用药调配室温度18~26℃,相对湿度40%~65%,保持一定量新风的送入。
静脉用药调配中心(室)洁净区的洁净标准应当符合国家相关规定,各功能室的洁净级别要求:一次更衣室、洗衣洁具间为十万级;二次更衣室、加药混合调配操作间为万级;层流操作台为百级。
13.2 静脉输液治疗中对手卫生的基本要求
推荐意见(21) 推荐在NICU中对极低出生体重儿行CVC相关操作时,洗手后戴无菌手套(1D)。
推荐说明 1项来自美国弗吉尼亚大学NICU的2014年基于洗手后戴无菌手套对预防早产儿迟发性感染效果的RCT[12],洗手后戴无菌手套为观察组(n=60),洗手后不戴手套为对照组(n=60),两组人口学、围生期状况差异均无统计学意义。以迟发性感染(出生后72 h发生的感染(血流感染、泌尿系统感染、脑脊液感染和NEC)为主要观察指标,本指南关注CLABSI。观察组4/2 374导管日血流感染(1.7/1 000导管日),对照组4/2 125导管日血流感染(1.9/1 000导管日),相对RR=0.9(95%CI:0.22~3.61)。绝对效应值:每1 000个导管日可减少0.2(95%CI:-1.5~4.9)例CLABSI的发生。次要结局指标(抗生素治疗、住院时间、死亡、医院费用、肠穿孔、严重的ROP、用氧天数、纠正胎龄36周用氧比例、胆汁淤积比例)组间差异均无统计学意义。

问题:洗手后戴无菌手套预防早产儿CLABSI的效果[推荐意见21]患儿或人群:早产儿; 场所: NICU; 干预: 洗手后戴无菌手套; 对照: 洗手后不戴手套结局患儿数量 (研究数量)相对效应值(95% CI)预期绝对效应值(事件数/导管日)对照组风险干预组风险风险差(95% CI)证据质量证据质量降级说明降低CLABSI发生率患儿数量:60/60(1项RCT)RR=0.9(0.22~3.61)1.9/1 0001.7/1 000-0.2/1 000(-1.5~5.0)极低操作者未施盲(-1); 不精确性:置信区间特别宽(-2)
13.3 消毒液的选择
推荐意见(22) 新生儿中心静脉置管前皮肤消毒,使用2%氯己定溶液和10%聚维酮碘减少CLABSI无差别(2B)。
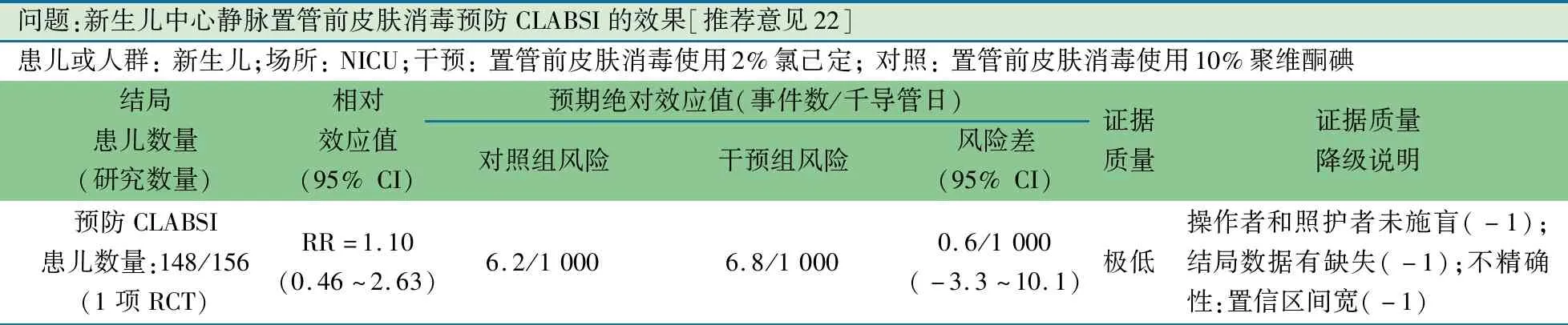
问题:新生儿中心静脉置管前皮肤消毒预防CLABSI的效果[推荐意见22]患儿或人群: 新生儿;场所: NICU;干预: 置管前皮肤消毒使用2%氯己定; 对照: 置管前皮肤消毒使用10%聚维酮碘结局患儿数量 (研究数量)相对效应值(95% CI)预期绝对效应值(事件数/千导管日)对照组风险干预组风险风险差(95% CI)证据质量证据质量降级说明预防CLABSI患儿数量:148/156(1项RCT)RR=1.10(0.46~2.63)6.2/1 0006.8/1 0000.6/1 000(-3.3~10.1)极低操作者和照护者未施盲(-1);结局数据有缺失(-1);不精确性:置信区间宽(-1)
推荐说明 1项来自爱尔兰2011至2014年2个中心的NICU早产儿中行CVC置管前不同消毒方式CLABSI的RCT[13]。2%氯己定溶液为观察组(n=148),10%聚维酮碘为对照组(n=156),两组胎龄、出生体重、产前类固醇暴露、剖宫产、多胎、CVC留置数量、总的导管日和平均每例留置CVC数量,差异均无统计学意义。CLABSI观察组10/1 465导管日(6.8/1 000导管日),对照组10/1 613导管日(6.2/1 000导管日),相对RR=1.10(95%CI:0.46~2.63)。绝对效应值:每1 000个导管日可增加0.6(95%CI:-3.35~10.11)例CLABSI的发生。
13.4 输液治疗中的标准预防措施
推荐意见(23) 推荐采用中华人民共和国卫生部医院感染管理规范[14](1D)。
标准预防:认定患者的血液、体液、分泌物、排泄物均具有传染性,须进行隔离,不论是否有明显的血迹污染或是否接触非完整的皮肤与黏膜,接触上述物质者,必须采取防护措施。其基本特点为:①既要防止血源性疾病的传播,也要防止非血源性疾病的传播;②强调双向防护,既防止疾病从患者传至医务人员,又防止疾病从医务人员传至患者;③根据疾病的主要传播途径,采取相应的隔离措施,包括接触隔离、空气隔离和微粒隔离。
14 血管通路的置入和拔除
14.1 血管通路的置入
14.1.1 置管环境的准备
推荐意见(24) 不建议打开中心静脉导管无菌包前向包中注入生理盐水,不改变置管后CLABSI的发生率(2B)。
推荐说明 1项2002年来自英国单中心RCT[15],以8 d至17.5岁行CVC置管的儿童为研究对象,观察组(n=25)在打开导管的CVC无菌包装前,向包装中注入生理盐水(以降低包装内的静电,以免静电吸附微生物),对照组(n=22)打开导管的无菌包装前不施以任何措施,主要观察指标置管后90 d CLABSI的发生事件数差异无统计学意义。
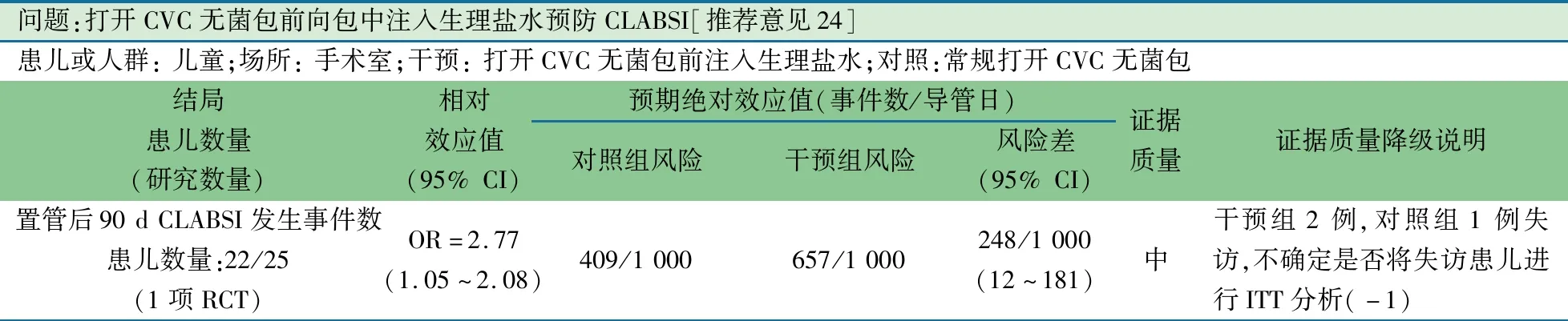
问题:打开CVC无菌包前向包中注入生理盐水预防CLABSI[推荐意见24]患儿或人群: 儿童;场所: 手术室;干预: 打开CVC无菌包前注入生理盐水;对照:常规打开CVC无菌包结局患儿数量 (研究数量)相对效应值(95% CI)预期绝对效应值(事件数/导管日)对照组风险干预组风险风险差(95% CI)证据质量证据质量降级说明置管后90 d CLABSI发生事件数患儿数量:22/25(1项RCT)OR=2.77(1.05~2.08)409/1 000657/1 000248/1 000(12~181)中干预组2例,对照组1例失访,不确定是否将失访患儿进行ITT分析(-1)
14.1.2 手卫生
推荐意见(25) 推荐采用中华人民共和国国家健康委员会医务人员手卫生规范[16](1D)。
手卫生为医务人员在从事职业活动过程中的洗手、卫生手消毒和外科手消毒的总称。本指南所指手卫生是指在医务人员进行与静脉输液治疗相关操作时所需要的手卫生。
14.1.3 置管部位消毒
推荐意见(26) 推荐采用中华人民共和国卫生部医疗机构消毒技术规定[17](1D)。
消毒:清除或杀灭传播媒介上病原微生物,使其达到无害化的处理。
穿刺部位皮肤消毒:①用浸有碘伏消毒液原液的无菌棉球或其他代替物品局部擦拭2遍,作用时间遵循产品说明;②使用碘酊原液直接擦拭皮肤表面2遍以上,作用时间1~2 min,待稍干后再用70%~80%乙醇脱碘,使用有效含量≥2 g·L-1氯己定-乙醇(体积分数70%)溶液擦拭2~3遍,作用时间遵循产品使用说明;④使用复方季铵盐消毒剂原液擦拭消毒,作用时间3~5 min;⑤其他合法、有效的皮肤消毒产品,按照产品的使用说明书操作。
消毒范围:各种诊疗性穿刺等消毒方法主要是涂擦,以注射或穿刺部位为中心,由内向外缓慢旋转,逐步涂擦,共2次,消毒皮肤面积应≥5 cm×5 cm(或消毒范围大于敷贴面积)。CVAD(CVC、PICC、TIVD)的消毒范围直径应>15 cm,至少应大于敷料面积(10 cm×12 cm)。
14.1.4 最大无菌屏障
推荐意见(27) 推荐采用中华人民共和国国家标准-导管相关血流感染预防与控制技术指南[18](1D)。
置管时严格执行无菌技术操作规程。应遵循最大限度的无菌屏障要求,置管部位应当铺大无菌单(巾),置管人员应当戴帽子、口罩、无菌手套,穿无菌衣。超声引导下置管时,超声套头及导管线应在无菌保护套包裹下。
14.1.5 置管过程相关技术
14.1.5.1 导管类型
推荐意见(28) 高风险儿科人群面临抗生素导管(利福平/二甲胺四环素浸渍)和标准导管选择时,建议选择抗生素导管(2D)。
推荐说明 汇总美国单中心历史对照研究、前瞻性和回顾性队列研究各1篇,1篇英国多中心RCT进行Meta分析[19-22]。纳入高风险儿科人群中接受抗生素涂层CVC置管(利福平/二甲胺四环素浸渍)和标准CVC置管,观察导管留置期间CLABSI的发生事件数。抗生素涂层CVC 26/6 606导管日,标准CVC 65/7 231导管日。图11显示,置入抗生素CVC较置入标准CVC的CLABSI发生率下降56%(OR=0.44,95%CI:0.28~0.70)。
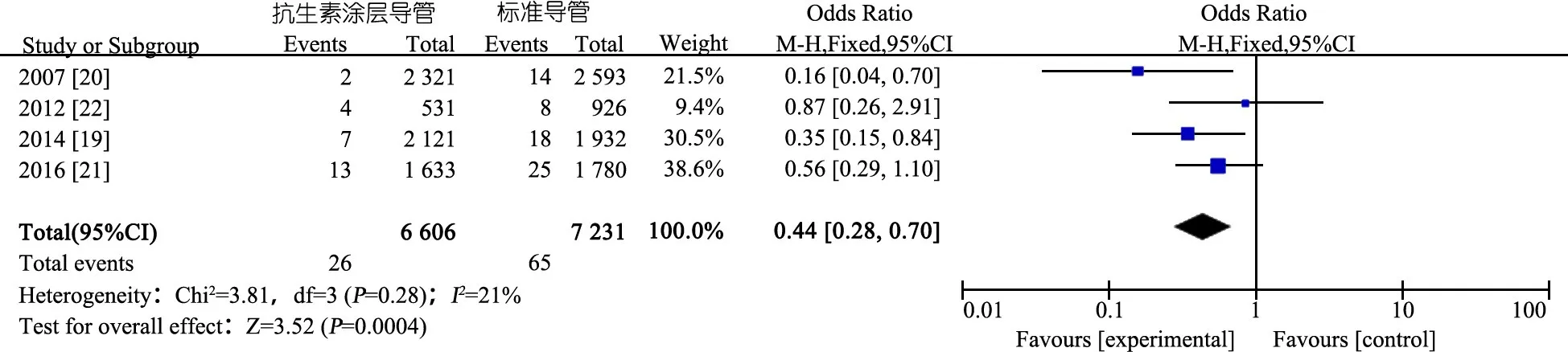
图11 抗生素涂层导管与标准导管预防导管相关血流感染的系统评价和Meta分析
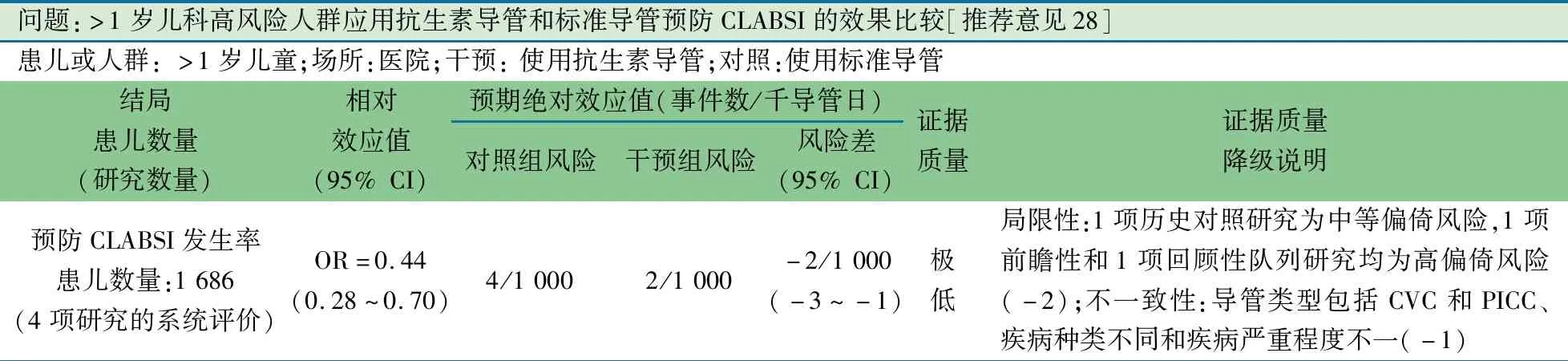
问题:>1岁儿科高风险人群应用抗生素导管和标准导管预防CLABSI的效果比较[推荐意见28]患儿或人群: >1岁儿童;场所:医院;干预: 使用抗生素导管;对照:使用标准导管结局患儿数量 (研究数量)相对效应值(95% CI)预期绝对效应值(事件数/千导管日)对照组风险干预组风险风险差(95% CI)证据质量证据质量降级说明预防CLABSI发生率患儿数量:1 686(4项研究的系统评价)OR=0.44(0.28~0.70)4/1 0002/1 000-2/1 000(-3~-1)极低局限性:1项历史对照研究为中等偏倚风险,1项前瞻性和1项回顾性队列研究均为高偏倚风险(-2);不一致性:导管类型包括CVC和PICC、疾病种类不同和疾病严重程度不一(-1)
1项基于在英格兰公共卫生系统网站数据库中2012年登记的英国数据[23],PICU患儿置入CVC导管8 831例(标准CVC 3 021例,抗生素涂层CVC 5 810例)行成本效应分析。治疗1例BSI费用1.1万英镑,估算使用标准导管比抗生素涂层导管发生BSI多232例,总的治疗费用255万英镑,抗生素涂层CVC与标准CVC每例成本相差36英镑,如8 831例全部以抗生素涂层导管计算,两者相差32万英镑,全部采用抗生素涂层导管费用比治疗232例BSI费用实际节省223万英镑。
推荐意见(29) 在新生儿人群中,银涂层较无涂层CVC导管预防CLABSI优势不确切(2C)。
推荐说明 1篇2015年发表于Cochrane的银涂层(n=45)与无涂层(n=41)CVC导管预防新生儿CVC CLABSI的RCT系统评价[24],两组在出院前和1岁矫正年龄时病死率差异均无统计学意义,银涂层组与无涂层组相比CLABSI发生率降低89%(RR=0.11,95%CI:0.01~0.87),留置时间(RR=2.3,95%CI:0.38~4.22)差异无统计学意义。
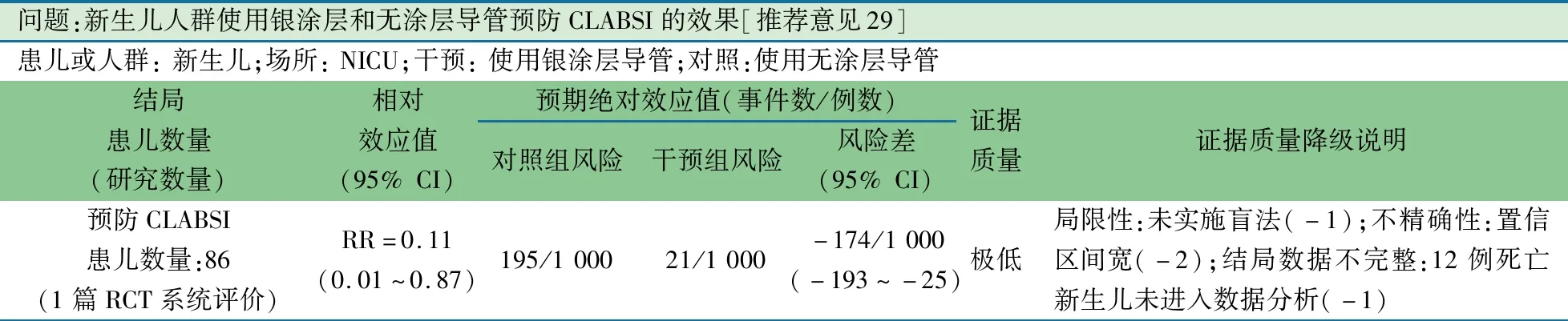
问题:新生儿人群使用银涂层和无涂层导管预防CLABSI的效果[推荐意见29]患儿或人群: 新生儿;场所: NICU;干预: 使用银涂层导管;对照:使用无涂层导管结局患儿数量 (研究数量)相对效应值(95% CI)预期绝对效应值(事件数/例数)对照组风险干预组风险风险差(95% CI)证据质量证据质量降级说明预防CLABSI患儿数量:86(1篇RCT系统评价)RR=0.11(0.01~0.87)195/1 00021/1 000-174/1 000(-193~-25)极低局限性:未实施盲法(-1);不精确性:置信区间宽(-2);结局数据不完整:12例死亡新生儿未进入数据分析(-1)
推荐意见(30) 肝素涂层较无涂层CVC导管预防导管相关性血栓优势不明显(1B)。
推荐说明 1篇2014年发表于Cochrane的关于肝素涂层(n=144)与无涂层(n=143) CVC用于0~18岁儿童后CVC导管相关性血栓的2项RCT的系统评价[25],肝素涂层组较无涂层组导管相关性血栓(彩色多普勒超声或静脉造影)发生率和置管后血小板减少症的发生率差异均无统计学意义。

问题: 儿科人群使用肝素涂层与无涂层导管预防导管相关血栓的效果比较[推荐意见30]患儿或人群:儿科;场所:医院;干预:使用肝素涂层导管;对照:使用无涂层导管结局患儿数量 (研究数量)相对效应值(95% CI)预期绝对效应值(事件数/千导管日)对照组风险干预组风险风险差(95% CI)证据质量证据质量降级说明预防导管相关性血栓患儿数量:144/143(2篇RCT的系统评价)RR=0.34(0.01~7.68)175/1 00059/1 000-116/1 0001)低不精确性:置信区间过宽(-2)

续表 置管后血小板减少症患儿数量:144/143(2篇RCT的系统评价)OR=0.73(0.38~1.39)133/1 00097/1 000-36/1 0001)中不精确性:置信区间宽(-1)
14.1.5.2 置管方法
推荐意见(31) 中心静脉置管推荐采用超声引导法进行穿刺(1C)。
推荐说明 基于1项队列研究和7项RCT[26-33]的超声引导和体表解剖标记穿刺置入CVC的系统评价/Meta分析,7项研究为颈内静脉置管,1项研究为股静脉置管。图12显示,超声引导置入CVC组和体表解剖标记穿刺组首次穿刺置管失败率分别为21.5%(96/447)和38.1%(171/449),OR=3.4(95%CI:1.2~9.7);图13显示,超声引导置入CVC组和体表解剖标记穿刺组穿刺相关并发症发生率分别为6.0%(27/447)和19.8%(89/449),OR=4.1(95%CI:1.3~12.8)。
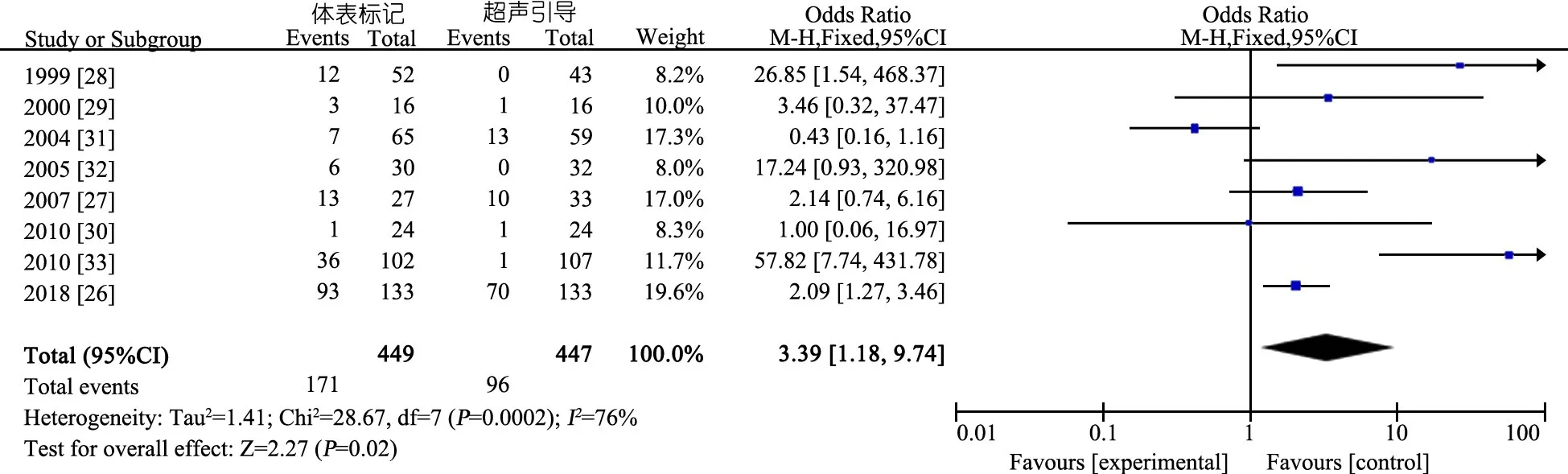
图12 体表解剖标记与超声引导穿刺比较中心静脉置管首次穿刺失败率
图13 体表解剖标记与超声引导穿刺比较中心静脉置管首次穿刺相关并发症
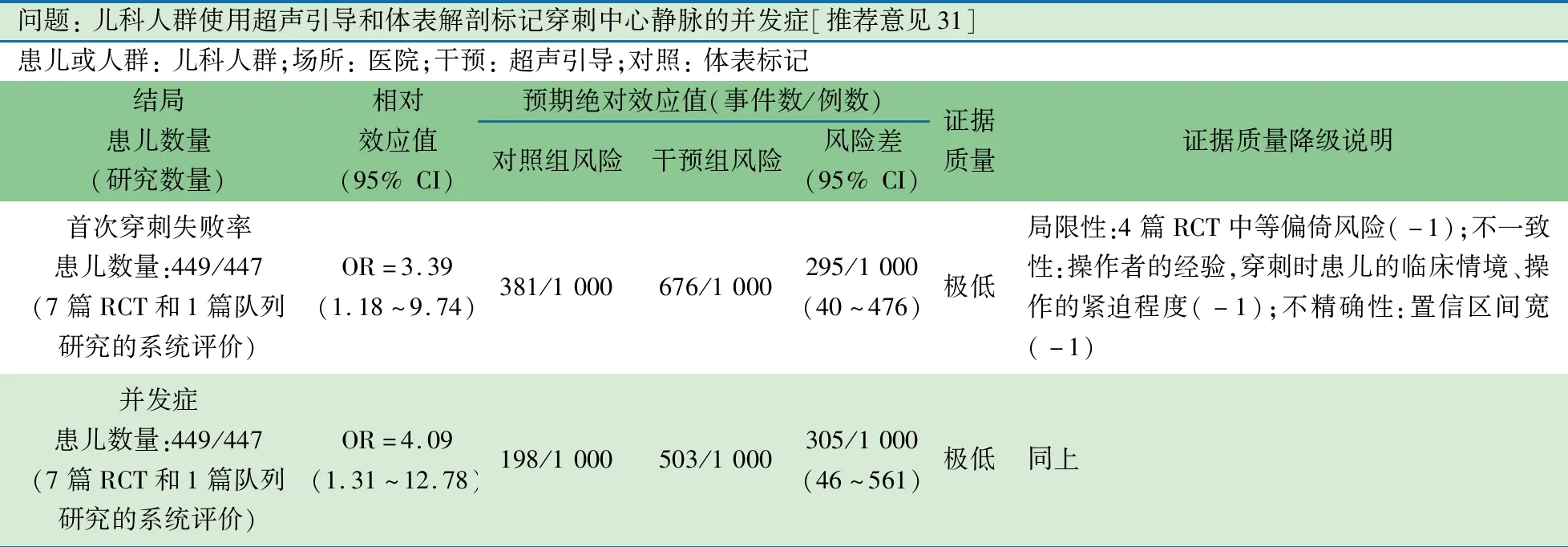
问题: 儿科人群使用超声引导和体表解剖标记穿刺中心静脉的并发症[推荐意见31]患儿或人群: 儿科人群;场所: 医院;干预: 超声引导;对照: 体表标记结局患儿数量 (研究数量)相对效应值(95% CI)预期绝对效应值(事件数/例数)对照组风险干预组风险风险差(95% CI)证据质量证据质量降级说明首次穿刺失败率患儿数量:449/447(7篇RCT和1篇队列研究的系统评价)OR=3.39(1.18~9.74)381/1 000676/1 000295/1 000(40~476)极低局限性:4篇RCT中等偏倚风险(-1);不一致性:操作者的经验,穿刺时患儿的临床情境、操作的紧迫程度(-1);不精确性:置信区间宽(-1)并发症患儿数量:449/447(7篇RCT和1篇队列研究的系统评价)OR=4.09(1.31~12.78)198/1 000503/1 000305/1 000(46~561)极低同上
推荐意见(32) 外周静脉穿刺选择超声引导时,没有显示出比通过体表标记穿刺有更高的成功率(2D)。
推荐说明 1项巴西单中心RCT[34],纳入12 d至17岁需要接受PIVC的外科择期手术患儿,PIVC穿刺方法为超声引导和体表标记(目测观察结合静脉触诊)。主要观察指标为置管成功率(置管有回血,推注生理盐水无不适)。335例患儿的382例次穿刺纳入分析。超声引导和体表标记成功率分别为85.6%(161/188例次)和91.8%(178/194例次)差异无统计学意义(P=0.059)。两组年龄、性别、营养状况、导致置管失败的临床倾向和治疗风险差异无统计学意义。
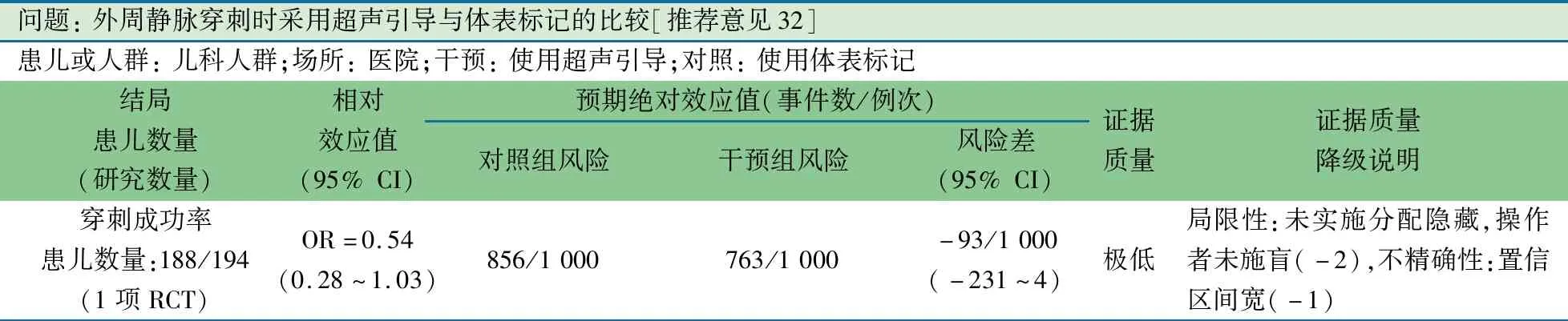
问题: 外周静脉穿刺时采用超声引导与体表标记的比较[推荐意见32]患儿或人群: 儿科人群;场所: 医院;干预: 使用超声引导;对照: 使用体表标记结局患儿数量 (研究数量)相对效应值(95% CI)预期绝对效应值(事件数/例次)对照组风险干预组风险风险差(95% CI)证据质量证据质量降级说明穿刺成功率患儿数量:188/194(1项RCT)OR=0.54(0.28~1.03)856/1 000763/1 000-93/1 000(-231~4)极低局限性:未实施分配隐藏,操作者未施盲(-2),不精确性:置信区间宽(-1)
推荐意见(33) 推荐床旁超声确定导管头端位置和CVC异位(1D)。
推荐说明 1项西班牙的单中心PICU中0~14岁需要CVC的非连续病例(n=40)[35],共置入51根CVC,置管后由有超声经验的医生即行床旁超声检查阅图,再行床旁X线胸片,由另1名PICU医生阅片。床旁超声和X线胸片区分导管头端位于心房内和心房外一致率94%(Cohen κ系数0.638),CVC异位一致率92%(Cohen κ系数0.670),差异均有统计学意义。床旁胸片X线测得的导管头端和上腔静脉与右心房交接处的距离大于超声测得值,MD=0.38 cm(95%CI:0.27~0.48),差异有统计学意义。
推荐意见(34) 建议置入静脉输液港港体位置位于锁骨下和第5肋间上(2D)。
推荐说明 1项美国单中心回顾性队列研究[36],纳入2007至2009年1~18岁外科置入和拨除TIVD的患儿,早期(<30 d)并发症:置管时出血、大血管损伤、气胸、伤口裂开;晚期(至拨除或再次手术更换港体)并发症:导管感染、移位、需要拔除港体的导管堵塞、渗漏、港体翻转;主要并发症:移位、再次手术更换港体。根据临床实际输液港皮下囊袋位置,归纳为SC(锁骨下,第5肋间上,167例)位置、LIM(沿胸壁外侧,第5肋间上,166例)位置和MIM(剑突,第5肋间下,46例)位置;在调整了手术年龄、性别、放置的侧和部位以及适应证后,LIM位置较SC位置,早期和晚期并发症发生率增加(OR=3.4,95%CI:2.0~5.8),港体移位发生率增加(OR=44.7,95%CI:11.9~167),再次手术更换港体发生率增加(OR=2.1,95%CI:1.1~3.8)。超重(BMI>25)是SC、LIM和MIM位置港体移位(OR=4.7,95%CI:1.2~18.2)和再次手术更换港体(OR=3.2,95%CI:1.1~9.3)的危险因素;在控制手术年龄、性别、BMI、放置侧和穿刺部位时,Cox比例风险回归分析发现,LIM位置是需要拔除导管的独立危险因素(OR=2.1,95%CI:1.2~3.7)。
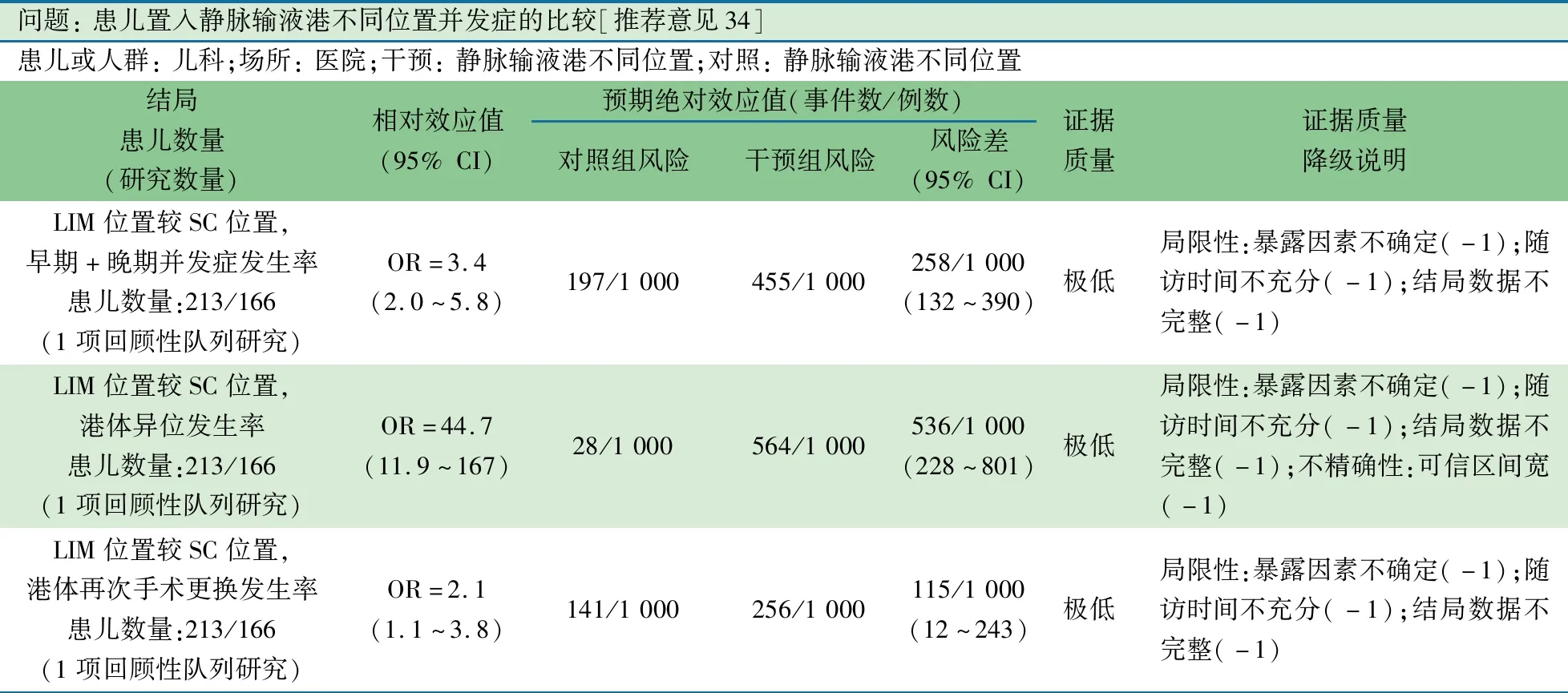
问题: 患儿置入静脉输液港不同位置并发症的比较[推荐意见34]患儿或人群: 儿科;场所: 医院;干预: 静脉输液港不同位置;对照: 静脉输液港不同位置结局患儿数量 (研究数量)相对效应值(95% CI)预期绝对效应值(事件数/例数)对照组风险干预组风险风险差(95% CI)证据质量证据质量降级说明LIM位置较SC位置,早期+晚期并发症发生率患儿数量:213/166(1项回顾性队列研究)OR=3.4(2.0~5.8)197/1 000455/1 000258/1 000(132~390)极低局限性:暴露因素不确定(-1);随访时间不充分(-1);结局数据不完整(-1)LIM位置较SC位置,港体异位发生率患儿数量:213/166(1项回顾性队列研究)OR=44.7(11.9~167)28/1 000564/1 000536/1 000(228~801)极低局限性:暴露因素不确定(-1);随访时间不充分(-1);结局数据不完整(-1);不精确性:可信区间宽(-1)LIM位置较SC位置,港体再次手术更换发生率患儿数量:213/166(1项回顾性队列研究)OR=2.1(1.1~3.8)141/1 000256/1 000115/1 000(12~243)极低局限性:暴露因素不确定(-1);随访时间不充分(-1);结局数据不完整(-1)
14.1.5.3 镇痛
推荐意见(35) 推荐穿刺置管前,局部使用或静脉给予麻醉药物,能舒缓患儿基于疼痛评分工具评估的疼痛(1B)。
推荐说明 1项来自美国9个中心的RCT[37],纳入在手背或肘窝区域进行静脉穿刺的3~18岁患儿,主要结局指标:3~7岁儿童采用Wong-Baker FACES量表,~18岁儿童VAS疼痛评分再转化为Wong-Baker FACES量表疼痛评分;次要结局指标:不良事件(穿刺和置管后即刻、15和30 min皮肤红斑、瘀点和出血)的发生。在穿刺或置管前1~3 min,干预组(n=269)局部喷利多卡因,对照组(n=266)喷安慰剂。两组性别、年龄、种族、操作种类差异均无统计学意义;干预组Wong-Baker FACES平均得分较安慰剂组降低了23%[(1.28±0.09)vs(1.67±0.09)],观察到-0.39(0.12)的镇痛效果,差异有统计学意义。
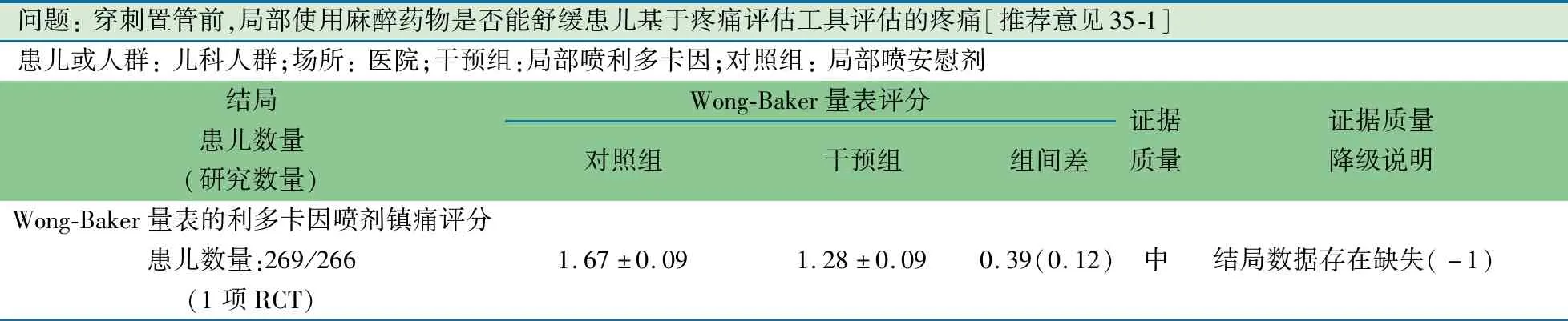
问题: 穿刺置管前,局部使用麻醉药物是否能舒缓患儿基于疼痛评估工具评估的疼痛[推荐意见35-1]患儿或人群: 儿科人群;场所: 医院;干预组:局部喷利多卡因;对照组: 局部喷安慰剂结局患儿数量 (研究数量)Wong-Baker量表评分对照组干预组组间差证据质量证据质量降级说明Wong-Baker量表的利多卡因喷剂镇痛评分患儿数量:269/266(1项RCT)1.67±0.091.28±0.09 0.39(0.12)中结局数据存在缺失(-1)
加拿大同一医院同一作者2006年和2007年RCT[38, 39],均以NICU早产儿为研究对象,2006年干预组为4%丁卡因凝胶(n=26),对照组为安慰剂(n=23);2007年在口服24%蔗糖水基础上,干预组为4%丁卡因凝胶(n=69),对照组为安慰剂(n=68);于置管前30 min在置管部位涂抹,录像记录穿刺置管准备时、过程中和恢复期3个时相新生儿面部表情,以PIPP疼痛量表为测量工具,主要结局指标:置管后第1 min PIPP量表疼痛评分;次要结局指标:置管后第2、3、4 min PIPP量表疼痛评分,第1、2、3、4、5、10 min的呼吸频率、血压、血氧饱和度。2个研究中2组出生体重、性别、胎龄、年龄、性别差异无统计学意义,主要、次要结局指标和不良事件差异均无统计学意义。
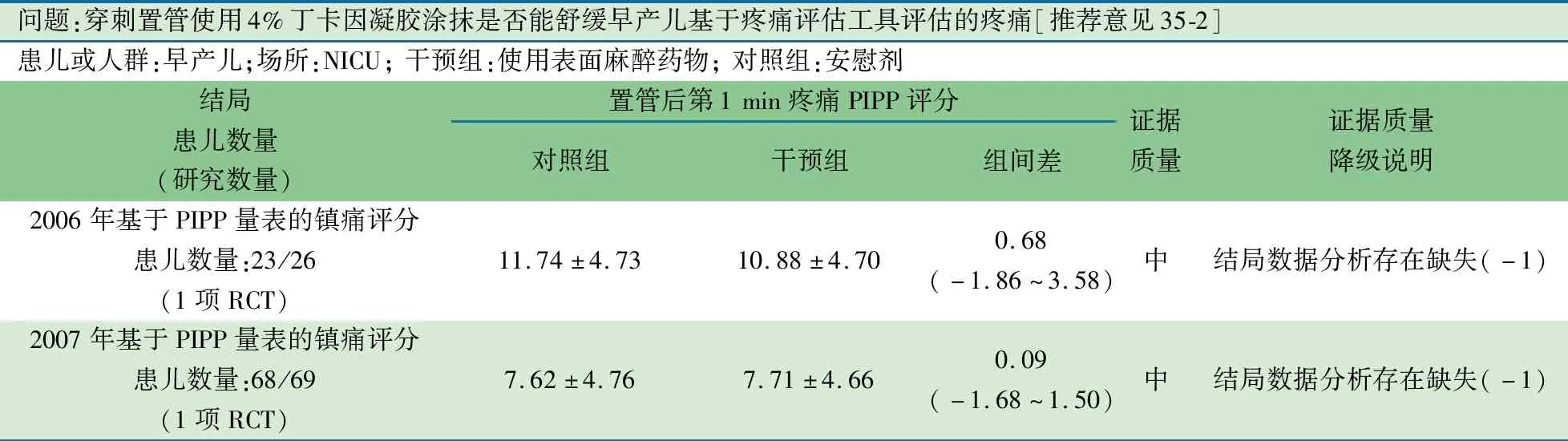
问题:穿刺置管使用4%丁卡因凝胶涂抹是否能舒缓早产儿基于疼痛评估工具评估的疼痛[推荐意见35-2]患儿或人群:早产儿;场所:NICU; 干预组:使用表面麻醉药物; 对照组:安慰剂结局患儿数量 (研究数量)置管后第1 min疼痛PIPP评分对照组干预组组间差证据质量证据质量降级说明2006年基于PIPP量表的镇痛评分患儿数量:23/26(1项RCT)11.74±4.7310.88±4.700.68(-1.86~3.58)中结局数据分析存在缺失(-1)2007年基于PIPP量表的镇痛评分患儿数量:68/69(1项RCT)7.62±4.767.71±4.660.09(-1.68~1.50)中结局数据分析存在缺失(-1)
1项加拿大2个中心参与的RCT[40],纳入在NICU接受无创呼吸支持且需置入CVC的新生儿:①对照组(不接受麻醉干预)20例,1例数据缺失;接受麻醉的新生儿由临床药师根据随机数字表分为3组;②外用组(4%丁卡因凝胶0.5 g)42例,1例置管取消、3例数据缺失;③静脉吗啡组(0.1 mg·kg-1)38例,3例数据缺失;④合用组(外用+静脉吗啡)31例,3例置管取消,3例数据缺失。录像记录穿刺置管准备时、过程中和恢复期3个时相新生儿面部表情,以PIPP疼痛量表为测量工具,主要观察指标:置管准备时、过程中的面部表情评分,(1)准备时:③vs①、④vs①、②vs③、②vs④组间差0.22~0.30,差异均有统计学意义;(2)过程中:③vs①、④vs①、④vs②组间差0.20~0.35,组间差异均有统计学意义。
1项加拿大单中心RCT[41],纳入NICU住院、胎龄≥27周、生长发育与胎龄相符、接受非紧急PICC穿刺的新生儿,临床药师根据随机数字表将其随机分配到干预组(丁卡因软膏,n=23)和对照组(安慰软膏,n=26),录像记录穿刺置管准备时、过程中和恢复期3个时相新生儿面部表情,PIPP疼痛量表作为结局评价工具,PICC置管前30 min软膏涂抹穿刺部位,主要观察指标为PICC置管时疼痛评分。两组胎龄、出生体重、性别、年龄、体重、生后1和5 min Apgar评分、新生儿急性生理评分、最近1次接受疼痛操作时间、最近1次接受镇痛药物时间和PICC置管时PIPP疼痛量表评分差异均无统计学意义。
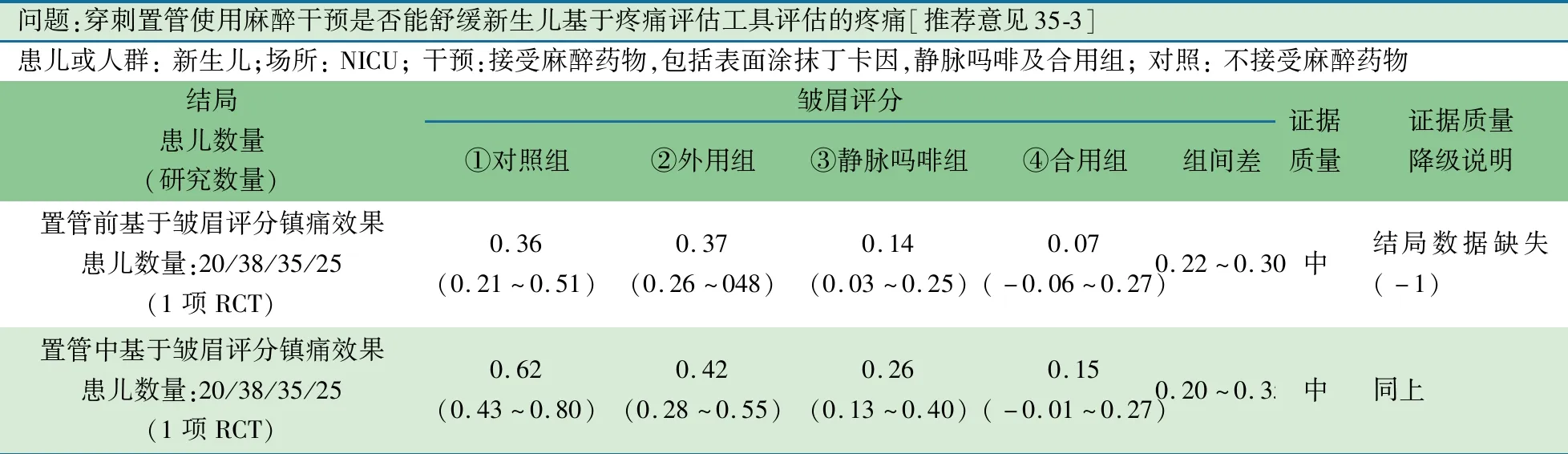
问题:穿刺置管使用麻醉干预是否能舒缓新生儿基于疼痛评估工具评估的疼痛[推荐意见35-3]患儿或人群: 新生儿;场所: NICU; 干预:接受麻醉药物,包括表面涂抹丁卡因,静脉吗啡及合用组; 对照: 不接受麻醉药物结局患儿数量 (研究数量)皱眉评分①对照组②外用组③静脉吗啡组④合用组组间差证据质量证据质量降级说明置管前基于皱眉评分镇痛效果患儿数量:20/38/35/25(1项RCT)0.36(0.21~0.51)0.37(0.26~048)0.14(0.03~0.25)0.07(-0.06~0.27)0.22~0.30中结局数据缺失(-1)置管中基于皱眉评分镇痛效果患儿数量:20/38/35/25(1项RCT)0.62(0.43~0.80)0.42(0.28~0.55)0.26(0.13~0.40)0.15(-0.01~0.27)0.20~0.35中同上
14.1.6 血管通路装置穿刺部位
推荐意见(36) 基于NICU患儿CLABSI发生事件,建议选择下肢非股静脉置入PICC(2C)。
推荐说明 4项病例对照研究的系统评价/Meta分析[42-45],纳入NICU住院期间经上肢静脉(头静脉、贵要静脉、腋静脉)和下肢非股静脉(大、小隐静脉等)置入PICC的新生儿,观察PICC CLABSI发生率,上肢静脉和下肢非股静脉CLABSI发生率分别为165/27 849导管日和46/11 579导管日。图14显示,上肢静脉是下肢非股静脉CLABSI发生率的1.5倍(OR=1.49,95%CI:1.06~2.07)。
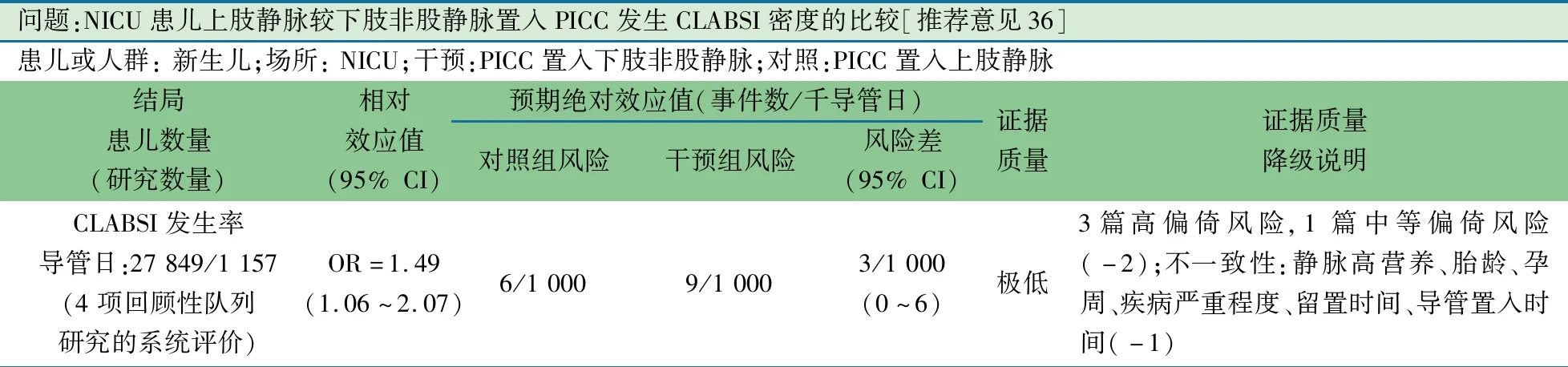
问题:NICU患儿上肢静脉较下肢非股静脉置入PICC发生CLABSI密度的比较[推荐意见36]患儿或人群: 新生儿;场所: NICU;干预:PICC置入下肢非股静脉;对照:PICC置入上肢静脉结局患儿数量 (研究数量)相对效应值(95% CI)预期绝对效应值(事件数/千导管日)对照组风险干预组风险风险差(95% CI)证据质量证据质量降级说明CLABSI发生率导管日:27 849/1 157(4项回顾性队列研究的系统评价)OR=1.49(1.06~2.07)6/1 0009/1 0003/1 000(0~6)极低3篇高偏倚风险,1篇中等偏倚风险(-2);不一致性:静脉高营养、胎龄、孕周、疾病严重程度、留置时间、导管置入时间(-1)
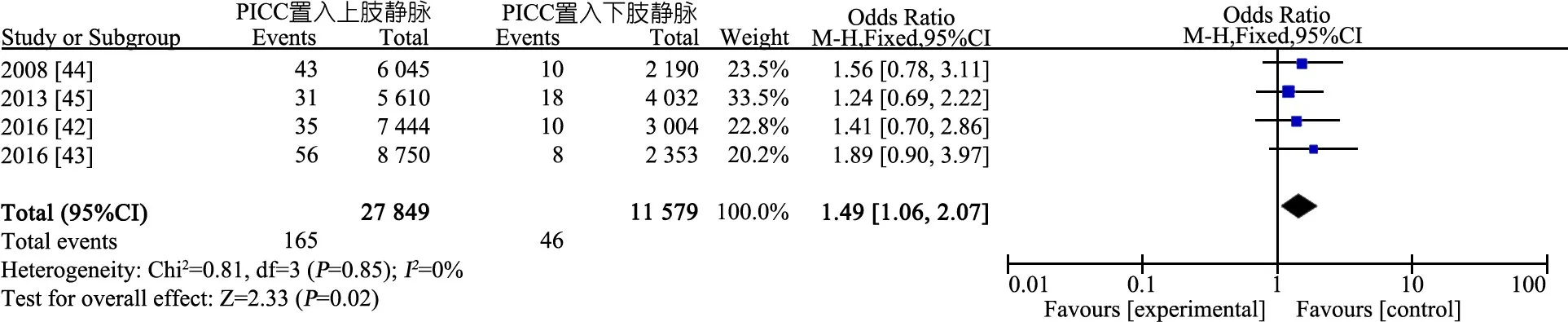
图14 PICC置入上肢静脉较下肢非股静脉CLABSI发生率的系统评价和Meta分析
推荐意见(37) 基于CLABSI风险,不建议院外转运过程中非隧道式CVC置管(2D)。
推荐说明 1项单中心回顾性队列研究[46],纳入PICU中置入CVC的0~11岁连续病例的382根导管[其中院内置管245根,院外置管137根(指转运前和转运中置管)],在未调整病例的诊断、来源科室、儿童死亡指数、导管穿刺部位和导管类型的情况下,院外置管CLABSI风险是院内置管的2.65倍(OR=2.65,95%CI:1.18~5.96)。
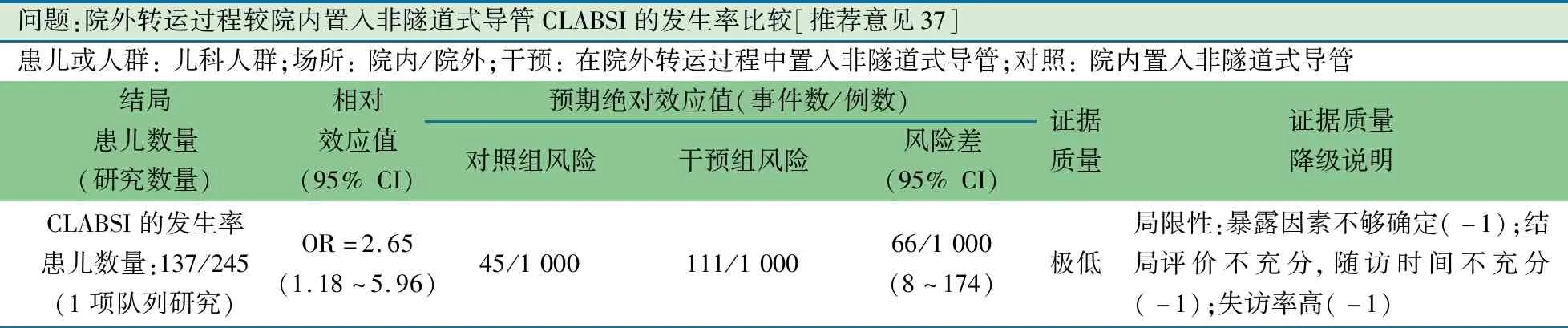
问题:院外转运过程较院内置入非隧道式导管CLABSI的发生率比较[推荐意见37]患儿或人群: 儿科人群;场所: 院内/院外;干预: 在院外转运过程中置入非隧道式导管;对照: 院内置入非隧道式导管结局患儿数量 (研究数量)相对效应值(95% CI)预期绝对效应值(事件数/例数)对照组风险干预组风险风险差(95% CI)证据质量证据质量降级说明CLABSI的发生率患儿数量:137/245(1项队列研究)OR=2.65(1.18~5.96)45/1 000111/1 00066/1 000(8~174)极低局限性:暴露因素不够确定(-1);结局评价不充分,随访时间不充分(-1);失访率高(-1)
推荐意见(38) 基于CLABSI风险,头臂静脉是非隧道式CVC导管置管静脉选项之一(2D)。
推荐说明 1项2018年来自法国单中心PICU[47]和西班牙单中心(NICU中出生体重<1 500 g且胎龄<34周的早产儿)[48]回顾性队列研究的系统评价/Meta分析,纳入在住院期间置入的非血液透析和血液滤过干预的CVC导管,分为头臂静脉置管和其他部位置管,观察不同置管部位CLABSI发生事件数。头臂静脉置管(6/2 114导管日)较其他部位置管(24/1 780导管日)CLABSI发生率下降76%(OR=0.24,95%CI:0.09~0.62),差异有统计学意义。

问题:儿童留置CVC时,头臂静脉与其他部位静脉比较CLABSI事件发生率[推荐意见38]患儿或人群: 儿科人群;场所: NICU/PICU;干预:头臂静脉穿刺CVC;对照: 其他静脉穿刺结局患儿数量 (研究数量)相对效应值(95% CI)预期绝对效应值(事件数/千导管日)对照组风险干预组风险风险差(95% CI)证据质量证据质量降级说明CLABSI发生率患儿数量:168/185(2项回顾性队列研究)OR=0.24(0.09~0.62)13/1 0003/1 000-10/1 000(-12~-5)极低局限性:均为高偏倚风险(-2);不精确性:置信区间宽(-2);不一致性:研究人群、疾病种类、置管方法不一致(-1)
14.2 血管通路的拔除
推荐意见(39) NICU中革兰阳性菌或革兰阴性菌所致的CLABSI早比晚拔管对处理脓毒症更有益。儿科人群中硅胶PICC中导管体外断裂后可选择修复,金黄色葡萄球菌属所致疑似CLABSI可尝试导管挽救(1C)。
推荐说明 基于加拿大1家三级儿童医院2010至2014年医疗影像系统、血管通路数据库(VAS)和介入放射数据库中的所有CVC数据[49],选取0~18岁留置PICC 30 d后发生第1次导管体外断裂的病例。主要观察指标:①PICC导管体外断裂后修复的成功率,②修复和原位换管后30 d内CLABSI的发生率。发生体外断裂的PICC导管共235根,采用修复处理161根,修复成功116根(72%),修复成功导管发生CLABSI 38.8%(45/116),直接拔除19根,采用直接原位换管74根,55例成功(74%), 直接原位换管成功后发生CLABSI 60%(33/55),在调整了使用抗生素情况后,直接原位换管发生CLABSI的风险是体外断裂后再修复的4倍(OR=3.9,95% CI:1.1~14.0),差异有统计学意义。
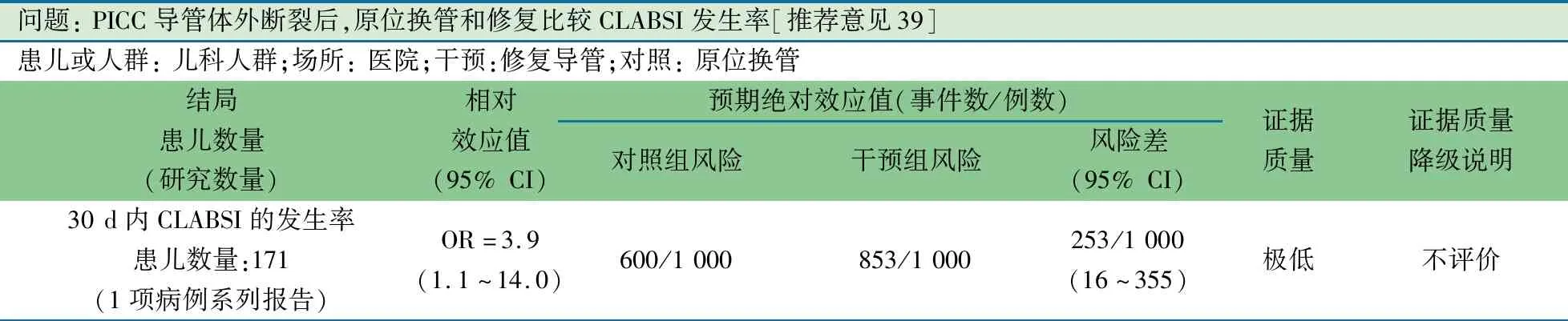
问题: PICC导管体外断裂后,原位换管和修复比较CLABSI发生率[推荐意见39]患儿或人群: 儿科人群;场所: 医院;干预:修复导管;对照: 原位换管结局患儿数量 (研究数量)相对效应值(95% CI)预期绝对效应值(事件数/例数)对照组风险干预组风险风险差(95% CI)证据质量证据质量降级说明30 d内CLABSI的发生率患儿数量:171(1项病例系列报告)OR=3.9(1.1~14.0)600/1 000853/1 000253/1 000(16~355)极低不评价
1项病例系列报告[50]纳入美国的2012至2015年从医院病历系统中筛选的年龄≤20岁、有1或多个金黄色葡萄球菌属血液培养阳性且CVC留置时间比发生血培养阳性的时间长48 h的连续病例,排除真菌性CLABSI和在血培养阳性结果12 h内死亡病例,由临床医生决定选择挽救导管治疗(抗生素封管、酒精封管、静脉抗生素治疗)和拔管。56/77例(72.7%)患儿置入的59根导管实施了挽救措施,44/56例(78.6%)挽救成功,21/77例(27.3%)直接拔管。
1项中国台湾单中心回顾性队列研究[51]纳入2001至2007年NICU首次发生BSI的早产儿,排除真菌感染、医生诊断脓毒症前死亡、早发型败血症者(生后7 d内脓毒症)。以早期拔管(脓毒症和血培养出现后≤3 d拔除PICC)和晚期拔管作为暴露因素。脓毒症发作后保留或移除PICC的决定是由新生儿主治医生或值班的高年住院医生做出。护士使用PICC时常规记录:置管部位、置管日期、发生BSI时的导管管理、拔除(更换)导管至与脓毒症相关的临床指标好转天数。观察指标:①早和晚拔管与脓毒症相关的临床指标缓解率,②第1次脓毒症相关的临床指标缓解后7~30 d由另外1个病原菌导致的第2次脓毒症(二次脓毒症),③上述2个指标的革兰阳性菌与革兰阴性菌感染的亚组分析。早期拔管99例,晚期拔管135例。早和晚拔管人群确诊脓毒症年龄差异有统计学意义,一般情况和新生儿治疗干预评分系统(呼吸、心血管、药物治疗、监护、营养状况、输液、治疗过程、输液装置种类中的60个条目) 等差异均无统计学意义。早比晚拔管的缓解率OR=1.41(95%CI:1.19~1.68),革兰阳性菌感染时早较晚拔管缓解率OR=1.24(95%CI:1.02~1.51) , 革兰阴性菌感染时早较晚拔管缓解率OR=1.77(95%CI:1.26~2.51);总体早比晚拔管的二次脓毒症发生率OR=0.24(95%CI:0.08~0.66)。
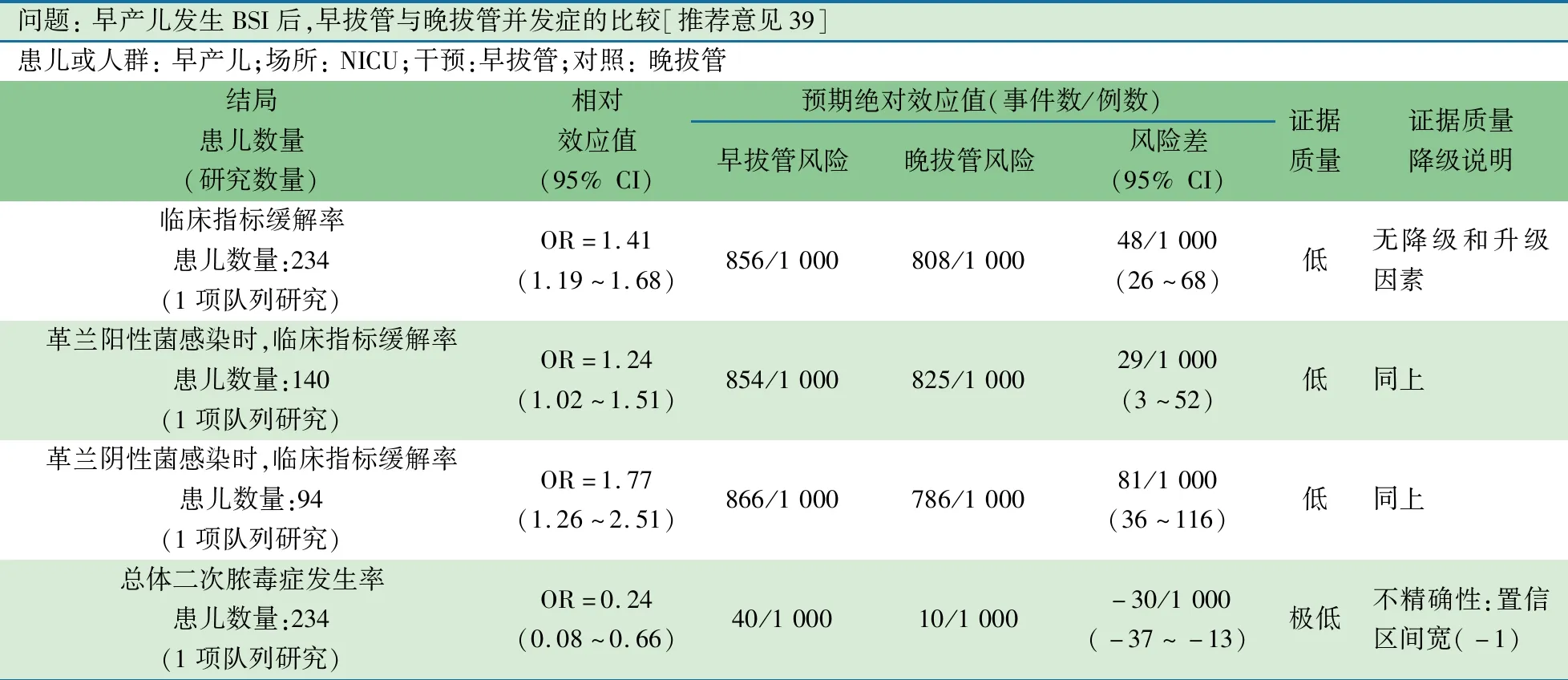
问题: 早产儿发生BSI后,早拔管与晚拔管并发症的比较[推荐意见39]患儿或人群: 早产儿;场所: NICU;干预:早拔管;对照: 晚拔管结局患儿数量 (研究数量)相对效应值(95% CI)预期绝对效应值(事件数/例数)早拔管风险晚拔管风险风险差(95% CI)证据质量证据质量降级说明临床指标缓解率患儿数量:234(1项队列研究)OR=1.41(1.19~1.68)856/1 000808/1 00048/1 000(26~68)低无降级和升级因素 革兰阳性菌感染时,临床指标缓解率患儿数量:140(1项队列研究)OR=1.24(1.02~1.51)854/1 000825/1 00029/1 000(3~52)低同上革兰阴性菌感染时,临床指标缓解率患儿数量:94(1项队列研究)OR=1.77(1.26~2.51)866/1 000786/1 00081/1 000(36~116)低同上总体二次脓毒症发生率患儿数量:234(1项队列研究)OR=0.24(0.08~0.66)40/1 00010/1 000-30/1 000(-37~-13)极低不精确性:置信区间宽(-1)
推荐意见(40) UVC置管留置14 d和至多28 d相比,不增加BSI发生风险(2B)。
推荐说明 2017年发表于Cochrane的基于1篇RCT的关于早期计划拔除UVC预防感染的系统评价[52],纳入留置UVC的新生儿,预计早期拔管组置管后14 d内计划移除UVC,预期管理组为允许留置UVC至少比干预组长7 d,或者未提前计划拔除时间是因临床情形拔除(因疑似或确诊BSI,或不再需要而拔管)。主要结局指标为BSI,次要结局指标为新生儿病死率等。早期拔管组(n=106)较预期管理组(n=104)BSI发生率差异无统计学意义(RR=0.65,95%CI:0.35~1.22),新生儿出院病死率差异无统计学意义(RR=1.12,95%CI:0.42~2.98)。
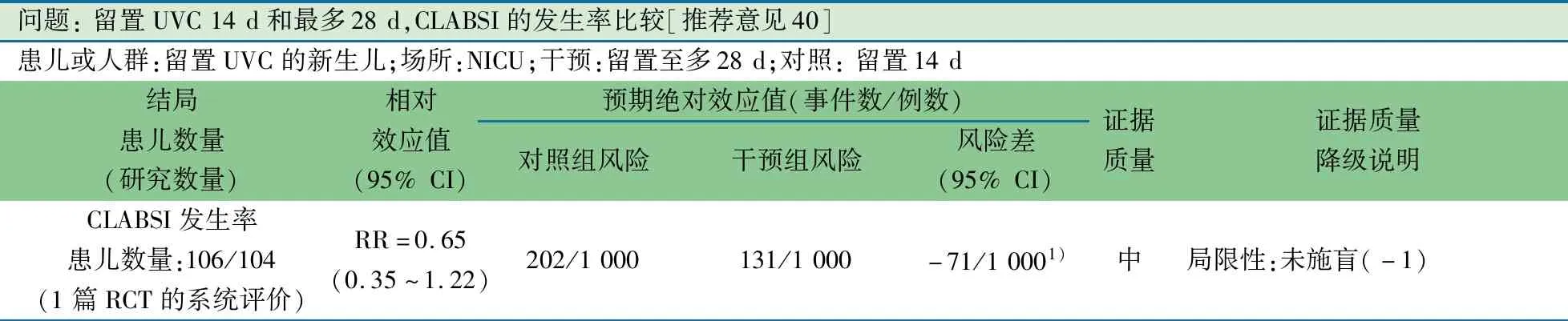
问题: 留置UVC 14 d和最多28 d,CLABSI的发生率比较[推荐意见40]患儿或人群:留置UVC的新生儿;场所:NICU;干预:留置至多28 d;对照: 留置14 d结局患儿数量 (研究数量)相对效应值(95% CI)预期绝对效应值(事件数/例数)对照组风险干预组风险风险差(95% CI)证据质量证据质量降级说明CLABSI发生率患儿数量:106/104(1篇RCT的系统评价)RR=0.65(0.35~1.22)202/1 000131/1 000-71/1 0001)中局限性:未施盲(-1)
14.3 拔管过程中的相关技术
推荐意见(41) 推荐采用JBI证据总结(2019)中的CVAD拔管过程的技术要点(2D)。
推荐说明 移除中心静脉导管要点:①PLT>50×109·L-1,INR<1.5;②患儿处于仰卧位;③移除导管时,指导患儿行Valsalva动作;④导管拔除后于穿刺点处覆盖闭合性敷料;⑤导管拔除后应检查导管的完整性;⑥怀疑导管相关血流感染,应做导管头端培养;⑦;出现拔管困难,应联系血管外科和介入专家以寻求建议[8, 53]。
15 血管通路使用和维护
15.1 有效冲管和封管
推荐意见(42) 一次性预充式注射器冲管较常规注射器抽取生理盐水冲管能明显降低CLABSI发生率(2D)。
推荐说明 1项土耳其2018年的单中心RCT[54],纳入血液肿瘤科住院使用TcCVAD或TIVD输液的0~18岁患儿,排除住院时间<48 h、最近48 h内血培养回报有细菌生长的患儿。干预组(n=23)为一次性预充式注射器冲管,对照组(n=25)为常规注射器生理盐水冲管;主要结局指标为CLABSI,次要结局指标为导管堵塞(不能抽血、血流迟缓和/或不能通过CVC冲管或输液);两组年龄、疾病诊断和导管类型差异均无统计学意义。干预组与对照组间CLABSI发生率(1.9/1 000导管日vs10.1/1 000导管日)差异有统计学意义,导管堵塞的发生率(1.9/1 000导管日vs5.6/1 000导管日)差异无统计学意义。
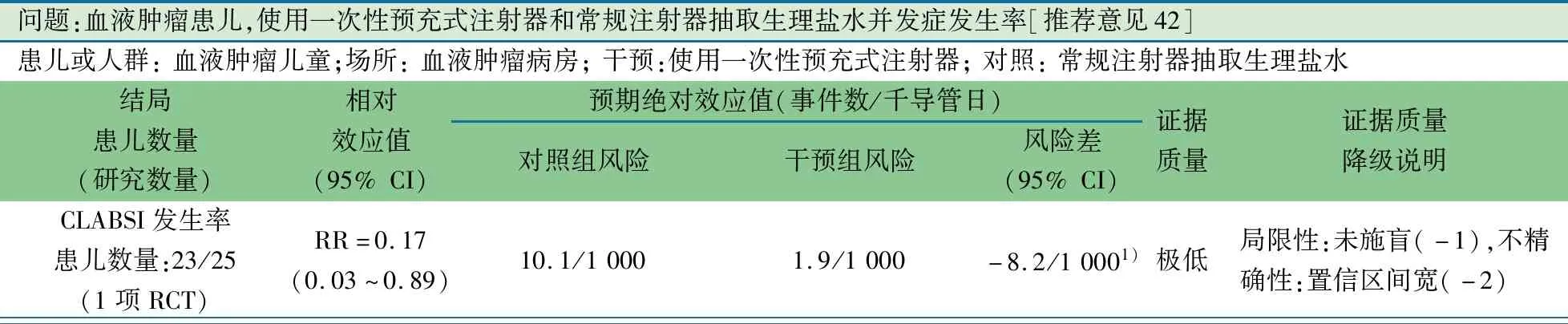
问题:血液肿瘤患儿,使用一次性预充式注射器和常规注射器抽取生理盐水并发症发生率[推荐意见42]患儿或人群: 血液肿瘤儿童;场所: 血液肿瘤病房; 干预:使用一次性预充式注射器; 对照: 常规注射器抽取生理盐水结局患儿数量 (研究数量)相对效应值(95% CI)预期绝对效应值(事件数/千导管日)对照组风险干预组风险风险差(95% CI)证据质量证据质量降级说明CLABSI发生率患儿数量:23/25(1项RCT)RR=0.17(0.03~0.89)10.1/1 0001.9/1 000-8.2/1 0001)极低局限性:未施盲(-1),不精确性:置信区间宽(-2)

续表 导管堵塞发生率患儿数量:23/25(1项RCT)RR=0.38(0.07~2.19)5.6/1 0001.9/1 000-3.7/1 0001)极低同上
推荐意见(43) 建议采用牛磺罗定、乙醇、抗生素和尿激酶封管液预防CLABSI(2D)。
推荐说明 2020年发表于《中国循证儿科杂志》的抗菌药物封管对留置CVC患儿降低导管相关血流感染发生风险的系统评价/Meta 分析[55],基于29 篇不同封管液(乙醇、牛磺罗定、尿激酶和抗生素)预防CLABSI或CRBSI或BSI的发生风险总的RR=0.36(95%CI:0.27~0.46),绝对效应值为每1 000个CVAD导管日可减少2例CLABSI或CRBSI或BSI事件数,其中8篇RCT为抗生素封管液,RR=0.48(95%CI:0.26~0.87);3篇RCT为尿激酶封管,RR=0.71(95%CI:0.53~0.95);10篇为乙醇封管,RR=0.31(95%CI:0.22~0.43);8篇为牛磺罗定封管,RR=0.27(95%CI:0.14~0.50)。1篇以盐酸封管治疗CLABSI或CRBSI或BSI的发生风险事件,RR=0.84(95%CI:0.52~1.37)。
对高危人群采用抗菌药物封管是有作用的,可实现将高浓度药物封管在导管中,同时不会使机体系统暴露于高浓度药物中。抗菌药物封管的效果可能被过分夸大了,体现在:①CLABSI的概念较为宽泛,特别是包括了BSI;②不同文献CLABSI诊断中包括可能、疑似和确定感染;③不同抗菌药物封管液的预防人群包括了CLABSI高风险和低风险人群;④发表偏倚非常明显,存在不同抗菌药物封管液的预防阴性结果未发表的可能性;⑤总体文献质量极低。对结论信心不足,进一步研究极有可能影响该疗效评估结果的可信度。
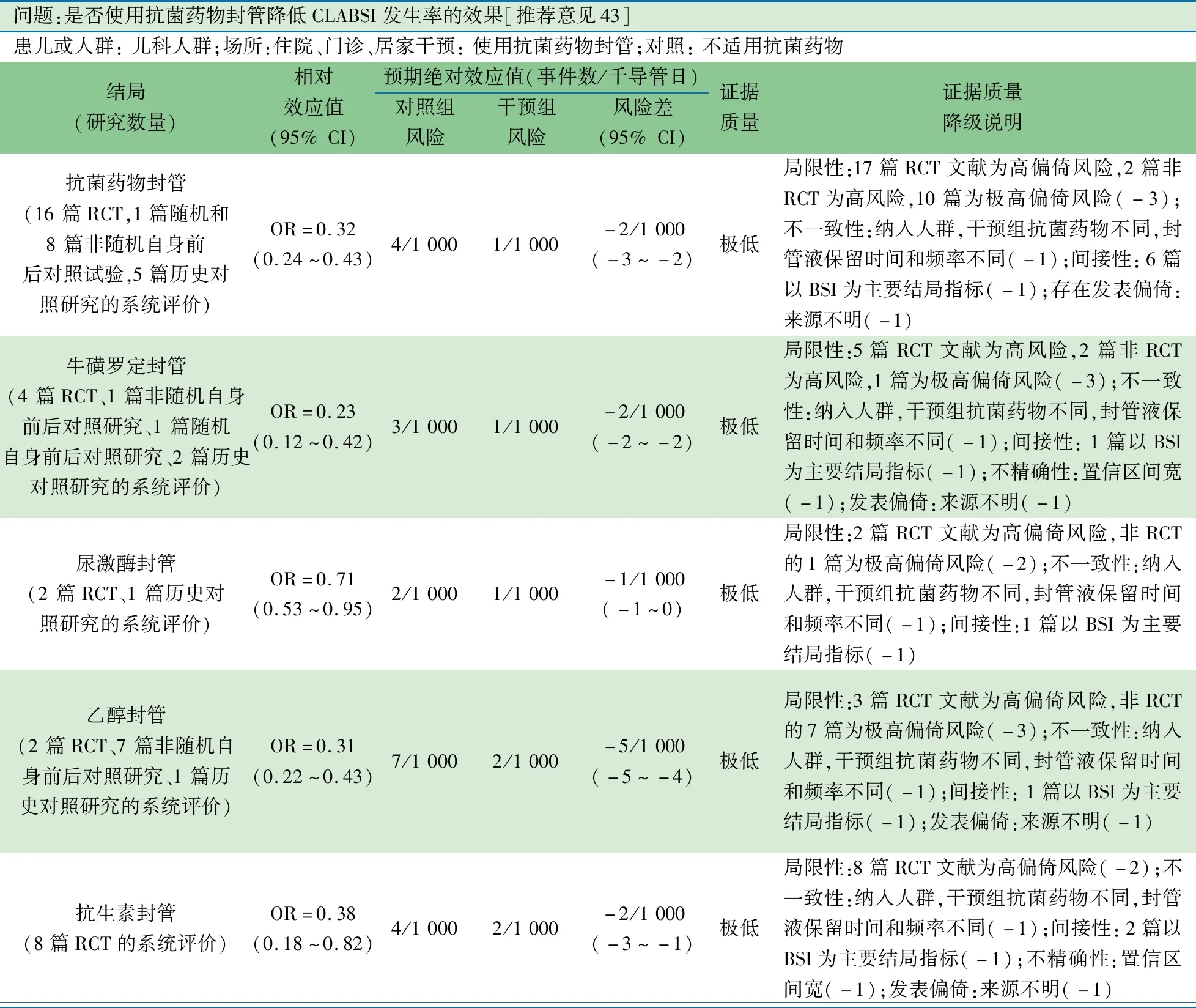
问题:是否使用抗菌药物封管降低CLABSI发生率的效果[推荐意见43]患儿或人群: 儿科人群;场所:住院、门诊、居家干预: 使用抗菌药物封管;对照: 不适用抗菌药物结局 (研究数量)相对效应值(95% CI)预期绝对效应值(事件数/千导管日)对照组风险干预组风险风险差(95% CI)证据质量证据质量降级说明抗菌药物封管(16 篇RCT,1篇随机和8 篇非随机自身前后对照试验,5篇历史对照研究的系统评价)OR=0.32(0.24~0.43)4/1 0001/1 000-2/1 000(-3~-2)极低局限性:17篇RCT文献为高偏倚风险,2篇非RCT为高风险,10篇为极高偏倚风险(-3);不一致性:纳入人群,干预组抗菌药物不同,封管液保留时间和频率不同(-1);间接性: 6篇以BSI为主要结局指标(-1);存在发表偏倚:来源不明(-1)牛磺罗定封管(4 篇RCT、1 篇非随机自身前后对照研究、1 篇随机自身前后对照研究、2 篇历史对照研究的系统评价)OR=0.23(0.12~0.42)3/1 0001/1 000-2/1 000(-2~-2)极低局限性:5篇RCT文献为高风险,2篇非RCT为高风险,1篇为极高偏倚风险(-3);不一致性:纳入人群,干预组抗菌药物不同,封管液保留时间和频率不同(-1);间接性: 1篇以BSI为主要结局指标(-1);不精确性:置信区间宽(-1);发表偏倚:来源不明(-1)尿激酶封管(2 篇RCT、1 篇历史对照研究的系统评价)OR=0.71(0.53~0.95)2/1 0001/1 000-1/1 000(-1~0)极低局限性:2篇RCT文献为高偏倚风险,非RCT的1篇为极高偏倚风险(-2);不一致性:纳入人群,干预组抗菌药物不同,封管液保留时间和频率不同(-1);间接性:1篇以BSI为主要结局指标(-1)乙醇封管(2 篇RCT、7 篇非随机自身前后对照研究、1 篇历史对照研究的系统评价)OR=0.31(0.22~0.43)7/1 0002/1 000-5/1 000(-5~-4)极低局限性:3篇RCT文献为高偏倚风险,非RCT的7篇为极高偏倚风险(-3);不一致性:纳入人群,干预组抗菌药物不同,封管液保留时间和频率不同(-1);间接性: 1篇以BSI为主要结局指标(-1);发表偏倚:来源不明(-1)抗生素封管(8篇RCT的系统评价)OR=0.38(0.18~0.82)4/1 0002/1 000-2/1 000(-3~-1)极低局限性:8篇RCT文献为高偏倚风险(-2);不一致性:纳入人群,干预组抗菌药物不同,封管液保留时间和频率不同(-1);间接性: 2篇以BSI为主要结局指标(-1);不精确性:置信区间宽(-1);发表偏倚:来源不明(-1)
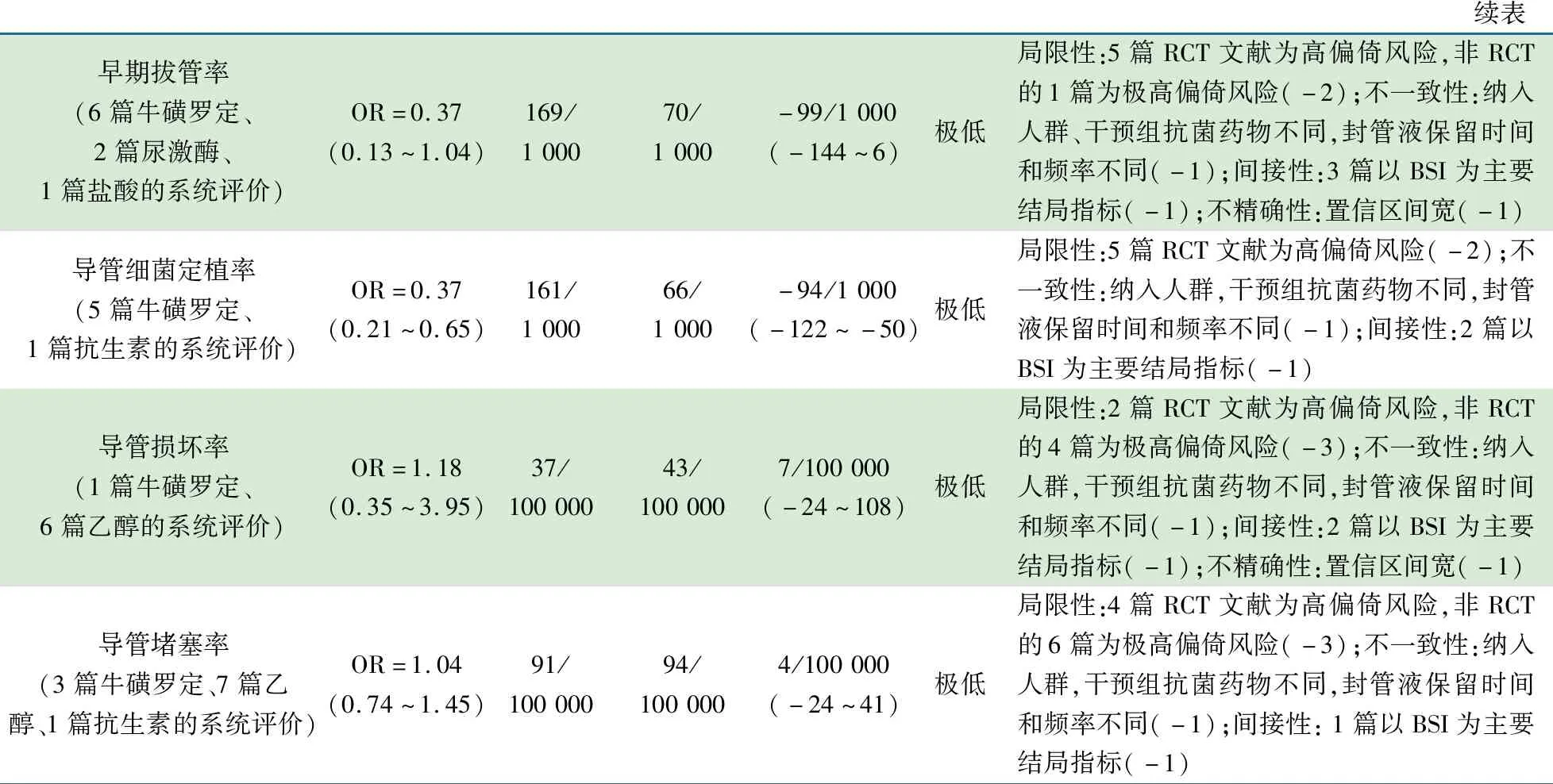
续表 早期拔管率(6篇牛磺罗定、2篇尿激酶、1篇盐酸的系统评价)OR=0.37(0.13~1.04)169/1 00070/1 000-99/1 000(-144~6)极低局限性:5篇RCT文献为高偏倚风险,非RCT的1篇为极高偏倚风险(-2);不一致性:纳入人群、干预组抗菌药物不同,封管液保留时间和频率不同(-1);间接性:3篇以BSI为主要结局指标(-1);不精确性:置信区间宽(-1)导管细菌定植率(5篇牛磺罗定、1篇抗生素的系统评价)OR=0.37(0.21~0.65)161/1 00066/1 000-94/1 000(-122~-50)极低局限性:5篇RCT文献为高偏倚风险(-2);不一致性:纳入人群,干预组抗菌药物不同,封管液保留时间和频率不同(-1);间接性:2篇以BSI为主要结局指标(-1)导管损坏率(1篇牛磺罗定、6篇乙醇的系统评价)OR=1.18(0.35~3.95)37/100 00043/100 0007/100 000(-24~108)极低局限性:2篇RCT文献为高偏倚风险,非RCT的4篇为极高偏倚风险(-3);不一致性:纳入人群,干预组抗菌药物不同,封管液保留时间和频率不同(-1);间接性:2篇以BSI为主要结局指标(-1);不精确性:置信区间宽(-1)导管堵塞率(3篇牛磺罗定、7篇乙醇、1篇抗生素的系统评价)OR=1.04(0.74~1.45)91/100 00094/100 0004/100 000(-24~41)极低局限性:4篇RCT文献为高偏倚风险,非RCT的6篇为极高偏倚风险(-3);不一致性:纳入人群,干预组抗菌药物不同,封管液保留时间和频率不同(-1);间接性: 1篇以BSI为主要结局指标(-1)
推荐意见(44) 抗生素锁合并系统抗生素治疗CLABSI效果不明显(1C)。
推荐说明 2013年发表于Cochrane基于2项RCT、1项非RCT关于应用抗生素锁合并其他封管锁治疗肿瘤儿童留置TcCVAD相关性感染的系统评价[56]。纳入<18岁留置TcCVAD的肿瘤儿童,2篇RCT为尿激酶联合与不联合系统抗生素,1篇非RCT为乙醇锁联合与不联合系统抗生素,尿激酶/乙醇+系统抗生素组与系统抗生素治疗组CLABSI的治愈率(RR=1.05,95%CI:0.63~1.77)、重复感染率(RR=0.97,95%CI:0.35~2.68)和过早移除导管率(RR=0.85,95%CI:0.71~1.01)差异均无统计学意义。
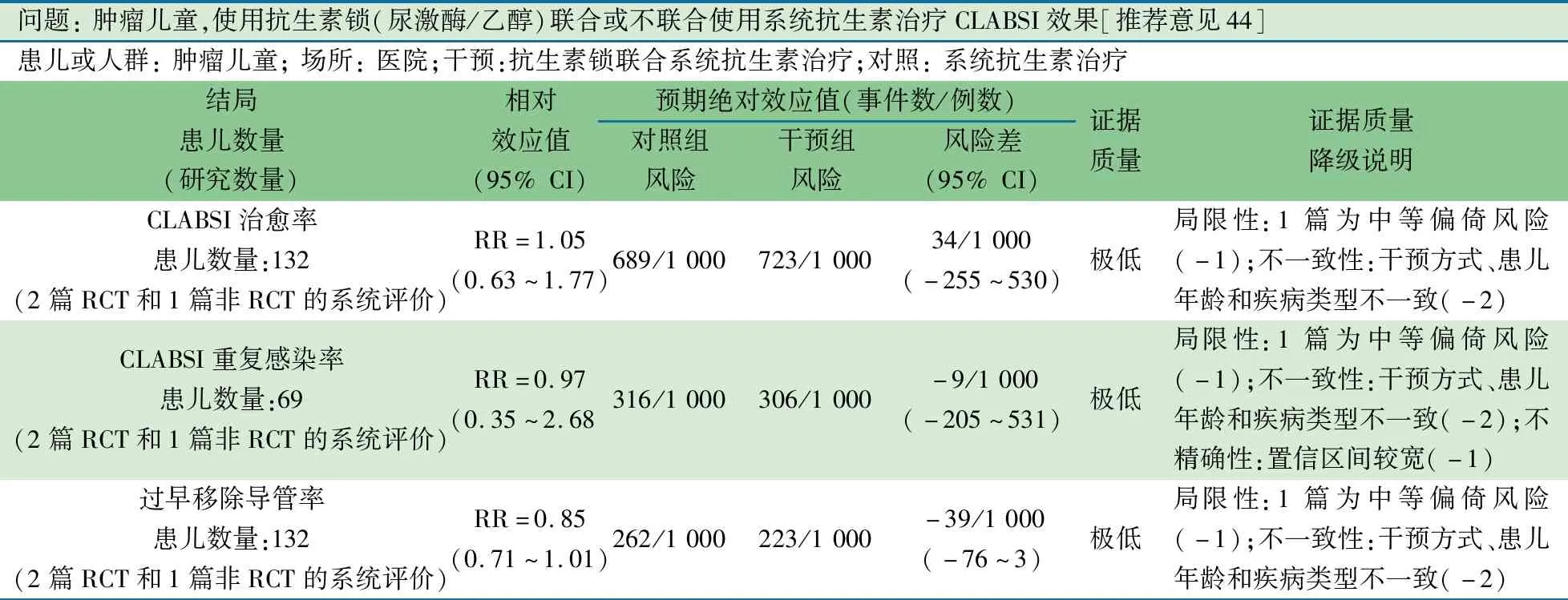
问题: 肿瘤儿童,使用抗生素锁(尿激酶/乙醇)联合或不联合使用系统抗生素治疗CLABSI效果[推荐意见44]患儿或人群: 肿瘤儿童; 场所: 医院;干预:抗生素锁联合系统抗生素治疗;对照: 系统抗生素治疗结局患儿数量 (研究数量)相对效应值(95% CI)预期绝对效应值(事件数/例数)对照组风险干预组风险风险差(95% CI)证据质量证据质量降级说明CLABSI治愈率患儿数量:132(2篇RCT和1篇非RCT的系统评价)RR=1.05(0.63~1.77)689/1 000723/1 00034/1 000(-255~530)极低局限性:1篇为中等偏倚风险(-1);不一致性:干预方式、患儿年龄和疾病类型不一致(-2)CLABSI重复感染率患儿数量:69(2篇RCT和1篇非RCT的系统评价)RR=0.97(0.35~2.68)316/1 000306/1 000-9/1 000(-205~531)极低局限性:1篇为中等偏倚风险(-1);不一致性:干预方式、患儿年龄和疾病类型不一致(-2);不精确性:置信区间较宽(-1)过早移除导管率患儿数量:132(2篇RCT和1篇非RCT的系统评价)RR=0.85(0.71~1.01)262/1 000223/1 000-39/1 000(-76~3)极低局限性:1篇为中等偏倚风险(-1);不一致性:干预方式、患儿年龄和疾病类型不一致(-2)
1项美国2014年的单中心回顾性队列研究[57],收集2009至2011年血液科、肿瘤科和干细胞移植科66例使用CVC患儿,发生124个CLABSI事件,乙醇封管+系统抗菌治疗组48例,单纯系统抗菌治疗组69例。调整了免疫受损状态和年龄<10岁后,乙醇封管+系统抗菌治疗组归因住院时间(从首次血培养阳性到首次血培养阴性的时间/开始乙醇封管到首次血培养阴性的时间)[(1.6±1.5) d]短于单纯系统抗菌治疗组[(2.9±3.0) d],差异有统计学意义;乙醇封管+系统抗菌治疗组中首次血培养阳性后即使用乙醇封管,其归因住院时间[(3.75±1.5) d]短于多次血培养阳性后再使用乙醇封管[(5.8±3.5) d],差异有统计学意义。
推荐意见(45) 外周短导管肝素较生理盐水冲管在使用时间和降低并发症方面有优势(2C~2D)。
推荐说明 2篇小剂量肝素应用于PIVC延长使用时间系统评价[58, 59],汇总2篇系统评价中的17篇原始文献重新进行了系统评价/Meta分析。使用PIVC的0~18岁儿童,肝素组:通过PIVC输注和间歇推注肝素(0.5~10 U·mL-1),对照组:生理盐水或不干预。主要结局指标为PIVC使用时间(使用至留置针拔除),次要结局指标为PIVC相关并发症、无法推注液体的堵管、静脉炎或静脉血栓、CLABSI、肝素相关性并发症(凝血异常、过敏反应、肝素诱导血小板减少等)。
图15显示,PIVC使用时间(h),新生儿人群干预组和对照组差异无统计学意义(MD=5.41,95%CI:-6.48~17.30);儿童人群干预组和对照组差异无统计学意义(MD=9.64,95%CI:-0.57~19.85)。新生儿+儿童人群PIVC使用时间,肝素组较对照组增加8.3 h(MD=8.27,95%CI:1.57~14.79)。
图16显示,并发症(含静脉炎及CLABSI),新生儿人群干预组和对照组差异无统计学意义(OR=0.83,95%CI:0.67~1.04);儿童人群肝素组和对照组差异无统计学意义(OR=0.74,95%CI:0.47~1.16)。新生儿+儿童人群并发症,肝素组较对照组减少12%(OR=0.82,95%CI:0.67~0.99)。
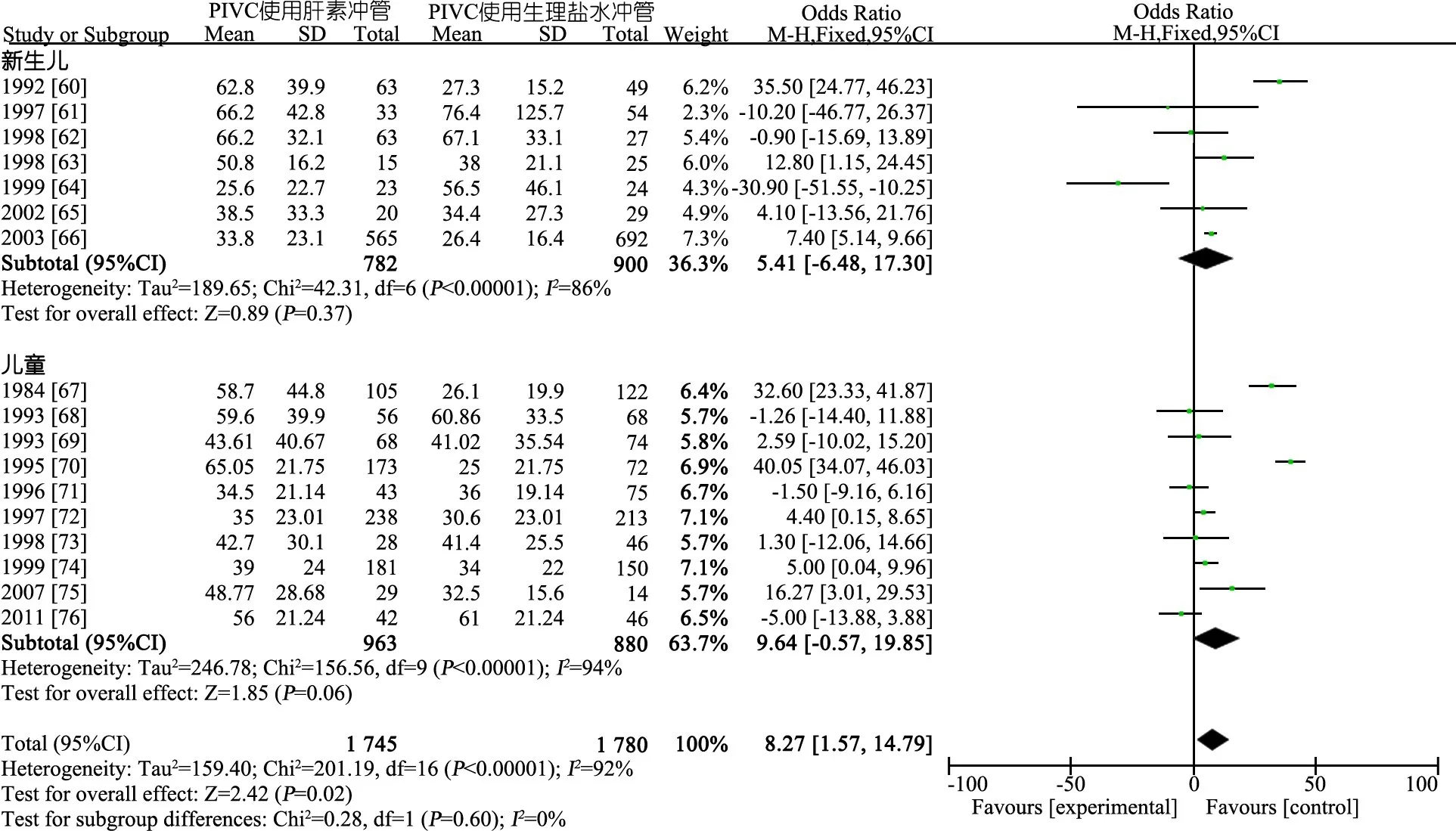
图15 PIVC使用肝素和生理盐水冲管比较PIVC使用时间的系统评价/Meta分析
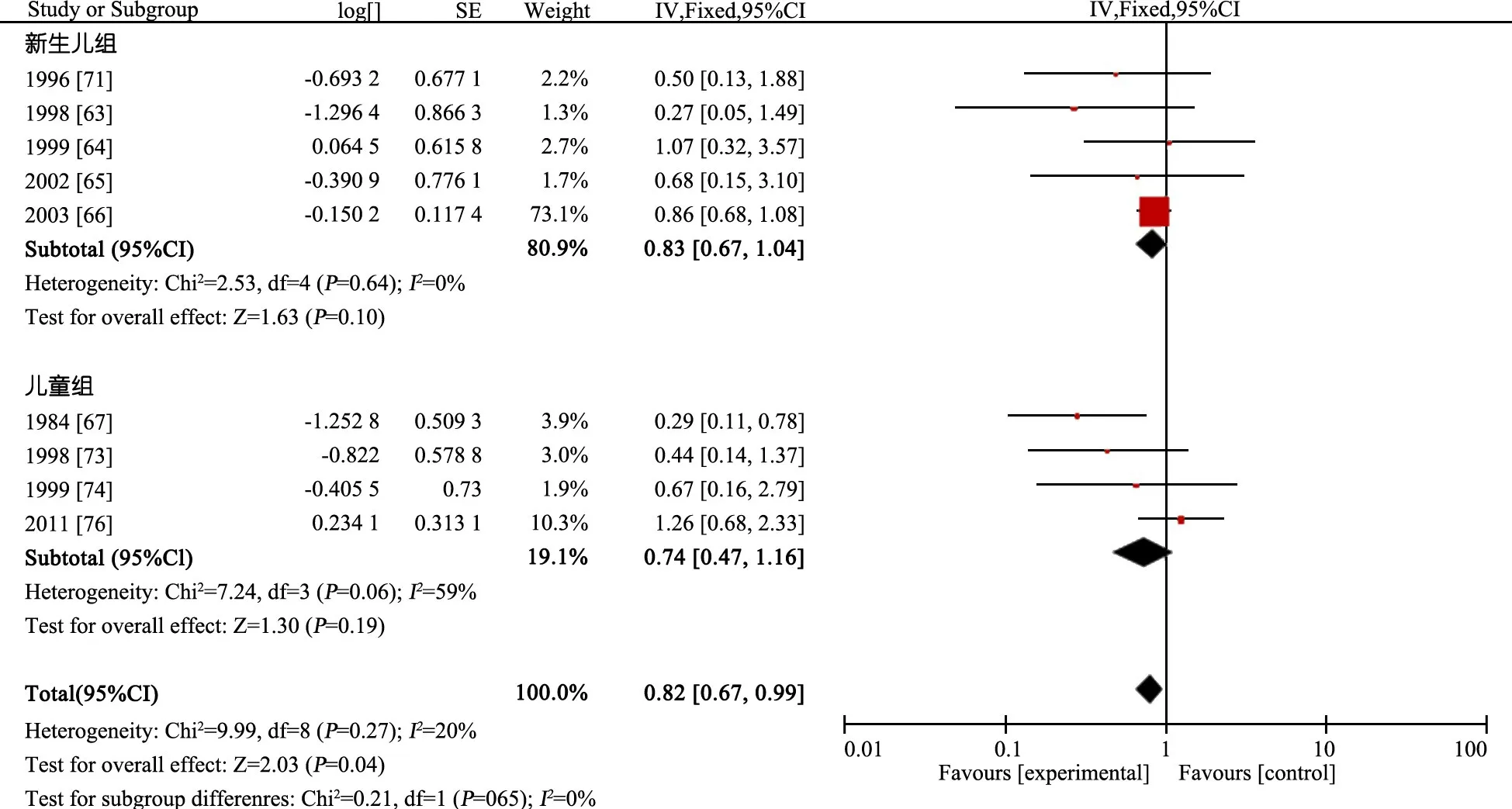
图16 PIVC相关并发症发生率的系统评价/Meta分析
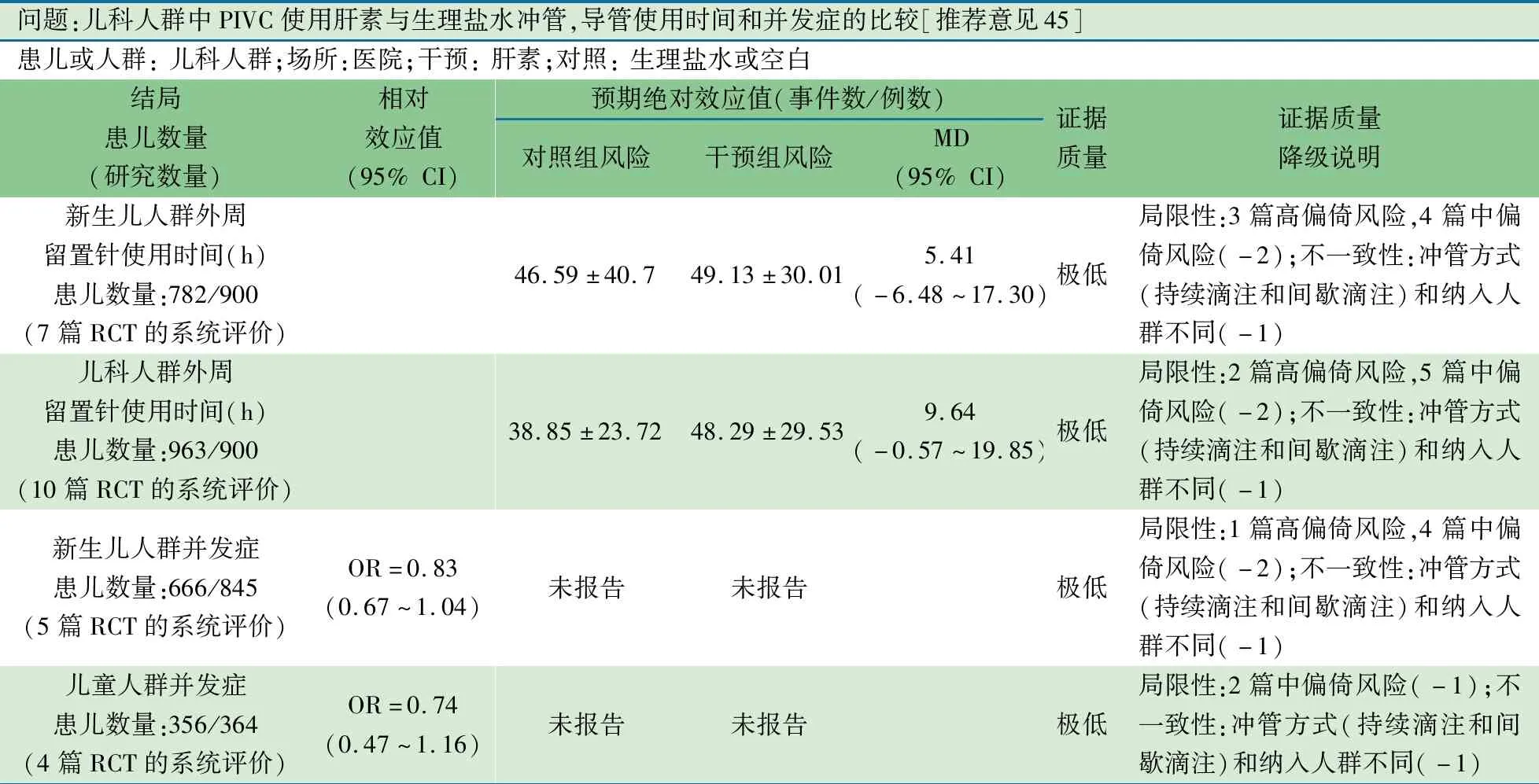
问题:儿科人群中PIVC使用肝素与生理盐水冲管,导管使用时间和并发症的比较[推荐意见45]患儿或人群: 儿科人群;场所:医院;干预: 肝素;对照: 生理盐水或空白结局患儿数量 (研究数量)相对效应值(95% CI)预期绝对效应值(事件数/例数)对照组风险干预组风险MD(95% CI)证据质量证据质量降级说明新生儿人群外周留置针使用时间(h)患儿数量:782/900(7篇RCT的系统评价)46.59±40.749.13±30.015.41(-6.48~17.30)极低局限性:3篇高偏倚风险,4篇中偏倚风险(-2);不一致性:冲管方式(持续滴注和间歇滴注)和纳入人群不同(-1)儿科人群外周留置针使用时间(h)患儿数量:963/900(10篇RCT的系统评价)38.85±23.7248.29±29.539.64(-0.57~19.85)极低局限性:2篇高偏倚风险,5篇中偏倚风险(-2);不一致性:冲管方式(持续滴注和间歇滴注)和纳入人群不同(-1)新生儿人群并发症患儿数量:666/845(5篇RCT的系统评价)OR=0.83(0.67~1.04)未报告未报告极低局限性:1篇高偏倚风险,4篇中偏倚风险(-2);不一致性:冲管方式(持续滴注和间歇滴注)和纳入人群不同(-1)儿童人群并发症患儿数量:356/364(4篇RCT的系统评价)OR=0.74(0.47~1.16)未报告未报告极低局限性:2篇中偏倚风险(-1);不一致性:冲管方式(持续滴注和间歇滴注)和纳入人群不同(-1)
推荐意见(46) 低剂量抗凝剂(肝素)具有明确的预防中心静脉导管血栓发生的作用。
推荐说明 基于纳入5篇多中心RCT(0~18岁)[77-81]、2篇单中心RCT[82,83](NICU、居家肠衰竭患儿)和1篇回顾性队列[84]的系统评价/Meta分析。管道类型包括PICC、TcCVAD及CVC。干预组:低剂量抗凝剂(肝素和低分子肝素)持续输注(0.5~3 U·mL-1),对照组:生理盐水或空白,主要结局指标为出现临床症状后超声和静脉造影确诊为CVAD相关血栓发生。图17显示,干预组(90/1 024)较对照组(188/1 201)CVAD相关性血栓的发生率下降49%(OR=0.51,95%CI:0.41~0.63)。低剂量肝素亚组(60/475)较对照亚组(138/489)相关血栓发生率下降了56%(OR=0.44,95%CI:0.34~1.56)。低分子肝素亚组(18/294)较对照亚组(35/452)CVAD相关性血栓发生差异无统计学意义(OR=0.71,95%CI:0.40~1.24);肝素加入至TPN中亚组(12/255)较对照亚组(15/260)CVAD相关性血栓发生率差异无统计学意义(OR=0.78,95%CI:0.38~1.59)。
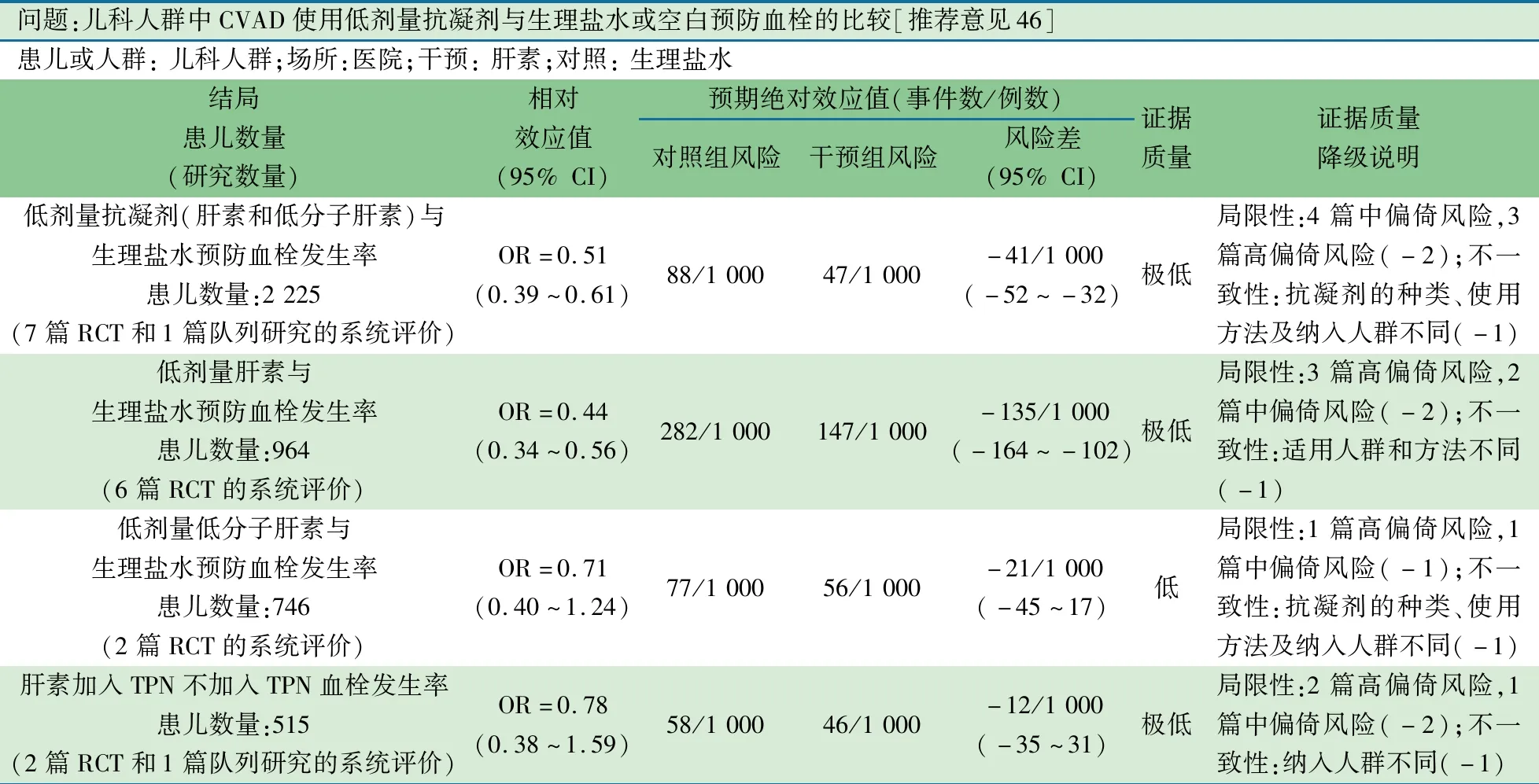
问题:儿科人群中CVAD使用低剂量抗凝剂与生理盐水或空白预防血栓的比较[推荐意见46]患儿或人群: 儿科人群;场所:医院;干预: 肝素;对照: 生理盐水结局患儿数量 (研究数量)相对效应值(95% CI)预期绝对效应值(事件数/例数)对照组风险干预组风险风险差(95% CI)证据质量证据质量降级说明低剂量抗凝剂(肝素和低分子肝素)与生理盐水预防血栓发生率患儿数量:2 225(7篇RCT和1篇队列研究的系统评价)OR=0.51(0.39~0.61)88/1 00047/1 000-41/1 000(-52~-32)极低局限性:4篇中偏倚风险,3篇高偏倚风险(-2);不一致性:抗凝剂的种类、使用方法及纳入人群不同(-1)低剂量肝素与生理盐水预防血栓发生率患儿数量:964(6篇RCT的系统评价)OR=0.44(0.34~0.56)282/1 000147/1 000-135/1 000(-164~-102)极低局限性:3篇高偏倚风险,2篇中偏倚风险(-2);不一致性:适用人群和方法不同(-1)低剂量低分子肝素与生理盐水预防血栓发生率患儿数量:746(2篇RCT的系统评价)OR=0.71(0.40~1.24)77/1 00056/1 000-21/1 000(-45~17)低局限性:1篇高偏倚风险,1篇中偏倚风险(-1);不一致性:抗凝剂的种类、使用方法及纳入人群不同(-1)肝素加入TPN不加入TPN血栓发生率患儿数量:515(2篇RCT和1篇队列研究的系统评价)OR=0.78(0.38~1.59)58/1 00046/1 000-12/1 000(-35~31)极低局限性:2篇高偏倚风险,1篇中偏倚风险(-2);不一致性:纳入人群不同(-1)
15.2 无菌操作技术(接头)
推荐意见(47) 推荐含2%氯己定的70%异丙醇溶液擦拭输液接头,每96 h更换无菌输液接头(1D)。
推荐说明 1项来自英国的单中心历史对照研究[85],纳入2006至2008年造血干细胞移植病房置入TcCVAD的患儿。干预组(2007至2008年)采用70%异丙醇(含2%氯己定)擦拭接头, 对照组(2006至2007年)采用70%异丙醇擦拭接头,干预组较对照组CRBSI降低9/1 000导管日(3/1 000导管日vs12/1 000导管日)。
1项来自美国单中心干细胞移植病房持续质量改进研究[73],阶段1:2009年11月至2010年7月,每96 h更换无菌输液接头;阶段2:2010年8月至2011年6月,每24 h更换无菌输液接头;阶段3:2011年7月至2012年1月 ,每96 h更换无菌输液接头,比较CLABSI的发生情况(除在输注血制品后应每24 h更换输液接头)。包括输血和输液条件下,阶段2(事件发生数/千导管日3.56,95%CI:1.53~5.67)较阶段1(事件发生数/千导管日0.41,95%CI:0.01~1.4)CLABSI增加,阶段3(事件发生数/千导管日0.03,95%CI:0.001~0.63)较阶段2 CLABSI下降;仅在输血情况下,阶段2(事件发生数/千导管日3.73,95%CI:1.63~6.71)较阶段1(事件发生数/千导管日0.46,95%CI:0~1.99)CLABSI增加,阶段3(事件发生数/千导管日0.004,95%CI:0.001~0.61)较阶段2 CLABSI下降。
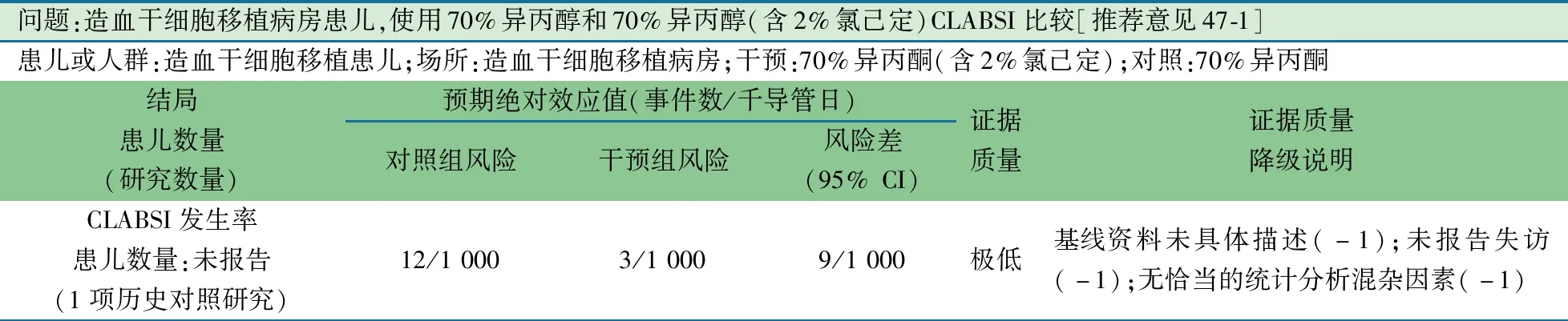
问题:造血干细胞移植病房患儿,使用70%异丙醇和70%异丙醇(含2%氯己定)CLABSI比较[推荐意见47-1]患儿或人群:造血干细胞移植患儿;场所:造血干细胞移植病房;干预:70%异丙酮(含2%氯己定);对照:70%异丙酮结局患儿数量 (研究数量)预期绝对效应值(事件数/千导管日)对照组风险干预组风险风险差(95% CI)证据质量证据质量降级说明CLABSI发生率患儿数量:未报告(1项历史对照研究)12/1 0003/1 0009/1 000极低基线资料未具体描述(-1);未报告失访(-1);无恰当的统计分析混杂因素(-1)
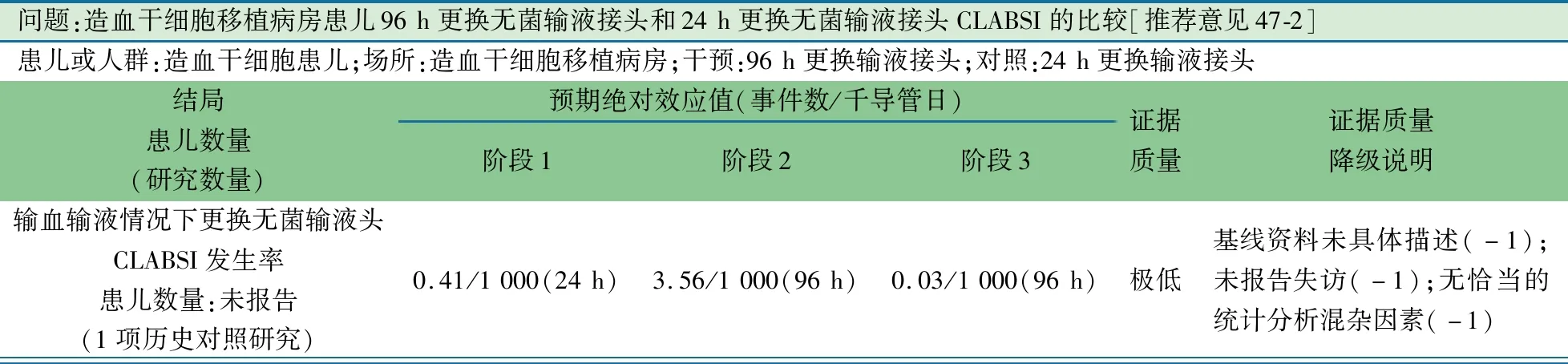
问题:造血干细胞移植病房患儿96 h更换无菌输液接头和24 h更换无菌输液接头CLABSI的比较[推荐意见47-2]患儿或人群:造血干细胞患儿;场所:造血干细胞移植病房;干预:96 h更换输液接头;对照:24 h更换输液接头结局患儿数量 (研究数量)预期绝对效应值(事件数/千导管日)阶段1阶段2阶段3证据质量证据质量降级说明输血输液情况下更换无菌输液头CLABSI发生率患儿数量:未报告(1项历史对照研究)0.41/1 000(24 h)3.56/1 000(96 h)0.03/1 000(96 h)极低基线资料未具体描述(-1);未报告失访(-1);无恰当的统计分析混杂因素(-1)

续表 仅在输血情况下更换无菌输液头CLABSI发生率患儿数量:未报告(1项历史对照研究)0.46/1 000(24 h)3.73/1 000(96 h)0.004/1 000(96 h)基线资料未具体描述(-1);未报告失访(-1);无恰当的统计分析混杂因素(-1);未采用盲法(-1)
推荐意见(48) 在NICU早产儿置入中心静脉导管时使用静脉过滤器可明显减少血栓、败血症或NEC并发症的发生(1B)。
推荐说明 1项来自荷兰单中心的RCT[87],纳入NICU置入UVC和PICC的RDS、窒息、肺炎、败血症、需要抗生素治疗的胎龄26~37周早产儿;干预组使用静脉过滤器,对照组不使用静脉过滤器;干预组在每次更换静脉过滤器时从静脉过滤器两端采样,对照组每4 d从输液装置中采样,在导管移除后均进行导管尖端培养,仅在怀疑败血症时采集血样;结局指标:主要并发症,包括血栓、败血症或NEC。两组胎龄、出生体重、机械通气和病死率差异均无统计学意义,干预组(8/44)较对照组(21/44)主要并发症少62%(RR=0.38,95%CI:0.19~0.77)。

问题: NICU新生儿中是否使用静脉过滤器并发症的比较[推荐意见48]患儿或人群:早产儿;场所:NICU;干预:使用静脉过滤器;对照: 不使用静脉过滤器结局患儿数量 (研究数量)相对效应值(95% CI)预期绝对效应值(事件数/例数)对照组风险干预组风险风险差(95% CI)证据质量证据质量降级说明CLABSI发生率患儿数量:88(1项RCT)OR=0.38(0.19~0.77)447/1 000258/1 000-22/1 000(-329~-64)中随机化过程不清楚(-1)
15.3 导管敷料
推荐意见(49) 置入中心静脉导管使用含抗生素(银离子、氯己定)敷贴不降低CLABSI的发生率(1D)。
推荐说明 2项来自美国单中心RCT的Meta分析[88,89],基于置入PICC导管的新生儿,干预组使用含银离子的敷贴,对照组使用普通透明敷贴。主要结局指标为CLABSI的发生率,图18显示,干预组与对照组CLABSI的发生率差异无统计学意义(OR=0.91,95%CI:0.41~2.04)。图18显示,基于美国(多中心NICU)、以色列(单中心0~18岁的CICU患儿)和土耳其(单中心血液肿瘤患儿)RCT研究的Meta分析[90-92],干预组使用含有氯己定的敷贴,对照组使用普通透明敷贴,结局指标为CLABSI的发生率,干预组较对照组CLABSI的发生率差异无统计学意义(OR=0.92,95%CI:0.49~1.72)。
汇总上述两个Meta分析结果后发现(图18),含有抗菌成分的敷贴(含银离子+氯己定)较不含任何抗菌成分的敷贴CLABSI的发生率差异无统计学意义(RR=0.92,95%CI:0.56~1.50)。

图18 含抗菌成分(银离子+氯己定)敷贴较不含抗菌成分敷贴的系统评价/Meta分析
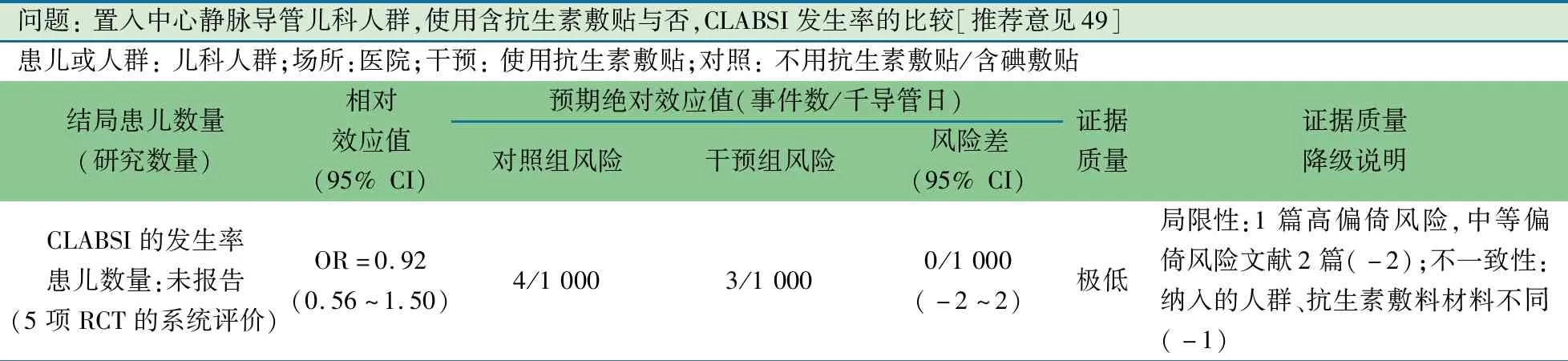
问题: 置入中心静脉导管儿科人群,使用含抗生素敷贴与否,CLABSI发生率的比较[推荐意见49]患儿或人群: 儿科人群;场所:医院;干预: 使用抗生素敷贴;对照: 不用抗生素敷贴/含碘敷贴结局患儿数量 (研究数量)相对效应值(95% CI)预期绝对效应值(事件数/千导管日)对照组风险干预组风险风险差(95% CI)证据质量证据质量降级说明CLABSI的发生率患儿数量:未报告(5项RCT的系统评价)OR=0.92(0.56~1.50)4/1 0003/1 0000/1 000(-2~2)极低局限性:1篇高偏倚风险,中等偏倚风险文献2篇(-2);不一致性:纳入的人群、抗生素敷料材料不同(-1)
1项美国单中心的RCT[89],纳入出生后72 h且出生体重500~1 500 g的置入PICC的新生儿。在置管后和导管维护时,观察组使用透明敷贴,干预组使用含银离子的敷贴,第1、7和28 d血液中银离子的浓度(ng·mL-1)干预组高于观察组(0.22±0.09vs7.60±20.93,0.23±0.14vs4.79±4.37,0.21±0.07vs3.19±3.23),差异均有统计学意义,但干预组银离子浓度远低于银离子致毒浓度(>200),无血清积累、皮肤损伤、肝肾功能改变、中枢神经系统改变。
15.4 导管有效固定
推荐意见(50) 以不同方式(聚氨酯透明敷贴、思乐扣、组织粘合剂和完全敷贴)固定中心静脉导管,发生导管故障及并发症无差别(1D)。
推荐说明 来自澳大利亚同一研究团队不同研究时间(前和后)的RCT[93,94],纳入PICC、住院时间>24 h和年龄<18岁患儿;使用网站随机化分为3组:思乐扣组(无缝线+思乐扣固定在导管末端+聚氨酯透明敷贴固定)、组织粘合剂组(1~2滴组织粘合剂+聚氨酯透明敷贴固定)和敷贴固定组(缝线+敷贴固定)。结局指标:从CVAD置入起至4周、研究结束、装置移除或出院的并发症(相关血流感染、穿刺点感染、堵塞、移位、静脉血栓、断裂)和故障(开始静脉治疗前即停止使用CVAD)发生率。3组导管故障及并发症发生率差异均无统计学意义(图19和20)。
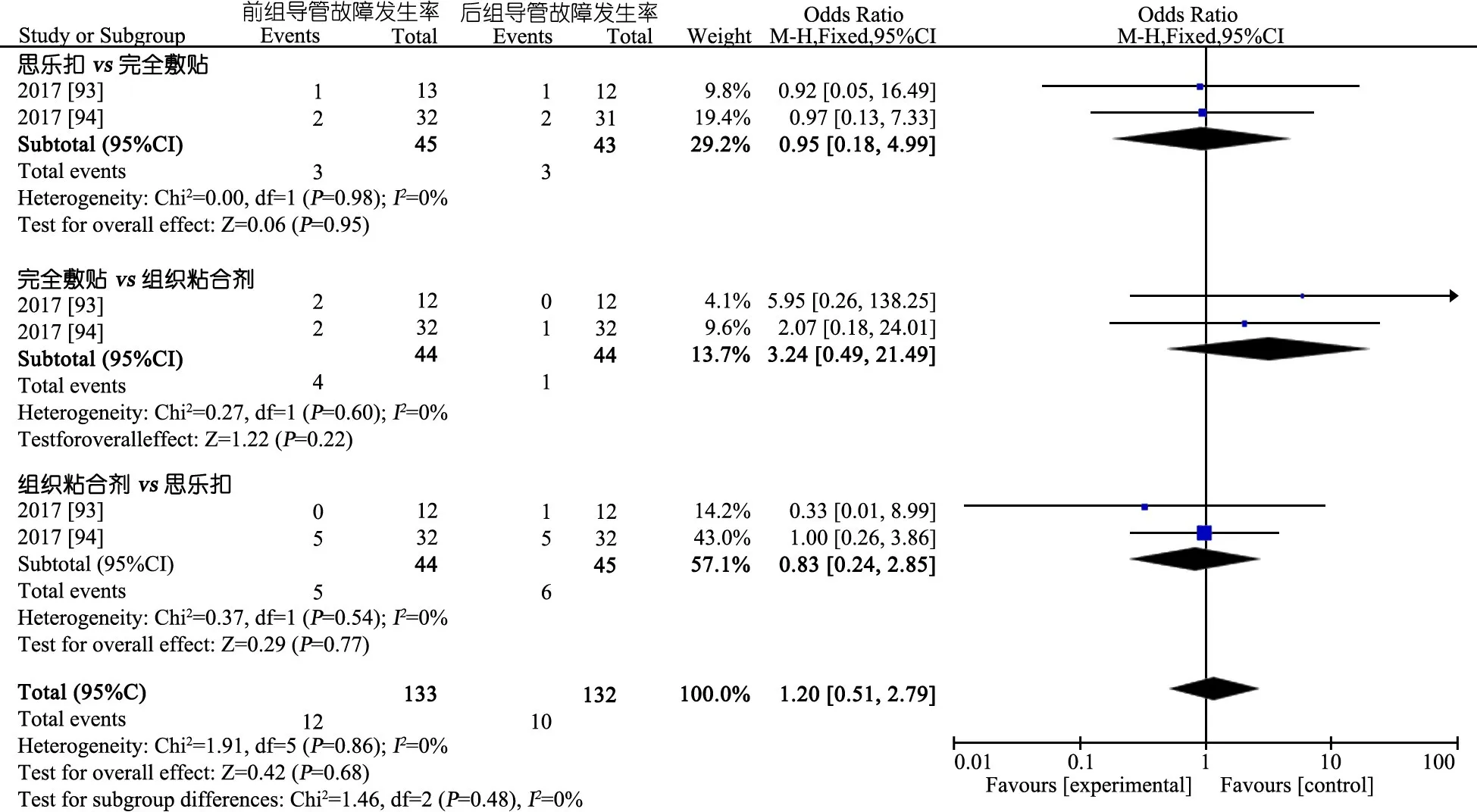
图19 不同方式固定中心静脉导管导管故障发生率的系统评价/Meta分析
1项美国的单中心非RCT[95],纳入2010至2012年非头部和肘部PIVC的2~17岁住院患儿。对照组(n=36)采用手臂板和胶带固定,干预组(n=44)采用思乐扣和透明敷贴固定,两组人口学资料差异无统计学意义。PICV拔除时,静脉炎(1vs0)、渗出(2vs2)、堵塞(3vs5)、断裂(1vs1)等差异均无统计学意义。
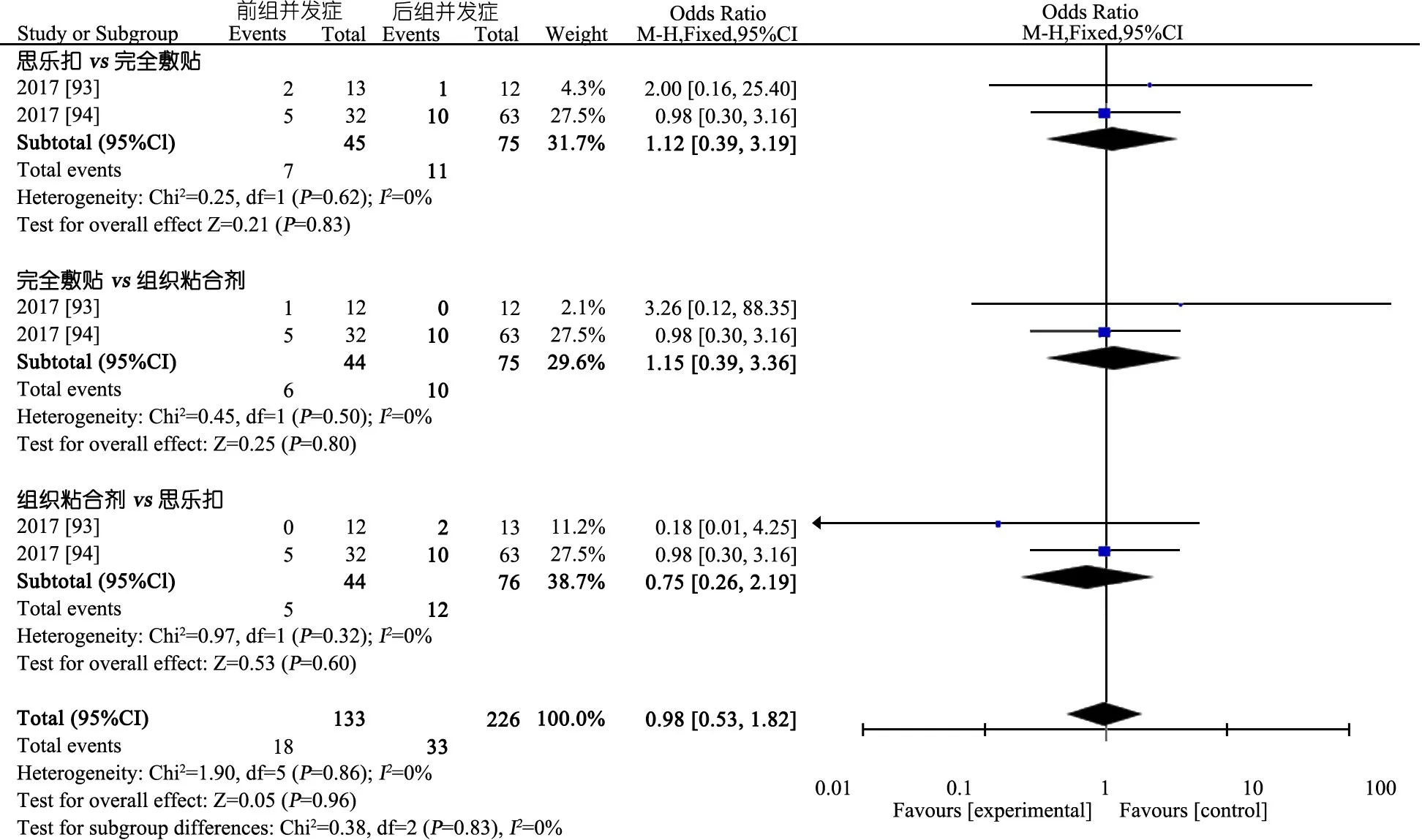
图20 不同方式固定中心静脉导管并发症的发生率的系统评价/Meta分析
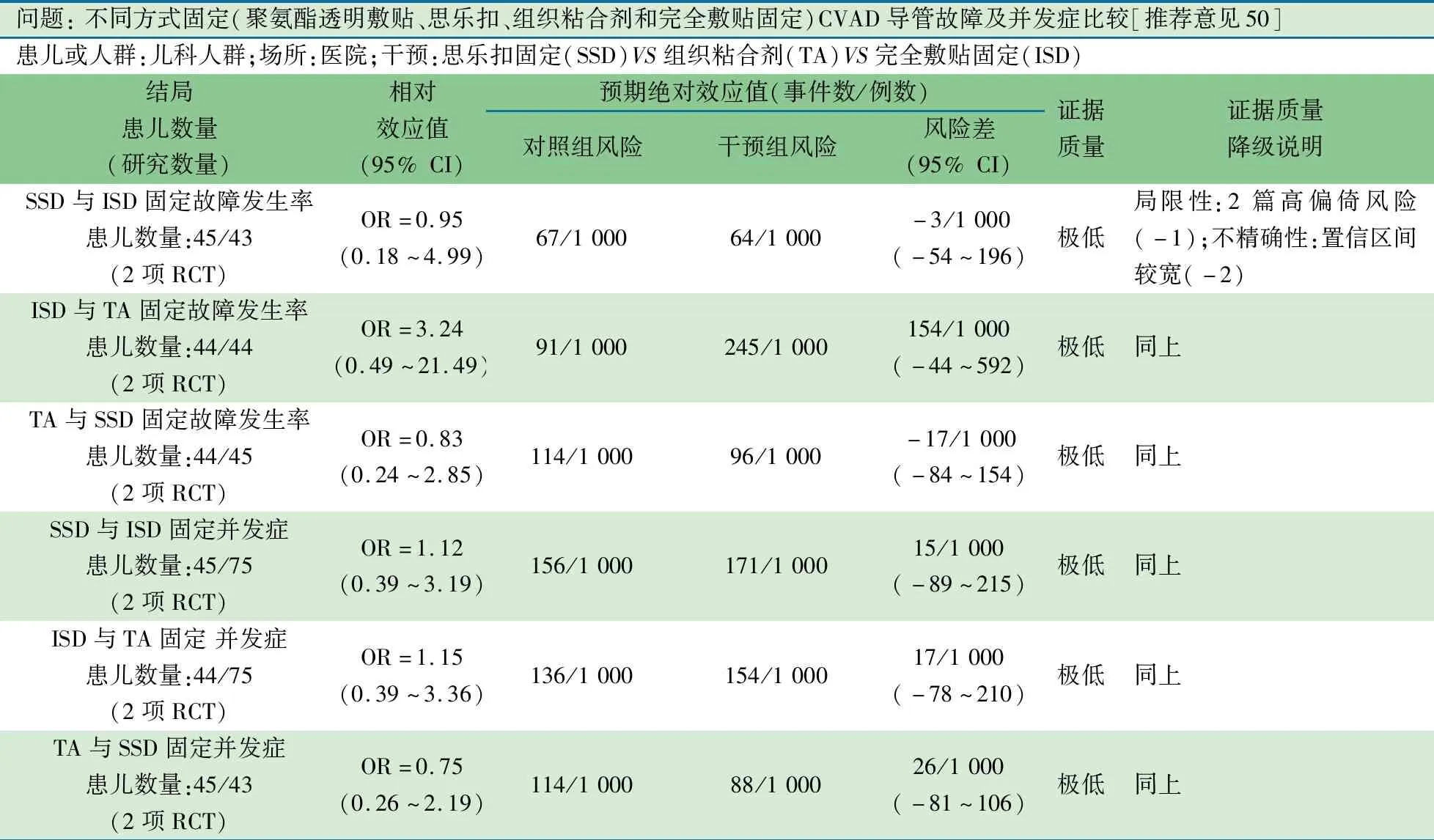
问题: 不同方式固定(聚氨酯透明敷贴、思乐扣、组织粘合剂和完全敷贴固定)CVAD导管故障及并发症比较[推荐意见50]患儿或人群:儿科人群;场所:医院;干预:思乐扣固定(SSD)VS组织粘合剂(TA)VS完全敷贴固定(ISD)结局患儿数量 (研究数量)相对效应值(95% CI)预期绝对效应值(事件数/例数)对照组风险干预组风险风险差(95% CI)证据质量证据质量降级说明SSD与ISD固定故障发生率患儿数量:45/43(2项RCT)OR=0.95(0.18~4.99)67/1 00064/1 000-3/1 000(-54~196)极低局限性:2篇高偏倚风险(-1);不精确性:置信区间较宽(-2)ISD与TA固定故障发生率患儿数量:44/44(2项RCT)OR=3.24(0.49~21.49)91/1 000245/1 000154/1 000(-44~592)极低同上TA与SSD固定故障发生率患儿数量:44/45(2项RCT)OR=0.83(0.24~2.85)114/1 00096/1 000-17/1 000(-84~154)极低同上SSD与ISD固定并发症患儿数量:45/75(2项RCT)OR=1.12(0.39~3.19)156/1 000171/1 00015/1 000(-89~215)极低同上ISD与TA固定 并发症患儿数量:44/75(2项RCT)OR=1.15(0.39~3.36)136/1 000154/1 00017/1 000(-78~210)极低同上TA与SSD固定并发症患儿数量:45/43(2项RCT)OR=0.75(0.26~2.19)114/1 00088/1 00026/1 000(-81~106)极低同上
16 输液治疗中的特殊预防措施和有害药物、废弃物的处理
推荐意见(51) 推荐采用中华人民共和国卫生行业标准(WS/T 433-2013)、中华人民共和国国务院令第380号和美国国家职业安全卫生研究所(NIOSH)在2016年列出的218种有害药物[96,97](1D)。
有害药物包括抗肿瘤药物、抗病毒药物、激素、生物工程药物等。由于在有害药物中占有重要比重的是抗肿瘤药物,因此,本指南中描述的有害药物的使用和处理,均指抗肿瘤药物。
化疗药物冲配的防护措施:①配制宜在Ⅱ级或Ⅲ级垂直层流生物安全柜内;②配药时操作者应戴双层手套,穿防护服,戴护目镜/防护面罩。其中双层手套的内层应为PVC手套,外层为乳胶手套,且外层乳胶手套应包住防护服的袖口;防护服应为一次性,材质宜为有聚乙烯涂层的聚丙烯,前襟完全封闭。配药操作台面应垫放渗透吸水垫;③配药开始前,先将密闭输液器连接至输液袋,然后排气,再将抗肿瘤药物从原液转移到输液袋,整个冲配过程推荐选用密闭装置以限制气雾的产生,如嵌入式手套袋、无针系统等。
抗肿瘤药物的静脉给药:①静脉给药时护士宜穿防护服,戴双层手套和一次性口罩,护目镜;②抗肿瘤药物输注完毕后,应先彻底冲洗整个输液管道,然后再断开输液器及其他输液导管;③给药护士脱下内层手套后,应用流动水和皂液洗手。
抗肿瘤药物溢出的处理:(1)抗肿瘤药物溢出是最常见的有害药物暴露,因此病区应常备抗肿瘤药物溢出包,内含防护服、N95口罩、护目镜、聚氯乙烯手套、乳胶手套、利器盒、镊子、纱布垫、毒性药物标识包装袋和自封袋。定点放置,并定期检查包内物品是否齐全,是否在有效期内。溢出包应放置于全体医务人员知晓的位置,并方便拿取。一旦开启,则需重新领取。(2)处理步骤:①操作者应穿戴好溢出包内防护用品。②树立警示牌,标明污染范围,碎裂的玻璃用镊子夹取装入利器盒,粉剂应使用湿纱布垫吸附擦拭,水剂应使用纱布垫直接吸附。污染表面应使用皂液/或去活剂(如果有)和清水反复冲洗。③如药液不慎溅在皮肤或眼睛内,应立即用清水反复冲洗。④记录外溢药物的名称、事件、溢出量、处理过程及受污染的人员。
化疗药物废弃物的处理:(1)各医疗机构应制定具体的抗肿瘤废弃物管理制度、规范处理措施及细则,包括但不限于以下内容。①抗肿瘤药物废弃物不等同于感染性废弃物等其他医疗废弃物,因此应与其他医疗垃圾分开收集;②所有被抗肿瘤药物污染的物品均应双层包装,并丢弃在有毒性药物标识的坚固、防漏、有盖容器中;③接受化疗药物治疗的患儿所使用的反复清洗的床单应放置在有特殊标记且防漏的织物袋中,与其他患儿的衣被分开收集和配送,并采用化学降解法单独洗涤。(2)抗肿瘤药物废弃物不能填埋或排入下水道系统,应做高温焚烧或化学降解处理。
准入和职业卫生:①为保证化疗药物的安全给予,所有使用和处理化疗药物的护士进行培训后方可工作;②对化疗药物使用和处理的培训内容应包括暴露的危害、化疗药物的理化性质、给药规范、溢出后的应急处理(每年2次,进行溢出的实战演习),化疗药物废弃物的处理;③定期对所有使用和处理化疗药物的工作场所进行空气有毒物质测定,对接触化疗药物的护士和其他工作人员进行职业健康体检,对备孕、怀孕以及在哺乳期中的护士宜调离化疗给药岗位。
17 导管并发症
17.1 CLABSI
推荐意见(52) 推荐标准化中心静脉导管干预策略,可降低CLABSI事件数/1 000个导管日(1D)。
推荐说明 1项2020年来自《中国循证儿科杂志》的基于标准的集束化CVAD干预策略在儿科CLABSI预防的Meta分析[98],以手卫生,置管过程中最大无菌屏障,浓度>0.5%的氯己定、碘、碘伏作为皮肤消毒剂,每日评估导管的必要性,及时拔除不必要的导管,根据患儿特点选择最佳置管部位(非股静脉)为标准集束化CVAD干预策略,以每1 000导管日CLABSI发生事件为结局指标,纳入41篇文献,均为历史对照研究,分别来自20个国家中136个NICU和30个PICU的数据,累计952 584个导管日,标准集束化CVAD干预前、后阶段分别为442 296和510 288个导管日,Meta分析结果显示,标准集束化CVAD干预策略后可降低NICU+PICU患儿CLABSI发生事件数,RR=0.40(95%CI:0.33~0.48),绝对效应值:每1 000个导管日可减少 3(减少4~减少3)例CLABSI。以NICU为干预场所,可以降低新生儿CLABSI发生事件数,RR=0.36(95%CI:0.29~0.45);绝对效应值:每1 000个导管日可减少 3(减少4~减少3)例CLABSI。以PICU为干预场所,可以降低PICU患儿CLABSI发生事件数,RR=0.54(95%CI:0.42~0.69);绝对效应值:每1 000个导管日可减少 4(减少5~减少3)例CLABSI事件数。
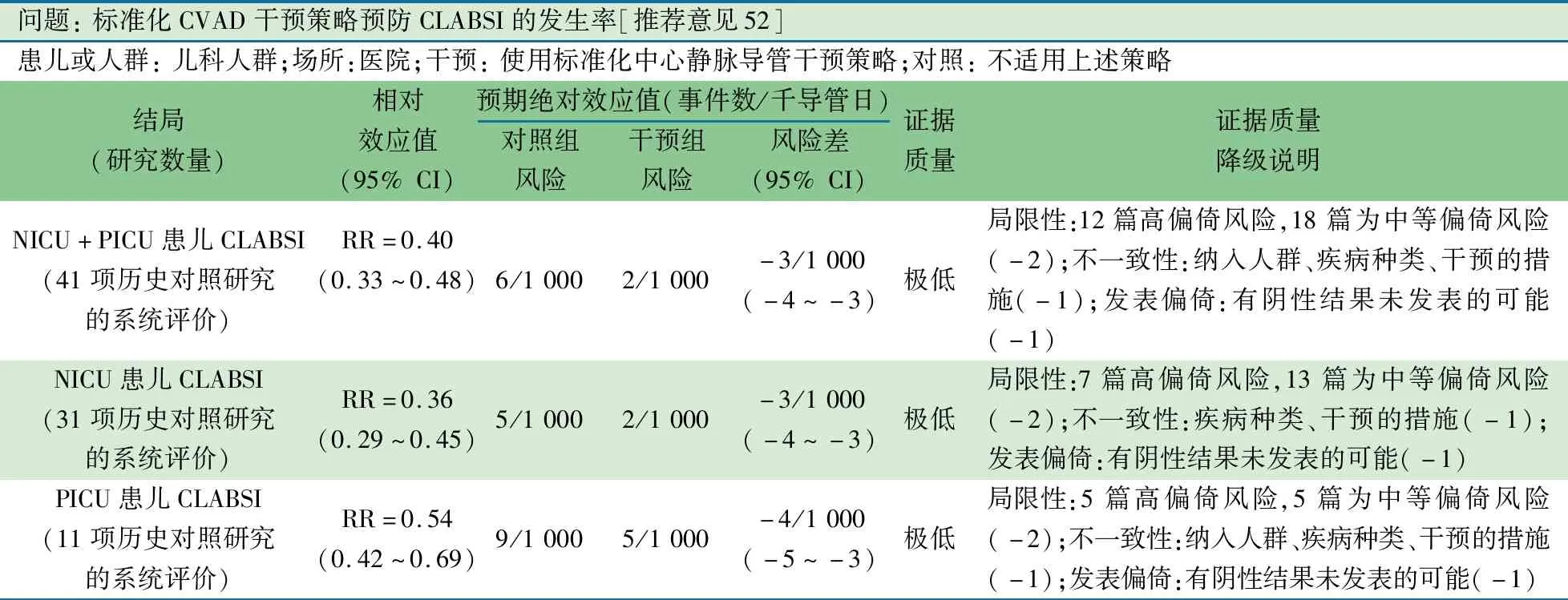
问题: 标准化CVAD干预策略预防CLABSI的发生率[推荐意见52]患儿或人群: 儿科人群;场所:医院;干预: 使用标准化中心静脉导管干预策略;对照: 不适用上述策略结局 (研究数量)相对效应值(95% CI)预期绝对效应值(事件数/千导管日)对照组风险干预组风险风险差(95% CI)证据质量证据质量降级说明NICU+PICU患儿CLABSI(41项历史对照研究的系统评价)RR=0.40(0.33~0.48)6/1 0002/1 000-3/1 000(-4~-3)极低局限性:12篇高偏倚风险,18篇为中等偏倚风险(-2);不一致性:纳入人群、疾病种类、干预的措施(-1);发表偏倚:有阴性结果未发表的可能(-1)NICU患儿CLABSI(31项历史对照研究的系统评价)RR=0.36(0.29~0.45)5/1 0002/1 000-3/1 000(-4~-3)极低局限性:7篇高偏倚风险,13篇为中等偏倚风险(-2);不一致性:疾病种类、干预的措施(-1);发表偏倚:有阴性结果未发表的可能(-1)PICU患儿CLABSI(11项历史对照研究的系统评价)RR=0.54(0.42~0.69)9/1 0005/1 000-4/1 000(-5~-3)极低局限性:5篇高偏倚风险,5篇为中等偏倚风险(-2);不一致性:纳入人群、疾病种类、干预的措施(-1);发表偏倚:有阴性结果未发表的可能(-1)
推荐意见(53) 儿科人群CVAD发生CLABSI的危险因素具有其专科的独特性,且治疗、管道因素相比人口学、基础疾病因素对CVAD发生CLABSI的影响更大(1D)。
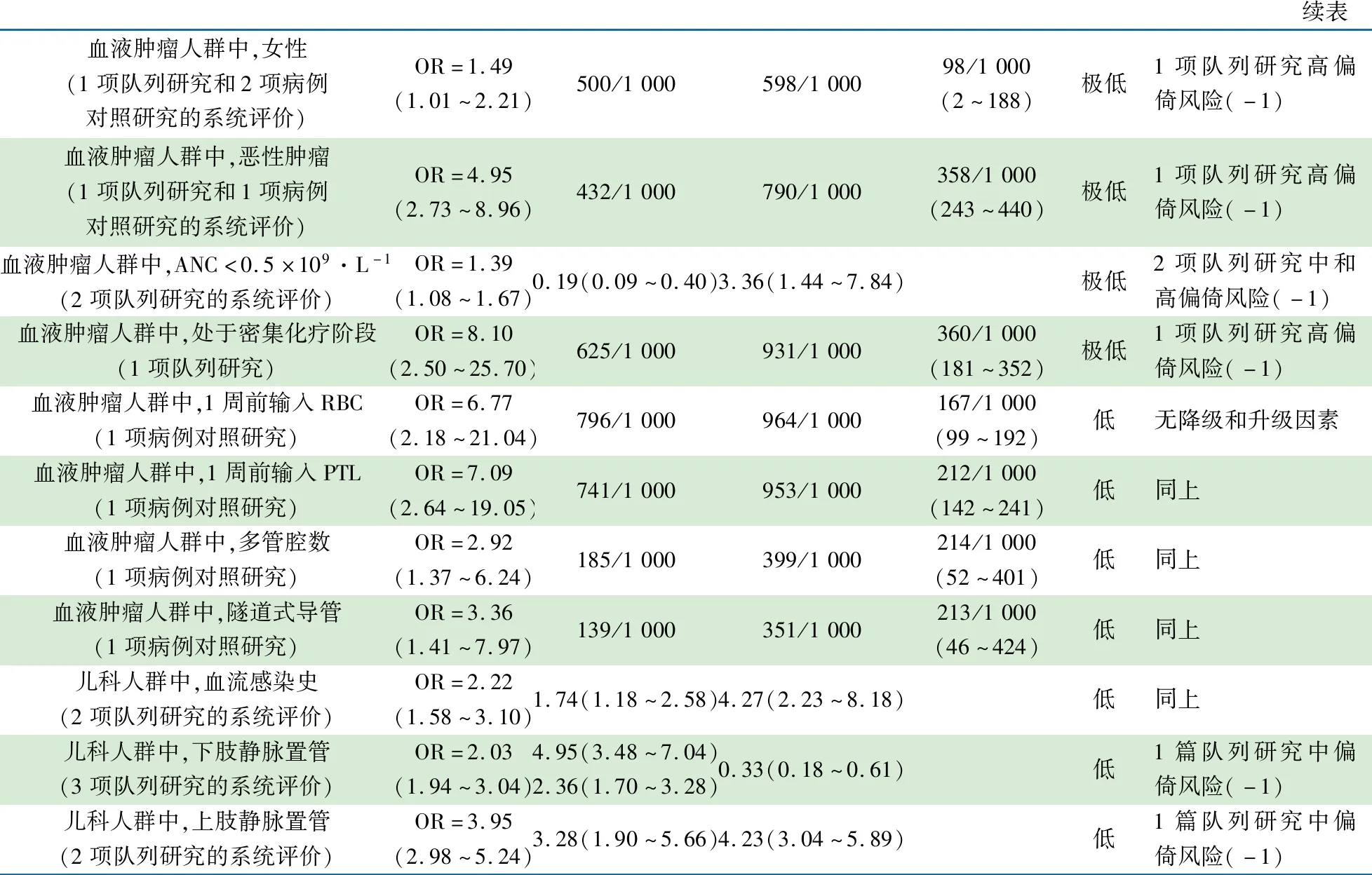
推荐说明 1项2020年来自《中国循证儿科杂志》的儿科中心静脉通路装置发生CLABSI相关因素的Meta分析[99]。纳入发表时间为2000年1月至2020年6月的关于儿童CVAD发生CLABSI的16篇文献(病例对照研究和队列研究),共计34 478 根CVAD和1585 358个导管日。①PICU发生CLABSI危险因素:体重<8 kg、特指心脏疾病、肿瘤疾病输入血制品、使用ECMO、机械通气、使用血管活性药物、肠外营养、胃肠道疾病、胃造口术后、股静脉置管、同时置管数>1根和长期管道;②NICU发生CLABSI危险因素:肠外营养、股静脉置管和置管时间>21 d;③血液肿瘤发生CLABSI危险因素:女性恶性肿瘤、处于密集进行化疗的阶段、ANC<0.5×109·L-1、输入血制品(RBC或PLT)、多管腔数和TcCVAD;④儿科人群发生CLABSI危险因素:血流感染史、上肢静脉和下肢静脉置管。
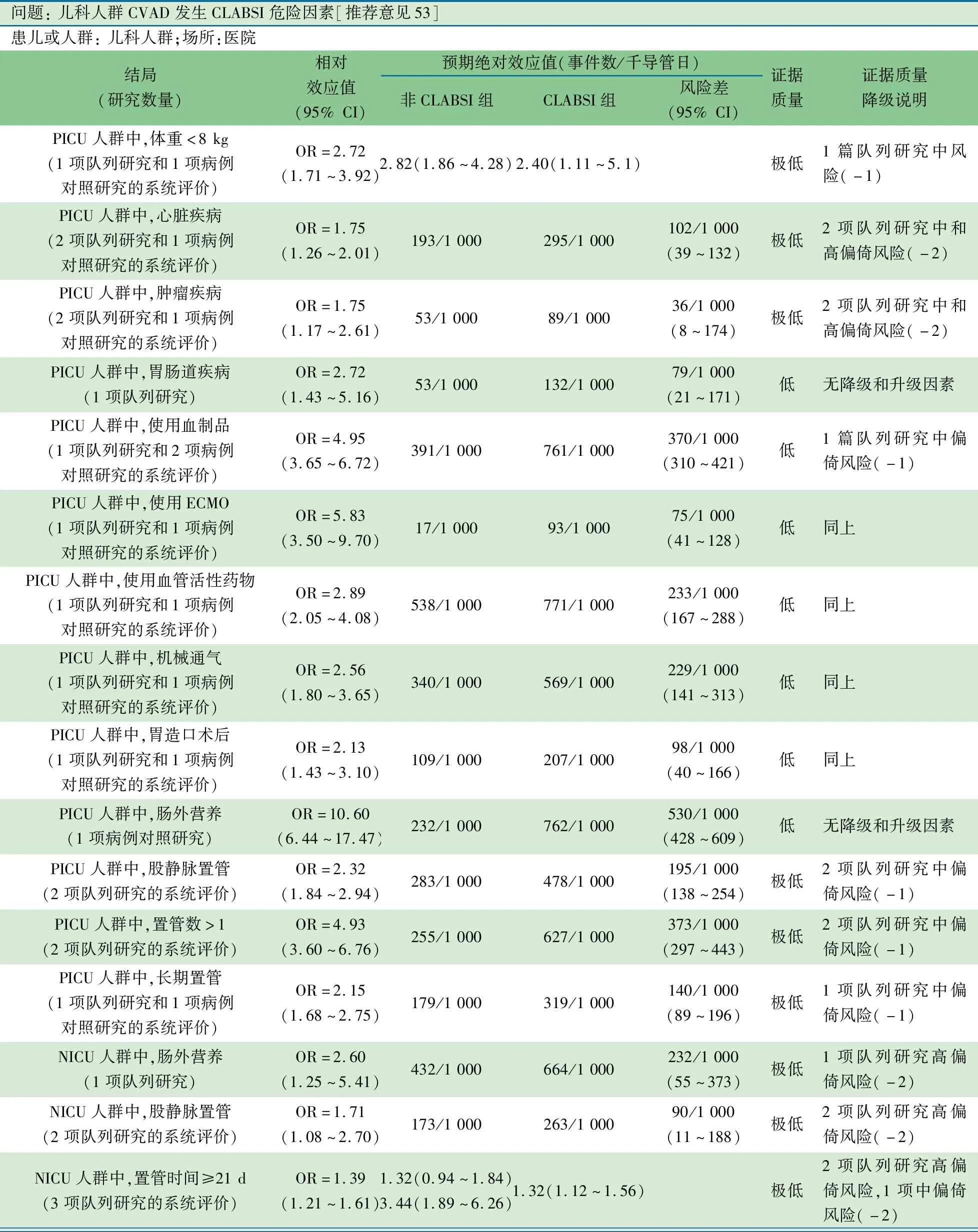
问题: 儿科人群CVAD发生CLABSI危险因素[推荐意见53]患儿或人群: 儿科人群;场所:医院 结局 (研究数量)相对效应值(95% CI)预期绝对效应值(事件数/千导管日)非CLABSI组CLABSI组风险差(95% CI)证据质量证据质量降级说明PICU人群中,体重<8 kg(1项队列研究和1项病例对照研究的系统评价)OR=2.72(1.71~3.92)2.82(1.86~4.28)2.40(1.11~5.1)极低1篇队列研究中风险(-1)PICU人群中,心脏疾病(2项队列研究和1项病例对照研究的系统评价)OR=1.75(1.26~2.01)193/1 000295/1 000102/1 000(39~132)极低2项队列研究中和高偏倚风险(-2)PICU人群中,肿瘤疾病(2项队列研究和1项病例对照研究的系统评价)OR=1.75(1.17~2.61)53/1 00089/1 00036/1 000(8~174)极低2项队列研究中和高偏倚风险(-2)PICU人群中,胃肠道疾病(1项队列研究)OR=2.72(1.43~5.16)53/1 000132/1 00079/1 000(21~171)低无降级和升级因素PICU人群中,使用血制品(1项队列研究和2项病例对照研究的系统评价)OR=4.95(3.65~6.72)391/1 000761/1 000370/1 000(310~421)低1篇队列研究中偏倚风险(-1)PICU人群中,使用ECMO(1项队列研究和1项病例对照研究的系统评价)OR=5.83(3.50~9.70)17/1 00093/1 00075/1 000(41~128)低同上PICU人群中,使用血管活性药物(1项队列研究和1项病例对照研究的系统评价)OR=2.89(2.05~4.08)538/1 000771/1 000233/1 000(167~288)低同上PICU人群中,机械通气(1项队列研究和1项病例对照研究的系统评价)OR=2.56(1.80~3.65)340/1 000569/1 000229/1 000(141~313)低同上PICU人群中,胃造口术后(1项队列研究和1项病例对照研究的系统评价)OR=2.13(1.43~3.10)109/1 000207/1 00098/1 000(40~166)低同上PICU人群中,肠外营养(1项病例对照研究)OR=10.60(6.44~17.47)232/1 000762/1 000530/1 000(428~609)低无降级和升级因素PICU人群中,股静脉置管(2项队列研究的系统评价)OR=2.32(1.84~2.94)283/1 000478/1 000195/1 000(138~254)极低2项队列研究中偏倚风险(-1)PICU人群中,置管数>1(2项队列研究的系统评价)OR=4.93(3.60~6.76)255/1 000627/1 000373/1 000(297~443)极低2项队列研究中偏倚风险(-1)PICU人群中,长期置管(1项队列研究和1项病例对照研究的系统评价)OR=2.15(1.68~2.75)179/1 000319/1 000140/1 000(89~196)极低1项队列研究中偏倚风险(-1)NICU人群中,肠外营养(1项队列研究)OR=2.60(1.25~5.41)432/1 000664/1 000232/1 000(55~373)极低1项队列研究高偏倚风险(-2)NICU人群中,股静脉置管(2项队列研究的系统评价)OR=1.71(1.08~2.70)173/1 000263/1 00090/1 000(11~188)极低2项队列研究高偏倚风险(-2)NICU人群中,置管时间≥21 d(3项队列研究的系统评价)OR=1.39(1.21~1.61)1.32(0.94~1.84)3.44(1.89~6.26)1.32(1.12~1.56)极低2项队列研究高偏倚风险,1项中偏倚风险(-2)
续表 血液肿瘤人群中,女性(1项队列研究和2项病例对照研究的系统评价)OR=1.49(1.01~2.21)500/1 000598/1 00098/1 000(2~188)极低1项队列研究高偏倚风险(-1)血液肿瘤人群中,恶性肿瘤(1项队列研究和1项病例对照研究的系统评价)OR=4.95(2.73~8.96)432/1 000790/1 000358/1 000(243~440)极低1项队列研究高偏倚风险(-1)血液肿瘤人群中,ANC<0.5×109·L-1(2项队列研究的系统评价)OR=1.39(1.08~1.67)0.19(0.09~0.40)3.36(1.44~7.84)极低2项队列研究中和高偏倚风险(-1)血液肿瘤人群中,处于密集化疗阶段(1项队列研究)OR=8.10(2.50~25.70)625/1 000931/1 000360/1 000(181~352)极低1项队列研究高偏倚风险(-1)血液肿瘤人群中,1周前输入RBC(1项病例对照研究)OR=6.77(2.18~21.04)796/1 000964/1 000167/1 000(99~192)低无降级和升级因素血液肿瘤人群中,1周前输入PTL(1项病例对照研究)OR=7.09(2.64~19.05)741/1 000953/1 000212/1 000(142~241)低同上血液肿瘤人群中,多管腔数(1项病例对照研究)OR=2.92(1.37~6.24)185/1 000399/1 000214/1 000(52~401)低同上血液肿瘤人群中,隧道式导管(1项病例对照研究)OR=3.36(1.41~7.97)139/1 000351/1 000213/1 000(46~424)低同上儿科人群中,血流感染史(2项队列研究的系统评价)OR=2.22(1.58~3.10)1.74(1.18~2.58)4.27(2.23~8.18)低同上儿科人群中,下肢静脉置管(3项队列研究的系统评价)OR=2.03(1.94~3.04)4.95(3.48~7.04)2.36(1.70~3.28)0.33(0.18~0.61)低1篇队列研究中偏倚风险(-1)儿科人群中,上肢静脉置管(2项队列研究的系统评价)OR=3.95(2.98~5.24)3.28(1.90~5.66)4.23(3.04~5.89)低1篇队列研究中偏倚风险(-1)
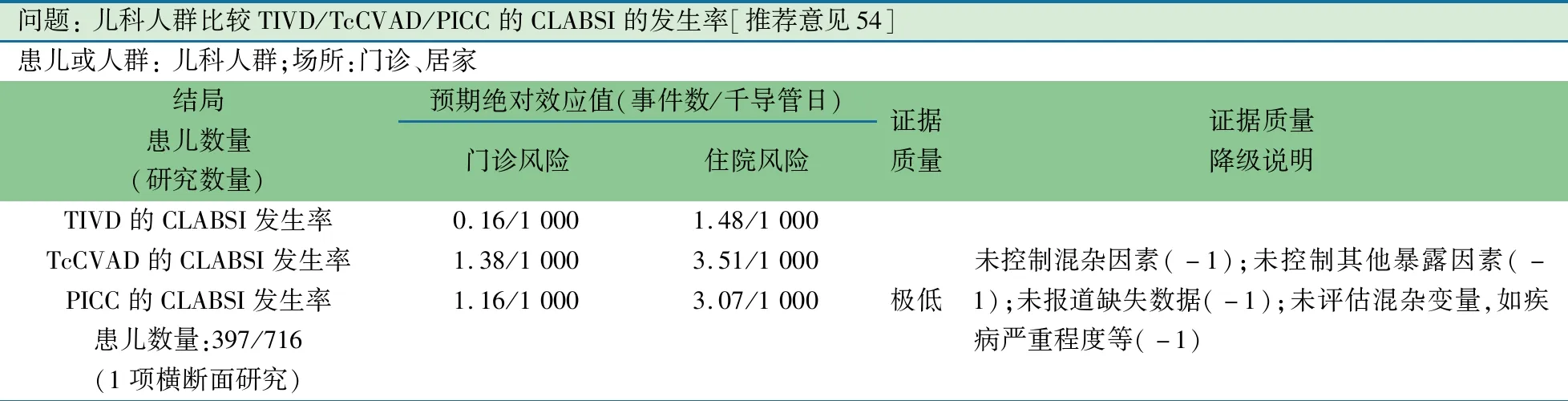
推荐意见(54) 置入式输液港较隧道式导管、PICC的CLABSI发生率更低(2D)。
推荐说明 1项2016年美国基于儿童医院协会儿童癌症和血液疾病网络数据库的多中心横断面调查[100],收集了2012年5月至2015年4月15个血液肿瘤和干细胞移植中心的血液/肿瘤患儿留置不同类型CVAD(TIVD、TcCVAD、PICC)CLABSI发生情况的数据。共纳入2 854 756导管日(住院患儿171 810导管日,门诊患儿2 682 946导管日),1 113个CLABSI事件(397例住院患儿和716例门诊患儿)。住院和门诊患儿TIVD、TcCVAD、PICC的CLABSI发生事件数(每1 000导管日)分别为1.48vs0.16、3.51vs1.38、3.07vs1.16,住院患儿CLABSI发生率高于门诊患儿;TcCVAD和PICC的CLABSI发生率高于TIVD,差异有统计学意义;在住院患儿中,TcCVAD和PICC的CLABSI发生率差异无统计学意义,但在门诊患儿中,TcCVAD和PICC的CLABSI发生率差异有统计学意义。
问题: 儿科人群比较TIVD/TcCVAD/PICC的CLABSI的发生率[推荐意见54]患儿或人群: 儿科人群;场所:门诊、居家 结局患儿数量 (研究数量)预期绝对效应值(事件数/千导管日)门诊风险住院风险证据质量证据质量降级说明TIVD的CLABSI发生率TcCVAD的CLABSI发生率PICC的CLABSI发生率患儿数量:397/716 (1项横断面研究)0.16/1 0001.38/1 0001.16/1 0001.48/1 0003.51/1 0003.07/1 000极低未控制混杂因素(-1);未控制其他暴露因素(-1);未报道缺失数据(-1);未评估混杂变量,如疾病严重程度等(-1)
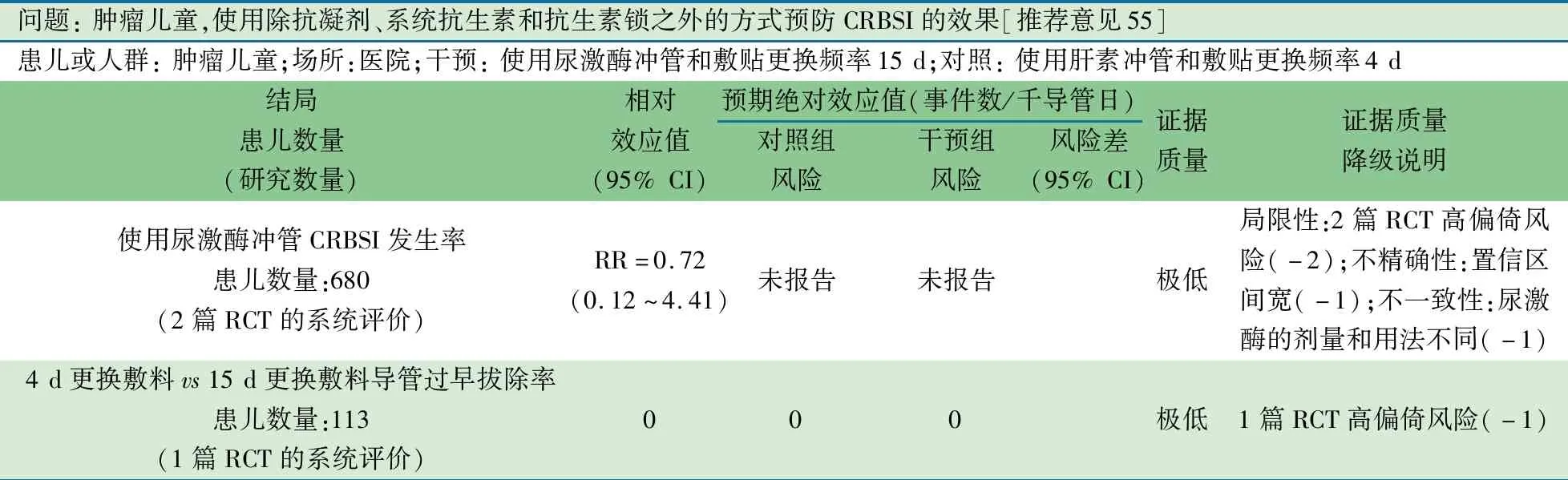
推荐意见(55) 预防肿瘤儿童TcCVAD相关性感染,尿激酶、敷贴更换频率作用不确定(1D)。
推荐说明 2010年 Cochrane基于18岁肿瘤儿童的预防留置TcCVAD相关性感染的3篇RCT的系统评价[101]。主要结局指标为CRBSI,次要结局指标为过早拔除导管,2篇干预组为尿激酶冲洗TcCVAD管路,对照组为肝素,CRBSI差异无统计学意义(RR=0.72,95%CI:0.12~4.41);1篇干预组导管敷贴每15 d更换1次,对照组导管敷贴每4 d更换1次,两组均未出现导管过早拔除。
问题: 肿瘤儿童,使用除抗凝剂、系统抗生素和抗生素锁之外的方式预防CRBSI的效果[推荐意见55]患儿或人群: 肿瘤儿童;场所:医院;干预: 使用尿激酶冲管和敷贴更换频率15 d;对照: 使用肝素冲管和敷贴更换频率4 d结局患儿数量 (研究数量)相对效应值(95% CI)预期绝对效应值(事件数/千导管日)对照组风险干预组风险风险差(95% CI)证据质量证据质量降级说明使用尿激酶冲管CRBSI发生率患儿数量:680(2篇RCT的系统评价)RR=0.72(0.12~4.41)未报告未报告极低局限性:2篇RCT高偏倚风险(-2);不精确性:置信区间宽(-1);不一致性:尿激酶的剂量和用法不同(-1)4 d更换敷料vs 15 d更换敷料导管过早拔除率患儿数量:113(1篇RCT的系统评价)000极低1篇RCT高偏倚风险(-1)
17.2 导管相关性血栓
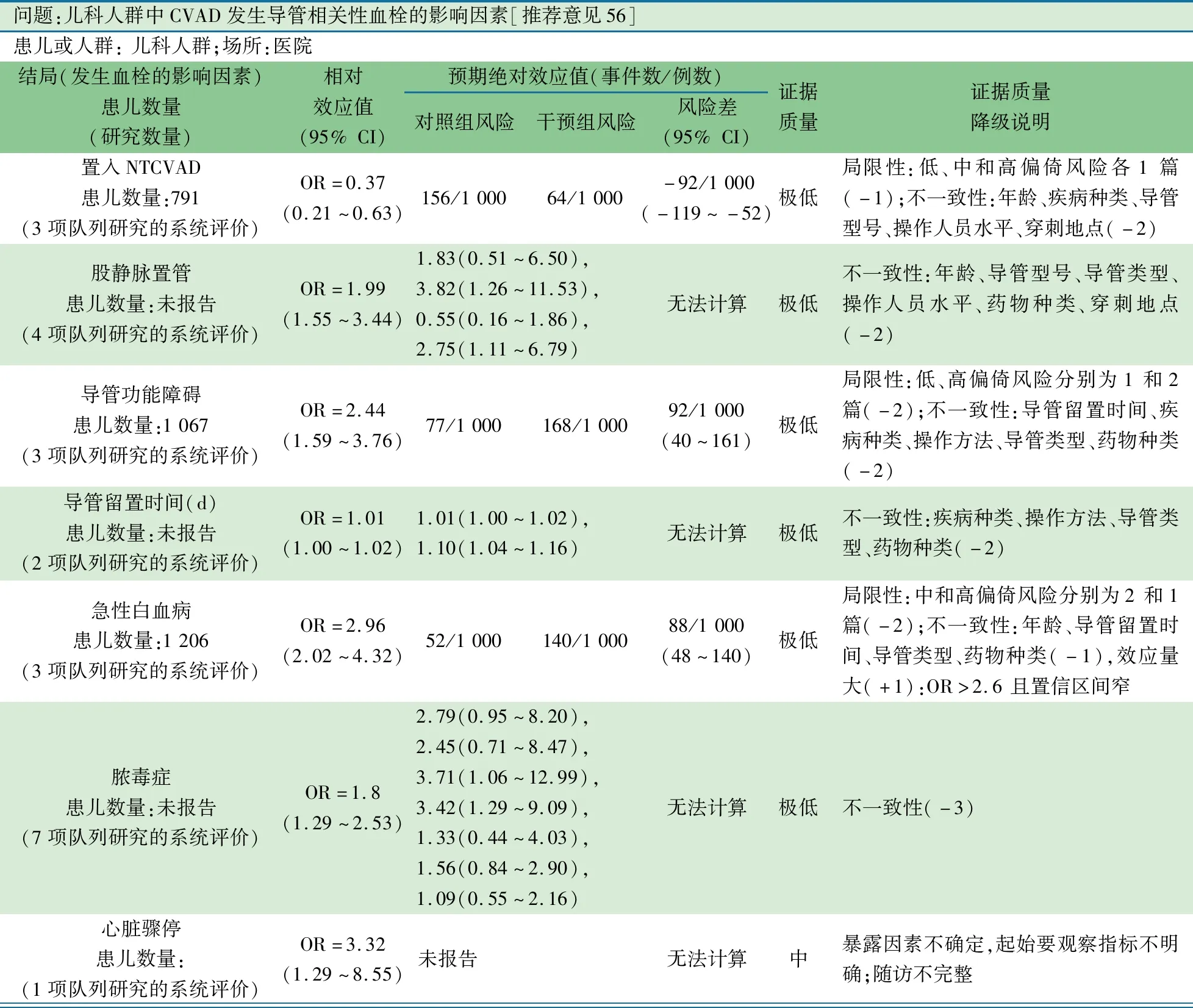
推荐意见(56) CVAD 相关血栓的发生中,NTCVAD是保护因素,急性白血病、脓毒症、股静脉置管部位、导管功能障碍、治疗使用肠外营养、导管留置时间长是重要的危险因素(1D)。
推荐说明 1项2020年来自《中国循证儿科杂志》的儿科CVAD 相关血栓发生的保护和危险因素的系统评价/Meta分析[3],纳入了13篇队列研究和1篇巢式病例对照研究,纳入置入CVAD 的住院新生儿至青少年人群,排除使用CVAD 行肾脏替代治疗的患儿,CVAD 相关性血栓的诊断均来自静脉造影或静脉超声检查(发生率3.3%~30.3%),3 848根CVAD 导管纳入分析,其中PICC 538根、NTCVAD 509根、TcCVAD 241根、TIVD 583根;颈内静脉置管360根,锁骨下静脉置管354根,股静脉置管162根;219 根导管出现导管功能障碍。CVAD因素中的NTCVAD、股静脉置管、导管功能障碍、导管留置时间每增加1 d,疾病状态因素中的急性白血病、脓毒症、心脏骤停、单心室,治疗过程中的使用门冬酰胺酶、输入肠外营养、使用糖皮质激素均为CVAD相关血栓的影响因素。
问题:儿科人群中CVAD发生导管相关性血栓的影响因素[推荐意见56]患儿或人群: 儿科人群;场所:医院结局(发生血栓的影响因素)患儿数量 (研究数量)相对效应值(95% CI)预期绝对效应值(事件数/例数)对照组风险干预组风险风险差(95% CI)证据质量证据质量降级说明置入NTCVAD患儿数量:791(3项队列研究的系统评价)OR=0.37(0.21~0.63)156/1 00064/1 000-92/1 000(-119~-52)极低局限性:低、中和高偏倚风险各1 篇(-1);不一致性:年龄、疾病种类、导管型号、操作人员水平、穿刺地点(-2)股静脉置管患儿数量:未报告(4项队列研究的系统评价)OR=1.99(1.55~3.44)1.83(0.51~6.50),3.82(1.26~11.53),0.55(0.16~1.86),2.75(1.11~6.79)无法计算极低不一致性:年龄、导管型号、导管类型、操作人员水平、药物种类、穿刺地点(-2)导管功能障碍患儿数量:1 067(3项队列研究的系统评价)OR=2.44(1.59~3.76)77/1 000168/1 00092/1 000(40~161)极低局限性:低、高偏倚风险分别为1 和2 篇(-2);不一致性:导管留置时间、疾病种类、操作方法、导管类型、药物种类(-2)导管留置时间(d)患儿数量:未报告(2项队列研究的系统评价)OR=1.01(1.00~1.02)1.01(1.00~1.02),1.10(1.04~1.16)无法计算极低不一致性:疾病种类、操作方法、导管类型、药物种类(-2)急性白血病患儿数量:1 206(3项队列研究的系统评价)OR=2.96(2.02~4.32)52/1 000140/1 00088/1 000(48~140)极低局限性:中和高偏倚风险分别为2 和1 篇(-2);不一致性:年龄、导管留置时间、导管类型、药物种类(-1),效应量大(+1):OR>2.6 且置信区间窄脓毒症患儿数量:未报告(7项队列研究的系统评价)OR=1.8(1.29~2.53)2.79(0.95~8.20),2.45(0.71~8.47),3.71(1.06~12.99),3.42(1.29~9.09),1.33(0.44~4.03),1.56(0.84~2.90),1.09(0.55~2.16)无法计算极低不一致性(-3)心脏骤停患儿数量:(1项队列研究的系统评价)OR=3.32(1.29~8.55)未报告无法计算中暴露因素不确定,起始要观察指标不明确;随访不完整
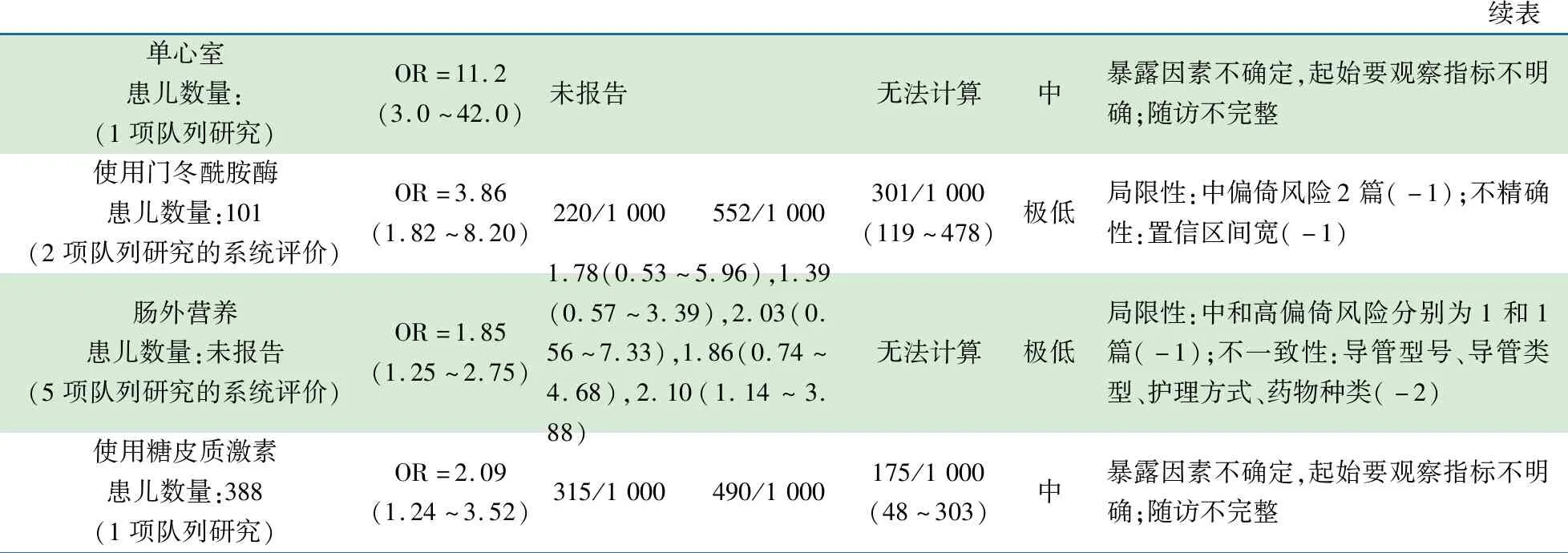
续表 单心室患儿数量:(1项队列研究)OR=11.2(3.0~42.0)未报告无法计算中暴露因素不确定,起始要观察指标不明确;随访不完整使用门冬酰胺酶患儿数量:101(2项队列研究的系统评价)OR=3.86(1.82~8.20)220/1 000552/1 000301/1 000(119~478)极低局限性:中偏倚风险2篇(-1);不精确性:置信区间宽(-1)肠外营养患儿数量:未报告(5项队列研究的系统评价)OR=1.85(1.25~2.75)1.78(0.53~5.96),1.39(0.57~3.39),2.03(0.56~7.33),1.86(0.74~4.68),2.10(1.14~3.88)无法计算极低局限性:中和高偏倚风险分别为1和1篇(-1);不一致性:导管型号、导管类型、护理方式、药物种类(-2)使用糖皮质激素患儿数量:388(1项队列研究)OR=2.09(1.24~3.52)315/1 000490/1 000175/1 000(48~303)中暴露因素不确定,起始要观察指标不明确;随访不完整
推荐意见(57) 在没有调整DVT病因的基础上,基于DVT的发生概率,选择PICC和NTCVAD没有更好的提示意义(2D)。
推荐说明 2013年1项单中心基于出院患儿信息库的横断面调查[102]。纳入2005至2012年所有入院的留置CVAD(隧道式导管和PICC)的<18岁患儿,排除CVC(例如经颈内静脉或锁骨下静脉)和同时留置多根CVC导管的患儿。深静脉血栓(DVT)诊断依据ICD-9。PICC导管发生DVT为2.55%(152/5 963),TcCVAD发生DVT为3.05%(29/952),差异无统计学意义(χ2=0.436,P=0.518)。
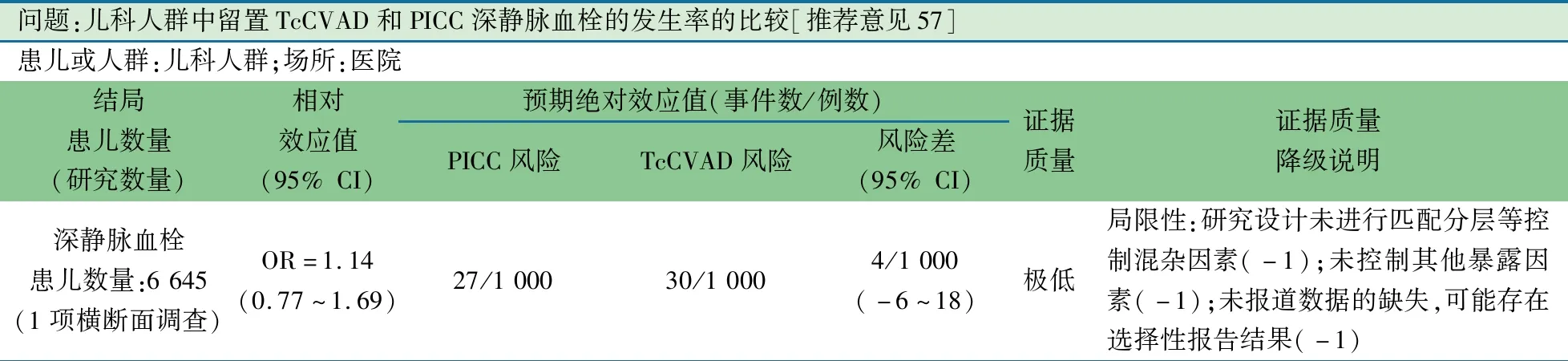
问题:儿科人群中留置TcCVAD和PICC深静脉血栓的发生率的比较[推荐意见57]患儿或人群:儿科人群;场所:医院 结局患儿数量 (研究数量)相对效应值(95% CI)预期绝对效应值(事件数/例数)PICC风险TcCVAD风险风险差(95% CI)证据质量证据质量降级说明深静脉血栓患儿数量:6 645(1项横断面调查)OR=1.14(0.77~1.69)27/1 00030/1 0004/1 000(-6~18)极低局限性:研究设计未进行匹配分层等控制混杂因素(-1);未控制其他暴露因素(-1);未报道数据的缺失,可能存在选择性报告结果(-1)
推荐意见(58) 选择从身体左侧或右侧置入CVC对降低静脉血栓事件(VTE)的发生没有显示出优劣;仅从降低VTE的发生角度来看,置入CVC可顺序选择颈静脉、锁骨下静脉、头臂静脉、股静脉(1B)。
推荐说明 1项来自北美9个中心的回顾性队列研究[103]。纳入1997至1999年6月龄至18岁的急性淋巴细胞性白血病(ALL)诱导化疗开始的2周内、留置CVC导管、接受了抗凝血酶预防治疗的连续患儿。排除曾对抗凝血酶任何成分过敏、有其他药物干扰或入组30 d后需要其他药物治疗性抗凝的患儿。85例患儿中29例(34%)发生VTE。在调整了年龄、身高、体重、性别、ALL严重分型后,logistic回归分析显示,经皮肤直接或静脉切开穿刺,CVC位置(身体左侧vs身体右侧、锁骨下静脉vs颈静脉)与VTE相关。经皮肤直接穿刺(21/45)是经静脉切开穿刺(8/40)置入CVC发生VTE的3.5倍(OR=3.5,95%CI:1.3~9.2),从身体左侧置入(19/43)是右侧置入(10/42)CVC发生VTE的2.5倍(OR=2.5,95%CI:1.0~6.4,P=0.048)。
1项欧美14个医疗中心的回顾性队列研究[104],纳入1998至1999年在上静脉系统或下静脉系统首次留置CVC或者留置CVC与既往位置相同、年龄<18岁的连续病例,排除6周内诊断任意位置存在VTE、在原确诊VTE处留置导管和不能进行静脉造影等患儿。158例中21例发生VTE。导管位置、患儿年龄、人种进入多因素分析,股静脉(6/19)是其他(锁骨下、头臂、颈)静脉(15/139)置入CVC发生VTE的5.2倍(OR=5.17,95%CI:1.18~22.3),头静脉(4/33)与锁骨下静脉(4/15)置入CVC发生VTE差异无统计学意义(OR=0.45,95%CI:0.13~1.58)。患儿不同年龄(6岁以上和以下)和不同人种(白人和非白人)置入CVC发生VTE差异无统计学意义。基于以上2个研究的Meta分析显示,颈静脉(14/126)较锁骨下静脉(26/65)置入CVC可少发生71%VTE(OR=0.29,95%CI:0.13~0.66)。
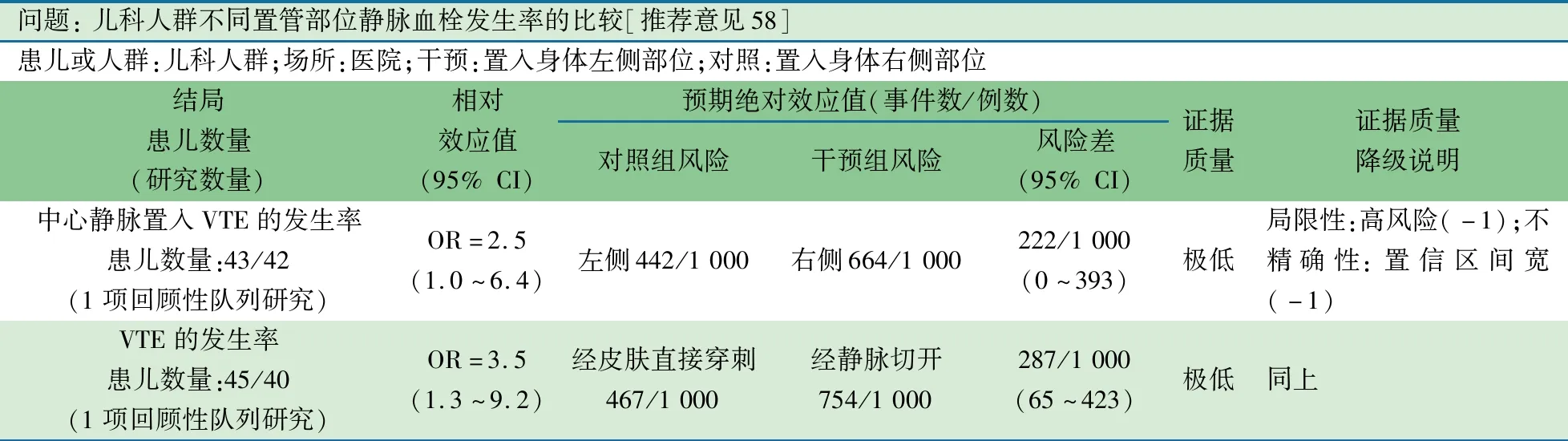
问题: 儿科人群不同置管部位静脉血栓发生率的比较[推荐意见58]患儿或人群:儿科人群;场所:医院;干预:置入身体左侧部位;对照:置入身体右侧部位结局患儿数量 (研究数量)相对效应值(95% CI)预期绝对效应值(事件数/例数)对照组风险干预组风险风险差(95% CI)证据质量证据质量降级说明中心静脉置入VTE的发生率患儿数量:43/42(1项回顾性队列研究)OR=2.5(1.0~6.4)左侧442/1 000右侧664/1 000222/1 000(0~393)极低局限性:高风险(-1);不精确性:置信区间宽(-1)VTE的发生率患儿数量:45/40(1项回顾性队列研究)OR=3.5(1.3~9.2)经皮肤直接穿刺467/1 000经静脉切开754/1 000287/1 000(65~423)极低同上
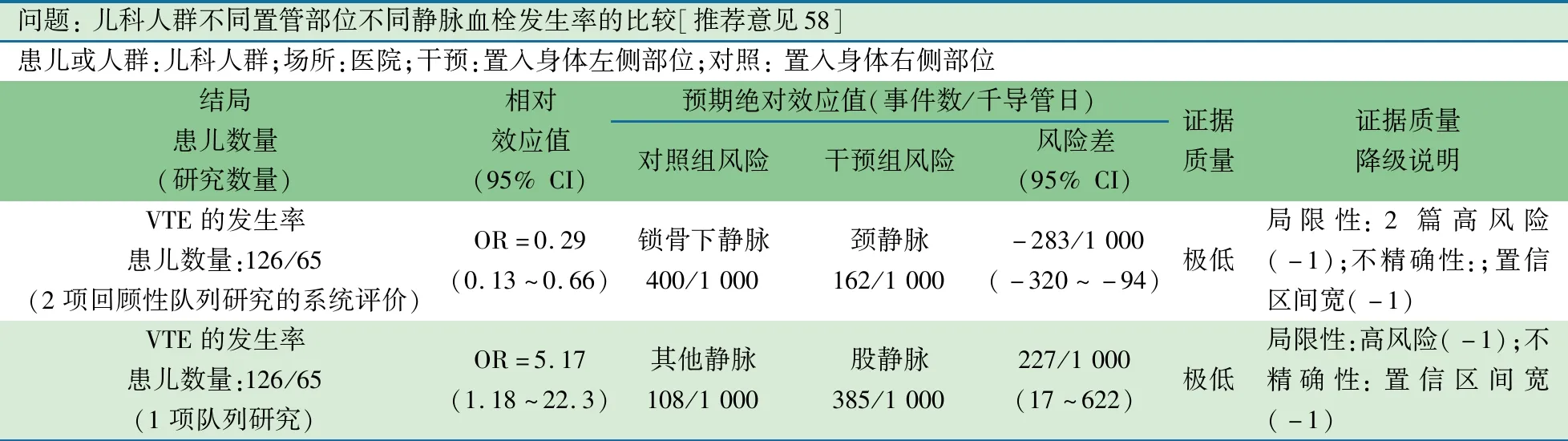
问题: 儿科人群不同置管部位不同静脉血栓发生率的比较[推荐意见58]患儿或人群:儿科人群;场所:医院;干预:置入身体左侧部位;对照: 置入身体右侧部位结局患儿数量 (研究数量)相对效应值(95% CI)预期绝对效应值(事件数/千导管日)对照组风险干预组风险风险差(95% CI)证据质量证据质量降级说明VTE的发生率患儿数量:126/65(2项回顾性队列研究的系统评价)OR=0.29(0.13~0.66)锁骨下静脉400/1 000颈静脉162/1 000-283/1 000(-320~-94)极低局限性:2篇高风险(-1);不精确性:;置信区间宽(-1)VTE的发生率患儿数量:126/65(1项队列研究)OR=5.17(1.18~22.3)其他静脉108/1 000股静脉385/1 000227/1 000(17~622)极低局限性:高风险(-1);不精确性:置信区间宽(-1)
推荐意见(59) 基于影像学诊断的CVC的DVT绝大多数是无症状的(1B)。
推荐说明 1项来自美国的单中心研究从病历中截取1999至2001年因肿瘤住院留置CVC导管数据[105],1项北美9个中心1997至1999年住院的急性淋巴细胞性白血病(ALL)留置CVC导管数据[103],1项加拿大单中心2010至2011年诊断为恶性肿瘤患儿的CVC数据[106],1项欧美14个中心1998至1999年儿科CVC数据[104],基于肝素、tPA处理仍堵塞,临床医生选择影像学诊断是否堵塞,美国单中心287例患儿中21例影像学诊断为导管相关的DVT(有症状5例,无症状16例),北美多中心85例患儿中29例影像学诊断为导管相关的DVT(有症状5例,无症状24例),加拿大单中心330例中73例影像学诊断为导管相关的DVT(有症状2例,无症状71例),欧美14个中心158例中21例影像学诊断为导管相关的DVT(有症状6例,无症状15例),合并数据显示,有症状DVT为18/144例,无症状DVT为126/144例(87.5%)。
推荐意见(60) DVT增加发生反复堵塞事件和感染的风险(1C)。
推荐说明 加拿大单中心330例中有73例影像学诊断为CVAD相关的DVT[106],观察在无症状VAD堵塞时,使用tPA处理前是否常规X线摄片,发现2例位置不正(TIVD插针位置不正、PICC内部断裂各1例)有组织型纤溶酶激活剂(tPA)治疗风险。调整了中心静脉导管的种类、性别、管腔数、年龄和留置时间后,无症状导管堵塞病例tPA使用前行X线检查可发现1.8%的tPA治疗风险。
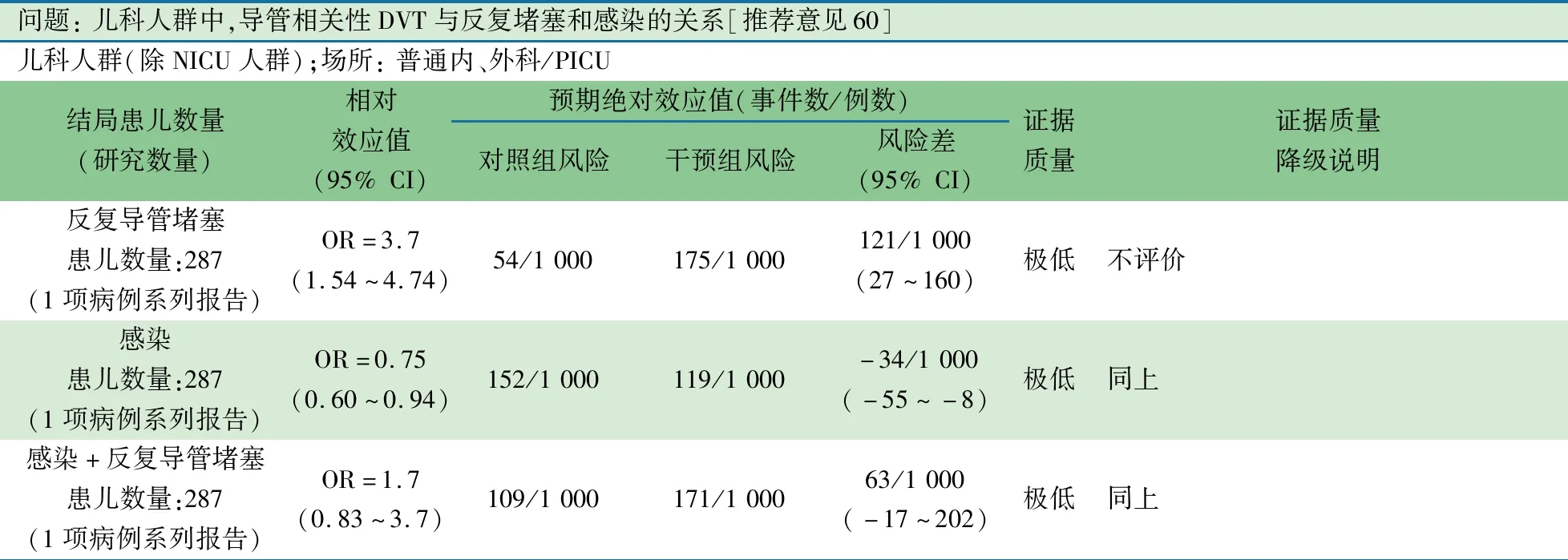
问题: 儿科人群中,导管相关性DVT与反复堵塞和感染的关系[推荐意见60]儿科人群(除NICU人群);场所: 普通内、外科/PICU结局患儿数量 (研究数量)相对效应值(95% CI)预期绝对效应值(事件数/例数)对照组风险干预组风险风险差(95% CI)证据质量证据质量降级说明反复导管堵塞患儿数量:287(1项病例系列报告)OR=3.7(1.54~4.74)54/1 000175/1 000121/1 000(27~160)极低不评价感染患儿数量:287(1项病例系列报告)OR=0.75(0.60~0.94)152/1 000119/1 000-34/1 000(-55~-8)极低同上感染+反复导管堵塞患儿数量:287(1项病例系列报告)OR=1.7(0.83~3.7)109/1 000171/1 00063/1 000(-17~202)极低同上
美国单中心[105]287例(444根CVC导管)患儿中21例(57根CVC导管)影像学诊断为导管相关的DVT,DVT组(10/57根)反复堵塞事件发生数是非DVT组(21/387根)的3.7倍(OR=3.7,95%CI:1.54~4.74),DVT组(16/57根)感染发生率较非DVT组(59/387根)下降了25%(OR=0.75,95%CI:0.60~0.94);DVT组(10/57根)同时存在堵塞和感染发生率是非DVT组(42/387根)的1.7倍(OR=1.7,95%CI:0.83~3.7)。
17.3 其他并发症
推荐意见(61) 普通内、外科和PICU环境中,患儿年龄越大(婴儿、学龄前、学龄),因并发症导致的PICC拔除的风险越低,导管头端不在中心位置可发生PICC非感染性并发症,PICU暴露可发生PICC感染性并发症(1D)。
推荐说明 2013年1项来自美国单中心PICC导管并发症危险因素的回顾性队列研究[107],纳入外科病区和PICU的全部患儿,以置入PICC为队列起点,以PICC拔除(因发生并发症或治疗结束不再需要时)为队列终点。1 807例患儿2 574根PICC导管46 021导管日进入分析。调整了导管留置时间、年龄、置管部位、PICU暴露、PICC置管指征和置入PICC的年龄,①PICC拔除的危险因素:导管末端不在中心位置(IRR=4.59,95%CI=3.69~5.69),年龄>1岁(IRR=0.75,95%CI:0.60~0.94),PICU暴露(IRR=1.24,95%CI:1.03~1.52);②导管非感染性并发症的危险因素为导管末端不在中心位置(IRR=4.56,95%CI:3.67~5.61);③导管感染性并发症的危险因素为ICU暴露(IRR=2.23,95%CI:1.43~3.48)。
18 指南工作组及其职责
18.1 指南工作组的组成 指南工作组由核心专家组、共识专家组、指南审稿专家组和文献初筛护士组组成。①核心专家群由复旦大学附属中山医院、复旦大学附属儿科医院护理部、临床指南制作和评价中心人员组成;②共识专家组由国内23家儿童医院或综合医院儿科从事儿童护理专业至少10年以上的专家组成;③审稿专家组由中华医学会儿科学分会护理学组(筹)全体成员组成;④文献初筛护士组由共识专家组所在医院的护理骨干组成,至少有3年以上护理工作经验,并具有英文文献阅读和理解能力。
18.2 指南工作组的职责
18.2.1 核心专家组主要工作 (1)指南选题产生:①检索儿童输液指南并提炼相关问题,并结合核心专家组的护理实践产生指南征求意见选题(11个维度和54个条目池雏形);②在共识专家组中经过信函和面对面讨论各1轮征求意见,总结归纳讨论意见后,确定9个维度,37个条目);③核心专家群讨论决定维度3、4、6和8为通过系统综述回答的问题,维度1、2、5、7、9为通过专家共识回答的问题。(2)系统综述回答的问题:①分别构建PICOS;②与文献检索专家多轮沟通调试检索词和检索式;③建立下载文献数据库并编码;④文献筛选标准建立和培训;⑤文献筛选质量控制;⑥文献评价和证据体的产生;⑦形成证据概要表;⑧基于证据、患儿及其家长价值观和卫生经济学产生推荐意见;⑨面对面专家外审会。(3)专家共识维度问题:①核心组起草共识问题初稿;②召开共识专家讨论会;③核心组归纳总结专家共识推荐意见。
18.2.2 共识专家组主要工作 ①参与指南选题维度和条目讨论,②参与专家共识维度面对面逐个维度和条目讨论和表决。
18.2.3 审稿专家组主要工作 参与系统综述推荐意见和专家共识的审稿。
18.2.4 文献初筛护士 对系统检索的文献进行筛选。
19 文献筛选结果
中文检索CBM和CNKI数据库查重后6 875篇;英文检索PubMed、Cochrane 图书馆和EMBASE数据库查重后20 487篇,检索和筛选流程如图21。
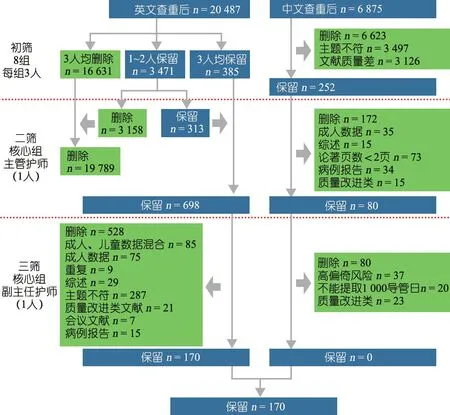
图21 文献筛选流程图
20 GRADE评价工具[108]
GRADE将RCT、诊断准确性研究组成的证据体初始作为高质量证据,观察性(队列、病例对照、横断面)研究组成的证据体初始作为低质量证据。降低证据质量的因素:①研究设计和实施的局限性:根据不同的研究类型选择相应的评价工具:病例对照研究和队列研究以NOS量表作为评价工具,满足11项中的8项及以上为偏倚风险低[109],横断面研究以AHRQ量表作为评价工具,满足13项中的9项以上为偏倚风险低[110],RCT以Cochrane系统评价员手册6条标准作为评价工具[108],非RCT以ROBINS-Ⅰ为工具[111],系统评价和Meta分析以AMSTAR作为评价工具[112];②效应量估计值不精确;③研究结果不一致性;④间接证据;⑤发表偏倚。仅针对观察性研究提升证据质量的因素:①效应值很大;②明确的混杂因素降低了疗效;③存在明显的量效关系。
21 更新计划
本指南预计每5年更新1次。当指南中推荐意见有新证据显示利弊方向发生相反或有新的干预出现时,将考虑对指南进行更新。
22 指南的制定主要事件时间表
2017年12月至2018年2月指南制定准备工作(既有指南筛选和评价)。
2018 年 3月 9日指南制做启动会在上海召开。
2018年4~5月,基于既有指南选题,建立指南选题维度和条目。
2018年6~8月对选题维度和条目PICO构建和文献检索。
2018年8~11月文献初筛。
2018年12月至2019年4月共识维度进行专家共识。
2018年11月至2019年6月指南文献二筛和三筛。
2019年7月至2020年3月指南文献提取和证据评价。
2020年3~8月指南推荐意见产生。
2020年8月至2021年2月20日指南撰写。
23 指南工作组
23.1 指南核心专家组 复旦大学附属中山医院:张玉侠;复旦大学附属儿科医院护理部:顾莺、王文超、王颖雯、康琼芳、季福婷;复旦大学附属儿科医院临床指南制作和评价中心:张崇凡、王瑞。
23.2 共识专家组 辽宁省大连市儿童医院:崔妮;安徽省儿童医院:王国琴;山东省济南市儿童医院:徐群;浙江大学医学院附属儿童医院:陈朔晖;苏州大学附属儿童医院:姚文英;郑州大学第一附属医院:杨芳;华中科技大学同济医学院附属同济医院:叶天惠;广东省深圳市儿童医院:付勤;南京医科大学附属儿童医院:李梅;陕西省西北妇女儿童医院:马莉;四川大学华西第二医院:赵秀芳;重庆医科大学附属儿童医院:郑显兰;首都医科大学附属北京儿童医院:张琳琪;广东省广州市妇女儿童医疗中心:林艳;陕西省西安市儿童医院:李荣;上海市儿童医院:陆群峰;中山大学附属第一医院:李智英;上海交通大学医学院附属上海儿童医学中心:陆红。
23.3 审稿专家组 复旦大学附属中山医院:张玉侠;首都医科大学附属北京儿童医院:张琳琪;浙江大学医学院附属儿童医院:陈朔晖;四川大学华西第二医院:赵秀芳;中国医科大学附属盛京医院:范玲;中国医学科学院北京协和医科大学协和医院儿科:孙静;上海交通大学医学院附属上海儿童医学中心:陆红;上海市儿童医院:陆群峰;重庆医科大学附属儿童医院:郑显兰;温州医科大学附属第二医院:张丽萍;南京医科大学附属儿童医院:李梅;江苏省南京市妇幼保健院:翁莉;安徽省儿童医院:王国琴;河南省郑州市儿童医院:石彩晓;山东省立医院:孙献梅;四川省成都市妇女儿童中心医院:王世平;河北省武汉市妇女儿童医疗保健中心:花芸;华中科技大学同济医学院附属同济医院:叶天惠;湖南省儿童医院:朱丽辉;广东省深圳市儿童医院:付勤;广东省广州市妇女儿童医疗中心:林艳;江西省儿童医院:刘晓姝;甘肃省妇幼保健院:李尕梅;陕西省西安市儿童医院:李荣;新疆维吾尔自治区乌鲁木齐儿童医院:刘彭;贵州省人民医院:朱小莉;复旦大学附属儿科医院:顾莺。
23.4 文献初筛护士组 辽宁省大连市儿童医院:李楠楠;安徽省儿童医院:许蕾;山东省济南市儿童医院:苏莉莉;浙江大学医学院附属儿童医院:陈晓飞;苏州大学附属儿童医院:杨巾夏;湖南省儿童医院:刘美丽;郑州大学第一附属医院:张汛滔;华中科技大学同济医学院附属同济医院:熊晓菊;广东省深圳市儿童医院:黄雀兰;中国医科大学附属盛京医院:盖丽、于新颖;南京医科大学附属儿童医院:孙小静;四川大学华西第二医院:马晶晶;重庆医科大学附属儿童医院:冷虹瑶;首都医科大学附属北京儿童医院:王春丽;广东省广州市妇女儿童医疗中心:春晓;陕西省西安市儿童医院:孙文华;上海市儿童医院:李有蔚;中山大学附属第一医院:杨红梅;上海交通大学医学院附属上海儿童医学中心:李倩;河南省儿童医院:王建丽;中山大学附属第一医院:杨红梅。
24 附表
24.1 置管操作流程 附表1~9。

附表1 外周静脉短导管或外周静脉留置针置管操作流程

续表 2 解释向患儿及家长解释外周静脉短导管置管的过程、风险及优势3 穿刺部位选择扎止血带,选择粗直、易见、弹性好、不易滑动的静脉,穿刺部位避开之前静脉穿刺部位、静脉分支、关节部位、触诊疼痛部位、有开放性伤口、瘢痕增生、曾发生过静脉炎或静脉外渗的部位4 皮肤消毒选择适合患儿的皮肤消毒液对穿刺处进行消毒,并充分待干5 穿刺置管扎止血带,检查外周静脉短导管可用性,进行静脉穿刺,见回血 后,将导管完全送入血管松开止血带6 固定用透明敷贴,采取“无张力粘贴法”,以穿刺点为中心覆盖整个导管7 冲封管消毒输液接头,脉冲式冲管,正压封管8 记录标记置管日期、时间和置管者9 健康宣教

附表2 新生儿PICC置管操作流程

续表 鞘,从穿刺鞘处匀速、缓慢送入PICC导管8.2 上肢置管时,导管送至腋下需将头转向置管侧,下颌靠近 胸部,继续送管;送入至所需长度后抽回血;抽到回血后,将穿 刺鞘退出血管9 固定9.1 连接输液接头;将导管适当做弧形弯曲,蝶翼置皮肤平整 处,避开骨突关节处以2条胶布交叉固定9.2 另取1条胶布固定在蝶翼和导管接口处;用透明敷贴,采 取“无张力粘贴法”,以穿刺点为中心覆盖整个导管及蝶翼10 冲封管消毒输液接头,脉冲式冲管,正压封管11 定位通过X线/超声/心电导引确定置入导管头端位置12 记录标记置管日期、时间和置管者。记录置管静脉、穿刺过程、导管总长、置入长度及外露长度、导管头端位置

附表3 儿童超声引导下PICC置管操作流程

续表 8.2 穿刺点以利多卡因皮下注射局麻;一手持超声探头对准预 穿刺血管,一手将穿刺针插入导针器进针8.3 超声屏幕见针头进入血管,回血从针头持续滴出后,经穿 刺针缓慢送入导丝,期间保持探头在位;沿导丝退出穿刺针; 用手术刀在导丝插入部位纵向作一切口8.4 置入血管穿刺鞘;从穿刺鞘处匀速、缓慢送入PICC导管; 上肢置管时,导管送至腋下需将头转向置管侧,下颌靠近胸 部,继续送管;送入至所需长度后抽回血;抽到回血后,将穿刺 鞘退出血管9 固定9.1 连接输液接头;将导管适当做弧形弯曲,蝶翼置皮肤平整 处,避开骨突关节处以2条胶布交叉固定9.2 另取1条胶布固定在蝶翼和导管接口处;用透明敷贴,采 取“无张力粘贴法”,以穿刺点为中心覆盖整个导管及蝶翼10 冲封管消毒输液接头,脉冲式冲管,正压封管11 定位通过X线/超声/心电导引确定置入导管头端位置12 记录标记置管日期和时间、操作者。记录置管静脉,穿刺过程,导管总长、置入长度及外露长度、导管头端位置13 健康宣教

附表4 新生儿PICC维护操作流程

附表5 儿童中心静脉导管(PICC、CVC)维护操作流程

续表 1.2 导管外露长度;双侧臂围/腿围;敷贴有无卷边、潮湿、污 染;穿刺点有无红、肿、分泌物及渗血;敷贴固定下皮肤有无 皮疹/湿疹;周围皮肤有无无张力性水疱及破损2 解释向患儿及其家长解释操作目的和操作过程3 建立无菌工作区,将穿刺所需用物以无菌技术置于工作区; 置管侧肢体下铺无菌治疗巾4 皮肤消毒4.1 戴清洁手套,用酒精棉棒对敷贴下皮肤及导管进行清洁 4.2 用洗必泰棉棒对敷贴覆盖下及周围皮肤和外露导管进行 消毒,范围大于敷贴面积;充分待干5 冲封管:消毒输液接头,接预冲式注射器,回抽,见回血后脉 冲式冲管,正压封管6 固定6.1 戴无菌手套,将导管适当做弧形弯曲,避开骨突关节处以2 条胶布交叉固定6.2 另取1条胶布固定在蝶翼和导管接口处;用透明敷贴,采 取“无张力粘贴法”,以穿刺点为中心覆盖整个导管及蝶翼7 记录标记维护日期、时间和操作者。导管外露长度,双侧臂围/腿围,敷贴覆盖下及周围皮肤情况,穿刺点情况,是否抽到回血,导管是否通畅。导管留置期间健康宣教内容

附表6 中心静脉导管(PICC、CVC)拔管操作流程

附表7 儿童静脉输液港插针操作流程

续表 肤有无红肿、疼痛、破损、皮疹/湿疹2 解释向患儿及其家长解释操作的目的和过程3 建立无菌工作区,将穿刺所需用物以无菌技术置于工作区4 皮肤消毒4.1 戴清洁手套,选择适合患儿的皮肤消毒液对港体处及周围 皮肤进行消毒4.2 充分待干,上铺洞巾,暴露港体5 预冲式注射器预冲蝶翼针,连接输液接头6 插针6.1 触诊港体后,以一手拇指、食指和中指固定输液港(勿过度 绷紧皮肤),一手持输液港插针经皮进入港体6.2 回抽见回血后脉冲式冲管,100 U·mL-1肝素盐水封管(剂 量根据港体大小),并夹管7 固定7.1 用透明敷贴,采取“无张力粘贴法”固定蝶翼针,确保贴合 胸壁皮肤7.2 延长管以胶布U型固定于同侧胸壁8 记录标记插针日期、时间和操作者。港体及周围皮肤情况,穿刺点情况,是否抽到回血,导管是否通畅9 健康宣教

附表8 儿童静脉输液港拔针操作流程

附表9 静脉输液操作流程
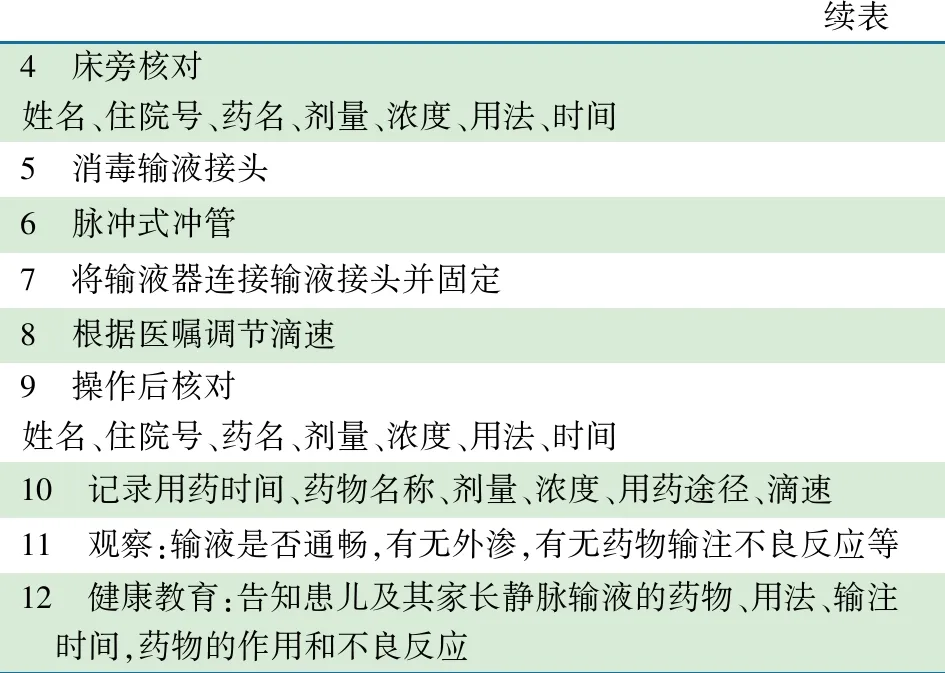
续表 4 床旁核对姓名、住院号、药名、剂量、浓度、用法、时间5 消毒输液接头6 脉冲式冲管7 将输液器连接输液接头并固定8 根据医嘱调节滴速9 操作后核对姓名、住院号、药名、剂量、浓度、用法、时间10 记录用药时间、药物名称、剂量、浓度、用药途径、滴速11 观察:输液是否通畅,有无外渗,有无药物输注不良反应等12 健康教育:告知患儿及其家长静脉输液的药物、用法、输注 时间,药物的作用和不良反应
24.2 置管宣教要点 附表10~14。

附表10 住院期间PIVC患儿宣教内容要点

附表11 住院期间外周Midline患儿宣教内容要点

附表12 住院期间PICC患儿宣教内容要点

附表13 住院期间CVC患儿宣教内容要点

附表14 住院期间TIVD患儿宣教内容要点
24.3 置管知情同意要点 附表15~20。

附表15 PIVC知情同意要点

续表 优势①操作简单,套管柔软,不易穿破血管,可在静脉内放置较长时间,避免患儿多次穿刺的痛苦;②门诊患儿可携带回家,不影响患儿活动及沐浴;③在患儿不需要时,需到医院由专业护理人员拔除潜在风险静脉炎、导管堵塞、PIVC置管失败、血栓形成、药物外渗、穿刺点出血及疼痛、导管材质过敏、固定材料过敏替代方案可考虑CVC或PICC替代

附表16 PICC知情同意要点

附表17 CVC(锁骨下静脉/腹股沟静脉/颈内静脉)知情同意要点

附表18 UVC知情同意要点

续表 的发生率;④方便监测病情,如监测动脉血气、动脉血压及中心静脉压等潜在风险脐血管穿破、置管失败、脐出血、血栓及导管纤维包裹形成、导管异位及导管断裂、腹胀、导管材质过敏、固定材料过敏替代方案可考虑CVC或PICC替代

附表19 Midline知情同意要点

附表20 TIVD知情同意要点

