大脑前动脉A1段优势供血与前交通动脉瘤发生破裂相关性分析
熊凡凡 曹玉林 杨光钊 王宇军 魏福全
颅内动脉瘤是造成蛛网膜下腔出血的常见原因之一。前交通动脉瘤(anterior communicating aneurysms,ACoA)约占颅内动脉瘤的25%。颅内动脉瘤常好发于血管分叉处,血流动力学改变在其发生、发展及破裂过程发挥极其重要的作用[1-2]。Wills 环为平衡双侧颈内动脉、前及后循环血流的重要途经[3]。然而,大量研究报道发现Wills 环存在不同类型的变异,其中Wills 环前循环变异约2%~22%[4-7]。Wills 环前循环变异主要表现为单侧大脑前动脉A1 段发育不良或缺如,从而单侧血流量增加,表现为单侧大脑前动脉A1 段优势供血,使得双侧血流动力学不平衡[3,8],可能促进前交通动脉发生。CT 血管成像(computerized tomography angiography,CTA)具有无创、便捷、可重复性强等特点,可以清晰显示Wills 环前循环变异情况。为此,本研究旨在通过CTA 技术探讨大脑前动脉A1 段优势供血与前交通动脉瘤的发生、破裂出血的相关性。
1 资料与方法
1.1 一般资料 回顾性分析本院2014 年1 月至2019年8 月48 例经数字减影血管成像(digital subtraction angiography,DSA)及CTA 证实为ACoA 患者临床及影像资料。同时,随机选取48 例无前交通动脉瘤患者设为对照组。前交通动脉组入选标准:(1)数字减影血管成像或临床证实为ACoA;(2)术前行头颅CTA 检查。对照组入组标准:(1)CTA 证实无前交通动脉瘤;(2)临床无ACoA 相关症状;(3)性别、年龄与前交通动脉组相匹配。前交通动脉组与对照组排除标准:(1)合并有其他血管畸形、肿瘤等继发大脑前动脉A1 段改变;(2)图像质量不佳,如运动伪影,颅底其他部位动脉瘤夹闭术后金属伪影。
1.2 检查方法 检查前准备:检查前禁食4~6 h。所有患者均使用SIEMENS SOMATON Definition Flash双源CT 行CTA 扫描,扫描采用Volume 模式,管电压100 kV,使用4D care 自动调节管电流技术,旋转时间0.5 s/r,准直器宽度128 mm×0.6 mm,机架旋转时间280 ms,螺距0.9 mm。扫描范围从颈2 椎体下缘至颅顶外板。造影剂及用量:于健侧肘正中静脉按顺序注射造影剂65 ml 和生理盐水30 ml,流速5 ml/s;造影剂浓度为350 mgI/ml。
1.3 图像后处理及分析 所有图像传送至工作站(ADW4.6 GE),由2 名神经影像医师进行解读CTA 图像,如有异议,经商议后取得一致意见。首先,对CTA原始图像进行容积再现(volume rendering,VR)、多平面重组(multiplanar reconstruction,MRP)以及最大密度投影(maximum intensity projection,MIP)多种方法进行重建,多角度旋转,观察前交通动脉是否存在动脉瘤。并测量动脉瘤瘤颈径,最大横径、最大高度及纵横比(动脉瘤垂直高度与瘤颈宽度的比值),见图1)。然后,观察双侧大脑前动脉A1 段是否存在优势供血,优势供血定义为一侧大脑前动脉A1 段直径大于另一侧大脑前动脉A1 段直径的50%(发育不良)或一侧不发育(缺如),见图2;并将其分为均衡组、优势供血组。最后,观察颅内是否存在蛛网膜下腔出血。
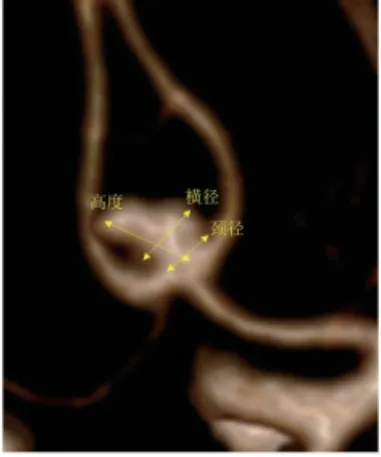
图1 前交通动脉瘤径线值测量示意图
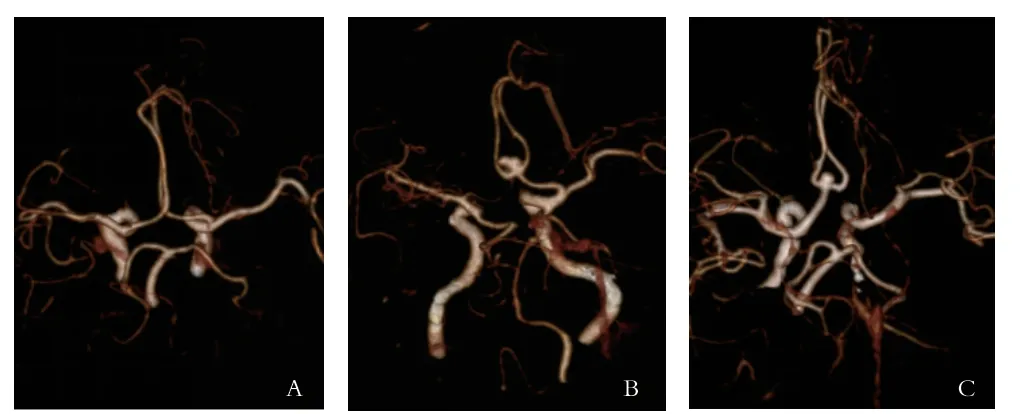
图2 大脑前动脉A1段优势供血示例。A示双侧大脑前动脉A1段对称,呈均衡型改变;B示右侧大脑前动脉A1段纤细,呈不对称左侧优势供血;C示左侧大脑前动脉A1段缺如,呈不对称性右侧优势供血;B和C示前交通动脉瘤
1.4 统计学方法 采用SPSS 20.0 统计软件。计量资料以(±s)表示,组间比较采用t检验;计数资料以n或%表示,组间比较采用χ2检验。以P<0.05 为差异有统计学意义。
2 结果
2.1 一般资料 共48 例ACoA 患者纳入研究,中位年龄57.89(15.16)岁,男33 例;其中20 例合并高血压,5 例糖尿病,6 例高血脂。ACoA 瘤颈径(3.37±1.67)mm,ACoA 最大横径(3.99±2.21)mm,ACoA 最大高度(5.57±3.32)mm,ACoA 纵横径比值(1.75±0.68)。48 例ACoA 患者中共有28 例发生破裂出血。
2.2 大脑前动脉A1 段优势供血与ACoA 发生 48 例ACoA 患者中,12 例右侧大脑前动脉A1 段缺如、6 例发育不良,10 例左侧大脑前动脉A1 段缺如、14 例发育不良,共42 例大脑前动脉A1 段优势供血。前交通动脉瘤组大脑前动脉A1 段缺如、发育不良及大脑前动脉A1 段优势供血比率明显高于对照组,差异具有统计学意义(P<0.05,见表1)。并且,是否存在大脑前动脉A1 段优势供血与ACoA 纵横径比值相关(P<0.05,图3A),大脑前动脉A1 段优势供血组ACoA 纵横径比值高于大脑前动脉A1 段均衡组。
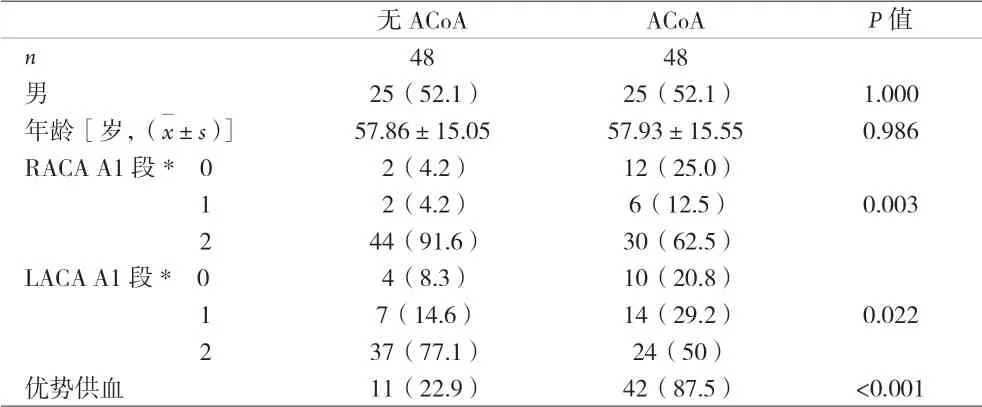
表1 大脑前动脉A1段变异与有无ACoA对比分析[n(%)]
2.3 大脑前动脉A1段优势供血与ACoA破裂 对48例ACoA 患者进行大脑前动脉A1 段优势供血亚组分析,大脑前动脉A1 段优势供血与ACoA 破裂无明显相关性(P>0.05,见图3B)。

图3 大脑前动脉A1段优势供血与ACoA纵横径比值、破裂出血对比分析。A. 大脑前动脉A1段优势供血患者ACoA纵横径比值明显高于均衡组(P<0.001,t=5.542);B. 大脑前动脉A1段优势供血与前交通动脉破裂出血不相关(P>0.05)
3 讨论
本研究发现大脑前动脉A1段优势供血与前交通动脉瘤相关,且大脑前动脉A1 段优势供血组瘤纵横径比值大于均衡组。但是,大脑前动脉A1 段优势供血与前交通动脉瘤破裂不相关。
大脑前动脉A1 段优势供血是Wills 环前循环常见的解剖变异,约2%~22%。陈述花等[9]对比分析发现CTA 与DSA 技术显示Wills 环解剖变异情况具有高度的一致性。本研究采用CTA 显示对照组大脑前动脉A1 段优势供血为22.9%,包括单侧发育不良或缺如,与文献报道基本一致[6-7]。前交通动脉瘤组中87.5%患者存在大脑前动脉A1 段优势供血,明显高于对照组。因此,本研究认为大脑前动脉A1 段优势供血与前交通动脉瘤相关,是形成前交通动脉瘤的危险因素。
多数颅内动脉瘤好发于血管分叉处或弯曲处,提示血流动力学改变是形成动脉瘤重要因素之一。本研究显示大脑前动脉A1 段优势供血ACoA 患者的瘤纵横径比值大于均衡组,间接表明ACA A1 段优势供血ACoA血管壁面切应力低。而低水平血管壁面切应力能触发炎症细胞介导的破坏性重塑途径[10],促进动脉瘤的进展。
基于血管壁面切应力改变,可能会增加前交通动脉瘤破裂的风险。但是,本研究发现大脑前动脉瘤A1段优势供血与前交通动脉瘤破裂不相关。可能原因是导致动脉瘤破裂的因素是多方面且复杂的,比如吸烟、瘤体形态不规则、A1-A2 夹角等。对于未破裂的前交通动脉瘤,是否需要干预及何时进行干预需要综合评估动脉瘤形态学特征、血流动力学特点来进行辅助决策。
大脑前动脉A1段优势供血可促进前交通动脉瘤形成,因此,在日常工作中,尤其是患者表现为动脉瘤临床症状时,CTA 检查时应该观察是否存在大脑前动脉A1 段优势供血。
本研究存在一定局限性。本研究为回顾性研究,样本量相对小,导致一定的偏倚,需要未来进一步大样本多中心前瞻性研究。
总之,大脑前动脉A1 段优势供血与前交通动脉瘤相关,是形成前交通动脉瘤危险因素,值得临床关注。大脑前动脉A1 段优势供血与前交通动脉瘤破裂不相关,不能作为临床干预的指标。

