无机与分析化学实验课程思政案例设计与探讨*
张丽影,那立艳,王 茹,华瑞年
(大连民族大学生命科学学院,辽宁 大连 116600)
2016年12月,习近平总书记在全国高校思想政治工作会议上指出,高校教育“要坚持把立德树人作为中心环节,把思想政治工作贯穿教育教学全过程,实现全程育人、全方位育人”[1]。无机与分析化学实验作为化学相关专业学生接触到的第一门基础实验课,其教学目标是使学生熟悉并掌握无机与分析化学实验的基本知识和基本操作技能,学会正确观察反应现象及数据处理方法,培养学生实事求是的科学态度,良好的实验素养,以及对问题的观察、分析、判断和解决的能力。教学内容上既包括基本技能训练,又适度增加综合性、设计性实验。如何找准课程思政点,通过何种途径加以实施,如何对思政教学效果进行评价,都需要在教学过程中不断思考并尝试。
HCl溶液的配制与标定是《无机与分析化学实验》中的必做实验,属于验证型实验[2]。实验内容上,利用基准物质Na2CO3对配置的HCl溶液进行浓度标定。实验操作上,主要为移液管和容量瓶的使用以及酸碱滴定。如何在这样一个原理清晰、操作相对简单的基础性实验中,挖掘课程思政点并通过行之有效的手段融入教学过程,笔者对这一案例进行了详细分析。
1 思政教学目标
1.1 知识素养
(1)掌握酸碱滴定的基本原理;(2)掌握酸碱指示剂的变色原理。
1.2 能力素养
(1)学习溶液的配制方法;(2)学习酸碱滴定基本操作;(3)掌握酸碱滴定的基本要点。
1.3 科学素养
(1)能够从物质结构变化的角度理解酸碱指示剂变色的本质。
(2)能够从化学计量点和滴定终点的差异出发,理解误差及科学的严谨性。
1.4 人文素养
理解和体会安全意识和规范操作在化学行业中的重要性,学会利用辩证唯物论的观点认识世界,透过现象看到本质。
2 思政融入点
根据设定的思政教学目标,将教学内容分解为四个部分,并在其中引入相应的思政点,具体如表1所示。
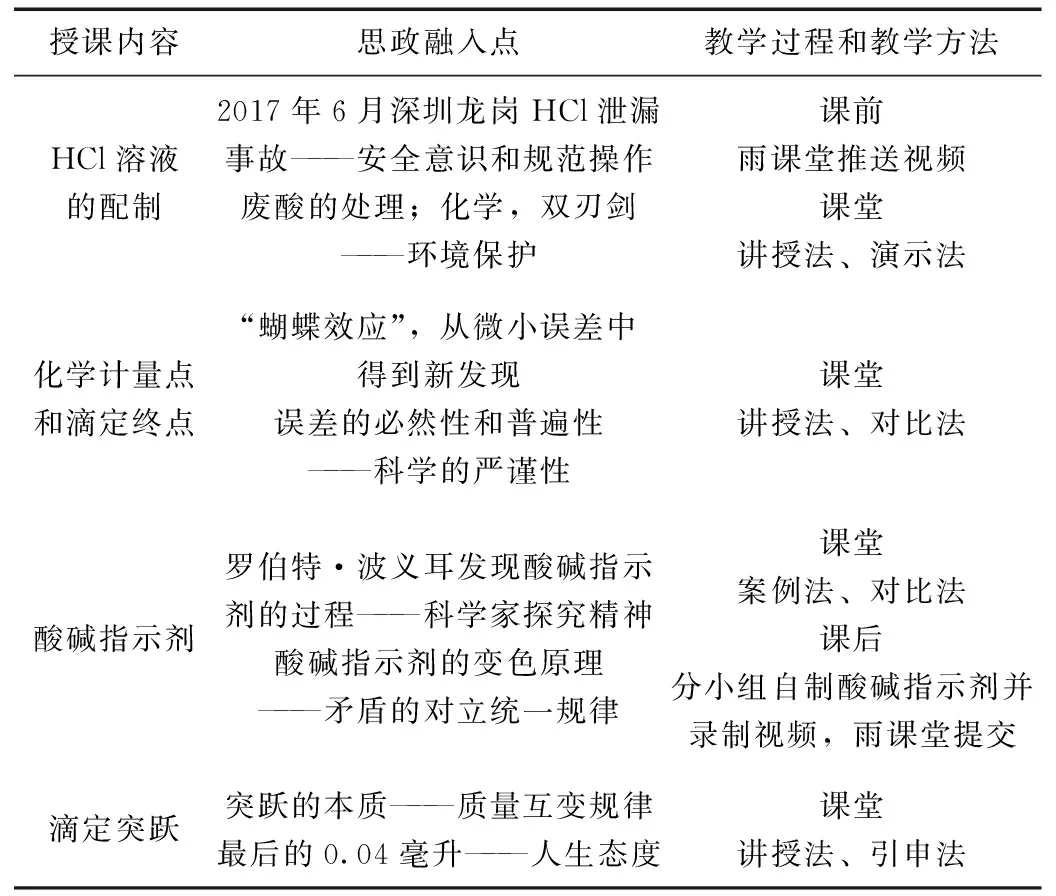
表1 《HCl溶液的配制与标定》课程思政融入点
3 教学过程及实施途径
3.1 HCl溶液的配制
(1)课前

图1 课前发送给学生的预习视频资料
利用雨课堂向学生推送预习视频,同时标注重点:浓盐酸(质量分数约为37%)具有极强的挥发性,打开盛有浓盐酸的容器后,HCl气体挥发与空气中的水蒸气结合产生盐酸小液滴,使瓶口上方出现酸雾。学生通过观看视频,初步了解盐酸的基本特性,主要用途,同时明确盐酸具有强烈的刺鼻气味,具有较高腐蚀性等特点。同时,以2017年6月深圳龙岗HCl泄露事故为例,使学生理解化学工业中,安全意识和规范操作的重要性。
(2)课堂
课堂上,首先与同学交流对HCl泄露事故的观后感,引出近年来国内高校化学实验室危险事故频发,如南京大学发生的甲醛泄露事故、北京交通大学发生的实验室爆炸等,指出实验室安全状况不容忽视,任何一个小小的疏忽,都是有可能酿成严重事故的隐患。在示范盐酸配制的过程中,指出每一步骤的注意事项及防护重点,强调必须严格遵守实验流程规定(如遇误将盐酸撒到身上并造成腐蚀时,除用大量水冲洗外,要涂抹硼碱或稀氨水中和)[3]。随后,通过介绍实验室及工业上常用的废弃HCl处理方法,引出环境保护问题。最后,回顾课前推送的预习视频,总结HCl虽危险,但其用途极为广泛,与人们的生产生活密切相关。不能因HCl的危害而拒绝使用,害怕使用,不能因噎废食,严格遵守操作规范,提高安全意识,即可有效避免危害。
3.2 HCl溶液的标定
HCl具有挥发性,因此配制的HCl溶液需要利用基准物质NaCO3标定方能确定其准确浓度。碳酸钠标定盐酸的化学反应方程式是:2HCl+Na2CO3=2NaCl+H2O+CO2
将本部分教学内容细化为三个方面,并逐一引入相应的思政点。
(1)化学计量点和滴定终点

图2 雨课堂发送给学生的习题
雨课堂发送选择题,了解学生对化学计量点和滴定重点概念的认知程度,明确化学计量点和滴定重点的差值即为滴定误差。误差与错误不同,错误是应该而且可以避免的,而误差是不可能绝对避免的。由洛伦兹提出的“蝴蝶效应”入手,引导学生认识到事物发展的结果,对初始条件具有极为敏感的依赖性。滴定过程中,药品称量的准确性、指示剂的匹配性、操作的规范性等,均对最终的误差产生影响。通过对不同指示剂变色范围的对比,计算终点误差值,进而引导学生对科学的严谨性进行讨论。
(2) 酸碱指示剂
像科学上的许多其它发现一样,酸碱指示剂的发现是化学家善于观察、勤于思考。勇于探索的结果。以玻义耳发现指示剂的过程为例,通过对科学家们严谨的治学精神、严密的科学方法、崇高的科学品质以及对真理的不懈追求的认识,培养学生的科学方法、科学精神与科学态度。
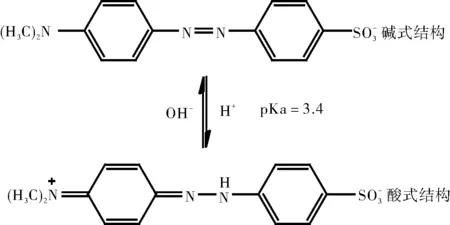
图3 甲基橙酸式结构和碱式结构
酸碱指示剂一般是某些有机弱酸或弱碱,或是有机酸碱两性物质,它们在酸碱滴定过程中参与质子转移反应,因分子结构的改变而引起自身颜色的变化,并且这种颜色伴随结构的转变是可逆的。例如酚酞,甲基橙等。酸碱指示剂的变色原理蕴含着深刻的哲学原理,即唯物辩证法的核心—矛盾的对立统一规律。指示剂的酸式结构和碱式结构就是对立的矛盾双方,它们之间具有相互排斥、相互分离的属性,在溶液中互相竞争者存在。另一方面,二者有具有相互吸引、相互联结的统一属性,它们共同存在于溶液之中,根据溶液中H+浓度的改变而相互转化,酸式结构失去一个H+离子后转变为碱式结构,反之碱式结构得到一个H+离子转化为酸式结构。二者之间存在相互影响、相互制约的关系。将唯物辩证法等基本哲学原理与科学认识论渗透到教学中,从辩证的视角看待无机与分系化学的概念、原理与方法,促进对化学理论的深入理解[4]。
(3)滴定突跃
Na2CO3标定HCl的过程是体系由碱性逐渐过渡到酸性的过程,随着溶液中H+浓度逐渐的积累,体系的pH值逐渐降低,缓慢发生变化。在化学计量点前后0.1%时,体系pH发生急剧下降,完成了由碱性到酸性的质变,完成了突跃。突跃的本质正是符合辩证唯物主义中的质量互变规律,即处于不断变化之中的事物,在其每次由一种性质变化到另一种性质的过程中,总是由微小的变化(即量变)慢慢积累开始,当这种积累达到一定程度就会导致事物由一个性质变化到另一个性质(即质变)[5]。
在标定过程中,如果消耗的HCl为20 mL,那么真正使溶液的pH发生急剧变化的,仅是19.98~20.02 mL之间的0.04 mL,这一小小的体积使体系的H+浓度近乎变化了10000倍。这正如人生的道路一样,如果把人生比作100步,99步是一半,1步是一半,最后一步的心理难度其实远远超过之前的99步,但这一步,却最为关键的,再多付出千分之二的努力,我们就可以实现人生的突跃。
4 教学效果评价
(1) 知识层面
掌握强酸溶液的配制及标定方法,理解误差的含义及酸碱滴定的本质。
评价方式:预习视频观看时间,课堂答题,弹幕、投稿发言情况。
(2)能力层面
掌握酸碱滴定的基本操作要点,并能够从微观物质结构变化的角度理解化学反应变化过程。
评价方式:自制指示剂并录制视频提交。
(3)素质层面
理解和体会安全意识和规范操作在化学行业中的重要性,学会利用辩证唯物主义思想认识世界。
评价方式:实验报告中增设实验体会一项。
5 结 语
本案例的思想政治素材主要以讲授和讨论为主。课前,利用雨课堂向学生推送HCl的性质及发生泄露事故的视频,引导学生认识到安全生产和规范操作的重要性。课上,示范HCl溶液的配制以及滴定过程,通过师生互动,教师向学生提问,引导学生认识HCl的重要作用,规范操作并合理处理废弃酸液,我们就能用好这把双刃剑。通过雨课堂发送习题,了解学生对误差的认识,通过引入“蝴蝶效应”的发现,引导学生认识到科学的严谨性。通过指示剂的发现过程,培养学生尊重科学史实,树立探究精神。通过酸碱指示剂的变色原理,滴定突跃的本质,使学生了解唯物辩证法中的矛盾对立统一规律和质量互变规律。最后,通过观察指示剂的变色,确定滴定终点,通过滴定的最后两滴液体,0.04 mL,启发学生对人生的思考,把握正确的人生态度和价值取向。
学生通过本实验的学习,即掌握了化学分析中酸碱滴定的基本技能,又从安全规范、科学素养、人生态度以及唯物辩证法的角度对这一化学过程有了更为深入的理解。

