腹腔镜逆行胆囊次全切除术对慢性胆囊炎伴胆囊结石患者体液免疫功能的影响
邓 勇
(广州医科大学附属第五医院肝胆外科 广州 510700)
慢性胆囊炎是胆囊持续的、反复发作的慢性炎症过程,临床症状多表现为腹痛、腹胀、恶心等,研究表明,慢性胆囊炎伴胆囊结石约占所有慢性胆囊炎的90%~95%[1]。目前,慢性胆囊炎伴胆囊结石患者以内科治疗为基础,其中符合手术指征的可考虑手术切除。临床应用腹腔镜逆行胆囊次全切除术治疗慢性胆囊炎伴胆囊结石较为广泛[2]。本研究对慢性胆囊炎伴胆囊结石患者60例进行考察,探究应用腹腔镜逆行胆囊次全切除术对患者的体液免疫功能影响,现将研究情况阐述如下。
1 资料与方法
1.1 一般资料
收集2018年12月~2019年12月经我院确诊的60例慢性胆囊炎伴胆囊结石患者,采取简单随机化分为对照组和观察组各30例。对照组男17例,女13例;年龄34~69岁,平均年龄(52.92±11.42)岁;病程1~4年,平均病程(1.90±0.72)年。观察组男15例,女15例;年龄32~71岁,平均年龄(52.01±9.57)岁;病程1~4年,平均病程(1.87±0.65)年。两组一般资料对比差异不显著(P>0.05),具有可比性。
1.2 纳入与排除
纳入:(1)符合《中国慢性胆囊炎、胆囊结石内科诊疗共识意见》[1]中关于慢性胆囊炎伴胆囊结石的诊断标准;(2)均具备手术指征;(3)结石直径>5mm;(4)术前3个月内未曾应用皮质醇激素治疗者。排除:(1)合并胆总管结石;(2)身体状况较差,不能耐受麻醉及手术者;(3)严重的肝肾功能不全者;(4)合并其他器官炎症或功能障碍者;(5)既往腹部手术史者;(6)哺乳期或妊娠期妇女。
1.3 方法
对照组行腹腔镜逆行胆囊全切除术,具体步骤:(1)患者采取仰卧位,气管插管全麻;(2)常规消毒后将气腹针插入腹腔,建立CO2气腹,人工气腹压力11~14 mmHg;(3)采用“四孔法”腹腔穿刺,于观察孔置入腹腔镜探头,探查胆囊及周围情况;(4)转换套管和电凝钩经主操作孔进入腹腔,沿浆膜电钝性剥离胆囊底部的粘连至Calot三角区的胆囊管;(5)游离胆囊管和胆囊动脉,夹闭后切除胆囊;(6)取出胆囊和结石,吸净胆汁;(7)解除气腹,冲洗创面,放置引流管,缝合切口。
观察组行腹腔镜逆行胆囊次全切除术,具体步骤:(1)~(3)与对照组一致;(4)转换套管和电凝钩经主操作孔进入腹腔,对胆囊周围的粘连进行分离处理,充分暴露胆囊管、壶腹和胆囊,对胆囊底部或胆囊壶腹部结石嵌顿的位置实施切开处理,将胆汁和小结石吸净;(5)保留胆囊后壁黏膜,将胆囊体及底部前壁切除,并电凝烧灼胆囊黏膜;(6)胆囊动脉夹闭后,将近壶腹部胆囊管进行游离、套扎并切断;(7)与对照组一致。
术后,两组均接受抗感染常规治疗。
1.4 观察指标
(1)手术指标(术中出血量、手术时间和术后通气时间);(2)比较两组术前和术后1周的炎症介质(IL-6)和免疫功能指标(IgM、IgA)的变化。
1.5 统计学方法
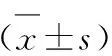
2 结果
2.1 手术指标
与对照组比较,观察组的术中出血量较少、手术时间较短(P<0.05),见表1。
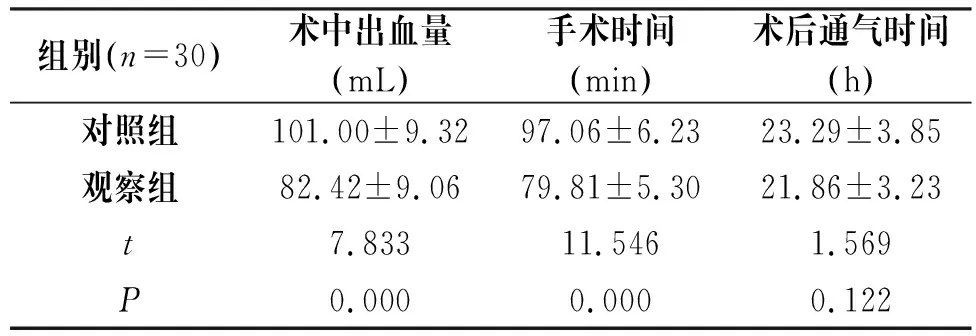
表1 两组手术指标比较
2.2 炎症介质和免疫功能指标
两组术后1周的IL-6与术前相比均显著升高,IgA与术前相比均显著降低(P<0.05),但两组间无明显差异(P>0.05),见表2。

表2 两组手术前后炎症介质和免疫功能指标比较
3 讨论
随着人们的膳食结构和生活状态改变,慢性胆囊炎伴胆囊结石的发病人群愈发常见[3]。研究表明,胆囊结石与慢性胆囊炎存在密切关系,胆囊内结石可反复阻塞胆囊管并刺激胆囊粘膜,久而久之导致慢性胆囊炎的发生[4]。近年来,因为具有创伤小、术后恢复快等优势,腹腔镜手术在临床应用价值大[5],然而在腹腔镜下进行胆囊逆行次全切除术和全切除术对患者机体创伤程度方面仍存在意见分歧。
本研究中,观察组的术中出血量和手术时间明显优于对照组,提示腹腔镜逆行胆囊次全切除术可有效缩短手术时间,减少术中出血量。分析原因可能是次全切除术无需逐步分离粘连组织,减少了手术时间,能够有效防止胆囊壁分离过程中因为层次辨别不清而导致的渗血。沈剑涛等[6]研究表明,手术对机体具有创伤性,可激活炎症介质及引起免疫抑制,故手术对机体的创伤程度可通过炎症介质与免疫功能指标进行监测。当机体受到创伤时,炎症介质被激活,IL-6随之升高。IgA、IgM是机体体液免疫相关指标,IgA是人体黏膜防护体系的重要参与蛋白,IgM是体液免疫初次应答中首先出现的抗体,正常时体液中免疫球蛋白浓度保持相对稳定水平,当机体受到创伤时,免疫球蛋白含量下降。
本研究结果显示,两组患者术后1周的IL-6水平与术前相比均呈升高趋势,IgA水平与术前相比呈下降趋势,说明两种术式均会对患者机体产生一定损伤。此外,两组患者术后1周后的IL-6、IgM和IgA并无明显差别,说明两种术式对慢性胆囊炎伴胆囊结石患者体液免疫功能的影响变化基本一致。
综上所述,腹腔镜逆行胆囊次全切除术在不影响慢性胆囊炎伴胆囊结石患者体液免疫功能的情况下,具有术中出血量更少、手术时间更短的优势。

