心肺联合超声在先天性心脏病婴儿术后机械通气脱机评估中的临床价值
李慕子,孟红,周宇子,李霞,李慧,张婷婷,章良,蒋显超,逄坤静,王强,王浩
先天性心脏病(先心病)心脏直视手术后的机械通气是术后监护的重要部分,尤其是对于婴幼儿期患儿[1]。过早地拔除气管插管影响婴儿心肺功能的恢复,导致二次插管、住院时间延长等,而呼吸机时间延长又会增加肺部感染、肺部损伤等并发症,因此撤离呼吸机的时机把握至关重要[2]。近年来肺超声在动态监测肺部疾病以及心脏术后肺部并发症中的应用已得到广泛认可,具有非侵入性、无辐射、可在床旁完成等优点[3-4]。而对于先心病婴儿,呼吸循环交互作用显著,脱机评估中既需要包括肺脏及膈肌功能,也需要评估心脏矫治情况及心功能,因此本研究将超声心动图联合肺超声,即心肺联合超声对拔管时机的评估提供综合的超声评价及定量指标,以期减少拔管失败等不良事件的发生率。
1 资料与方法
1.1 研究对象及分组
选取2020 年2 月至2020 年6 月期间阜外医院手术婴儿109 例,年龄1 个月~1 岁,平均年龄(0.70±0.25)岁,其中男性67 例,女性42 例。纳入标准:(1)1 个月~1 岁先心病婴儿;(2)接受全麻体外循环下一期心脏矫治手术。排除标准:(1)术前机械通气状态;(2)术前X 线胸片或CT 检查包括以下异常:气胸、肺炎、胸腔积液、气管或支气管狭窄;(3)二次或姑息性心脏手术;(4)计划性有创-无创序贯通气治疗。
达到以下标准婴儿进行自主呼吸试验(SBT)及脱机:心肺功能稳定,吸入氧浓度<50%,呼气末正压(PEEP)<5 cmH2O、辅助呼吸次数低于5 次/min,且自主呼吸潮气量≥5 ml/kg 后复查动脉血氧分压(PaO2)≥80 mmHg(1mmHg=0.133 kPa),二氧化碳分压(PaCO2)≤50 mmHg 达到脱机标准。根据是否脱机失败分为脱机成功组(n=84)及脱机失败组(n=25)。脱机失败标准:(1)SBT 失败:SBT 过程中出现心率增快、鼻翼煽动、呼吸浅快、进行性PaO2下降或PaCO2增高;(2)拔除气管插管后48 h 内重新插管。
1.2 仪器与方法
1.2.1 检查仪器
采用GE vivid Ⅰ型彩色多普勒超声诊断仪,心脏及膈肌检查选择6 S 心脏相控阵探头,探头频率3~5 MHz,肺部超声检查选择9 L 线阵高频探头,探头频率7~12 MHz。
1.2.2 心肺联合超声检查
婴儿于第一次拟脱机或SBT 前进行床旁心肺联合超声检查。超声心动图检查:评估心脏畸形矫治是否满意,包括是否有室间隔缺损残余分流,是否有中度及以上瓣膜反流等;测量并记录左心室射血分数(LVEF),三尖瓣反流压差并计算肺动脉收缩压。肺动脉收缩压大于1/2 动脉血压者定义为肺动脉高压。
肺超声检查:仰卧及侧卧或俯卧,以左右两侧前、侧、后胸壁上下肺野共十二分区对婴儿进行肺部超声检查。肺部评分标准为[5]:0=正常肺超声声像:肺滑动征或A 线,偶有1~2 条孤立B 线;1=肺通气功能中度损失,表现为多条界限清楚的B 线;2=肺通气功能严重丧失,多条相互融合的B 线;3=肺通气功能严重丧失,包括肺实变、肺不张、气胸、胸腔积液。对于每个区域各肋间逐一扫查,以声像图最差者代表这一区域。
膈肌超声检查:仰卧位,探头置于锁骨中线与肋弓下缘交界处,使声束垂直于膈肌中后1/3 部位,应用M 型超声测量膈肌活动度。膈肌功能障碍定义为膈肌活动度小于1 个肋间及任意一侧的膈肌矛盾运动,即主动吸气时膈肌向胸腔内移动[6]。
1.2.3 临床指标收集
心肺联合超声检查同时刻记录临床监测指标,包括心率、血压、中心静脉压(CVP),以及同时刻动脉血PaO2、动脉血PaCO2、N 末端B 型利尿肽原(NT-proBNP)、手术体外循环(CPB)时间及主动脉阻断(ACC)时间。
1.2.4 随访
随访术后恢复情况、肺部并发症发生情况、呼吸机时间和重症监护病房(ICU)入住 时间等直至出院。
1.3 统计学方法
采用SPSS 19.0 统计软件进行统计学分析。对计量资料进行正态性检验,符合正态分布的采用均数±标准差表示,均数比较采用t检验,不服从正态分布者采用中位数(P25,P75)表示,均数比较采用Mann-Whitney U 检验。计数资料采用例数和百分率表示,组间比较采用Pearson 卡方检验。以可能的预测撤机结局的超声参数为自变量,进行Logistic回归分析,计算OR 及95% CI。绘制ROC 曲线,计算AUC 评价超声指标对于脱机失败的预测价值。以P<0.05 为差异具有统计学意义。
2 结果
1.2 两组婴儿一般情况比较(表1)
脱机失败组婴儿与脱机成功组比较,年龄[(0.51±0.21)岁vs.(0.76±0.23)岁],体重[(6.28±1.03)kg vs.(7.83±1.42)kg]均较小,差异具有统计学意义(P均<0.01)。两组婴儿性别及术前LVEF 差异无统计学意义(P均>0.05)。脱机失败组CPB 及ACC 时间均较脱机成功组长,差异具有统计学意义(P均<0.01)。两组婴儿心内畸形包括:房间隔缺损,室间隔缺损,动脉导管未闭,法乐四联症,右心室双出口,肺静脉异位引流,心内膜垫缺损。
表1 脱机成功组与脱机失败组婴儿临床指标及超声参数比较(±s)
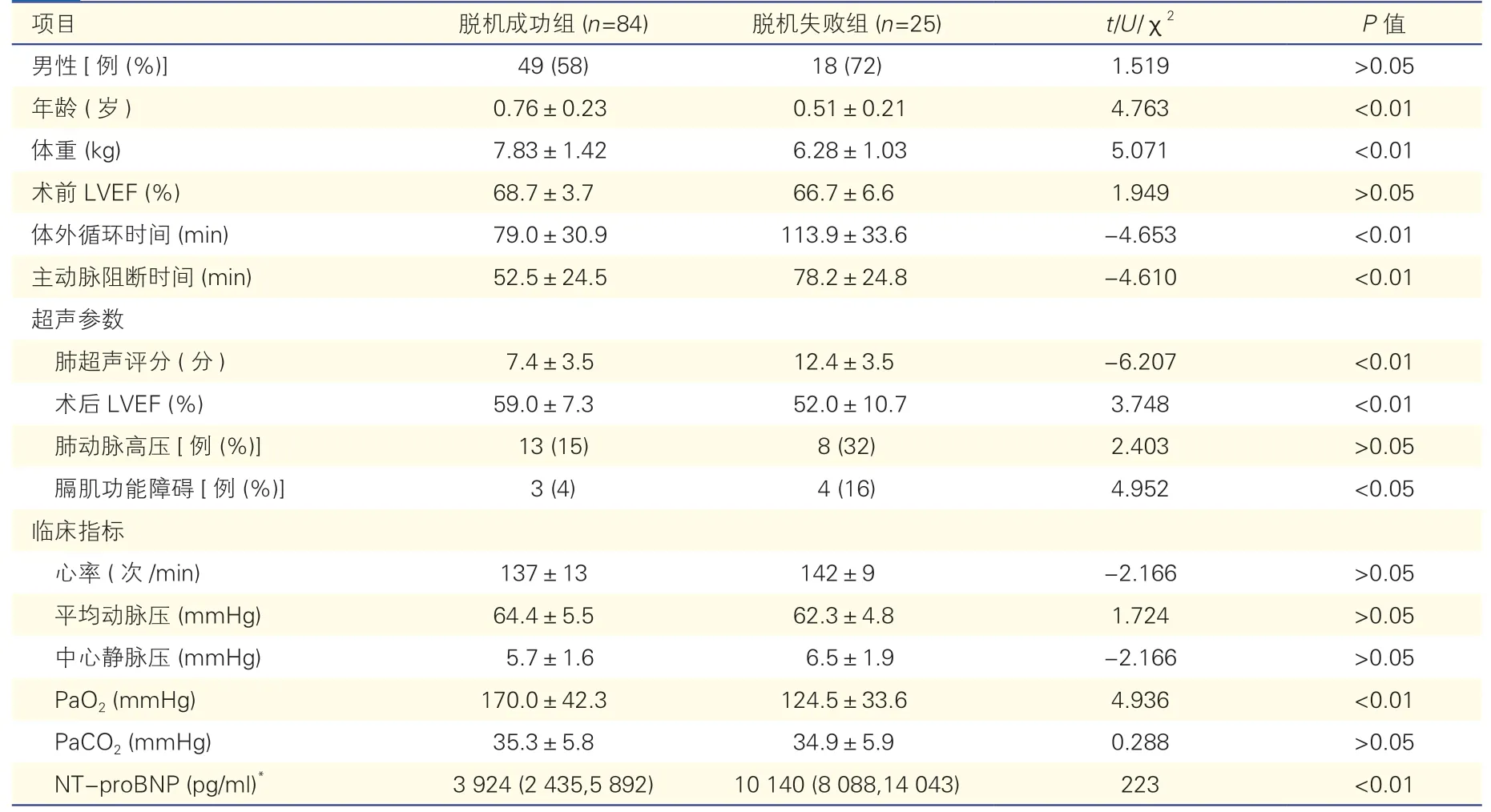
表1 脱机成功组与脱机失败组婴儿临床指标及超声参数比较(±s)
注:LVEF:左心室射血分数;PaO2:动脉血氧分压;PaCO2:动脉血二氧化碳分压;NT-proBNP:N 末端B 型利尿肽原。*:以中位数(P25,P75)表示。1 mmHg=0.133 kPa
2.2 心肺联合超声检查结果及指标参数
所有婴儿心肺联合超声检查均为阳性结果(图1)。肺超声阳性表现有:多发或融合B 线、白肺、肺实变伴支气管充气或充液征、碎片征。肺超声评分2~17 分,平均(8.57±4.08)分,脱机失败组婴儿肺超声评分较脱机成功组高(P<0.01)。超声心动图检查所有婴儿心脏畸形矫治情况基本满意,脱机成功组LVEF 较脱机失败组高,其中LVEF<40%者脱机成功组3 例,脱机失败组8 例,差异均有统计学意义(均P<0.05)。合并肺动脉高压者脱机成功组13 例,脱机失败组8 例,两组差异无统计学意义(P>0.05)。膈肌功能障碍者均表现为膈肌运动减低,脱机失败组婴儿较脱机成功组多(P<0.05)。两组婴儿脱机前心率、平均动脉压、CVP、PaCO2差异均无统计学意义(均P>0.05)。脱机失败组NT-proBNP 高于成功组,PaO2低于成功组(P均 <0.01),差异均有统计学意义(表1)。

图1 先天性心脏病婴儿术后肺超声表现
2.3 超声指标预测脱机失败效能
以肺超声评分为标准预测脱机失败的AUC 为0.84,标准误0.0446,95%CI:0.748~0.923,最佳截断值为13 分,敏感度为60%,特异度91%。Logistic回归分析结果示肺超声评分≥13 分,LVEF<40%及膈肌功能障碍均与脱机失败显著相关(P均<0.05),见表2。联合肺超声评分≥13 分、LVEF<40%及膈肌功能障碍预测脱机失败的AUC 为0.88,敏感度72%,特异度99%,标准误0.0386,95%CI:0.804~0.955,见图2。

表2 预测脱机失败的Logistic 回归多因素分析
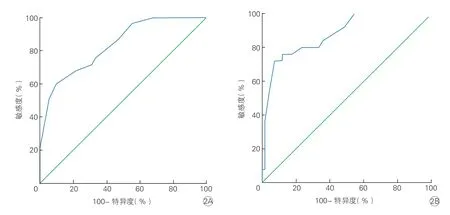
图2 超声参数预测脱机失败的ROC 曲线
2.4 随访结果
所有婴儿均在治疗后拔管成功,治愈出院。脱机成功组婴儿中位ICU 入住时间2(2,4)d,中位呼吸机时间9(6,22)h,脱机失败组婴儿中位ICU 入住时间6(4,10)d,中位呼吸机时间74(45,123)h,脱机失败组均较脱机成功组长,差异有统计学意义(均P<0.05)。脱机失败原因包括:心功能不全(10 例),肺部并发症者(包括肺水肿,肺不张及气胸;共9 例),毛细血管渗漏综合征(4 例),肺动脉高压(1 例),呼吸无力(1 例)。
3 讨论
先心病婴儿术后脱机困难的常见原因有以下3种:心功能不全;肺原性因素,包括胸腔积液、肺不张、肺炎、膈肌麻痹等;神经原性因素,包括镇静药及肌松药物的残留作用[7]。脱机失败会导致心脏二次损伤、呼吸机时间延长,进而增加医疗成本及婴儿病死率[8],因此脱机前准确的评估指标对于识别脱机失败高风险患儿至关重要。既往脱机评估主要依靠临床监测指标以及血气分析,本研究应用心肺联合超声直接评估心脏、肺脏以及膈肌功能,预测指标全面,联合预测脱机失败的AUC 为0.88,具有较高的敏感度及特异度。
肺超声近年来已被证实对于肺部疾病以及心脏术后肺部并发症的诊断优于X 线胸片,且无辐射及转运风险,是优质的床旁监测工具[9]。先心病婴儿在CPB 下手术,导致炎性介质释放、肺间质水肿,且术中肺脏相对缺血,术后造成再灌注损伤[10-11]。CPB 介导的肺损伤主要表现为血管外肺水增加,Agricola 等[12]针对心脏病术后患者的研究证实了B线数量与金标准PICCO 法测量的血管外肺水呈正相关。肺损伤程度与CPB 时间呈正比,尤其对于婴幼儿[13]。本研究中脱机失败组婴儿较成功组婴儿的CPB 时间长,且肺超声评分高,说明了脱机失败组婴儿肺部损伤情况更重,从而导致拔管失败率增加。
肺超声可以在SBT 前或SBT 结束时评估肺通气损失从而预测脱机是否能成功。Soummer 等[14]的研究证实了肺超声评分对预测脱机失败的准确性,在该研究中肺超声评分<13 分可用于预测脱机成功,肺超声评分>17 分预测脱机失败。在本研究中肺超声评分≥13 即预测脱机失败,较其评分低,考虑原因有以下几点:(1)本研究中研究对象为1 个月至1 岁龄婴儿,不同于其研究对象为成人,婴儿生理性储备有限,因此较低评分即对其通气功能有较大影响;(2)本研究中肺超声检查时间为SBT 前,Soummer 等[14]进行的研究中检查时间为SBT 时,而SBT 过程中会导致进一步肺通气损失从而评分增高。由于心脏术后婴儿病情变化快,因此本研究采用SBT 前进行心肺联合超声检查,更为安全,且更具有可操作性及临床应用价值。
由于婴幼儿肋间肌及腹肌薄弱,因此膈肌运动障碍时代偿能力低下,导致脱机困难。超声是目前先心病术后膈肌麻痹的首选诊断工具,可以床旁了解患儿的膈肌运动状态,从而指导撤机[15]。本研究中脱机失败组膈肌功能障碍比例较脱机成功组高,也是脱机失败因素之一。本组婴儿膈肌运动降低者,在后续治疗中均自行恢复,无膈肌麻痹患儿。
心脏直视手术后造成心肌损害,心脏泵功能低下,且脱机后胸腔内压力从正压转为负压,回心血量增加,左心室舒张末期压力增加,左心室做功增加,易诱发心原性肺水肿。既往研究示LVEF<40%是心脏手术后呼吸机时间延长的独立危险因素[13]。本研究中脱机失败组较脱机成功组LVEF 低,NTproBNP 高,且应用肺超声评分预测脱机失败的敏感度为60%,而结合LVEF 及膈肌运动后敏感度为72%,由于部分婴儿为心功能不全导致脱机失败,因此也说明脱机评估需应用心肺联合超声结合心脏、肺脏、膈肌功能才能提高准确性。
本研究为单中心研究,未选取新生儿及大于1岁的幼儿患者,因此尚需要多中心、多年龄段的大样本量研究验证及补充本研究结论。本研究中超声心动图指标未评估心脏舒张功能,由于低龄婴幼儿组织多普勒尚缺乏公认参考值范围,且先心病婴儿常存在二尖瓣狭窄及反流等而影响二尖瓣口前向血流充盈早期峰值流速(E 峰)的应用。
综上所述,床旁心肺联合超声对心脏术后婴儿预测呼吸机撤离具有较高的诊断价值,且具有无创、安全、便捷的优势,具有较高可行性及临床价值。
利益冲突:所有作者均声明不存在利益冲突

