艾司洛尔对脓毒症大鼠心肌保护作用及其可能机制
(青岛大学附属医院重症医学科,山东 青岛 266100)
脓毒症是指机体对感染的反应失调导致的危及生命的器官功能障碍[1]。虽经多年努力,其病死率仍居高不下,最新的流行病学调查显示,脓毒症病人的病死率高达64%[2],继续寻找有效的治疗药物对降低病死率至关重要。脓毒症发病机制极其复杂,其中包括交感神经过度激活,体内儿茶酚胺大量释放,心脏是儿茶酚胺超载的主要靶器官[3],也是脓毒症发展过程中最常见的受损靶器官,肾上腺素能系统的激活可能是发生脓毒症心功能障碍的重要机制之一。因此,有研究人员试图应用β1肾上腺素受体阻滞剂拮抗肾上腺素能系统的过度激活。近年来的研究证实,β1受体阻滞剂在拮抗交感神经活性[4]、抑制炎症反应[5]、减轻高分解状态[6]、改善脓毒症病人预后[7]等方面具有显著效果,另外,β1受体阻滞剂在心肌保护方面可发挥独特作用,对于脓毒症病人具有良好的临床应用前景。β肾上腺素受体已被证实表达于外周血单个核细胞,而外周血单个核细胞上存在的Toll样受体(TLRs)炎症通路。TLRs是一种跨膜蛋白,它能够识别病原微生物相关分子模式(PAMPs),例如革兰阴性菌脂多糖(LPS),LPS与脂多糖结合蛋白(LBP)结合形成复合物,LPS/LBP复合物随即被单核细胞表面的CD14所识别并结合,然后进一步与TLR4相结合,通过髓样分化蛋白88(Myd88)依赖性信号传导通路启动细胞内信号传导,导致转录因子核因子-κB(NF-κB)的激活和易位,释放多种炎症因子。艾司洛尔作为一种高选择性β1受体阻滞剂,具有起效快、作用时间短的特点,且通过红细胞代谢,不受肝、肾功能的影响,尤其适用于危重病人。前期已有研究证实艾司洛尔可减轻心肌损伤,但其具体机制尚不清楚。因此,本实验从TLR4/Myd88/NF-κB信号通路角度,探讨艾司洛尔在脓毒症心肌保护中的作用机制,以期为脓毒症心肌损伤的治疗提供理论和实验基础。
1 材料与方法
1.1 实验动物
取雄性清洁级SD大鼠60只,体质量为330~360 g,由青岛大学动物实验中心提供,于室温18~28 ℃、相对湿度40%~60%、12 h昼夜循环的环境中适应性喂养1周。
1.2 主要药物、试剂与仪器
盐酸艾司洛尔注射液(山东齐鲁制药有限公司);肌钙蛋白I(TnI)、肿瘤坏死因子α(TNF-α)、白细胞介素-1(IL-1)试剂盒(北京索莱宝科技有限公司),TLR4抗体(北京索莱宝科技有限公司产品),Myd88抗体(英国Abcam公司),NF-κΒ p65抗体(Cell Signaling Technology公司),β-actin多克隆抗体(Elabscience公司),山羊抗兔IgG(Elabscience公司);酶标仪(美国Thermo Fisher,MK3),显影仪(法国Vilber Fusion,FX5),双目光学显微镜(日本Olympus,BX53)。
1.3 动物分组与处理
采用随机数字法将大鼠分为假手术组(Sham组)、脓毒症组(Model组)和艾司洛尔组(ES组),每组20只。所有大鼠术前12 h禁食,可自由饮水。Model组和ES组依照文献方法行盲肠结扎穿孔术(CLP法)制备脓毒症动物模型[8]:大鼠以100 g/L水合氯醛(5 mL/kg)腹腔注射麻醉,固定后沿腹前正中线切开皮肤约2 cm,沿腹白线切开,打开腹腔,探查并找到盲肠,用3-0丝线结扎盲肠远端,同时保持肠道通畅,用18号针头做两处穿刺,轻轻挤压盲肠将两滴肠内容物挤至腹腔,还纳盲肠,逐层缝合腹壁切口。Sham组探查盲肠后立即还纳关腹,不行盲肠结扎穿孔。造模成功后各组均行右侧股静脉穿刺术,ES组持续微量泵入艾司洛尔稀释液1 mL/h(15 mg·kg-1·h-1),共计6 h;Sham组、Model组持续泵入等量生理盐水。各组术后1 h内均经股静脉给予30 mL/kg生理盐水模拟液体复苏。本实验中动物处置方法符合动物伦理学标准。
1.4 检测指标
1.4.1大鼠存活率 由3名研究人员在不知分组情况下观察所有大鼠一般状态,实验大鼠出现精神萎靡、毛发竖立、眼鼻出血、腹泻等症状,则提示脓毒症造模成功。同时,计算各组大鼠的存活率。
1.4.2血清TnI、TNF-α和IL-1测定 所有存活大鼠均于造模后24 h再次麻醉,腹主动脉取血2 mL,静置30 min后,以3 000 r/min离心15 min,分离上清,按照试剂盒说明书,采用干式免疫荧光定量法测定TnI浓度,采用酶联免疫吸附试验方法分别测定TNF-α、IL-1浓度。
1.4.3心肌组织病理学观察 术后24 h麻醉处死大鼠,分离大鼠心脏,取左心室游离壁,以4 ℃生理盐水洗净血污,用40 g/L多聚甲醛固定72 h以上,流水洗净甲醛,梯度脱水,二甲苯透明,石蜡包埋,5 μm厚连续切片,经摊片、烤片后进行苏木精-伊红染色,封片后在光学显微镜下观察心肌组织学变化。从心肌变性坏死、出血、间质水肿和中性粒细胞浸润等方面观察心肌病变分布情况,并采用半定量评分系统进行评分[9],组织病理评分为0~4分,分别代表病变受累率0、25%、50%、75%和100%。由3名高年资病理科医师在不知分组情况下同时进行组织病理学检查并给出分数,取平均值。
1.4.4Western blot检测心肌组织TLR4、Myd88和NF-κB蛋白表达 用电子天平称取100 mg心肌组织,组织剪剪碎后,按每20 mg组织加入200 μg组织细胞裂解液,用玻璃匀浆器匀浆,裂解后的样品以12 000 r/min离心10 min,取上清液,用BCA法检测蛋白浓度。配制100 g/L的SDS-PAGE分离胶及50 g/L的浓缩胶,经过上样、蛋白电泳、转膜、封闭后,分别加入TLR4(1∶1 000)、Myd88(1∶1 000)及NF-κB(1∶1 000)抗体稀释液,4 ℃孵育过夜,洗膜后加入二抗(1∶5 000)稀释液,于室温下孵育2 h,洗膜后加入超敏ECL发光液进行显影,采用Image J软件分析各条带光密度值。
1.5 统计学方法

2 结 果
2.1 各组大鼠存活率的比较
术后24 h,Sham组大鼠死亡2只,存活率为90.0%;Model组死亡9只,存活率为55.0%;ES组死亡7只,存活率为65.0%。Model组大鼠存活率较Sham组显著降低(χ2=6.14,P<0.05),而ES组与Model组存活率比较差异无显著性(χ2=0.42,P>0.05)。盲肠结扎穿孔术后,Model组、ES组大鼠均出现精神萎靡、毛发竖立、眼鼻出血、腹泻等脓毒症症状,而Sham组大鼠未出现上述症状。
2.2 各组大鼠心肌组织病理学变化
光镜下Sham组心肌细胞结构正常,纤维肌丝束排列紧密,未见明显水肿、充血、变性以及坏死等;Model组可见心肌细胞大量坏死,呈空泡样变性,心肌纤维明显水肿,排列疏松,部分心肌纤维断裂,细胞核肿胀,间质水肿、炎性细胞浸润;ES组与Model组相比心肌细胞坏死减少,心肌纤维排列欠规整,间质无明显水肿,仍有少量炎性细胞浸润。心肌组织病理评分Model组(2.45±0.69)>ES组(1.77±0.73)>Sham组(0.83±0.71),差异具有显著意义(F=18.84,P<0.05)。
2.3 各组大鼠血清TnI含量的比较
Model组大鼠血清TnI含量较Sham组明显升高,ES组大鼠血清TnI含量较Model组明显降低,差异有统计学意义(F=231.82,P<0.05)。见表1。
2.4 各组大鼠血清TNF-α、IL-1含量的比较
Model组大鼠血清TNF-α、IL-1含量较Sham组明显升高,ES组大鼠血清TNF-α以及IL-1含量较Model组明显降低,差异有显著性(F=335.21、602.11,P<0.05)。见表1。
表1 各组大鼠血清TnI、TNF-α和IL-1含量比较
2.5 各组大鼠心肌组织TLR4、Myd88及NF-κB蛋白表达的比较
Model组大鼠心肌组织中TLR4、Myd88以及NF-κB蛋白表达较Sham组明显升高,而ES组大鼠心肌组织中TLR4、Myd88及NF-κB蛋白表达较Model组明显降低,差异有统计学意义(F=17.15~95.92,P<0.05)。表明艾司洛尔可抑制脓毒症大鼠心肌组织中TLR4、Myd88及NF-κB蛋白的表达。见图1、表2。
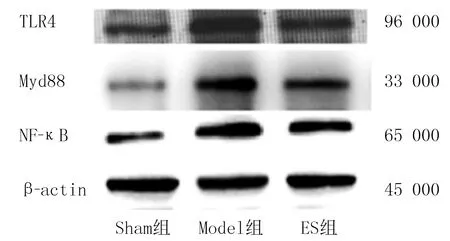
图1 各组大鼠心肌组织TLR4、Myd88及NF-κB蛋白表达电泳图
表2 各组大鼠心肌组织TLR4、Myd88及NF-κB蛋白表达比较
3 讨 论
脓毒症是重症医学领域的常见病、多发病,已成为沉重的公共卫生负担。心肌损伤是脓毒症导致的常见的器官功能障碍之一,其发病机制复杂,涉及全身炎症网络系统激活、免疫功能障碍、冠状动脉低灌注或不均匀灌注、氧化应激、Ca2+超载、线粒体功能障碍等[10-12]。虽然许多病理生理机制被提出,但每种机制的全部影响尚未阐明。目前临床上通过测量生物标志物(心肌肌钙蛋白、脑钠肽)和使用超声心动图,可以很容易地识别脓毒症病人的心脏功能障碍。然而,尚无针对脓毒症心肌抑制的特异性治疗方法。当前治疗常通过液体复苏、血管活性药物的支持确保足够的心室充盈,优化血流动力学稳定性,在很大程度上仍属于支持性治疗。未来的研究应集中在纠正特定病理生理学异常的靶向治疗上。
艾司洛尔作为一种β受体阻滞剂,因具有负性肌力作用以往通常被认为不适合用于脓毒症休克的治疗。随着对脓毒症病理机制的不断深入研究,人们发现脓毒症病人的典型特征是肾上腺素能系统过度激活,强烈的肾上腺素能刺激可产生多种毒副作用,包括心脏效应,如心率、心肌收缩力和心肌能量需求增加,以及心脏外效应,如高分解状态、高凝状态、全身炎症细胞因子的释放调节。因此,人们对在脓毒症病人中使用β肾上腺素能阻滞剂越来越感兴趣,目的是减轻交感神经过度刺激引起的副作用。SUZUKI等[5]的实验结果显示,连续输注艾司洛尔可改善CLP法所致脓毒症大鼠的各项心功能指标,表明艾司洛尔可改善脓毒症大鼠心肌氧利用率,作者认为艾司洛尔的这种心脏保护作用可能是通过阻断过度的β肾上腺素能刺激、减少β肾上腺素能受体密度而实现的。这一观点也得到了国内学者的认同[13-14]。另有研究显示,艾司洛尔还可通过抑制炎症递质的表达,提高脓毒症病人的心脏效应[15-16]。除此之外,β受体阻滞剂在治疗脓毒症方面也表现出生存率上的优势,例如,LIU等[17]研究表明,艾司洛尔可降低脓毒症休克病人28 d死亡率,同时缩短ICU住院时间。由此可见,艾司洛尔在治疗脓毒症所致心肌损伤方面具有积极作用。
文献报道,盲肠结扎穿孔术后24 h心肌损伤最明显,是观察脓毒症心肌损伤最合适的时间点[18]。本实验模型评价结果显示,造模24 h后开腹可见腹腔大量渗出伴有恶臭,盲肠末端充血坏死,同时心肌组织病理切片镜下可见心肌细胞大量坏死,心肌纤维明显水肿、排列疏松,部分心肌纤维断裂,细胞核肿胀,间质水肿、炎性细胞浸润,提示脓毒症造模成功。TnI是目前检测心肌细胞损伤的“金标准”[19],不仅可以作为诊断脓毒症心肌损伤的指标,还可以作为病情严重程度和预后的指标[20]。LABUGGER等[21]的研究发现,在脓毒症过程中,心肌细胞损害多为细胞亚微结构的改变,心肌内肌钙蛋白裂解为较小片段,心肌细胞膜通透性增加,从而导致血浆肌钙蛋白水平的升高。因此,本实验选择TnI作为脓毒症后心肌损伤及其程度的评价指标。本文结果显示,Model组大鼠的血清TnI浓度较Sham组显著升高,提示采用CLP法可诱导脓毒症心肌损害,ES组的TnI浓度较Model组显著降低,表明艾司洛尔能够减轻脓毒症大鼠心肌损伤。
脓毒症时,LPS可促进大量细胞因子释放,从而引发一系列炎症反应,过度炎症反应可导致器官功能障碍,尤其是心脏。TNF-α在脓毒症发病早期起关键作用,它是启动炎症级联反应的始动因子,抑制TNF-α信号能有效改善内毒素血症引起的心肌损伤[22]。例如,糖皮质激素在抑制TNF-α的同时,可以减轻脓毒症大鼠的心肌抑制[23];阿托伐他汀可以抑制TNF-α的表达,减轻炎症反应,从而减轻脓毒症大鼠的心肌损伤[24]。与以往研究相一致,本实验也证实脓毒症大鼠血清中TNF-α的表达水平明显增加,通过外源性给予艾司洛尔,可以明显降低TNF-α的表达。另外,炎症因子IL-1也在脓毒症心肌损伤中发挥重要作用[25]。例如,黄芪多糖能够抑制脓毒症大鼠心肌组织IL-1的表达,从而减轻心脏损害[26]。本文研究结果显示,Model组大鼠血清中IL-1的表达水平较Sham组明显增加,而艾司洛尔可以明显降低IL-1的表达水平。以上结果提示,艾司洛尔可能通过降低炎症因子TNF-α和IL-1的表达,抑制炎症反应,从而改善脓毒症心肌损伤。
TLRs是一种跨膜蛋白,它能识别PAMPs,通过Myd88依赖性信号传导通路启动信号传导,激活细胞内NF-κB信号通路,启动炎症因子转录[27]。近年来,对TLR4/Myd88/NF-κB信号通路的研究涉及器官移植、神经系统疾病、呼吸系统疾病、肾脏疾病、肿瘤、内分泌系统疾病等多个领域。ZHOU等[28]采用CLP法建立脓毒症大鼠模型,证实了抗TLR4单抗预处理可抑制TLR4/Myd88信号通路,减轻炎症反应。本研究进一步探讨了艾司洛尔调控脓毒症大鼠心肌炎症反应的作用机制,结果显示,艾司洛尔能显著抑制TLR4、Myd88、NF-κB蛋白的表达。表明TLR4/Myd88/NF-κB信号通路可能参与了脓毒症大鼠的心肌损伤及炎症反应。
综上所述,艾司洛尔能够减轻炎症反应和心肌损伤,其作用机制可能与抑制TLR4/Myd88/NF-κB信号通路的激活有关。这将为脓毒症大鼠心肌损伤的预防和治疗提供新的研究方向。但本实验存在未设置艾司洛尔浓度梯度、观察时间短等不足,因此,艾司洛尔在脓毒症心肌保护中的剂量和作用时间仍需进一步研究。

