ADU制备AUC工艺的优化研究
唐儒煜,胡锦明
(中核二七二铀业有限责任公司,湖南 衡阳 421002)
三碳酸铀酰铵(以下简称AUC)晶体,属单斜晶系斜方体晶体[1]148,各晶面具有不同的生长速度,是铀纯化体系中的一个重要中间产物[2]。在中国经典的天然铀湿法纯化工艺中[3],需要生产棱柱状、颗粒粗、核纯级的AUC晶体,供生产化学活性高、适用于干法氢氟化过程的核纯级二氧化铀[4]181;通常采用重铀酸铵(以下简称ADU)制备AUC[5]94。随着工艺控制条件的变化,制备的AUC晶体差异较大,既可生产平均粒径较大(≥40 μm)的AUC,也可生产平均粒径较小(≤35 μm)且近似球形的AUC[6]354。为满足后续生产要求,对ADU制备AUC的反应条件进行研究,了解AUC结晶过程的内在规律及其影响因素,优化反应条件,提高粗晶产率,减少或避免平均粒径较小的AUC产生,对工业生产的成本和质量控制,具有非常重要的意义。
1 ADU制备AUC工艺原理
经过初步水冶加工的天然铀浓缩物(主要是重铀酸盐)或经初步处理的铀氧化物(主要是UO2、U3O8、UO3),均含有大量杂质,需要进一步纯化,以得到适于后续转化加工的产物[7]1。
在中国经典天然铀湿法纯化工艺中,首先采用硝酸溶解天然铀浓缩物或铀氧化物,然后经TBP-磺化煤油萃取、微硝酸反萃取制得核纯级的硝酸铀酰溶液,再经氨水沉淀制得核纯级的ADU[5]94。然后在ADU中添加过量(NH4)2CO3溶液,使(NH4)2U2O7固体与(NH4)2CO3溶液反应,生成溶于水的NH4+和[UO2(CO3)3]4-;同时由于溶液中存在过量的(NH4)2CO3,通过NH4+的同离子盐析作用[7]78,[UO2(CO3)3]4-以(NH4)4[UO2(CO3)3]晶体的形态结晶析出,其化学反应式为[8]30
(NH4)2U2O7+6(NH4)2CO3+3H2O→2(NH4)4[UO2(CO3)3]+6NH4OH。
(1)
2 试验部分
2.1 主要原料
ADU,铀湿品位为54.56%,取自天然铀湿法纯化工业生产现场。反应剂是用碳酸氢铵和氨水配制的不同浓度(NH4)2CO3溶液,溶液中ρ(NH4HCO3)≤20 g/L、ρ(NH4OH)≤15 g/L。碳酸氢铵为农用级(GB/T 3559—2001),w(N)≥17.1%。氨水为工业级(HG/T 5353—2018),w(NH3)含量≥20%,ρ(CO32-)≤1.0 g/L。
2.2 试验方法
在小型结晶器中进行试验。取1 L一定铀浓度的ADU浆体置于结晶器中;在一定搅拌速度下,将一定浓度的反应剂以一定的速度加入到结晶器中,用温度计测定反应过程中的温度变化;加完反应剂后,保持温度继续搅拌3 h,在室温下老化24 h;然后真空过滤,用无水酒精洗涤滤饼3~5次,最后在50 ℃下干燥5 h。
2.3 分析方法
用粒度分析仪分析样品的平均粒径;用三碳酸铀酰铵及二氧化铀中铀的测定法(EJ/T 786—93)测定样品的铀含量;用酸碱中和滴定法测定样品的(NH4)2CO3含量。
3 试验结果与讨论
3.1 ADU浆体铀浓度对制备AUC晶体的影响
将ADU调配成不同浆体铀浓度,研究ADU浆体铀浓度对制备AUC晶体的影响。试验条件:ADU浆体体积1 L;ρ[(NH4)2CO3]=480 g/L;温度55 ℃;搅拌速度1 000 r/min。试验结果见表1。

表1 ADU浆体铀浓度对制备AUC晶体的影响
试验表明:当ADU浆体c(U)=2.059 mol/L时,结晶母液的铀含量和AUC晶体平均粒径均比较理想;将ADU浆体c(U)≥2.471 mol/L时,提浓难度递增;当ADU浆体c(U)<2.059 mol/L时,反应速度过快,产生的细晶较多;当ADU浆体c(U)≤1.639 mol/L时,制备AUC效率较低,且产生的废水量较大。综合考虑经济性和可操作性,ADU浆体c(U)控制在2.0 mol/L左右较为适宜。
3.2 反应剂浓度对制备AUC晶体的影响
配制不同浓度的(NH4)2CO3,研究 (NH4)2CO3浓度对制备AUC晶体的影响。试验条件:ADU浆体体积1 L;c(U)=2.0 mol/L;反应温度=55 ℃;搅拌速度=1 000 r/min。试验结果见表2。

表2 反应剂(NH4)2CO3浓度对制备AUC晶体的影响
从表2可知,(NH4)2CO3浓度越高,AUC晶体的平均粒径越大。试验还发现:(NH4)2CO3溶液浓度越高,氨越易发挥,(NH4)2CO3越易析出;(NH4)2CO3溶液浓度越低,溶液体积越大,废水产生量也越大。综合考虑,反应剂(NH4)2CO3浓度控制在480 g/L左右较为适宜。
3.3 反应剂加入量对制备AUC晶体的影响

加入不同体积的反应剂,研究反应剂(NH4)2CO3溶液加入量对制备AUC晶体的影响。试验条件:ADU浆体体积1 L;c(U)=2.0 mol/L;ρ[(NH4)2CO3]=480 g/L;反应温度=55 ℃;搅拌速度=1 000 r/min。试验结果见表3。

表3 反应剂加入量对制备AUC晶体的影响
从表3可知,AUC晶体的平均粒径和结晶母液的(NH4)2CO3浓度均随反应剂体积的增加而增加,结晶母液的铀浓度随反应剂体积的增加而减少。当n[(NH4)2CO3]/n(U)≥5.26时,AUC晶体的平均粒径较大,且结晶母液铀含量也较小。综合考虑,反应剂(NH4)2CO3溶液的加入量,控制在n[(NH4)2CO3]/n(U)≈6为宜。
3.4 反应剂加入速度对制备AUC晶体的影响
AUC晶体的各结晶面具有不同的的生长速度。在AUC盐析结晶过程中,UO22+-NH4+-CO32--H2O体系的过饱和度是影响AUC晶粒形状和粒径的主要因素[1]149。
以不同速度加入反应剂(NH4)2CO3溶液,研究反应剂加入速度对制备AUC晶体的影响。试验条件:ADU浆体体积1 L;c(U)=2.0 mol/L;ρ[(NH4)2CO3]=480 g/L;n[(NH4)2CO3]/n(U)≈6;反应温度=55 ℃;搅拌速度=1 000 r/min。试验结果如图1所示。
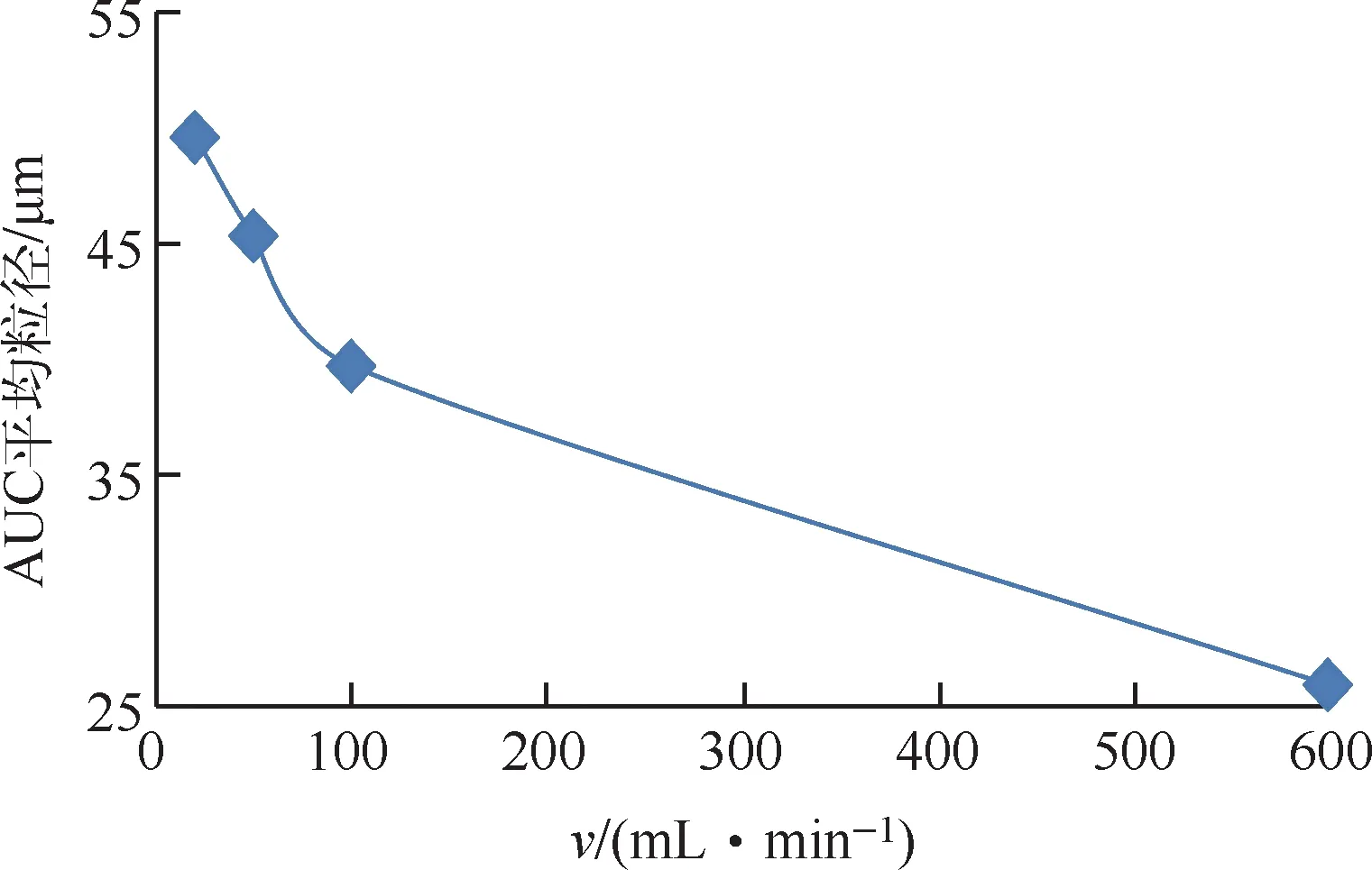
图1 反应剂加入速度对制备AUC晶体的影响
从图1可看出:AUC晶体的平均粒径随反应剂加入速度的增大而降低。根据试验结果并依据结晶学原理[10]得出:当反应剂加入速度≤100 mL/min时,反应体系过饱和度较低,晶体按照其晶习缓慢生长,可得到平均粒径比较大的晶体;当反应剂加入速度>100 mL/min后,反应体系过饱和度增加,造成晶核增加,使晶体不再按照其晶习生长,而是不同程度地变为同向生长,制得平均粒径较小的AUC晶体。综合考虑,ADU制备AUC时,应缓慢(速度≤100 mL/min)加入反应剂,以控制反应体系处于较低的过饱和度,以获得较高粗晶产率。
3.5 反应温度对制备AUC晶体的影响
AUC在水中的溶解度随温度升高而近于线性增大[9]109。在温度低于60 ℃时,AUC的溶解度随温度上升而增大,这有利于细晶的溶解和晶体的长大,能提高粗晶产率;但AUC在较高温度(>60 ℃)溶液中不稳定,会分解成不溶性的碳酸铀酰,且随着温度进一步升高,AUC分解速度加快[7]79,反应式为[8]31
(NH4)4[UO2(CO3)3]→UO2CO3↓+2H2O+2CO2↑+4NH3↑。
(2)
另外,(NH4)2CO3为弱酸弱碱盐,其水溶液呈碱性。在70 ℃时(NH4)2CO3水溶液开始分解,且随着温度升高,分解速度增大,反应式为
(NH4)2CO3→2NH3↑+H2O+CO2↑。
(3)
在不同温度下,研究反应温度对制备AUC晶体的影响。试验条件:ADU浆体体积1 L、c(U)=2.0 mol/L;ρ[(NH4)2CO3]=480 g/L、反应剂加入速度≤100 mL/min;n[(NH4)2CO3]/n(U)≈6;搅拌速度=1 000 r/min。试验结果见表4。

表4 反应温度对制备AUC晶体的影响
从表4可知:当反应温度≤50 ℃时,AUC晶体平均粒径也偏小;当温度在50~60 ℃时,AUC晶体平均粒径比较大。试验还发现:当反应温度≤50 ℃时,生成的AUC晶核较多,得到的晶体中细晶较多。这是由于温度偏低,导致溶液中离子扩散速度较慢,晶体难以长大;当反应温度>50 ℃后,得到的AUC结晶产物平均粒径较大、易于过滤且含水量较低,这是由于温度升高,细晶溶解加快,粗晶长大加速。结合试验情况,并综合考虑碳酸铀酰沉淀及溶液中氨挥发等因素,ADU制备AUC的反应温度控制在(55±5)℃为宜。
3.6 搅拌速度对制备AUC晶体的影响
分别在低速搅拌(500 r/min)、中速搅拌(1 000 r/min)、高速搅拌(1 500 r/min)下进行试验,研究搅拌速度对制备AUC晶体的影响。试验条件:ADU浆体体积1 L、c(U)=2.0 mol/L;ρ[(NH4)2CO3]=480 g/L、加入速度≤100 mL/min;n[(NH4)2CO3]/n(U)≈6;反应温度=55 ℃。试验结果如图2所示。

图2 搅拌速度对制备AUC晶体的影响
从图2可知:当搅拌速度为1 000 r/min时,AUC晶体平均粒径比较大;当搅拌速度为1 500 r/min 时,得到的AUC晶体其平均粒径较小;当搅拌速度为500 r/min时,反应速度较慢,试验中可明显观察到结晶器底部粘附ADU,反应不均匀。这是由于搅拌速度过快时,易造成二次接触产生晶核过多,导致平均粒径变小;同时AUC晶体也容易被打碎,不利于晶体长大。综合考虑,ADU制备AUC反应的搅拌速度控制在1 000 r/min左右为宜。
4 结论
在ADU浆体c(U)=2.0 mol/L、反应剂ρ[(NH4)2CO3]=480 g/L、反应剂加入速度≤100 mL/min、n[(NH4)2CO3]/n(U)≈6、反应温度=(55±5)℃、搅拌速度=1 000 r/min的条件下,可制得平均粒径较大(≥40 μm)的AUC晶体。较低的溶液过饱和度,有利于晶体按其晶习生长,进而制得平均粒径较大的AUC。

