α-Al2O3相变机理及制备工艺研究进展
吴宇峰,张铁军,张家萌,毕作振,雷 鸣,毕 科
(1.北京邮电大学理学院,北京 100876;2.陆军装备部驻上海地区航空军事代表室,上海 200233;3.山东中新铝基新材料有限公司,淄博 255000)
0 引 言
α-Al2O3具有许多优良性能,包括高熔点、高硬度、结构精确、高机械强度、绝缘、耐酸碱性等[1-2]。因此,α-Al2O3在耐火材料[3]、陶瓷材料[4]、研磨抛光材料[5]、化工材料[6]等领域都有着广泛应用;同时,由于其优良的电子和光学性能,也被用于制备结构电子和光学材料[7];此外,α-Al2O3电导率低,绝缘性能和介电性能好,常用于集成电路板和YAG激光晶体[8]。
根据O2-的排列结构,可以将Al2O3的晶体结构分为面心立方(FCC)和六角密排(HCP)两类。根据Al3+晶格的不同也可以将Al2O3划分为不同的晶型。Al2O3的晶型有十几种,常见的晶型有α-、θ-、κ-、γ-、δ-和η-等。表1是常见晶型与晶体结构的对应关系[9-10]。其中,α-Al2O3是最稳定的相,具有较大的晶格能,它的晶体结构如图1(a)所示,对于α-Al2O3来说,O原子紧凑排列形成六角型,Al原子填充八面体空隙的三分之一,晶格常数a和c分别是0.475 9 nm和1.299 1 nm。在特定的温度和压力等条件下,除了α相之外,氧化铝的其他相都可以发生转变,成核和晶粒生长机理在其中起到关键作用。其他相之间的转变属于位移式相变,从其他相转变为α相则属于晶格重构,是一种不可逆相变[11]。工业上通常以Al(OH)3为原料制备α-Al2O3,在生成α-Al2O3过程中,粒子之间会发生一个脱羟基过程,如图1(b)所示。α-Al2O3微晶的生长过程可以看作是不同颗粒间羟基在高温下相互作用脱水的过程。随着温度的升高,氧离子空穴浓度也会增加,直到羟基完全脱除。在较高的温度下,粒径较小的微晶会黏结在一起导致晶体的生长,使比表面积急剧减小[12]。研究发现,制备氧化铝的过程存在四个相变路线,如图1(c)所示,所有路径终点均指向α相。路线Ⅰ与路线Ⅳ相似,以路线Ⅱ和路线Ⅲ为主的α-Al2O3制备过程因适合工业化、规模化生产而更具有研究价值。可以看到,由于晶格重构需要大量的能量,无论哪一条路线的最后一步都需要非常高的温度。

表1 相与晶体结构的对应关系[9-10]
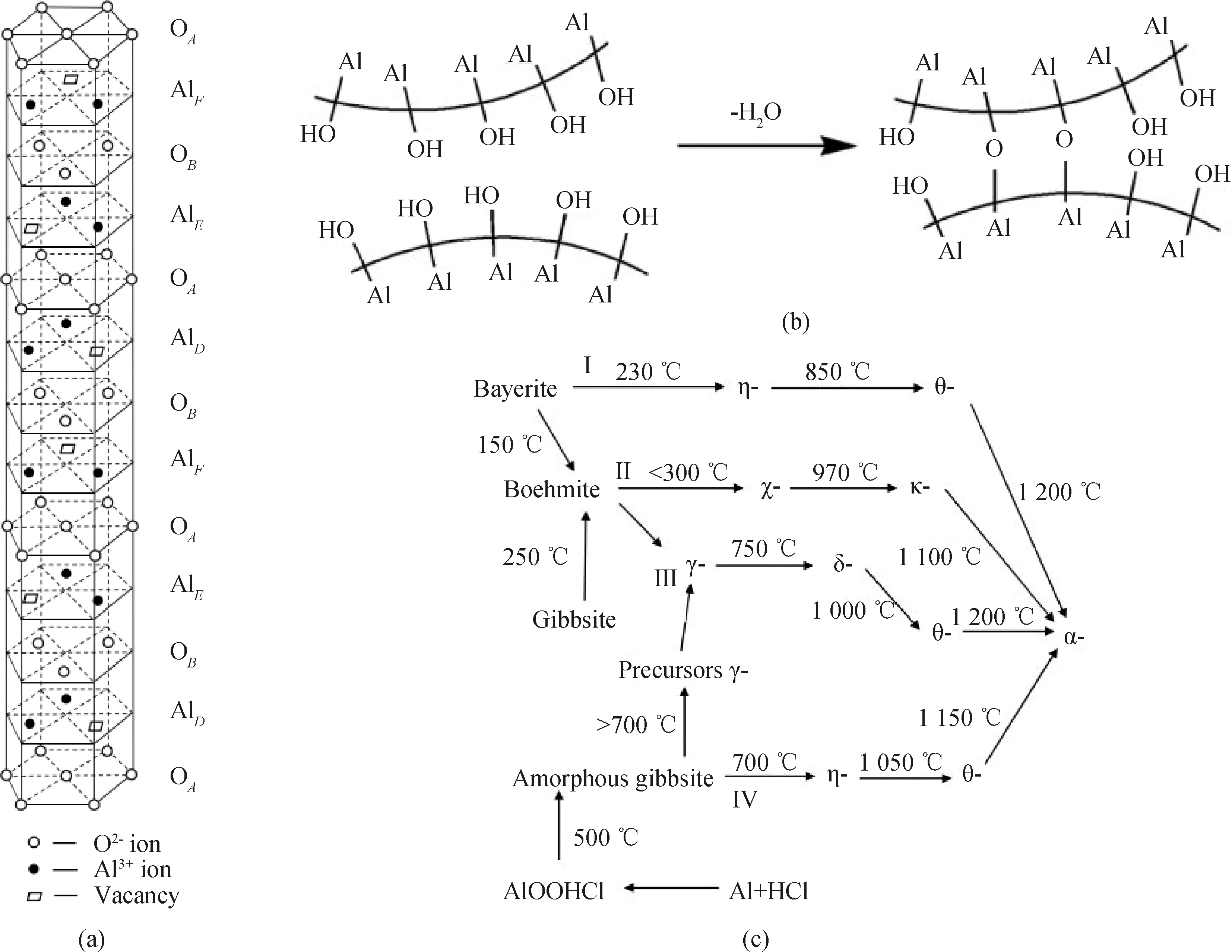
图1 (a)α-Al2O3结构示意图;(b)相邻氧化铝颗粒间脱羟基过程示意图[13];(c)四种相变路线[14]
因此,基于α-Al2O3的广泛应用,其评价指标与实际应用需求紧密相关,其晶粒的成核生长机理和制备工艺极其重要。本文结合α-Al2O3的制备路线分别阐述α-Al2O3的相变机理和制备工艺,并介绍相关的研究工作进展。
1 评价指标
一般情况下,α相转化率、α-Al2O3含量、Na2O和Fe等杂质含量会作为氧化铝质量评价的普遍指标。由于不同领域对α-Al2O3的性能有不同要求,因而各领域都存在更加细化的评价指标。如表2所示,该表列举了α-Al2O3在电子陶瓷材料领域、耐火材料领域以及打磨抛光材料领域的部分主要评价指标。可以看出,各行业对氧化铝的需求和评价呈现多样性和复杂性。

表2 三种应用领域中氧化铝材料的部分主要评价指标
在电子陶瓷材料领域,氧化铝多应用于LED衬底、锂电池以及膈膜镀层等前沿行业,这些行业通常对氧化铝的纯度和粒度有严格要求。目前,对纯度的需求最高可达到5N级即99.999 99%,对粒径的需求在50 nm以下。在此基础上,还进一步要求材料具有更弱的膨胀性、更强的介电性以及更高的材料强度,以保证电子器件的正常运转。
在耐火材料领域, α-Al2O3的主要评价指标是耐火度、比热容、高温结构强度和热膨胀性。耐火度在一定程度上能反应材料耐高温性,一般大于1 580 ℃的材料可称为耐火材料;高比热容能使得耐火材料在吸收热量时具有较低的升温速率;越大的高温结构强度值和越低的热膨胀值能保证材料在高温下的结构越稳定。该类材料多是通过优化α-Al2O3的微观结构和颗粒大小分布来减少水分吸收、增加流变属性[15]。
而在打磨抛光材料领域,α-Al2O3粒径、形貌以及莫氏硬度是评价α-Al2O3性能的关键指标,它直接影响抛光亮度和磨削力。氧化铝粒径越小,则打磨材料目数越大,打磨更加精细,更适用于尖端精细器件。从形貌上分析,传统的球形磨料具有成本低、寿命长和自锐性强等优点;而六角平板状磨料由于能均匀分布在工件表面,受力平均,因而耐磨性能得到较大提升,且能更好地保护工件。莫氏硬度作为另一项重要指标,能反映磨料的耐用程度。在相同情况下,硬度越高的磨料,用量会越少,可极大地降低抛光成本。由此可以看出,α-Al2O3的具体应用受到多项指标的共同限制,而氧化铝的制备工艺对α-Al2O3性能具有决定性影响,所以对制备工艺的研究将推动该材料的发展、促进其广泛应用。
2 α-Al2O3的成核和生长机理
1982年,Dynys等[16]通过对Al2O3微观结构的研究首先提出了α-Al2O3的相变可以分为两个阶段:相的成核和颗粒的生长。在整个相变过程中会消耗极大的能量,煅烧温度通常高于1 300 ℃,其中大部分的能量用于克服成核势垒形成α核,而剩余的能量则用于克服表面能量以促进晶粒生长。
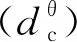

图2 (a)从θ相到α相成核和生长过程示意图[17-18];(b)用“剪切”的方式将θ相“超临界”结晶转化为α相[21];(c)扩散成核相形成双尺寸分布,晶体从θ迅速增长α[21]
然而,Bagwell[21]根据实验结果对成核机理中dcθ到dcα的过程又做出进一步解释:相变通过扩散成核进行。扩散成核的能量势垒产生于核和原相势垒之间新形成的一个表面上。在基材或晶界上,非均匀成核的自由能势垒比均匀成核的自由能势垒要小的多,特别是在非均匀成核和与均匀成核相具有相似晶体结构的情况下。由于扩散成核在晶面和晶界处更为有利,因此预计α-Al2O3将在θ-Al2O3晶体表面或在晶体间的连接处成核。晶体大小是扩散成核的必备条件,因为θ-Al2O3晶体必须足以生成强有力的异质α-Al2O3成核位点。α晶体大小的分布类似于图2(c)所示。α-Al2O3蠕虫状的微观结构特点也是源于生长过程。总的说来,Bagwell指出α-Al2O3的成核过程是一个典型的扩散成核过程,并没有必要先增大到临界尺寸阶段进行过渡。一般情况下,观察到的过渡阶段晶体成核和生长是在α-Al2O3孕育时间内形成,超大α核并不来源于剪切θ-Al2O3大晶体,而是来源于成核后α-Al2O3的快速增长。因此,到目前为止人们仍对α-Al2O3的相变过程存在不同意见。
3 α-Al2O3制备的研究进展
α-Al2O3的合成方法主要可以分为三类,分别是固相、液相和气相合成:固相合成方法包括机械研磨法[15,22-24]、激光烧蚀法[25]、火焰喷涂法[26]、煅烧法[27-36]等;液相合成方法包括溶胶-凝胶法[37-43]、水热法[44]、沉淀法[45]和微乳液[46]等;气相合成方法包括等离子体热分解法[47],蒸汽沉积法[48]等。下面针对这三类合成方法进行具体的介绍。
3.1 固相合成法
固相合成方法通常是以工业氧化铝或氢氧化铝为原料,经过高温煅烧后生成α-Al2O3。但煅烧温度过高会引起氧化铝粒径增大和颗粒聚集现象,导致α-Al2O3的高温性能受到较大影响[49],因此通常采用机械球磨或加入矿化剂的方法来改善产品的质量。Tonejc等[28]发现高能球磨相当于一个热处理过程,能够用于α-Al2O3的制备。但机械球磨的生产成本高,产品纯度低,因此不适合工业生产[50]。

工业上大约需要1 300 ℃以上的高温才能生成α-Al2O3。如果在制备过程中不添加矿化剂,最终制得α-Al2O3的微观结构为蠕虫状,如图3(a)所示。为了进一步改善α-Al2O3的产品质量,在近15年里,许多研究学者对矿化剂的作用和α-Al2O3的制备过程进行了大量研究。崔香枝等[31]在Al(OH)3中加入质量分数1%Al2O3晶种和3%AlF3后发现Al2O3在950 ℃时即可完成α相变,很大程度上降低了相变温度。尹周澜等[32]发现NH4F对Al2O3相变的促进作用比AlF3更明显,仅加入质量分数1%NH4F,即可在1 100 ℃左右完成α相变。这些研究都能够证明含氟矿化剂能有效降低煅烧温度,主要归因于F-的加入可以提高α-Al2O3在高温时的蒸气压,并改变其结晶模式,使其形成方式由固相传质变为气相传质,极大地促进α-Al2O3晶体的生长[29]。同时,当温度升高时,NH4F等物质分解产生与Al2O3反应的气体,抑制Al2O3晶体等轴生长并加速片状化,最终制得氧化铝如图3(b)所示。研究人员发现含氯矿化剂也有类似的作用,但效果要低于含氟矿化剂,并可能会使α-Al2O3堆积成块状。部分情况下,含氯矿化剂的加入也可能导致针状产物[51],如图3(c)所示。此外,添加NH4NO3能够促进α-Al2O3晶体形成椭圆状,这是由于NH4NO3在高温下发生分解反应生成硝酸,硝酸可与氧化铝反应并使得气相中的氧化铝的含量增加[13]。同时,添加NH4F和NH4Cl的复合矿化剂能够减少α-Al2O3的横向和纵向生长的差异,使其形成如图3(d)所示的类圆块状[33]。
硼酸也是常用的α-Al2O3矿化剂之一。李峰克等[34]发现硼酸可以加快α-Al2O3蠕虫聚合的分离, 添加硼酸后制备出的氧化铝如图3(e)所示。硼酸作为矿化剂制得的晶体一般类似于液滴和柱状,结晶表面光洁。随着硼酸添加量的增大,Na2O的含量先增加后减少,因此适量的硼酸有助于α-Al2O3产品具有更高的纯度。陈若愚等[50]研究了pH值对相变的影响,发现使用盐酸控制pH值能够影响α-Al2O3的含量和大小。其中,随着盐酸溶液pH值的降低,α-Al2O3的相变转化率逐渐增大,晶粒尺寸也随之增大。盐酸的作用机理与含氟矿化剂相似。
此外,研究人员[29]也通过显微镜发现MgO能够抑制α-Al2O3晶粒生长。MgO在低温下聚集在Al2O3晶体表面,抑制了α-Al2O3晶体的生长。随着烧结温度的升高,MgO在Al2O3表面形成等轴向镁铝尖晶石,进一步阻碍α-Al2O3晶体的生长。
除了矿化剂会对α-Al2O3性能产生影响外,Chang等[35]发现Al2O3晶体的大小和形状也能够在一定程度上影响相变。固相合成中,Al2O3主要是由Al(OH)3高温脱水而成,当Al2O3粒径小于10 nm时,氧化铝可以直接从χ相转变为α相(路径Ⅱ),不经过κ相转变阶段。并且,活化能随着颗粒尺寸的减小而减小,氧化铝煅烧温度也随之降低。但如果颗粒被碎片化处理破坏,生长过程就会受到阻碍。另外,Lamouri等[36]研究了升温速率对α-Al2O3的影响。他们发现当升温速率控制在5 ℃/min时,α-Al2O3具有密集和均匀的微观结构,如图3(f)所示,可以看到较少孔隙、较大密度和清晰明显的晶界。孔隙致密化的原因很可能是由于在向α-Al2O3转化过程中形成了一个粗糙的、蠕虫状的孔隙结构,这一发现有助于高密度α-Al2O3的制备。孙春晖等[33]也研究了前驱体预处理对氧化铝粉末形貌的影响。在预先对原料进行热处理过程中,原料的结构和颗粒形貌基本保持不变,α-Al2O3形成时出现较大的体积收缩。α-Al2O3的热稳定性与前驱颗粒的结晶度有关,结晶度越高,在高温下的热稳定性越好。
3.2 液相制备
工业氧化铝中存在碱金属氧化物(尤其是Na2O)等杂质,为了改善这种情况,通常采用溶胶-凝胶法以铝盐与酸或碱反应制备氧化铝前体,然后高温煅烧制备α-Al2O3。这种方法的煅烧温度低,得到的氧化铝纯度高。但制备工艺复杂,对原料纯度要求高,很难实现大规模的工业化生产。
在溶胶-凝胶法制备α-Al2O3的过程中添加α-Al2O3晶种是很常见的一种方法,目的是为了让氧化铝从θ相转变为α相。Kumagai等[38]发现了α-Al2O3粒子或晶种可以作为θ-到α-Al2O3转化的成核位点。Oh等[39]的研究表明,这种转化依赖于温度和晶种浓度,尽管在不添加晶种的情况下,需要的陈化时间短于添加晶种的情况,但添加晶种更有助于降低活化能、降低相变温度,在更短时间内成核和相转变。Wen等[19]研究了相变过程中的尺寸控制,发现通过不同热处理方法制备的α-Al2O3具有不同的初级晶粒尺寸,一旦相变完成,就可能发生热絮凝现象。因此,热处理技术是制备纳米α-Al2O3粉末的关键,较高的升温速率和较短的加热时间有助于合成单分散的纳米级α-Al2O3粉体,如图4(a)所示。Sharma等[40]提出在溶胶-凝胶法制备α-Al2O3过程中pH值是关键的工艺参数,pH值决定了最终产物的相、大小和形态。实验中,当pH值为2.5时, α-Al2O3颗粒尺寸为70 nm,形状是球形;当pH值增加到12时,颗粒尺寸增加到750 nm,形状变为六角形,如图4(b)和(c)所示。因而,可以通过调控pH值的大小来控制α-Al2O3颗粒的最终形态,以合成适用于不同领域的α-Al2O3粉体。Bell等[41]通过控制搅拌速度、固体负载等合成变量发现它们对α-Al2O3的形成和生长有决定性的影响。此外,Rajaeiyan等[42]报道了合成方法对α-Al2O3表面积、颗粒形态以及尺寸的显著影响。在相同的温度煅烧后, 由共沉淀法制备的α-Al2O3颗粒表面积大于由溶胶-凝胶法制备的α-Al2O3颗粒表面积,并且由前者制备所得的颗粒形状是近球形或不规则六边形,而由后者合成的颗粒则更多为球形,结构也更加统一、尺寸更小,如图4(d)和(e)所示。

图3 (a)未添加矿化剂制备α-Al2O3的SEM照片[32]; (b)添加含氟矿化剂制备α-Al2O3的SEM照片[51]; (c)添加含氯矿化剂制备α-Al2O3的SEM照片[51]; (d)添加含复合矿化剂制备α-Al2O3的SEM照片[51]; (e)添加硼酸制备α-Al2O3的SEM照片[51]; (f)升温速率为5 ℃/min制备α-Al2O3的SEM照片[36]
3.3 气相制备
化学气相淀积(CVD)在气相合成中是最为经典的方法, 但相关报道较少,该方法常用于制备适用于航空航天领域的α-Al2O3涂层材料。
Fredriksson等[43]研究了AlC13/CO2/H2气体混合物氛围中Al2O3层在SiO2衬底上的沉积过程。κ-到α-A12O3的相变发生于沉积过程的开始,相变的同时α-A12O3的晶粒也进行生长,形成尺寸更大的α-A12O3晶体。其中,温度、CVD系统气体泄漏率和杂质会促进相变和α-A12O3的形成。沉积过程中温度越高,α相形成越早;沉积装置气体的泄漏率越高,越会促进κ-到α-A12O3相变;杂质的存在会改变κ-A12O3的正常生长模式和每一层的生长方向,制备的氧化铝颗粒如图4(f)所示。同时,杂质的存在也会促进α相变,在一定程度上增大了α相含量。Borsella等[52]研究了利用激光驱动气相前驱体合成纳米氧化铝粉末。他们把气相反应物放在一个特定的区域内用激光照射,在温度梯度很大的情况下,可以在局部达到很高的温度。这种方法的初始成核速率非常高,而且粒子一离开热区,生长就会因为温度的骤降而突然终止。因此,产生的粒子是超细和球形的,在大小上几乎是单分散的,纯度也很高。通过这种方法,可以制备预期大小、形状、分布和纯洁的α-A12O3晶体,但难以大量生产是最为关键的问题,不过这种方法已经为α-A12O3的合成带来了一个新的思路。

图4 (a)单分散纳米α-Al2O3粉体的TEM照片[19]; (b)pH=2.5时制备α-Al2O3的TEM照片[41]; (c)pH=12时制备α-Al2O3的TEM照片[41]; (d)由共同沉淀法制备α-Al2O3的TEM照片[42]; (e)由溶胶-凝胶法制备α-Al2O3的TEM照片[42]; (f)含有Cr杂质α-Al2O3的SEM照片[43]
4 结语与展望
α-A12O3作为工业上极其重要的材料,在许多领域具有广泛应用,因而针对α-A12O3的研究也具有极高价值和实际意义。目前,α-A12O3的制备方法有固相、液相以及气相三种,固相、液相合成方法中分别主要以机械研磨法、燃烧法,和溶胶-凝胶法、沉淀法制备α-A12O3粉末,气相合成方法则主要是通过化学气相沉积法制备氧化铝薄膜。基于这些方法可使α-A12O3制备满足多个领域的应用,所以针对制备过程中α-A12O3晶粒的影响因素,如温度、pH值、矿化剂类型等,已经存在较为成熟的研究结论。
值得注意的是,当前对α-A12O3成核生长机理方面的研究仍较为欠缺,如前文所述的同步剪切成核机理与扩散成核机理仍存在争议,清晰的成核机理有助于实现α-A12O3的精细制备。因此,当下氧化铝行业的共同追求目标应有3点:(1)明确的成核机理;(2)粒径更小、纯度更高、成本更低的α-A12O3;(3)进一步掌握通过调整合成条件控制α-A12O3晶粒形貌的技术。未来这3点目标的实现将赋予α-A12O3材料更加可观的使用价值,该材料的应用领域也会因此得到一定程度的扩展,所以如何实现这3点目标将会是α-A12O3未来研究的重点和发展方向。

