肠道微生物对疫苗免疫效果影响的研究进展
陈斯谦 吴边 柳陈坚 李晓然
(1. 昆明理工大学生命科学与技术学院,昆明 650500;2. 云南省第一人民医院 昆明理工大学附属医院,昆明 650032)
疫苗作为一类通过激活机体免疫系统发挥预防、治疗作用的药物而受到广泛使用。其在进入体内后会对机体免疫系统进行刺激,引起免疫应答,进而导致免疫细胞分化等过程,对个体产生保护作用。在该系列过程中,由于个体差异等因素,机体所使用的疫苗并不能如期地发挥作用。肠道微生物是居住在宿主肠道中的微生物总称,因其对宿主生长发育等过程具有重要作用而被称为人类第二基因组。近年来对于肠道微生物与宿主免疫系统相互作用的领域研究备受关注,大量文献表明肠道微生物对宿主免疫系统各个过程有着重要作用,并且影响着宿主免疫系统的免疫应答;此外,肠道微生物还能够对机体服用的药物进行代谢,这都可能影响疫苗的药效。本文系统总结了肠道微生物对于疫苗作用效果影响的研究进展。
1 微生物对疫苗的作用概述
1.1 肠道菌群概述
肠道菌群是在宿主肠道中居住的微生物总称,其组成在宿主整个生命历程中呈现一定的变化趋势。在两岁以前宿主肠道微生物群落组成呈现无规律变化[1-2],这种变化主要受饮食、抗生素使用、病毒感染、分娩方式(顺产,剖腹产)以及环境洁净度影响[3-4]。随着宿主免疫系统发育成熟,宿主肠道微生物群落会在门的组成水平上趋于稳定[1-2],并以放线菌门(Actinobacteria)、拟杆菌门(Bacteroidetes)、厚壁菌门(Firmicutes)、变形菌门(Proteobacteria)以及软壁菌门(Tenericutes)为主[5]。各门的比例以及当中微生物的组成受宿主基因组,外界环境,饮食等因素影响而存在差异,进而影响宿主免疫以及代谢。
1.2 特定肠道菌群对疫苗效果的影响
研究表明特定的微生物类群会影响疫苗的效果,多见于口服疫苗相关研究中,如属于肠道中肠杆菌-拟杆菌属(Enterobacteria-Bacteroides)的类群以及解没食子酸链球菌(Streptococcus gallolyticus),双歧杆菌科中的长双歧杆菌(Bifidobacterium longum)的longum亚种和infantis亚种这些微生物与疫苗口服后宿主免疫应答以及免疫细胞的丰度呈正相关,而肠道中的拟杆菌门,属于变形菌门的假单胞菌目(Pseudomonadales)则相反[6-7]。这类临床研究的缺陷在于仅报道特定菌群与接种疫苗后免疫应答的强弱相关性而没有作更为深入的机理研究。
1.3 益生菌对疫苗的影响
在众多类型的肠道微生物中,益生菌被研究得较多,大量文献报道其对宿主肠道具有调控作用。益生菌是肠道中存在的一大类微生物总称,它们能对宿主产生益生的生理特性。益生菌包括酪酸梭菌,乳酸菌,酵母,放线菌,双歧杆菌,嗜酸乳杆菌等[8]。我们先前研究发现,由乳杆菌(Lactobacillus)发酵制成的功能食品能够明显改善肠道运输,并且能够改变肠道菌群的组成,这表明益生菌对肠道的功能具有较大影响,服用益生菌后能够使肠道微生物群落朝着有利于宿主健康的方向发展[9-10]。
益生菌能够对肠道免疫系统进行调控,部分益生菌(乳杆菌,双歧杆菌,链球菌以及乳酸菌)已被证实能够激活或抑制宿主体内的MAPK及NF-κb这两条免疫相关的主要通路而影响宿主免疫应答[11]。另一方面,与疫苗引起免疫应答相关的免疫球蛋白(Ig)亦受到相关益生菌的调控。如干酪乳杆菌(Lactobacillus casei)可以增加宿主小肠固有层总的slgA水平,以及IL-6,并且不产生由益生菌所诱导的特异性的slgA[12]。在一项关于轮状病毒感染的实验发现,给予小鼠双歧杆菌(双叉双歧杆菌(Bifidobacterium biofidum),婴儿双歧杆菌(Bifidobacterium infant))处理后,小鼠病毒感染率显著降低,并且肠道黏膜针对轮状病毒特异性IgA的抗体滴度增加[12]。此外,另有报道表明肠道中的益生菌提高了宿主疫苗特异性 IgG(IgG1 和 IgG3)含量[13],并且肠道中双歧杆菌占优势时可能会在增强婴儿胸腺发育和对口服和注射疫苗的反应[7]。值得关注的是,上述研究表明宿主并不会对益生菌产生特异性的Ig将细菌清除,这有可能归功于益生菌本来就是正常肠道中存在的有益菌群,除了不会受到肠道免疫系统的攻击外还对宿主免疫发育作出贡献。相反,有了益生菌对宿主免疫系统的辅助,宿主在受到抗原(如疫苗)刺激后,引起了更加激烈的免疫反应,产生更加大量的,针对抗原的特异性浆细胞、记忆细胞以及Ig,从而提高了应答效应。
1.4 抗生素使用与无菌环境
肠道菌群会影响疫苗效用,而抗生素以及无菌环境不存在于正常的肠道微生物群落。越来越多运用抗生素以及无菌动物进行的研究显示这类特殊的肠道环境会对宿主免疫系统造成影响。结肠处的能量代谢很大程度上依赖于肠道菌群,而肠道免疫系统成熟过程中需要大量的能量来满足细胞分化,成熟,迁移以及分泌相关免疫调控细胞因子,缺乏菌群的小鼠结肠细胞表现出能量缺乏状态,包括TCA循环,丙酮酸脱氢复合酶的活性降低[14]。而这种肠道状态会对体内其他免疫器官的发展造成损伤,包括免疫细胞类型丰度、淋巴组织发育和对病原体敏感性[15]。在这种缺乏肠道菌群的肠道环境中,宿主小肠和结肠常常伴随着树突状细胞、CD4+细胞,CD8+T细胞、调节性T细胞(FoxP3+)、Th1细胞(IFNγ+)和B细胞减少[16],并且肠道中对于抗病毒起关键作用的 IL-1b、TNF-a 、 IL17以及IgA等细胞因子减少。这预示着缺乏微生物的肠道对于抗原的刺激敏感性较低,因此可能难以对疫苗产生正常应答。宿主健全的免疫系统成熟以及发挥正常功能需要稳定健全的肠道微生物群落存在,而无菌或抗生素处理后的肠道环境会导致免疫系统发展受阻。
关于上述特殊肠道环境对疫苗应答鲜有报道,但有研究表明抗生素造成免疫系统缺损导致了疫苗不能正常发挥疗效。流感疫苗是当今最普遍的一类疫苗,宿主抗生素的服用会打破肠道微生物群落的稳定,而机体过往获得的抗流感病毒免疫力的抗体反应会因此而减弱。此外,肠道菌群因抗生素而导致的紊乱会导致血清次级胆汁酸减少,这种现象与 AP-1/NR4A 信号和炎症体激活高度相关,并且还观察到服用抗生素以及正常人群两组由疫苗产生的IgG1 应答存在差异[17]。这项研究表明宿主在缺少肠道中某些微生物的作用,导致了以往接受了抗原刺激的记忆B细胞作用减弱,间接减弱了以往注射疫苗的效用。但这种对于记忆B细胞减弱的效应是由于肠道微生物的缺失导致的细胞数量损失还是记忆B细胞激活后产生的抗体减少导致的还有待更为深入的研究。
2 肠道微生物对疫苗作用的可能途径
2.1 肠道微生物可能通过调节免疫系统影响疫苗效果
肠道微生物对于疫苗的效应很有可能是其产生的次生代谢物作用结果。人类肠道中定居着种类繁多的微生物,因此其代谢类型也具有多样性。而报道得较多的是肠道微生物通过产生短链脂肪酸(SCFA)以及胆汁酸而对宿主免疫系统产生作用(图 1)。
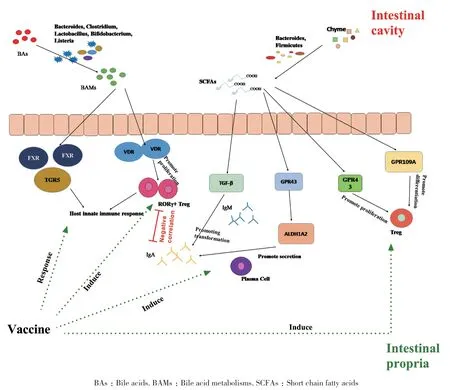
图1 肠道微生物通过影响宿主免疫系统进而影响疫苗作用效果的可能路径Fig.1 The possible pathways of affecting vaccine effects in intestinal microorganism by affecting the host immune system
2.2 肠道微生物可能会对疫苗产生直接作用
2.1.1 短链脂肪酸 哺乳动物体内的短链脂肪酸(short chain fatty acids,SCFAs)以乙酸、丙酸和丁酸含量最高。拟杆菌门和厚壁菌门是肠道中最丰富的门,拟杆菌门的成员主要产生乙酸盐和丙酸盐,而厚壁菌门主要在人体肠道中产生丁酸盐[18]。据前所述,肠道中拟杆菌门与厚壁菌门的丰度与疫苗产生的特异性免疫相关,因此推测是此类肠道微生物产生的短链脂肪酸作用于宿主免疫系统进而影响了该过程。SCFAs可直接调节宿主的免疫系统并维持其稳态,其主要通过与短链脂肪酸受体GPR43结合诱导中性粒细胞趋化和调节性T细胞(regulatory T cells,Treg)的增殖;介导G蛋白偶联受109A(GPR109A)的活化诱导Treg分化;诱导肠上皮细胞的转化生长因子-β(TGF-β)表达间接使B细胞分泌的免疫球蛋白发生转化并导致IgA的产生或通过GPR43诱导醛脱氢酶家族1成员A2(ALDH1A2)表达,进而促进B细胞分泌IgA[19-20]。这3个方面进行的,形成了肠道微生物(拟杆菌门与厚壁菌门)-短链脂肪酸-免疫系统-抗原这一调控轴。而疫苗作为抗原的一类,进入人体后必然会引起该调控轴的反应。
2.1.2 胆汁酸 胆汁酸是机体胆固醇分解代谢产生的一类胆烷酸衍生物,肠道中参与胆汁酸代谢的微生物包括拟杆菌,梭菌、乳酸菌、双歧杆菌和李 斯 特 菌(Bacteroides,Clostridium,Lactobacillus,Bifidobacterium,Listeria)[21-22]。在此过程中,游离至肠道的胆汁酸受到肠道菌群的作用而转化为胆汁酸代谢物,并由肠道菌群维持着两者的平衡。目前认为该过程是通过调控核胆汁酸受体FXR和质膜受体TGR5进行的[23]。胆汁酸水解酶则是众多微生物酶其中重要的一种,其可将结合型胆汁酸转化为非结合型胆汁酸或通过磺化、氧化、差向异构、脱羟基等催化修饰直接改变胆汁酸结构[24]。而微生物作用后的胆汁酸产物通过维生素D影响着肠道RORγ+Treg的数量,这一细胞类群常被认为在机体免疫应答中发挥着主要作用[23,25]。此外,小鼠实验显示IgA浆细胞能够从肠道中发生转移,并且肠道中的RORγ+ Treg与 IgA 水平呈现负相关[26-27],这表明上述的细菌类群对疫苗的影响存在一条通路,即上述微生物类群通过FXR和TGR5对胆汁酸的代谢进行调控,生成的胆汁酸代谢影响着RORγ+ Treg类群的丰度,进而对机体中疫苗作用于免疫细胞产生的IgA含量产生影响。
肠道微生物会对宿主体内药物进行修饰,许多从中药里分离的有效成分被认为需要经过肠道微生物的结构修饰变为活性构象发挥疗效[28],而药物经肠道微生物和酶的作用常发生脱糖基、脱甲基、脱羟基、水解、氧化还原等反应[29-30],导致在肠道中活性增强,失活或产生毒副作用[31-32]。许多中药成分在经过肠道菌群的作用后活性会得以提高,例如人参中主要的原人参二醇型皂苷-人参皂苷Rb1,通过肠道微生物逐步去糖基化为化合物K和20(S)-原人参二醇,这两种物质都被实验证明具有比人参皂苷Rb1更好的生物利用度和生物活性[33]。
口服疫苗直接与人体小肠黏膜接触,通过黏膜上皮细胞表达II类主要组织相容性抗原(MCH)进行抗原转运和呈递,抗原传递给I类T辅助性淋巴细胞(Th1),促使B淋巴细胞分泌型IgA抗体,形成细胞毒淋巴细胞及记忆型细胞。IgA型抗体由黏膜上皮细胞转送至肠道或呼吸道内,阻止外来病原微生物结合;IgA抗体也可以通过补体和抗体介导的细胞毒性作用参与病原微生物的杀伤和清理[34]。虽然肠道微生物直接修饰疫苗成分的研究尚未报导,但推测口服类疫苗会受到肠道微生物的直接作用。并且因其通过小肠吸收发挥作用,所以受小肠中的微生物影响较大。从总体上讲,许多疫苗的本质是碳水化合物这一大类物质,包括多糖类疫苗,而肠道菌群特别适合对药物进行糖苷水解,因为许多细菌门,特别是拟杆菌门和厚壁菌门,它们都编码有丰富的糖苷水解酶基因,因此含有糖苷键的药物或辅料在暴露在肠道环境中极易被降解。此外,这种对于糖苷键的分解并不是靠某一类微生物进行一次加工完成的,细菌在多糖发酵中常常发挥协同作用,通过在无菌小鼠肠道上单一定植真杆菌(Eubacterium rectale),多形芽孢杆菌(Bacillus thetaiotaomicron)或两者共同定植建立的人类肠道微生物群的简化模型揭示了这种协同作用。在真杆菌,多形芽孢杆菌相互共存的肠道环境中,真杆菌上调了自身许多糖苷水解酶的表达,而直杆菌下调了其聚糖降解酶的产生,但却上调了寡糖和单糖转运蛋白的表达。当处于共定居状态时,多形芽孢杆菌专注于多糖降解,而直形芽孢杆菌专注于对多形芽孢杆菌产生的多糖降解产物的进一步加工[35]。这一互动提示了上述两种细菌对于口服多糖等疫苗可能存在连续性的降解作用(图2),导致部分失活,降低其生物利用度,因此在生产工艺中需考虑这种降解作用,对具有糖苷键的疫苗进行糖基化以防治糖苷键水解或加以特定佐剂用作保护。

图2 多糖类口服疫苗作用原理及小肠中的微生物对其降解作用Fig. 2 Reaction principle of polysaccharide oral vaccine and its degradation by microorganisms in small intestine
3 肠道微生物影响宿主免疫系统发育
肠道微生物会影响宿主免疫系统发育,而疫苗作用的原理是通过特定的抗原激活机体特异性免疫应答,这需要宿主免疫系统的参与。近年来越来越多报道证明肠道微生物对宿主免疫系统表型构造以及免疫应答起着重要作用,这类作用常被认为主要通过上述短链脂肪酸、丁酸盐及维生素等物质发挥的功效。肠道微生物在生命的早期已存在,我们之前的研究结果显示人体至少在胎儿时期就已暴露在有菌环境,在所有胎便样品中,变形菌门(Proteobacteria)丰度最高,而由上文得知,肠道中的变形菌门丰度与口服疫苗的活性呈负相关,这表明孕期胎儿的肠道环境对于口服疫苗的药效会产生负面作用;除了一般的细菌外还存在产甲烷古生菌(Methanobrevibacter),这一以往被认为是肠道不健康的指示菌种[36]。在生命早期,宿主免疫系统还未成熟且缺乏适应性免疫的情况下,肠道微生物分泌未知的代谢物通过STAT3磷酸化以IL-23和IL-22依赖的方式激活上皮内淋巴细胞(IEL)和固有淋巴样细胞3(ILC3),宿主则通过IL-23,ILC3,IL-22和IEC形成反馈回路调控肠道微生物群,保持了早期生命免疫系统与肠道菌群的动态平衡。
随着生命周期推进,肠道微生物的丰度提高,并随着小肠近端到直肠远端的顺序逐渐递增,大量的肠道微生物定植在宿主结肠隐窝处,与宿主肠上皮细胞相邻。而肠上皮细胞被认为是免疫细胞的一种[37],能够对宿主免疫系统进行调节[38]以及直接与菌群相互作用,如肠道某些特定菌株(Segmented filamentous,Bacteroides fragilis)能够通过与肠道上皮细胞接触引起一系列的免疫反应导致肠道T细胞亚群改变,招募末端回肠中Th17细胞的积聚,并通过细胞的TLR2通路进而促进 Foxp3+调节性 T 细胞的发育等作用[39-40]。这些研究再一次表明了肠上皮细胞是微生物与宿主免疫系统以及疫苗与微生物间接互作的媒介以及传导使者。
肠道微生物除了能够维持宿主免疫系统稳态以外,还能参与宿主免疫系统修复。在一项通过骨髓移植而重构化疗破坏的免疫系统的癌症患者队列研究中发现,肠道中的粪杆菌属(Faeclibacterium),瘤胃球菌属(Ruminococcus)以及阿克曼菌属(Akkermansia)的组合能够明显增加血液中的白细胞数量,进而说明了这3个属的某些微生物可能存在一定的串联式协同互作,通过某一通路来重新激活,修复宿主免疫系统。此外,除了这3个微生物类群以外,部分能够产生短链脂肪酸,细胞壁分子以及能够介导胆酸盐降解,维生素B1合成以及丁酸盐形成的微生物亦与骨髓移植后患者体内白细胞数目相关[41],而执行这类功能的微生物通常被认为是正常人体肠道中占主导的菌群。以往也有相当数量的关于正常人体或正常实验动物的肠道菌群移植到患病动物体内的实验,这些研究内容涉及癌症,老年痴呆,皮肤移植等方向,结果或多或少表明了正常的肠道菌群能够改善患病动物的症状,但这些研究缺乏相应的肠道代谢组数据。根据患病动物在接受移植后的肠道微生物组成,我们大致可以相信这两者肠道的代谢情况是相当的,进而可以大体认为恢复正常的肠道微生物产生的代谢物有助于患病宿主恢复,包括对宿主免疫系统的修复。由此可见,肠道微生物维系了宿主正常的免疫环境,而这也是疫苗发挥作用的前提。
4 展望
随着系统生物学等学科的发展以及组学测序的普及,使我们能够更深入,系统地研究肠道微生物与宿主免疫的关系。相比于传统研究方法,近年来兴起的单细胞测序技术提高了免疫系统环境中各个过程的分辨率,使得研究能够聚焦于宿主免疫中的微小变化;而宏基因组、蛋白组、16S测序技术也因技术的发展而使成本大大降低,得到普及。以上种种促使该领域在短短几年内迅速发展。肠道菌群对于宿主免疫成熟、恢复以及正常运行的作用不容小觑,该方向的研究为免疫治疗、系统免疫药物用药提供了很好的指导。对于肠道微生物与疫苗之间的相互作用,近年来也被陆续报道,而该方向处于起步阶段,有待后续研究阐明更深入的系统关系,肠道菌群对于新冠疫苗这一类通过免疫应答发挥疗效的药物作用到底会造成何种影响,这也是值得探讨的问题。但我们可以从过往研究中得到启发,基于肠道菌群的作用对以往疫苗剂型进行改良以及疫苗研发的思考,使其能够更好地在机体发挥疗效以及减小毒副作用。·

