卫矛醇通便功能人体试验研究
王殿奎,马永华,刘仁民
(中唯国际生命科技有限公司,天津 300381)
0 引 言
便秘既是一个独立的证候,又是多种疾病中的一个症状,发生年龄的分布遍及整个年龄段,根据起病时间的长短分为急性便秘和慢性便秘,根据发病机制分为机械性便秘和功能性便秘。便秘的典型症状是排便困难,伴腹胀,大便次数减少。患者长期吸烟、喝酒及刺激性饮食可引起大便习惯改变,出现便秘。应积极就诊,通过药物治疗及生物反馈治疗,使大便通畅。进行饮食调理是预防便秘和减轻便秘损伤的重要方法之一,合理膳食,同时搭配功能性膳食补充剂是及其重要的防治便秘途径。本研究对单一食用一定剂量的卫矛醇对人体的通便作用进行研究。
由玉米芯和木糖母液中提取的卫矛醇是植物萃取产物之一。卫矛醇(Dulcitol)别名为甜醇(Galactitol)、半乳糖醇、己六醇,CAS号为608-66-2,白色结晶或结晶性粉末,无臭,味甜,化学式为C6H14O6,化学结构式见图1,分子量为182.17,熔点为187℃~190℃,在水中溶解度较低,易溶于沸水,微溶于乙醇。根据国家食品安全风险评估中心安全性评估意见(报告编号:C2015012)[1],以玉米芯及木糖母液为原料制得的卫矛醇,推荐食用量为每日2 g,适宜人群为除婴幼儿之外的其他人群。
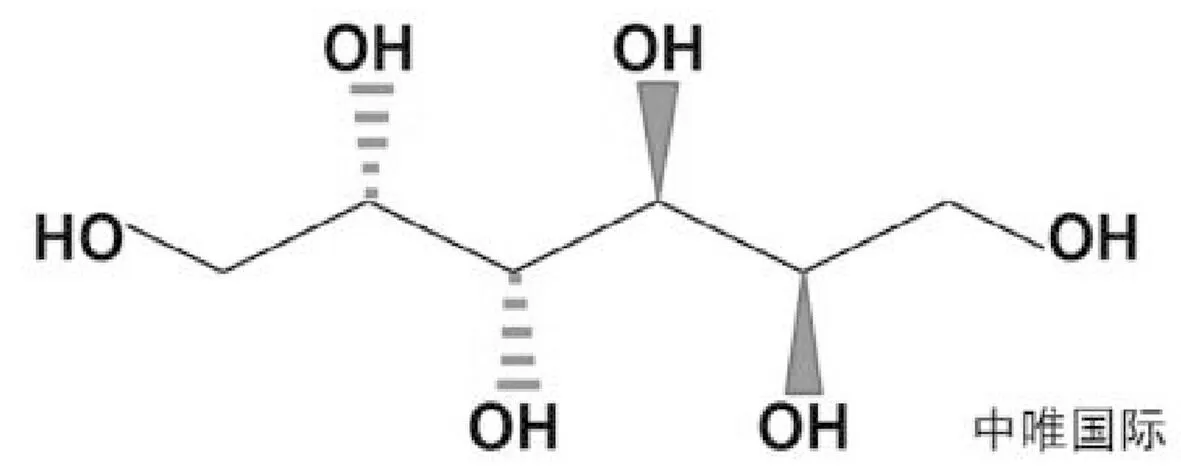
图1 卫矛醇分子结构式Fig.1 Molecular structural formula of dulcitol
为了开展卫矛醇通便功能人体试食试验研究,观察单一食用卫矛醇对人体通便功能的作用,将本研究的试验剂量确定为人体每日摄入2 g卫矛醇,以晶体直接服用。依据《保健食品检验与评价技术规范》(2003版)[2],进行为期14 d的人体试食试验,观察其对人体便秘的缓解作用。
1 对象和方法
1.1 样品
卫矛醇(中唯国际生命科技有限公司提供,山东福田药业有限公司生产)样品性状:白色结晶性粉末,规格2 g/袋,批号20190620。安慰剂:规格2 g/袋,包装与样品性状、颜色和大小完全一致。
1.2 仪器与试剂
日立7180全自动生化分析仪(日本株式会社日立高新技术生产);桂林优利特300全自动尿液分析仪(桂林优利特电子集团有限公司生产);Sysmex-K21 三分类血液分析仪(Sysmex公司生产);Sysmex血细胞分析稀释液(Sysmex公司生产);KX-21全自动血液分析仪(日本希森美康公司生产);BS-800全自动生化分析仪(深圳迈瑞公司生产);优利特URIT尿八联试纸(桂林优利特电子集团有限公司生产);利德曼生化试剂盒(北京利德曼生化股份有限公司生产);日本协和生化试剂盒(日本协和医药株式会社生产);日本一化生化试剂盒(日本第一化学药品株氏会社生产);原丁试剂(上海阿拉丁生化科技股份有限公司生产);德国CENTRONIC试剂(德国CENTRONIC公司生产)。
1.3 试食剂量及时间
试食组服用卫矛醇,每日1次,每次1袋,口服。对照组采用安慰剂对照。按盲法进行试食试验。受试样品给予时间14 d。试验期间不改变原来的饮食习惯,正常饮食。
2 试验结果
2.1 一般资料
纳入受试者59例,按年龄、性别、病程随机分为试食组和对照组。有效病例52例,试食组26例,对照组26例。52例受试者国籍分布见表1。试食期间受试者精神正常,饮食、睡眠、小便、血压、心率均无异常表现;胸透、心电图、腹部B超未见异常;受试者在试食期间无恶心、胀气、腹泻、腹痛不良反应;试食前两组一般情况、便秘程度情况见表2。

表1 受试者国籍分布Tab.1 Nationality distribution of subjects
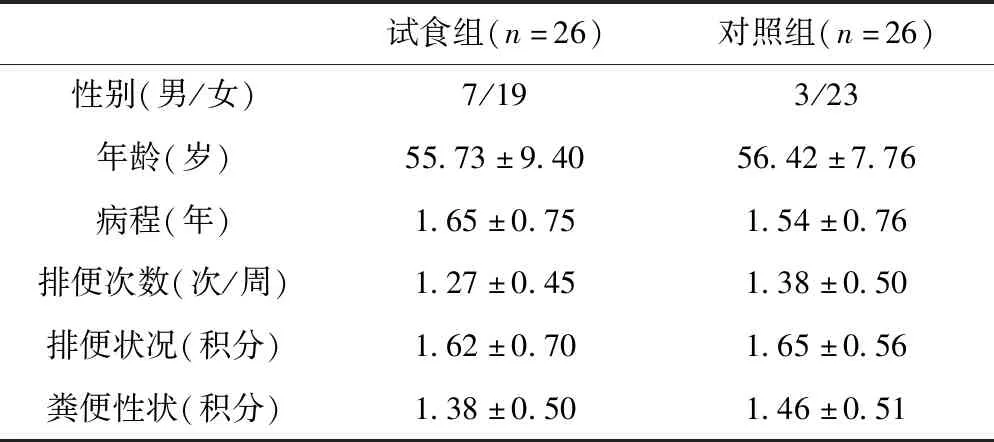
表2 试食前一般情况比较Tab.2 Comparison of general condition before test
从表2、表3中可见,试食组和对照组试食前性别、年龄、病程及血压、心率均无显著差异(P>0.05),说明两组具有可比性。
表3 试食前后心率和血压变化比较Tab.3 Comparison of heart rate and blood pressure changes before and after
2.2 对便秘人群功效指标的影响
试食前后便秘程度自身比较见表4。

表4 试食前后试食组与对照组便秘程度自身比较Tab.4 Self comparison of constipation degree before and after test in test group and control
由表4可以看出试食前后的自身比较。试食组的排便次数增加(P<0.01)、排便状况、粪便性状均有改善(P<0.05)。对照组的排便次数、排便状况、粪便性状均无显著性差异(P>0.05)。
试食后两组便秘程度的组间比较见表5。
表5 试食后两组便秘程度组间比较Tab.5 Comparison of constipation degree before and after test between two
表5结果表明,试食后与对照组比较,试食组的排便次数增加(P<0.05)、排便状况、粪便性状均有改善(P<0.05)。
试食前后两组纤维素类食物摄入量自身比较见表6。
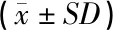
表6 试食前后两组纤维素类食物摄入情况Tab.6 Situation of cellulose food intake before and after test between two
由表6可见,试食组和对照组纤维素类食品摄入量试食前后自身比较及两组间比较均无显著差异(P>0.05)。
2.3 对便秘人群安全指标的影响
试食前后两组血、尿、便的自身比较见表7。
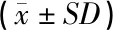
表7 试食前后两组血尿常规自身比较Tab.7 Self comparison of routine urine test of two groups before and after
从表7可见,两组受试者的红细胞、白细胞、血小板、血红蛋白均处于正常范围,且两组试食前后自身比较差异无显著性(P>0.05);两组受试者尿、便常规(除大便性状)试食前后均基本正常。
试食前后血液生化指标的自身比较见表8。
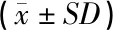
表8 试食前后血液生化指标自身比较Tab.8 Self comparison of blood biochemical index before and after
表8表明,两组受试者的血清总蛋白、白蛋白、谷丙转氨酶、谷草转氨酶、甘油三酯、总胆固醇、肌酐、尿素、血糖均基本处于正常范围内;且两组试食前后自身比较差异均无显著性(P>0.05)。
2.4 受试者脱失率
纳入受试者59例,试食组30例,对照组29例,试食组有4例、对照组有3例未按规定参加体格检测,符合受试者排除标准。有效受试者试食组26例、对照组26例。试食组、对照组受试者脱失率分别为13.3%、10.3%。
2.5 不良反应观察
未见过敏及其他不良反应,不良反应情况见表9。

表9 试食后两组在试食期间过敏及其他不良反应情况Tab.9 Irritability and other adverse reaction situation of two groups during test
3 结果
(1)采用自身与组间两种对照设计,52例符合要求的有效受试者,其中试食组26人,对照组26人。对照组采用安慰剂对照,试食组按要求服用卫矛醇,每日1次,每次1袋,口服。服用14 d后,试食组试食前后自身比较排便次数明显增加(P<0.01)、排便状况和粪便性状两项指标积分明显下降(P<0.05);试食后试食组与对照组比较,排便次数明显增加(P<0.05)、排便状况和粪便性状两项指标积分明显改善(P<0.05)。根据《保健食品功能学评价程序与检验方法规范》(2003年版)中通便功能人体试食试验的判定标准,结果显示,卫矛醇具有通便功能。
(2)试食前后三天膳食调查结果显示,试食组和对照组纤维素类食品摄入量试食前后自身比较和组间比较差异均无显著性(P>0.05);试食前后纤维素类食物的比例均无改变,说明饮食因素对试验结果无影响。
(3)试食者胸透、腹部B超、心电图均基本在正常范围。试食卫矛醇前后,除试食后大便性状改善外,血、尿、大便及肝肾功能各项检测指标均基本在正常范围,说明本品对试食者身体健康无不良影响。
(4)在试食卫矛醇过程中未观察到过敏及不良反应(恶心、胀气、腹泻、腹痛等)。
4 讨论
便秘的产生还有疾病因素:直肠与肛门病变,局部病变导致排便无力,结肠完全或不完全性梗阻,肠易激综合征,腹腔或盆腔内肿瘤压迫,全身性疾病使肠肌松弛、排便无力等。也有相关疾病伴随发生,如痔疮、肛裂、肛周脓肿、直肠炎、膈肌麻痹等。应在门诊检查确定病因后加以治疗。
人体试食试验表明,经植物萃取得到的卫矛醇具有通便功能,可在调节肠道微生物方面发挥大的作用。经口服卫矛醇进入胃腔后,在胃酸环境下(pH值约在3和4)得到充分溶解。人体胃肠道内没有水解卫矛醇的酶系统,因此它不被消化吸收而直接在胃的渗透压作用下进入大肠内,优先为乳酸杆菌所利用[3]。卫矛醇除改善人体内微环境外,还起到调节胃肠、抑制肠内腐败物质、改变大便性状、防止便秘的作用。结合卫矛醇对人体肠道菌群改变的结果[4]认为卫矛醇具有潜在的益生元特性。由于它对人体无毒副作用,卫矛醇是一项非常优秀的益生元物质。
美国达尼斯科公司(DBA杜邦营养与健康)生产的一种儿童奶粉添加成分—2’-岩藻乳糖[5]中,含有其他碳水化合物的限量为6%,包括3-岩藻乳糖、2-岩藻糖基-d-乳糖、岩藻糖基半乳糖、葡萄糖、半乳糖、岩藻糖、山梨醇、卫矛醇、甘露醇和三己糖,这是婴幼儿食品中首次明确标明含有卫矛醇成分,但含量比较小。
由于本研究的试验剂量确定为人体每日摄入2 g卫矛醇,与卫矛醇动物毒理试验结果[6]对比是非常小的,这主要是从卫矛醇人体安全性考虑。对卫矛醇高摄入量下人体肠道微生物的影响以及对人体消化系统及免疫系统作用机理[7]等方面都有待进一步研究。

