熔盐辅助法制备碳化钛材料的研究进展
王 珍,凌永一,王子昊,张 婧,贾全利,刘新红
郑州大学材料科学与工程学院,郑州 450052
碳化钛化学组成为TiC0.47-0.99,其键型是由离子键、共价键和金属键混合组成,晶体结构为NaCl型[1].碳化钛具有许多优异的性能,例如:具有较高的熔点(3067 ℃)、较高的导热率(16.7 W·m−1·K−1)、较高的杨氏模量(410~450 GPa)和维氏硬度(28~35 GPa)等,因此,其在机械、化工、电子、冶金等工业的关键技术领域得到了广泛应用[2−6].TiC粉体可用于制造刀具、砂轮,还可与氧化铝(Al2O3)、氮化硅(Si3N4)和碳化硅(SiC)等其他陶瓷结合而制造耐高温或耐腐蚀性的结构部件[7−8].TiC也可用作涂层材料,将TiC结合在基体表面用来改变基体表面的性质以提高其某方面的性能,如:聚变堆中的抗氚涂层、挖掘机截齿涂层以及电极材料的涂层等.TiC粉体的颗粒大小、粒径分布及其显微结构、涂层与基体结合的程度、涂层的厚度等都与其应用效果直接相关.不同形态的TiC在应用时对其要求不同,在制作刀具、砂轮或其他复合材料时,理想的TiC粉体应无团聚且粒径分布均匀、颗粒尺寸小;而TiC涂层则要求其具有优良的抗氧化性、耐磨性和高硬度等.近年来,TiC的制备方法不断改进和发展,至今除传统碳热还原法外,还有熔盐辅助法(MSS)、等离子体法、冲击波法等十几种方法[9−10],在这些制备方法中,熔盐辅助法因具有反应温度低、反应时间短、绿色高效等优点而常被采用.本文对几种熔盐辅助法合成TiC粉体、纤维、涂层等的研究现状进行了综述,期望为碳化钛及其复合材料的制备提供技术参考.
1 熔盐辅助法制备 TiC 概述
Arendt[11]于1973年首次采用熔盐辅助法在PbO–Al2O3–SiO2等液相体系中制备出BaFe12O19和SrFe12O19粉体后,该合成法在制备无机材料中得到了迅速的发展.熔盐辅助法是指在反应过程中用一种或几种低熔点的金属盐类作为反应介质,温度控制在金属盐熔点以上,反应物置于熔融的盐中,经过一系列的化学和物理转变来合成材料的一种方法,反应结束待到熔盐冷却后,再用合适的溶剂将盐类溶解,过滤、洗涤后便得到合成产物[12−13].熔盐具有高温下的稳定性、低黏度、较高的离子迁移率等性质,当温度升高到熔盐的熔点以上,反应物的结构在熔盐介质中重新排列并迅速扩散,产物颗粒通过形核过程和生长过程而逐渐形成[14].因此,采用熔盐辅助合成法有以下优点:
(1)对原料的分散、扩散有着明显影响,对产物颗粒的形核和生长过程以及产物的形貌特征、产物的组成和粒径等方面都起着十分重要的作用[15].
(2)与固态合成相比,熔盐辅助合成法更容易达到热力学稳定状态,合成时间短、制备温度更低[16].
(3)在溶液中进行反应时,生成物之间较难聚集,因此可减少粉体团聚现象,产品成分较均匀[17].
(4)熔盐辅助合成法不仅可制备出具有特定形貌和结构的粉体颗粒,还可合成许多难熔的、合成温度较高的化合物,以满足无机材料制备过程中的各种要求[18−19].
因此,熔盐种类的选择、熔盐的用量、原料与盐的比例等都是重要的工艺参数,均需要合理地控制.熔盐辅助合成法虽然引入了熔盐杂质,但在反应结束后对熔盐进行反复清洗,可有效地去除杂质,得到高纯度的产物.
2 熔盐辅助法制备 TiC
在合成TiC的过程中常用的熔盐为碱金属氯化物,如:NaCl、LiCl、KCl,或由两三种碱金属氯化物组成的熔盐体系.在采用熔盐法制备TiC的过程中常常结合其他的制备方法一起使用,如微波法、金属热还原法等,目前熔盐辅助法制备TiC大致可以分为五类:熔盐辅助碳热还原法、熔盐辅助电化学法、熔盐辅助金属热还原法、熔盐辅助直接碳化法和熔盐辅助微波合成法.
2.1 熔盐辅助碳热还原法制备 TiC
熔盐辅助碳热还原法是制备TiC最常见的一种方法.在传统碳热还原法制备中,需要较高的温度(> 1550 ℃)和较长的时间.与传统碳热还原法相比,熔盐辅助碳热还原法在球磨原料时加入碱金属盐作为辅助剂,低熔点的熔盐可将合成温度降至800~950 ℃,合成TiC温度显著降低.在合成过程中,首先将原料和熔盐在研钵中或高能球磨机中混合均匀,然后放入炉内烧成,合成示意图如图1[20]所示.
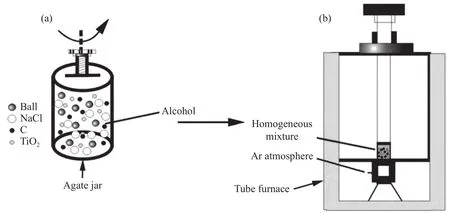
图1 熔盐辅助碳热还原法制备 TiC 的实验过程示意图.(a)球磨罐;(b)管式炉[20]Fig.1 Schematic of the experimental process of preparing TiC by molten salt-assisted synthesis: (a) agate jar; (b) tube furnace[20]
采用熔盐辅助法制备TiC粉体时,常用的钛源有TiO2、K2TiF6和Ti粉等,原料的粒度、形貌、合成时间和温度等对所制备的TiC粉体的粒径及显微结构有重要影响,原料种类也会致使制备TiC的机理不尽相同.Cao等[21]以金刚石颗粒(粒径为 3~10 nm)为碳源,以 K2TiF6为钛源,以NaCl和KCl为混合熔盐,采用熔盐辅助碳热还原法于 900 ℃ 下 1 h合成了粒径约为 10 nm的球状TiC粉体.其反应机理为:钛源溶解并沉积在金刚石纳米粒子上,金刚石作为反应模板,与表面沉积的钛层反应生成TiC.钛与碳的反应受扩散控制,因此反应温度和时间对合成TiC影响很大:短时间或低温可制备出TiC/金刚石壳/核结构,而较长时间和较高温度可制备出完整的TiC颗粒.Yang等[22]以Ti粉(粒径为325目)为钛源,以乙炔黑(粒径为30~45 nm)和多壁碳纳米管(直径为20~40 nm)以及石墨烯(平均层数为 5~6 层,平均层厚< 3 nm,片层尺寸为 5~15 μm)为碳源,在 800~900 ℃ 的NaCl–KCl混合熔盐体系中保温2 h制备了粒径约为50 nm的TiC粉体.生成的TiC单个粒子由于范德华力和静电力导致轻微团聚,有些TiC粒子团聚成纳米棒和纳米片,如图2所示.温度升高到750 ℃便开始有TiC生成,随着温度升高,Ti6O、TiO2、TiOCl2等相逐渐消失,当温度升到850 ℃时,产物中只有TiC相;图3为制备过程示意图.当Ti粉和乙炔黑在熔盐中时,乙炔黑作为模板漂浮在熔盐顶部,少量 Ti粉溶解形成 Ti (II)和 Ti (III),Ti (II)迁移到乙炔黑表面,并与乙炔黑表面C原子反应生成TiC,反应式如下:

图2 TiC 粉体显微结构.(a)棒状纳米结构 TiC;(b)片状纳米结构TiC[22] Fig.2 Microstructure of TiC powders: (a) TiC nanorods; (b) TiC nanorod sheets[22]

图3 Ti粉与乙炔黑反应在 NaCl–KCl熔盐中生成 TiC 的示意图[22]Fig.3 Schematic of TiC formation in NaCl–KCl molten salt using Ti powder and acetylene black[22]

熔盐辅助碳热还原法制备TiC粉体除所用原料易得、廉价,工艺简单等优点外,还可以制备出不同形貌的TiC颗粒,如:八面体状、柱状和立方状等.Song 等[20]将锐钛矿型 TiO2(粒径< 7.4 μm)、炭黑(粒径< 8.4 μm)和 NaCl熔盐球磨均匀后放入管式炉中,在1500 ℃保温3 h制备了具有化学计量比的粒径约为10 μm的TiC粉体,TiC结晶良好,有八面体和圆柱形两种形态,其显微结构如图4所示.原料之间的比例和合成温度对制备TiC粉体均有影响:在较低的1300 ℃温度下产物为TixOy和低化学计量比的TiCx;温度升高至1500 ℃后产物中只有TiC,因此较高的温度和较高的C/TiO2摩尔比(>3∶1)有利于纯TiC粉体的制备.

图4 TiC 粉体显微结构.(a)八面体 TiC;(b)柱状 TiC[20]Fig.4 Microstructure of TiC powders: (a) octahedral TiC; (b) columnar TiC[20]
熔盐辅助法相比于其它方法所制备出的TiC粉体在结构上有明显差异,为探究熔盐辅助合成法与高温自蔓延合成法(SHS)对合成TiC粉体的影响,梁宝岩等[23]以纯度> 95.0%的碳纳米管为碳源,纯度>99.0%的钛粉(平均粒度为53 μm)为钛源,分别采用熔盐辅助合成法和SHS法合成了两种形态尺寸的TiC粉体,粉体结构如图5所示.采用SHS法在1000 ℃下合成的TiC颗粒粒径较大,外层组织和内层组织有差异,表层TiC粒度为1~2 μm,内部粒度约为0.6 μm,产物的孔洞较多.在等质量的NaCl和KCl熔盐辅助制备时,在1100 ℃下反应1 h得到了较细的TiC颗粒,颗粒间团聚现象明显,内外部组织不一致,表面与内部颗粒粒度分别为0.40、0.15 μm.

图5 TiC 粉体的显微结构.(a)SHS 方法合成;(b)熔盐辅助法合成[23]Fig.5 Microstructure of TiC powders by different methods: (a) SHS method; (b) molten salt-assisted method[23]
TiC具有较高的耐磨性和较高的化学稳定性等,因此TiC涂层常用作材料的保护层.吕品等[24]以NaCl和KCl为混合熔盐体系,用炭复合材料、TiO2、Ti粉为原料,在850~950 ℃下制备了TiC涂层.随温度升高,在炭复合材料表面生成的TiC涂层厚度增加,在950 ℃下烧成可得到结构较好的TiC纤维和颗粒,TiC颗粒有效地填充在纤维之间的空隙,形成了致密的涂层结构.此外,作者还研究了TiC涂层的抗氧化性,涂层氧化后可生成TiO2,从而封填部分裂纹和孔隙,使得涂层具有一定的防氧化能力.不同温度下所制备的TiC涂层结构有所差异,在950 ℃下制备的涂层抗氧化性能最好,涂层试样氧化12 h后失重率仅为5.09%.
除TiC粉体和TiC涂层以外,熔盐辅助合成法亦可以合成TiC纤维.Li等[25]采用熔盐辅助碳热还原法,以纳米热解炭黑和多壁碳纳米管(MWCNTs)为碳源,TiO2/Ti混合粉为钛源,用 LiCl/KCl为混合熔盐,以碳源与钛源2∶1的摩尔比,在坩埚中950 ℃下制备了化学计量比约为0.95的单晶TiC纳米纤维,其直径小于100 nm、长度在几十微米范围,如图6所示.对合成纤维进行分析后发现纤维表面有TiO2残留,用稀HF对产物进行酸洗得到了纯净的TiC纳米纤维.作者对比了灯炭黑(固体球形颗粒)、热炭黑(固体球形颗粒)、热解炭黑(空心球状)、MWCNTs(纤维状)等碳源种类及形貌差异对TiC纳米纤维形成的影响:与热解炭黑和MWCNTs相比,更大、更无序的灯炭黑和热炭黑材料产生的TiC纤维较少,因此具有适当结晶度和尺寸较小的碳源可能是单晶TiC纳米纤维非均相生长的关键因素.研究Ti/TiO2摩尔比从1∶1增至4∶1时对产物的影响,发现Ti/TiO2等摩尔比时TiC纳米纤维的产量最高,并且只有TiO2或TiO为钛源时没有TiC纤维生成.

图6 熔盐法制备的碳化钛纳米纤维 SEM 照片.(a)HF 处理之前;(b)HF 处理之后[25]Fig.6 SEM images of titanium carbide nanofibers prepared using molten salt-assisted method: (a) before HF acid treatment; (b) after HF acid treatment[25]
TiC基复合粉体制备也常用熔盐辅助法,借助熔盐环境,多种原料粉体可以更充分地分散与混合.Yang等[26]以粒度为70 μm、纯度为99.9%的镍、钛、碳粉体为原料,以纯度较高的NaCl和KCl为熔盐介质,首先将Ni–Ti–C混合粉体在常温下放入行星球磨机中进行球磨,之后将混合好的粉体冷压成坯体后放入坩埚中,在800 ℃下制备了以球状TiC颗粒为主要相的TiC/NiTi复合粉体.制备的复合粉体所用的烧成时间很短(30 min)、成本较低,实验过程简便易控、容易操作,且形成的TiC颗粒形状较为均匀、形状边缘光滑.但形成的TiC是一种非化学计量化合物,C/Ti的原子比约为0.48~1.
熔盐辅助碳热还原法制备TiC所用的原料易得、廉价,工艺流程简单,操作难度较低;可以制备出多种形态结构的TiC,如:TiC粉体、涂层及纤维,八面体状、柱状、立方状TiC等.虽然TiC的制备受实验过程中诸多因素的影响,如:原料之间的比例、原料的种类、原料与盐之间的比例以及温度和时间等工艺参数,但只要合理控制好这些因素可以实现快速获得结晶良好且符合化学计量比的TiC.
2.2 熔盐辅助电化学法制备 TiC
熔盐辅助电化学法(FFC)最早是由剑桥大学的Fray、Farthing和Chen三位学者提出[27],FFC法电解池装置如图7所示.FFC法最早是用来制备难熔金属以及稀有金属及其合金,如钛(Ti)、铬(Cr)、铪(Hf)、铌(Nb)等[28−32].所谓熔盐辅助电化学法,就是利用电能加热并转换为化学能,将某些金属盐类熔融并作为电解质进行电解,以提取和提纯金属的冶金过程.在采用熔盐辅助电化学法制备TiC时,首先将含钛物质电解为Ti,然后Ti与C反应生成TiC,具体方法是将钛源和碳源混合均匀后制备成反应阴极,将阴极和阳极放入提前预电解制备成的熔盐介质中,通入恒位电压进行电解,电解完成后将阴极产物进行水煮、酸洗、干燥后便得到了TiC.
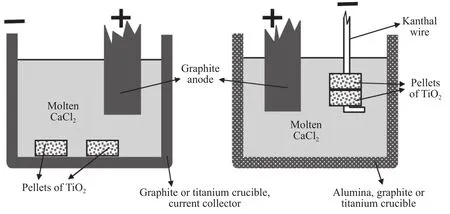
图7 FFC 法电解池示意图[27]Fig.7 Schematic of FFC electrolytic cell[27]
在电解过程中,阴极的制备至关重要,其质量好坏直接关系到TiC粒径尺寸、结构形貌等方面,而制备阴极所用原料、烧成时间以及烧成温度等工艺参数对阴极的质量影响显著.白鑫涛[33]以Na2TiO3为钛源,将Na2TiO3与C放入CaCl2熔盐中来制备TiC粉体.以Na2TiO3为钛源制备的阴极片的合适烧成条件为:压力为40 MPa,900 ℃下保温2 h.当对阴极电解8 h后得到了较为单一的片状TiC.郎晓川等[34]在探究烧成时间、烧成温度对所制备阴极强度的影响时,以TiO2、CaO、石墨粉为阴极材料,制备出了CaTiO3–C复合阴极,阴极的最佳制备条件为1300 ℃下煅烧2 h.以预电解的 CaCl2和 NaCl为混合熔盐,在 750 ℃ 下用 3.2 V电压对制备的复合阴极电解15 h,阴极产物经过水洗、酸洗后得到了纯净的TiC粉体,粉体颗粒呈不规则球状,颗粒粒径约为0.3 μm,粒度分布均匀.该实验过程容易控制,但阴极的制作过程比较复杂、耗时较长;合成产物中还会出现副产物CaCO3,需要进行水洗除去残余的熔盐、水洗加酸洗除去CaCO3后,才能得到纯净的TiC粉体.此外,原料比例、电解时间、温度等都对电解过程有着显著影响.崔富晖[35]首先将炭黑和Na2TiO3混合,在4 MPa下压片并在氩气保护下400 ℃烧成来制备阴极片,然后在 850 ℃ 下通过 3.1 V 恒压电解 5~7 h 制备出粒径为5 μm左右的TiC粉体.NaOH和Na2TiO3的添加可以改变TiO2–C的烧成工艺,随着Na2TiO3添加量的增加,阴极产物转化为TiC的速率增加,完全电解时间也明显缩短.通过添加NaOH和Na2TiO3达到了降低阴极片制备能耗、提高阴极的强度、提高电解速率的效果.
在熔盐辅助电化学法制备TiC的过程中,常用作钛源的物质有TiO2、TiCl4、富钛炉渣和Na2TiO3等,而采用不同原料合成TiC的机理并不相同.熔盐辅助电化学法制备TiC的机理至今仍是研究热点,目前主要存在两种解释:一种解释是阴极的氧化物在电解过程中得到电子后,氧离子被电离进入溶液,进而在阳极以气体的形态逸出,而钛留在阴极与碳结合生成TiC[36]:

另一种解释是熔盐中的碱金属离子(如Ca2+)在阴极得到电子后生成金属单质(如Ca),金属单质进一步还原阴极中的钛氧化物得到金属钛,金属钛进而与碳反应生成TiC:

为探讨熔盐辅助电化学法制备TiC的机理,Zhang 等[37]以 TiO2和 C 为原料,在 900 ℃ 煅烧 6 h制备出TiO2/C复合阴极.在900 ℃下,用CaCl2作为熔盐电解质,对复合阴极以3.0 V恒位电压电解6 h后,对阴极产物进行水洗、酸洗后,成功制备了含氧的TiC粉体,该粉体颗粒尺寸均匀,未出现明显的团聚现象.以TiO2为钛源电解合成TiC的机理为:在电解时TiO2与CaO首先生成了CaTiO3,电解延长至1.5 h时,产物主要由Ti2O、CaTiO3和TiC组成,当电解时间延长至12 h后产物中只有TiC相.整个过程中 Ti4O7、Ti3O5和 Ti2O3等相没有出现,TiO2直接还原为TiO,加快了电化学反应的速度.该产物中没有原料残留,但是产物中氧含量较高.陈孔豪[38]也发现在NaCl–CaCl2熔盐中,电解TiO2/C是以直接的电化学还原为主,并不一定需要Ca2+先还原成单质Ca,再由Ca还原TiO2;但也不能排除在电解过程中这种钙热还原方式的存在.
熔盐辅助电解TiO2和炭黑混合物制备TiC的过程十分复杂,不但涉及TiO2的还原反应,还包括氧离子和钛离子在固相中的扩散,氧离子在熔盐中的迁移和扩散,以及还原出的钛和碳之间的相互扩散等过程.谢江生等[39]在探究熔盐辅助电化学法制备TiC的机理时发现,氧离子在固相中的传质受阴极反应速度控制.首先将TiO2(粒径为0.5 μm)和炭黑球磨后制成阴极,石墨为阳极,将阴、阳两极放入2.4 V电压下预电解2 h的CaCl2熔盐中,在 850 ℃ 下用 3.1 V 电压电解 5 h 合成超细的TiC粉体,其粒径为1~3 μm.经不同时间电解后所得阴极产物的物相不同,电解开始时有中间相CaTiO3出现,电解5 h后得到纯净TiC相,因此推测阴极的反应机理为TiO2首先在电解过程中生成CaTiO3等中间产物,然后被还原成单质钛,随后还原出的钛与碳相互扩散并发生反应生成TiC.制备出的TiC粉体纯度较高且颗粒细小(粒径为1~3 μm).在制备过程中,电解反应速度受阴极的反应速度影响较大,因此阴极的制作十分关键.Yan等[40]在探究合成机理的过程中也发现,氧在CaTiO3中向CaTiO3/C/电解质三相界面的扩散可以成为整个电化学动力学中的速率决定步骤.其用 CaCl2–NaCl混合熔盐在 850 ℃ 下对 TiO2和C(碳钛摩尔比为 1∶1)组成的阴极电解 4 h,阴极产物经处理后得到了化学计量比为Ti0.55C0.45的TiC纳米粉体,TiC较为纯净,颗粒为不规则形状,平均粒径为20 μm左右,但粒径分布不均,且颗粒相互交连出现一定团聚现象,如图8所示.

图8 CaCl2–NaCl混合熔盐中合成的 TiC 粉体的显微结构[40]Fig.8 Microstructure of TiC powders synthesized in CaCl2–NaCl mixed molten salt[40]
熔盐辅助电化学法也可以合成TiC基复合粉体,如:TiC/SiC复合碳化物粉体、TiCxOy粉体等.Chen等[41]以石墨粉、富钛炉渣(TiO2质量分数为74.9%,SiO2质量分数为11.13%)等为原料,以NaCl和CaCl2的混合物为熔盐,通过熔盐辅助电化学法制备出了纯度大于97%且分散性良好的TiC/SiC复合粉体.合成产物的纯度较高,熔盐的加入也降低了电解的温度;但在电解过程中形成了CO、CO2等有害气体,产品中的杂质元素也较多,且由于富钛炉渣中元素种类复杂,致使电解过程十分复杂.张臻等[42]以高钛渣和石墨粉为原料,利用石墨棒在CaO–CaCl2–NaCl熔盐中电解制备出了粒径分布均匀、平均值约为50 nm的球形TiC/SiC纳米级复合粉体,粉体粒径较小,但制备的产品含有少量的金属杂质,且生成的一些中间产物较难还原.在电解过程中,电解时间、槽电压等参数的控制也十分重要.张琳琳等[43]首先将TiO2和碳粉制备成电解池阴极材料,以石墨为阳极材料,借助熔盐辅助电化学的方法在电解质CaCl2熔盐中,于 900 ℃ 下保温 6 h 制备出了 TiCxOy粉体.改变反应物之间的比例可以改变产物中的物相,碳含量增加后TiCxOy相的含量也随之增加,当TiO2∶C摩尔比为2∶1时,可以得到单一的TiCxOy的产物.其制备步骤相对同类研究较为简单,省去了熔盐的预电解步骤,但是合成的产物出现明显的团聚现象,如图9所示.

图9 TiCxOy 粉体的显微结构[43]Fig.9 Microstructure of TiCxOy powders[43]
熔盐电化学法制备出的TiC粉体一般细小(微米级别),产物纯净,较少团聚,但是制备工艺复杂,需要经过阴极制备、熔盐预电解等步骤,整个实验过程耗时较长.实验结束后阴极孔内一般会有熔盐残留,必须经过一定的水洗、酸洗处理后才可得到纯净的TiC[44].在这种方法制备TiC的过程中,不仅原料比例、温度、时间等因素对制备TiC有影响,阴极的制备过程、阴极质量的好坏、电解电压、电解时间等诸多因素也对TiC的形成有影响.相较于熔盐辅助碳热还原法,熔盐辅助电化学法制备TiC的过程和机理更复杂,且影响因素和不可控因素更多.
2.3 熔盐辅助金属热还原法制备 TiC
与碳相比,活性金属具有更强的还原性,如Ca、Mg等强还原性金属的加入,易把钛源(钛氧化物、钛氯化物等)还原成金属钛,钛进而与碳反应形成TiC粉体.熔盐的加入可以使金属粉末在较低的温度下熔融,从而可以加快金属与含钛物质之间的还原反应,使得整个反应时间缩短.
Lee[45]采用金属 Mg还原 TiCl4和 CCl4,制备了超细海绵块状的TiC粉体其结构如图10所示.在1173~1373 K下液态的Mg与气态的TiCl4和CCl4分别反应释放出Ti和C原子,在液态Mg表面,两种原子反应生成细小的TiC颗粒,反应如式(6)所示.CCl4(挥发度远高于 TiCl4)的用量对制备的TiC计量比有一定影响,使用化学当量110%的CCl4配制溶液时可以制备出质量较好的TiC0.95,但随着其使用量的增加,残留的游离碳量有所增加.TiC的形成与加料的速度和气相的压力也有关,在较高的进料速率下,单位体积内的TiC非化学计量核数增多,当TiCl4和CCl4与液态镁接触的气压较高时,原子核的平均自由程变小,易于原子核的凝聚和生长.使用化学当量为105%的CCl4溶液,在进料速率为 0.3334 g·s−1、反应温度为 1273 K的条件下制备的TiC质量最好,产物为TiC0.95,游离碳的质量分数约为1.0%.这种方法合成的TiC粉体中含有游离碳,且还原后需要用真空除去MgCl2的残余相和过量的Mg,但制备过程中不会形成 TiCl3、C6Cl6、TiCl2等中间相.


图10 海绵块状的 TiC 结构[24]Fig.10 TiC structure of sponge block[24]
丁娟[46]以二氧化钛为钛源、炭黑为碳源、金属Mg粉为还原剂,将质量比为3∶1的熔盐与反应物混合均匀后放入真空干燥箱中,在110 ℃下干燥 24 h,然后加 Mg,在 750~1100 ℃ 流动氩气保护的管式炉中,反应1~5 h制备出了粒径为0.39 μm、比表面积为 89.76 m2·g−1的 TiC 粉体.产物中含有未反应的镁,用HCl溶液浸泡产物,然后用去离子水反复清洗直至无Cl−1为止,最后经干燥后获得最终产物.金属钛/碳摩尔比对合成TiC化学计量有一定影响:熔盐与反应物的质量比为1∶3、Ti∶C摩尔比为1∶0.8较为适合,合成的TiC结晶性能良好、颗粒细小、尺寸均匀.
这种方法制备的TiC粉体晶体尺寸较小,通常为纳米级别,化学计量比高(> 0.96)、纯度高,但产物中通常含有残留碳、金属或金属化合物,且制备的TiC易形成硬团聚,需破碎后才可得到TiC粉体.在实验过程中需要合理调控金属还原剂与原料之间的比例,若金属还原剂用量过少则不能使原料反应完全,从而有游离碳残留在样品中;而金属还原剂过量又会为后续产品处理、清洗工作带来负担,并影响产物的纯度.
2.4 熔盐辅助直接碳化法制备 TiC
熔盐辅助直接碳化法常用来制备TiC涂层.传统直接碳化法制备TiC涂层时常以金属Ti为钛源,以C为碳源,Ti与C直接反应生成TiC,但这种方法受到原料尺寸的限制,反应时间相对较长(5~20 h),且制备出的反应物团聚严重.而利用熔盐介质在高温下的媒介作用,加快钛离子的传质速率,使其较快、较均匀地扩散到石墨的表面并与石墨发生原位反应生成TiC层.石墨在空气中容易氧化、对水的润湿性较差[47].而在石墨表面包覆TiC涂层,不仅可以提高石墨表面的润湿性,还可以提高材料的抗氧化性,改善界面性能[48−49],因此在一定程度上扩大了石墨材料的应用范围.如:含碳浇注料中由于石墨对水的润温性差,石墨部分聚集或漂浮在分散介质的表面,不易形成分散均匀的体系,用涂覆TiC涂层的办法改善石墨的润湿性,可以提高材料的整体性能.在石墨表面合成TiC涂层时除了非均相成核法[50]、溶胶–凝胶法[51]、化学气相沉积法[52−53]外,熔盐辅助法也是种常用方法.
自2008年Li等[54]采用熔盐法制备出TiC涂层后,用这种方法制备涂层得到迅速发展.Li等[55]在流动的氩气中,以金属钛粉为钛源,在碳纤维上成功镀覆了一层TiC涂层,其将钛源和熔盐混合物包覆好碳纤维后放入坩埚中,在900~950 ℃下反应1~5 h后得到的TiC涂层结构完好,表面光滑,平均厚度800 nm.反应时间和Ti/C摩尔比对碳纤维表面TiC涂层厚度有一定的影响,TiC涂层的厚度不仅随反应时间的延长而增加,而且随钛碳摩尔比的增加而增加.一定厚度的涂层可以使涂层碳纤维的硬度提高,而涂层过厚会致使涂层与碳纤维界面处易出现裂纹.丁军等[56]在混合熔盐 NaCl–NaF 中,用金属钛粉(粒径≤ 10 μm)和天然鳞片石墨(粒径为200~300 μm)为原料,探究温度、原料比例对生成TiC的影响:当钛和石墨的摩尔比为 1∶3、烧成温度 1400 ℃、保温 3 h时,TiC的生成量达到最大值,TiC平均晶粒尺寸为1~3 μm,其显微结构如图11所示.

图11 石墨表面的 TiC 涂层显微结构图[56]Fig.11 Microstructure of TiC on graphite surface[56]
除Ti/C摩尔比、保温时间、烧成温度等工艺参数外,熔盐的种类对TiC涂层的制备也有一定影响.董志军等[57]在不同的熔盐介质(NaCl–KCl–KF、KCl–LiCl–KF、KCl–KF)中用金属 Ti粉和聚丙烯腈碳纤维(PAN)作为反应原料,在氩气保护下900 ℃反应3 h制备了包覆碳纤维的TiC涂层,涂层厚度为纳米级别.在KCl–KF中形成的TiC的衍射峰强度最低,而在KCl–LiCl–KF熔盐体系中合成的TiC涂层的表面最光滑,且结构形貌最好,推测可能是因为不同的熔盐提供的阴离子的种类不同而引起的TiC晶粒的生长方向不同.此外,反应物Ti粉与PAN质量比< 49时,随熔盐量的增加涂层厚度逐渐增大.研究涂层生长的动力学发现,涂层厚度的平方与反应时间有较好的线性相关性,涂层的生长是由扩散控制的.
在熔盐辅助直接碳化法制备TiC涂层过程中,当在反应温度合适的条件下,反应时间的控制十分重要,反应时间过短则TiC涂层与基体的结合程度低,涂层质量不能满足要求,不仅不能提高机体的性能反而使基体表面成分不均匀;而反应时间过长会导致涂层厚度过厚,虽能提高基体的硬度但是涂层与基体的结合界面处易出现裂纹.
2.5 熔盐辅助微波法制备 TiC
微波是一种 300 MHz~300 GHz 的电磁波,若以熔盐辅助微波法则可以借助微波快速、均匀加热和熔盐辅助低温合成的优势更快、更好地合成TiC.其基本原理就是利用材料在高频电场中的介质损耗,将微波能转变成热能而进行加热.这种方法最大的优势在于合成时间极短,通常在2 h之内便可以得到TiC,合成的TiC晶体结构良好,合成过程绿色环保、步骤简单,可实现整体均匀加热.
梁宝岩等[58]采用熔盐法结合微波辐照工艺,将平均粒度为53 μm的钛粉和平均直径为10 μm的碳纤维(Ti∶C摩尔比为1∶4)与NaCl和KCl熔盐混合均匀后,置于900 ℃的微波炉中保温2 h后制备出了1 μm厚包覆碳纤维的TiC涂层,形成的TiC晶粒为约0.2 μm.这种采用微波辐照结合熔盐法合成TiC的工艺相比于传统碳热还原法合成TiC明显降低了合成温度(900 ℃)、缩短了合成时间(2 h),更为绿色环保,合成的 TiC 晶粒细小、结构良好、颗粒分布均匀,但是其所用原料为微米级别,成本较高.
3 结论
现代MSS法规模大、工艺成熟,利用该方法合成无机材料因具有合成温度低、反应时间短,节能高效等优点,近年来常被用来制备TiC材料.至今,相关研究主要通过在熔盐体系中改变反应物之间的比例,借助热还原或电化学还原原理,合理调节反应温度、时间、电解电压等参数,成功制备出多种TiC材料.这些研究成果,对改变当前传统方法制备TiC材料单一和技术附加值低的缺点,推进现代TiC制备工业进一步发展具有重要的技术和经济意义.TiC材料由于其独特的性能将在生物医学、电子、冶金等工业具有较好应用前景,为此,通过对其研究现状的归纳总结并分析,提出TiC今后发展的方向和重点:
(1)用熔盐辅助法制备TiC材料时需进一步优化原料间的比例,控制合成温度、合成时间,优化球磨和预电解等工艺参数,才可更好地制备出优质且符合工业应用需要的TiC材料.
(2)熔盐辅助法在制备材料过程中存在一个共性问题,即产物中会有熔盐残留,而盐的除去过程耗时耗力,需要经过多次水洗或酸洗,特别是在熔盐辅助碳热还原法制备TiC时,经过多次清洗后,熔盐也较难除净,致使其组分难以精准控制.因此,今后的研究重点还应当放在合理控制反应原料与熔盐之间的比例、高效及彻底去除残余熔盐的新工艺等方面的研究.
(3)熔盐辅助电化学法制备TiC技术的发展,尤其是规模化应用,仍然受到若干问题的困扰和制约.其中,针对不同原料特点通过选择合理的熔盐组成以及电解参数,保证电解槽稳定连续化运行,是实现TiC组成精准调控和成分均匀的关键问题.
(4)合成的TiC粉体存在纯度难以控制,粉体易团聚、形貌不易调控,合成的TiC涂层均匀性、厚度和结合强度有待提高等问题.研究新的合成工艺来制备形貌和粒径可控、成分均匀、不团聚的高质量TiC应被重点关注.

