基于高通量测序重茬草莓土壤细菌和真菌多样性分析
肖 蓉,张春芬,邓 舒
(山西农业大学果树研究所,山西 太原 030031)
生产中大棚草莓种植每年都要换新苗,因此重茬在所难免。连作障害是制约草莓发展的最大因素,据调查,连作4年草莓能减产40%以上[1]。目前,大家公认的连作障害的形成机理主要包括连作土壤中病原微生物积累[2]、土壤营养元素失衡[3]、化感作用[4-6]3个方面。而土壤微生态失衡是研究者所公认的连作障害发生的根本。其中微生物因素在整个连作障碍发生发展过程中一直扮演着关键角色。
在土壤这个黑匣子中到底有多少微生物,以及他们之间的结构信息、群体相互作用、与植物重茬障碍之间的关系等等吸引着人们持续而深入的研究。由于目前土壤中可培养的微生物仅占土壤微生物总数的1%左右,因此依赖于平板培养技术来研究土壤微生物生态显然是不够的[7]。近些年来,随着现代生物技术和基因组学的蓬勃发展,以土壤中全部微生物基因组DNA序列为依据的微生物分子生态学研究方法正日益成为大家普遍接受的方法[8]。
本研究以同一个农业园区新茬草莓大棚和连作3年的重茬草莓大棚土壤为研究对象,直接提取草莓根际土壤总DNA,通过Illumina Miseq测序平台对新茬土壤及重茬土壤细菌和真菌结构及功能多样性进行比较分析,旨在找到重茬土壤中的优势细菌和真菌类群,从微生物生态学角度研究草莓重茬障害发作时的生物学病因,为草莓重茬障碍防治提供理论依据。
1 材料与方法
1.1 供试土样
土壤样品采自山西省太原市阳曲县同一个农业园区新茬草莓大棚和连作3年的重茬草莓大棚,于6月草莓刚收获结束后采样。每个大棚内按“S”形于大棚中间随机挑选草莓植株4株,整株挖出置于冰盒中用无菌袋带回实验室,抖掉根部多余的土后用无菌毛刷刷取根际土,4个土样混合成1个样置于无菌离心管中,新茬土壤样品命名为XJS1,重茬土壤样品命名为CJS1。各类型选取4座大棚为采样地,共获得XJS1和CJS1样本各4个,视为4次重复。
1.2 土壤微生物总DNA提取及测序
土壤微生物总DNA提取方法参考本课题组前期方法[9]。用0.8%琼脂糖凝胶电泳检测DNA的完整性后用Nanodrop 2000分光光度计测定其浓度,DNA合格样品送生工生物工程(上海)股份有限公司完成后续多样性测序工作。细菌多样性测序选取V3-V4区作为靶向扩增区域,真菌多样性测序选取ITS1-ITS2区作为靶向扩增区域。
1.3 数据处理与分析
采用Excel软件对各样本丰富度进行分析。
2 结果与分析
2.1 细菌多样性分析
2.1.1 多样性指标
原始测序数据通过质控后,新茬大棚土壤(XJS1)中共获得33 198条序列,分归于24 968个OTUs;3年重茬大棚土壤(CJS1)中共获得29 399条序列,分归于23 307个OTUs。表1展示了两种大棚土壤的细菌多样性,可见,新茬大棚土壤的Shannon指数为8.092 6,Simpson指数为0.001 6,Chao-1指数为24 863;重茬大棚土壤的这3个多样性指数分别为7.583 1、0.008 7和23 415。Shannon指数常用来综合体现物种丰富度和均匀度;Simpson指数被用来评估环境中微生物多样性,其数值越大代表样本群落多样性越低;Chao-1指数在生态学中也是估计物种种数的常用指标。根据OTUs数目及多样性指标可以看出,重茬3年后土壤中细菌物种多样性及丰富度降低。

表1 土壤中细菌的多样性指数
2.1.2 门水平上丰富度差异分析
经过软件RDP classifier处理后,对所有序列进行细菌群落分类。新茬土壤中共涉及到29个门,重茬土壤中共涉及到25个门。图1和图2是两种土壤类型中的优势细菌在门水平的丰度占比分布图。可知,未分类的细菌群(Unclassified),在两种生境中均占比很大,分别占17.04%和24.48%,说明土壤中还有许多未可培养的细菌。除了这类细菌外,变形菌门(Proteobacteria)在两种生境中均是丰度第一的优势细菌,在新茬土壤中与重茬土壤中丰度分别占51.39%和50.44%;其次是拟杆菌门(Bacteroidetes),分别占17.09%和13.21%;另外,疣微菌门(Verrucomicrobia)、厚壁菌门(Firmicutes)、浮霉菌门(Planctomycetes)和疣微菌门(Verrucomicrobia)在两种生境中的丰度值均高于1%。新茬土壤中丰度值高于1%的还有酸杆菌门(Acidobacteria,2.23%)和绿弯菌门(Chloroflexi,1.21%)。其余各类群所占比例较少。
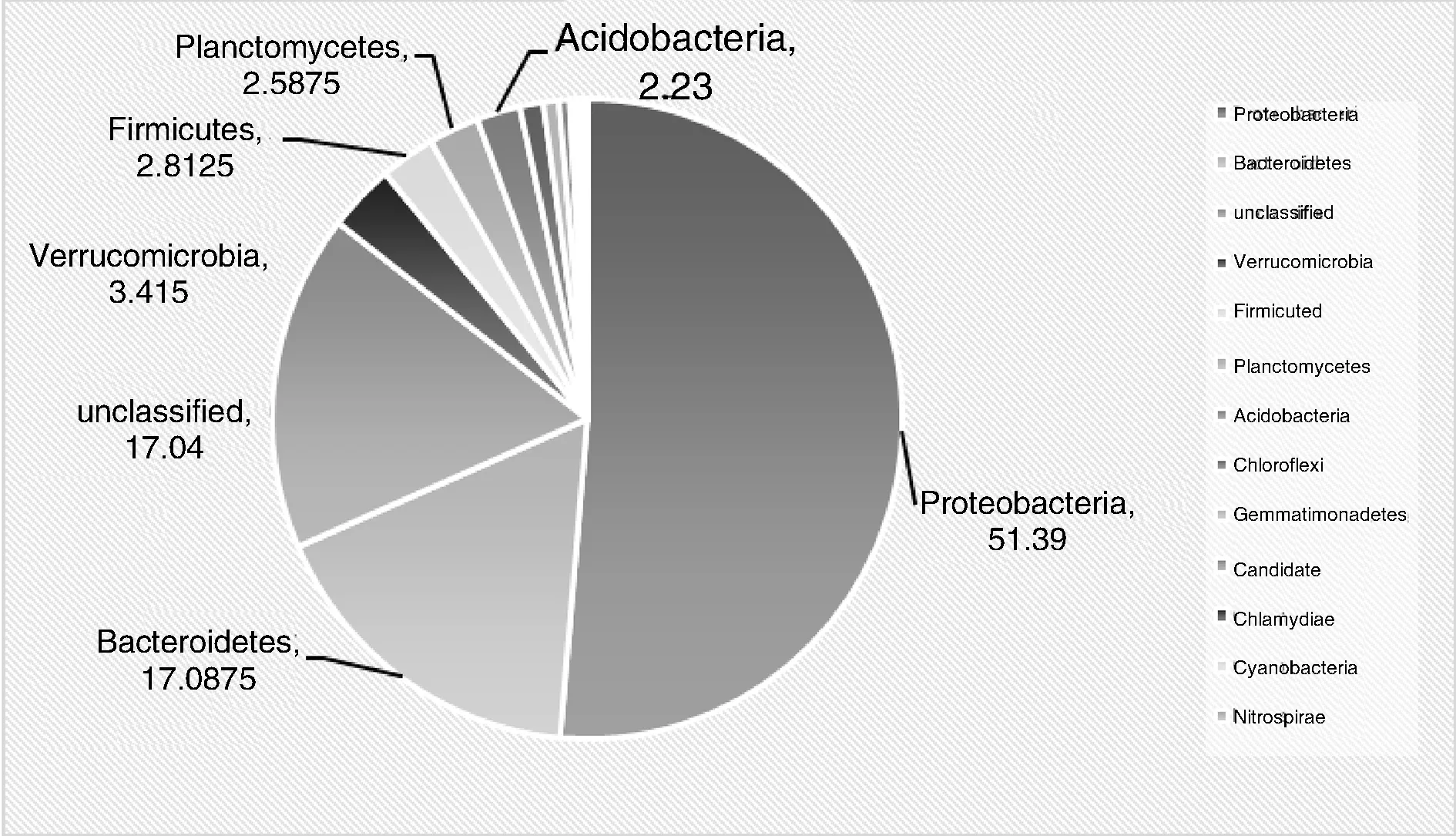
图1 新茬土门水平细菌丰度占比分布图
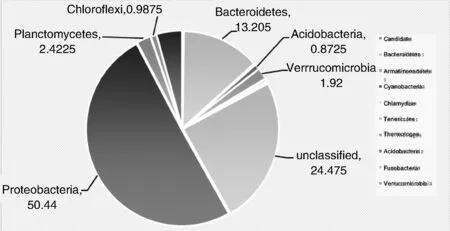
图2 重茬土门水平细菌丰度占比分布图
2.1.3 属水平上上丰富度差异分析
从属水平看,新茬土壤中共涉及到831个属,丰度值高于1%的属有17个。重茬土壤中共涉及到817个属,丰度值高于1%的属有15个。说明新茬土中细菌多样性高于重茬土。图3展示了新茬土壤与重茬土壤优势细菌类群丰度分布。可见,在各属上,两种生境中丰富度含量也有差异:在新茬土中,丰度最高的前3位是鞘氨醇单胞菌(Sphingomonas)、根瘤菌(Rhizobium)、假单胞菌(Pseudomonas),丰度值分别占6.16%、5.28%、4.91%;在重茬土中,丰度最高的前3位是节杆菌(Arthrobacter)、Olivibacter、根瘤菌,丰度值分别占16.22%、8.20%、6.14%。与新茬土相比,重茬土中鞘氨醇单胞菌、地杆菌(Pedobacter)和Skermanella丰度显著降低,分别由6.16%、4.78%和4.26%降低为2.33%、0.09%和0.66%;重茬土中节杆菌和肠杆菌(Enterobacter)丰度显著升高,分别由4.78%、1.34%升高为16.22%、5.86%。

图3 新茬土壤(XJS1)与重茬土壤(CJS1)优势细菌类群属水平丰度分布图注:XJS1指新茬大棚土壤;CJS1指重茬大棚土壤。
2.2 真菌多样性分析
2.2.1 多样性指标
新茬大棚土壤中共获得23 377条序列,分归于795个OTUs;3年重茬大棚土壤中共获得22 484条序列,分归于881个OTUs。表2展示了两种大棚土壤的真菌多样性指数,可见,重茬3年后土壤中真菌类群OTU数量、Shannon指数、Chao1指数均升高,Simpson指数降低,表明重茬3年后土壤中真菌物种多样性增大。

表2 土壤中真菌的多样性指数
2.2.2 门水平上丰富度差异分析
从门水平上看,新茬土壤与重茬土壤中分别检测到26.87%和5.69%的unclassified和unclassified-Fungi,说明两种生境中均含有较多的未知菌,但相对而言,重茬土壤中未知菌较少。除此之外,子囊菌门(Ascomycota)为两种生境中的第一优势菌,新茬土壤中与重茬土壤中丰度分别占61.14%和72.60%;新茬土壤中丰度排名第二的为担子菌门(Basidiomycota),占11.36%,该菌在重茬土壤中丰度占比下降为8.57%;两组差异较大的菌为接合菌门(Zygomycota),该菌在新茬土壤中含量很低,丰度仅占0.54%,但重茬3年后的土壤中该菌丰度快速增长至13.08%。

图4 新茬土壤(XJS1)与重茬土壤(CJS1)优势真菌类群门水平丰度分布图注:XJS1指新茬大棚土壤;CJS1指重茬大棚土壤。
2.2.3 属水平上上丰富度差异分析
图5是新茬土壤与重茬土壤真菌在属水平上的聚类条形图,可以看出两种生境中的各个样本各自聚为一类,真菌组成和丰度有明显的差异。具体来看,新茬土壤中真菌共检测到94个属,重茬土壤中真菌共检测到101个属。新茬土壤中丰度值高于1%的属只有8种,而重茬土壤中有14种。说明经过3年重茬种植草莓后,土壤中真菌总的多样性增多,且某些类群真菌大量增加。另外,新茬土壤中unclassified和unclassified_Fungi类群丰度比例总共占65.96%,重茬土壤中这两大类群占48.72%,二者差异显著,说明在新茬土中非培养真菌或未被人类分离获得的真菌比例较高,重茬3年后,土壤中这类真菌比例降低,而人们所熟悉的、已获得纯培养物的真菌种类丰度增高。

图5 新茬土壤(XJS1)与重茬土壤(CJS1)真菌在属水平上的聚类图注:XJS1指新茬大棚土壤;CJS1指重茬大棚土壤。
图6是新茬土壤与重茬土壤中属水平上丰度值比例大于1%的优势真菌类群分布图。可见:在新茬土壤中占优势的Cadophora、链格孢属(Alternaria)、茎点霉属(Phoma)、柄孢壳菌属(Podospora)和Athelia属真菌在重茬土壤中均不再占优势,Athelia属在重茬土中没有被检测到。取而代之,在重茬土壤中占优势的真菌为青霉菌属(Penicillium)、被孢霉属(Mortierella)、枝顶孢属(Acremonium)、枝孢属(Cladosporium)、Plectosphaerella、unclassified-Ascomycota、镰刀菌属(Fusarium)、丝核菌属(Rhizoctonia)、轮枝菌属(Verticillium)和赤霉菌属(Gibberella)等。两种生境中的真菌菌群呈现明显差异。

图6 新茬土壤(XJS1)与重茬土壤(CJS1)优势真菌类群属水平丰度分布图注:XJS1指新茬大棚土壤;CJS1指重茬大棚土壤。
3 结论与讨论
本研究结果表明,重茬3年后土壤中细菌数量减少、真菌数量上升,这与前人的研究结果相似。甄文超等研究指出,连续种植草莓的农田土壤微生态环境有利于真菌的增殖而不利于细菌和放线菌,草莓根际和根表微生物真菌种群数量上升、细菌和放线菌的增殖减少,最终导致连作障碍发生[10]。薛超指出重茬土壤微生物从细菌主导型向真菌主导型转化[11]。
本研究结果表明,重茬3年后,新茬土壤中丰度最高的鞘氨醇单胞菌被节杆菌属取代,肠杆菌属丰度显著升高。王志刚从植物根际获得一株鞘氨醇单胞菌,能高效解磷和分泌IAA,促进连作西瓜生长[12]。另外,很多文献都指出鞘氨醇单胞菌和节杆菌与多环芳烃、苯酚、菲等芳香族污染物的降解有关[13-15]。而肠杆菌具有缓解镉-砷富集对植物的胁迫[16]、降解植物的次生代谢产物缩合单宁(原花青素)[17]、降解除草剂阿特拉津的功能[18, 19]。因此,这可能暗示该园区土壤中有有机物污染。
本研究发现,重茬3年后的土壤真菌优势菌与新茬土壤大相径庭。原来在新茬土壤中占优势的真菌丰度值大幅下降,而新崛起的丰度值增高的真菌大多与植物病害发生相关。比如重茬土壤中占优势的丝核菌能引起多种植物(包括草莓)的黑根病、立枯病、叶腐病、茎腐等病害,是植物真菌病害防治的主要对象,也是草莓产区普遍发生的病害之一[20];轮枝菌属导致黄萎病[21];镰刀菌属可危害多种植物,破坏植物的维管束系统,引起植物萎蔫死亡和器官腐烂,是生产上防治最艰难的土传病害之一,在草莓上可引起枯萎病[22]。另一类占据优势地位的菌是营腐生生活的菌属,比如青霉菌和接合菌,这类菌常生长在腐烂的蔬菜、水果、肉类和各种潮湿的有机物上。由此可以推测:重茬3年的草莓地土壤中积累了相当数量的植物病原菌,残枝败叶的积累养育着一批腐生菌,土壤真菌环境不容乐观。另外,值得注意的是,该园区新茬土壤中检测到优势菌链格孢菌和茎点霉属细菌,链格孢菌能够引起植物黑斑病、腐烂病等,也能引起草莓采后黑腐病[23];茎点霉菌寄主广泛,能够引起多种植物叶斑病、茎枯病等,其中部分种是检疫性植物病原菌[24],提示该地块虽然是第1年栽种草莓,但前茬作物留下的病原菌也不容忽视。
综上所述,对于细菌来讲,重茬3年后土壤中细菌物种多样性及丰富度降低;变形菌门和拟杆菌门是两种生境中的优势细菌;在属水平上,新茬土中,丰度最高的前3位是鞘氨醇单胞菌、根瘤菌和假单胞菌,而在重茬土中,丰度最高的前3位是节杆菌、Olivibacter和根瘤菌;与新茬土相比,重茬土中鞘氨醇单胞菌、地杆菌和Skermanella丰度显著降低,而节杆菌和肠杆菌丰度显著升高。对于真菌来讲,重茬3年后土壤中真菌物种多样性增大;在门水平上,子囊菌门为两种生境中的第一优势菌;接合菌门在新茬土壤中含量很低,但重茬3年后的土壤中该菌丰度快速增长;在属水平上,新茬土壤中含有植物病原菌链格孢菌和茎点霉菌,重茬3年后枝顶孢属、被孢霉属、镰刀菌属等病原菌大量积累。因此,重茬土壤中细菌多样性降低、真菌多样性增高,病原真菌积累是引起草莓连作障碍的主要原因。

