体外棕榈酸诱导自噬调节奶牛淋巴细胞炎症通路
李树森 杨晓燕 李 莹 邓清华 薛江东 王新波 张玉明 杜立银
(内蒙古民族大学 动物科学技术学院,内蒙古 通辽 028000)
棕榈酸(Palmitic acid,PA)是一种16碳长链饱和脂肪酸,血浆中PA占总脂肪酸含量比例较高,对脂质代谢相关疾病的发展起到关键性作用,如肥胖、糖尿病和心血管疾病等。PA不仅可通过β氧化作为一种能量来源,还可作为多种疾病发生发展的标志性分子。此外,还可促进细胞膜合成,构成细胞膜骨架,作为致癌信号脂质,如甘油磷脂、鞘脂和醚脂质等[1-2]。多项研究表明,PA可诱导机体炎症反应的发生[3-5]。
自噬作为一种稳态机制出现,调节受损蛋白质和细胞器的周转,并通过回收细胞内成分帮助缓冲各种细胞应激。研究表明,许多人类疾病的发病机制与自噬失调有关,包括癌症、感染、退行性疾病和代谢性疾病[6]。自噬机制被认为是一种应激反应,支持真核生物单细胞在病变条件下生存,可能通过调节能量稳态和/或通过蛋白质和细胞器降解途径来实现。自噬机制参与细胞应激反应通路(包括参与控制免疫反应和炎症的通路)调节,自噬蛋白可以和免疫信号分子直接相互作用[[7-8]。在适应性免疫中,自噬蛋白也发挥一定功能,包括免疫系统的发展和内稳态,以及抗原呈递[8]。患有脂肪肝的奶牛,体内细胞长期处于高脂环境下,容易发生自噬现象[9]。
越来越多的证据表明自噬与炎症之间具有重要联系。自噬蛋白在免疫诱导和抑制炎症反应中起作用,免疫和炎症信号在自噬的诱导和抑制中同样起作用[10]。在敲除小鼠胚胎造血干细胞自噬基因Atg5后,体内的自噬蛋白SQSTM1积聚增加,减少了B细胞、CD4+T细胞及CD8+T细胞数量,并导致胚胎造血干细胞的死亡[11-13]。在造血细胞缺乏自噬基因Atg16L1的小鼠中,IL-1β和IL-18水平显示升高,炎症小体激活关键的促炎细胞因子,表明自噬基因可以激活炎症信号通路[14-15]。另外,小鼠巨噬细胞特异性的自噬基因缺失使得大量炎症因子IL-1β释放,导致引发葡萄膜炎[16]。
尽管多项研究已经表明PA在巨噬细胞和星形胶质细胞中损害自噬,导致炎症反应增强[17-18]。但PA对淋巴细胞自噬功能的影响尚未被探索,PA是否可以通过诱导奶牛淋巴细胞的自噬影响免疫功能。因此,本试验通过分离并培养奶牛淋巴细胞,探讨体外不同浓度的PA是否可以通过诱导淋巴细胞自噬调节炎症反应应答,并分析其作用机制。
1 材料与方法
1.1 主要试剂
棕榈酸(Sigma公司,P0500-100G)粉末;胎牛血清、双抗、RPMI-1640(Themo公司, PM150122);Trizol Reagent (Invitrogen公司);反转录试剂盒、实时荧光定量PCR试剂盒和qRT-PCR扩增试剂(Taka-Ra公司);Percoll分离液(GE Healthcare, 17-0891-09);生理盐水;红细胞裂解液(TIANGEN公司,S1821);3-甲基腺嘌呤(3-methyladenine, 3-MA)(Selleck公司,S2767)粉末。
1.2 淋巴细胞的分离与培养
抽取健康奶牛(内蒙古民族大学实验基地) 50 mL 新鲜血于抗凝管中,与PBS 1∶1稀释。Percoll原液与生理盐水混合配制成1.084 g/mL的分离液,取4 mL分离液于离心管中,将PBS稀释后的抗凝血2 mL小心叠加在分离液上,1 500 rpm水平离心25 min,可观察到4个细胞层,从上至下分别为:死细胞残片和血小板层、单核细胞层、淋巴细胞层、中性粒细胞及红细胞层。分离淋巴细胞,加入RPMI-1640完全培养基(含10%胎牛血清),接种于24孔板,每孔2×106个细胞。
1.3 棕榈酸(PA)的溶解
用0.01 mol/L的NaOH溶液配置10 mmol/L的棕榈酸储存液,于70 ℃水浴中加入脱脂BSA,0.22 μm滤头过滤,分别配置0、0.1、0.5、和1 μg/mL质量浓度的PA,现用现配。
1.4 试验设计
试验分为5个处理组(表1),每组3个重复,以平均数±标准差进行数据分析。
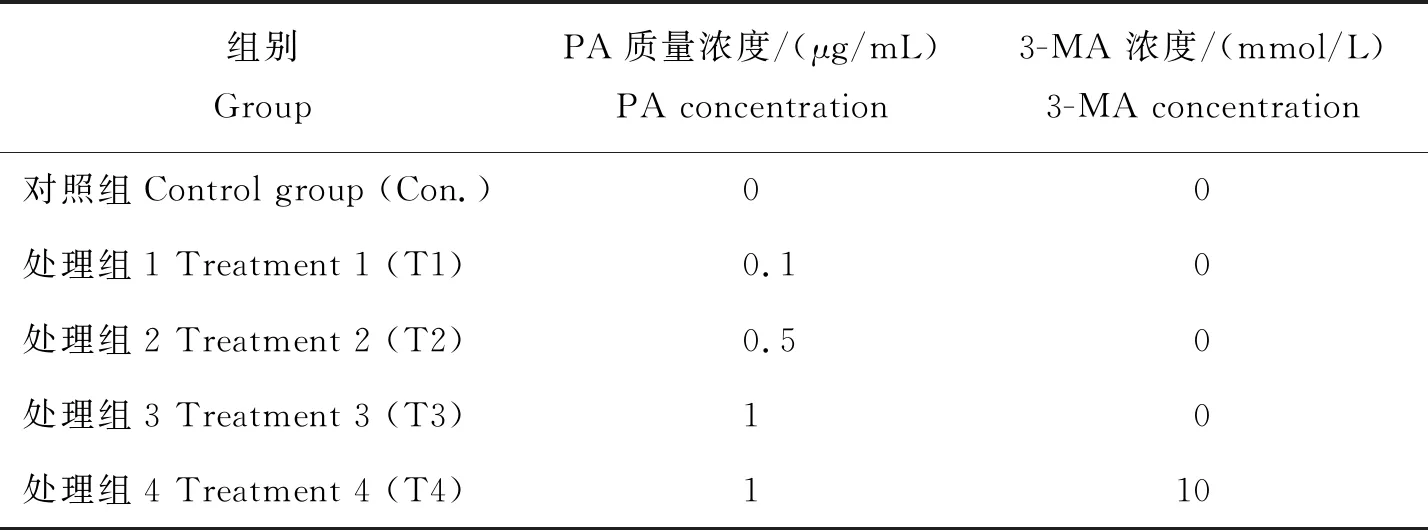
表1 试验设计Table 1 Experimental designing
1.5 CCK-8法检测细胞活性
按照每孔100 μL细胞液,约2×105个细胞接于96孔板。37 ℃,5% CO2预培养1 h,向孔内加入不同浓度棕榈酸,培养3 h后,每孔加入10 μL CCK-8溶液,再孵育4 h,酶标仪测定450 nm处吸光度。
1.6 qRT-RCR检测
收集棕榈酸处理的淋巴细胞,Trizol法提总RNA,微量分光光度计测定RNA浓度,使用反转录试剂盒反转录为cDNA,采用SYBR Green Ι qRT-PCR试剂盒检测自噬及炎症通路关键因子mRNA转录水平。

表1 qRT-PCR引物设计Table 1 Primer design of qRT-PCR
根据Genbank中LC3B、Beclin1、mTOR、UKL1、SQSTM1、IL-1β、IL-6、TNF-α和β-actinmRNA序列和引物设计原则,利用Primer 5.0软件设计引物。qRT-RCR反应体系(20 μL)如下:ROX 10 μL;上游引物1 μL、下游引物1 μL;模板cDNA 1 μL;ddH2O 7 μL。反应条件为:95 ℃预变性3 min;95 ℃变性15 s;60 ℃ 退火15 s,共计45个循环。
1.7 数据处理
采用SPSS 17.0进行数据处理,采用单因素方差分析(ANOVA)和多重比较分析(LSD),以P<0.05为差异显著,P<0.01为差异极显著。
2 结果与分析
2.1 PA对细胞活力的影响
CCK-8结果显示,与空白对照组相比,随着PA浓度逐渐升高,细胞活性逐渐降低;而与1 μg/mL PA处理组相比较,添加1 μg/mL PA+3-MA处理后,细胞活性显著增强(图1)。这表明PA可能通过自噬影响细胞活性。
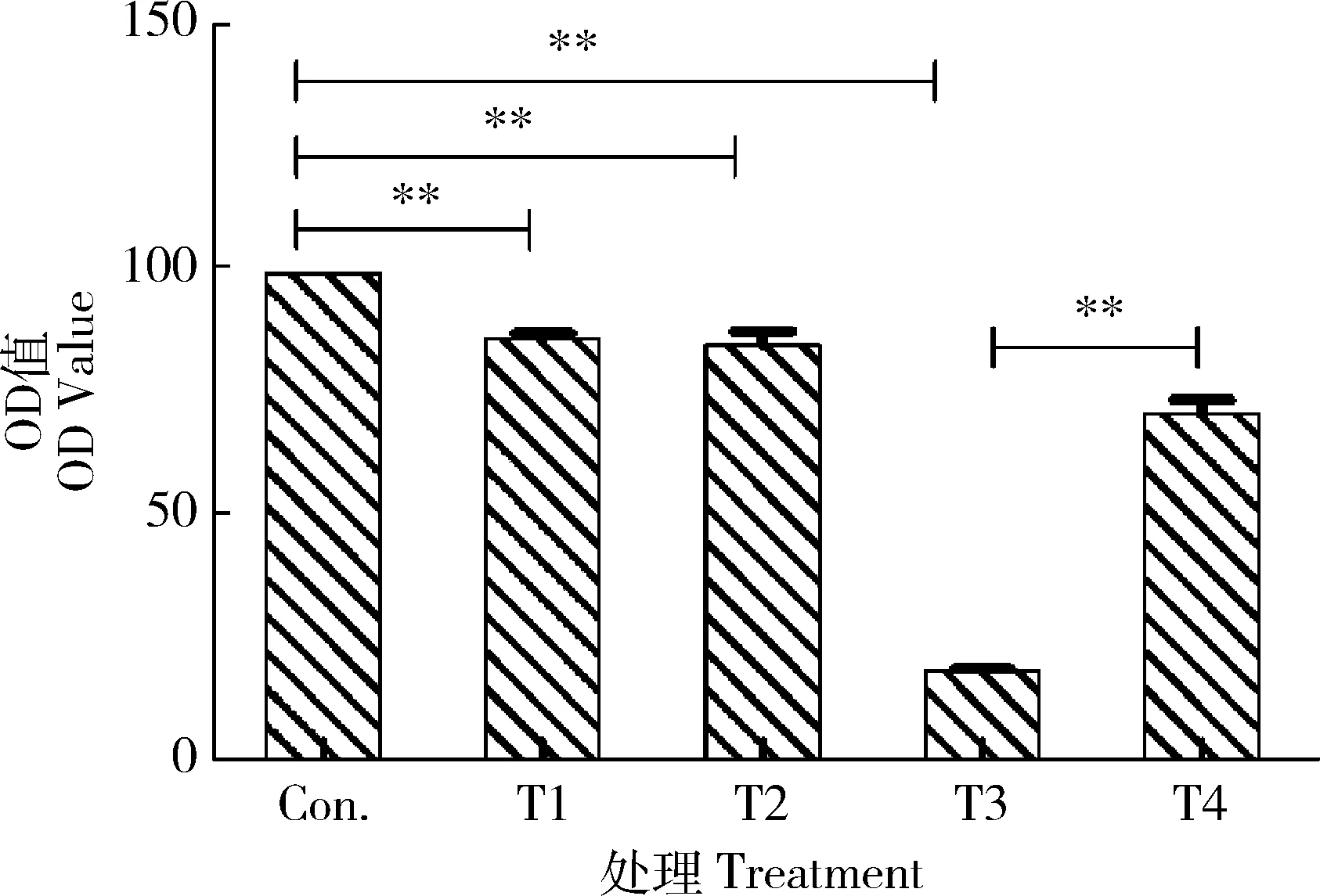
*为显著差异P<0.05,**为极显著差异P<0.01。* Significant difference P<0.05, ** Extremely significant difference P<0.01.图1 CCK-8检测淋巴细胞细胞活性Fig.1 Detection of cell viability of lymphocyte by CCK-8
2.2 PA诱导奶牛淋巴细胞自噬相关基因mRNA的表达
如图2所示,不同浓度PA处理细胞3 h后,与对照组相比,ULK1和LC3BmRNA表达极显著增加(P<0.01)(图2(b)和(d)),mTOR、SQSTM1和Beclin1mRNA表达极显著降低(P<0.01)(图2(a)、(c)和(e));添加3-MA后,与1 μg/mL PA处理组相比较,SQSTM1和Beclin1极显著增加,而LC3BmRNA表达极显著降低(P<0.01)。表明PA可以诱导奶牛淋巴细胞自噬。
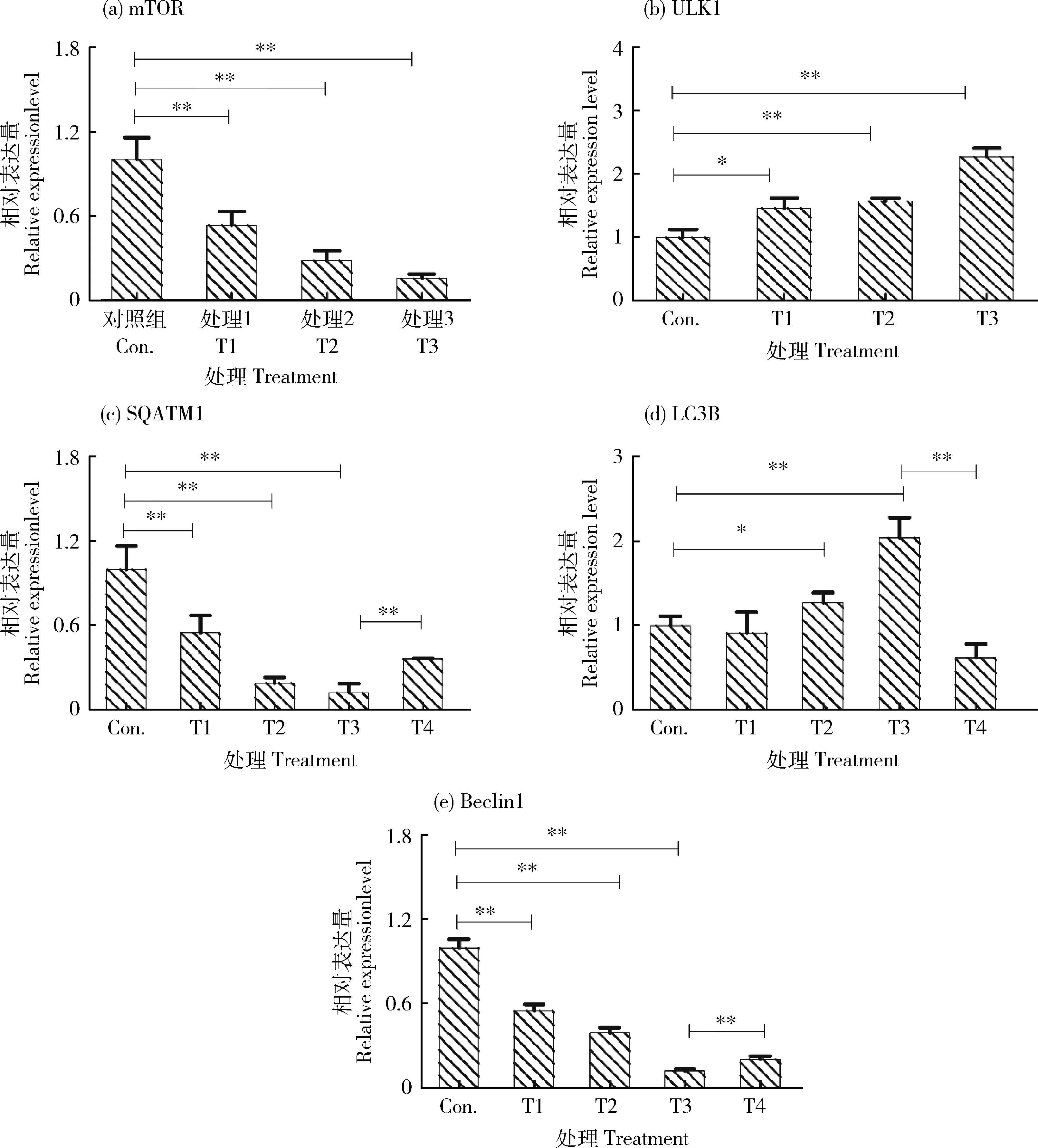
图2 PA诱导淋巴细胞自噬基因mRNA表达Fig.2 The mRNA expression of autophagy related gene in lymphocytes treated with PA
2.3 PA通过自噬调节奶牛淋巴细胞促炎细胞因子mRNA的表达
如图3所示,与对照组相比较,PA处理组显著增加IL-1β和IL-6mRNA的表达(P<0.01)(图3(a)和(b)),而显著抑制TNF-αmRNA的表达(P<0.01)(图3(c));与PA处理组相比较,PA+3-MA处理组中IL-1β和IL-6 mRNA的表达极显著降低,这表明PA可以通过自噬调节炎症反应(P<0.01)。
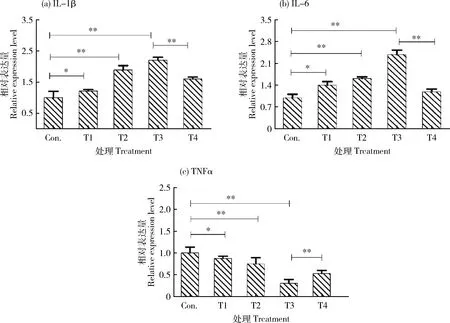
图3 PA诱导淋巴细胞促炎因子mRNA的表达Fig.3 The mRNA expression of proinflammatory factor in PA-treated lymphocytes..
2.4 PA通过自噬调节奶牛淋巴细胞促炎细胞因子的释放
如图4所示,与对照组相比较,PA处理组显著增加IL-1β和IL-6的释放(P<0.01)(图4(a)和(b)),显著抑制TNF-α的释放(P<0.01)(图4(c));与PA处理组相比较,PA+3-MA处理组中IL-1β和IL-6释放量极显著降低(P<0.01),进一步表明PA可通过自噬调节炎症反应应答。
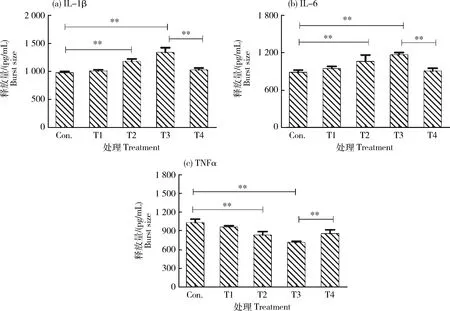
图4 PA诱导淋巴细胞促炎细胞因子分泌的释放水平Fig.4 Level of proinflammatory cytokine in lymphocytes induced by PA
3 讨 论
脂肪肝奶牛机体类似2型糖尿病患者(T2DM),长期存在慢性炎症,主要由血液中的高浓度脂肪酸(PA)造成,高水平的PA环境导致细胞对PA的摄取增加。临床和流行病学研究表明,血浆PA水平升高(而不是其他饱和脂肪酸)可能与代谢综合征有关[19-21]。另外,PA可以显著诱导小胶质细胞促炎因子IL-1β、IL-6和TNF-α的释放[22-24]。这与本研究中IL-1β和IL-6水平的显著升高一致,不同的是,其对TNF-α的分泌产生了抑制作用,这可能与细胞的差异性相关。
研究表明,高浓度的脂肪酸在肥胖和糖尿病等疾病的发病机制中起着重要作用,血液中淋巴细胞长期浸润在高浓度脂肪酸中,由于脂毒性改变其功能[25],而自噬被认为是调节脂质代谢和脂毒性的重要机制,如肝细胞通过自噬来消化和利用脂滴既脂肪的溶酶体降解途径[26-27]。本研究中,通过分离并培养奶牛淋巴细胞,体外PA诱导淋巴细胞建立奶牛脂肪肝体内环境模型,研究PA通过诱导自噬调节奶牛淋巴细胞的炎症信号通路,并分析其机制。
自噬是维持细胞稳态的重要机制,直接影响细胞活性,药理学或遗传抑制自噬导致凋亡细胞死亡[28],自噬损伤与代谢性疾病,以及其它病理生理条件有关[29]。若能消化和利用脂肪滴,降低脂肪酸浓度,可使肝细胞发生自噬促进细胞内脂质代谢[30-32]。在本研究中,随着PA浓度的升高,自噬基因表达被显著抑制,这可能与细胞种类和棕榈酸浓度不同有关。自噬是一个细胞内降解过程,重新利用大分子和受损的细胞器,以及在代谢功能障碍条件下提供能量[31]。自噬通过TRIF依赖的TLR4信号通路来调节,siRNA抑制TRIF,完全阻止了LPS诱导RAW264.7细胞GFP-LC3的自噬表达,表明LPS通过TRIF依赖性TLR4信号通路诱导自噬[33]。同样,TLR介导细胞自噬,自噬也会反过来调节炎症反应应答。有研究表明,TRAF3通过激活TLR4使TBK1被激活,TBK1对P62介导的自噬具有调节作用,证明了细胞自噬机制可以负反馈调节TLR和炎症信号通路[34]。当自噬被药物抑制后,LPS激活的炎症小体被显著抑制,炎症细胞因子IL-1β和IL-18的释放量显著下降,进一步证明自噬能调控炎症反应应答。本研究中,自噬被抑制后,促炎细胞因子释放和mRNA表达显著下降,这表明PA可以通过诱导淋巴细胞自噬调节炎症反应应答。这些结果有助于理解和阐明脂肪肝奶牛并发症的分子机制,以及为治疗奶牛脂肪肝提供了新的理论依据。

