肝肾纤维化动物模型的研究进展及评价
庄子锐王明亮张婷苏鹏亮邵久针印鑫彭蕴茹∗沈明勤∗
(1.南京中医药大学,南京 210028;2.江苏省中西医结合医院,南京 210028)
纤维化可发于多器官,其实质是慢性损伤长时间超出实质细胞修复能力,导致器官结构破坏、功能减退,最终脏器硬化和衰竭,目前有效疗法只有疾病晚期器官移植[1]。而肝、肾作为人体的两大免疫和代谢器官,更加容易遭受各种原因的损伤,使得肝肾处于慢性损伤的状态。在亚太地区,每年经由纤维化发展的肝硬化、肾硬化及其并发症成为亚太地区的主要死亡原因之一。因此,慢性肝病和慢性肾病一直都是研究的热点,对慢性肝病和慢性肾病的部分机制、药物筛选也有详尽的研究和说明,但在实际临床中以及在肝、肾纤维化实验模型的建立过程中,肝肾总是在功能和血液动力学方面体现紧密联系。除此之外,由于一些传统中药的肝肾同治功效需要适宜的动物模型来用进行现代科学研究与阐释。因此,近年来逐渐有人尝试建立一种肝肾纤维化的新复合模型以适应当代需求。
作为慢性疾病的早期阶段,早期纤维化阶段被普遍认为具有可逆性,并非不可逆的“疤痕组织”[2]。因此,阻断早期肝肾纤维化进程可以成为治疗慢性肝肾疾病新的切入点,使慢性肝肾病在早期阶段就有治愈的可能性。目前针对肝肾纤维化有效的药物非常有限,因此,能成功建立更加贴近临床的疾病模型,成为突破阻断纤维化、逆转肝肾硬化的关键点之一。本文总结了肝纤维化、肾纤维化和肝肾纤维化复合模型常用的建立方法,初步探讨了模型机制、对比了不同方法间的优缺点,旨在为建立更贴近人类临床肝肾纤维化的模型提供参考(见图1)。
1 肝纤维化模型
1.1 化学试剂法
多采用四氯化碳、硫代乙酰胺、N-亚硝基化合物等。四氯化碳模型主要以脂肪变性为主,适合于一般肝纤维化的机制和药物研究;硫代乙酰胺在体内与肝细胞化学反应致其坏死,此模型更适合于肝硬化初期阶段的研究;N-亚硝基化合物在机体内更依赖于氧化应激反应造成损伤。
1.1.1 四氯化碳(carbon tetrachloride,CCl4)
四氯化碳(CCl4)为无色有毒的挥发性液体,具有令人愉快的气味,使用过程中实验人员应注意防止吸入CCl4。因其诱导肝纤维化模型的高复制性、与人类纤维化病理变化的高相似性成为目前应用最为广泛的化学药物。CCl4诱导肝纤维化的分子机制现在还尚不完全清楚,但Dong等[3]联合利用转录、蛋白质组学分析和生物网络技术,证实CCl4毒性主要涉及氧化还原、氧化应激反应,途径主要包括视黄醇代谢、花生四烯酸代谢等。
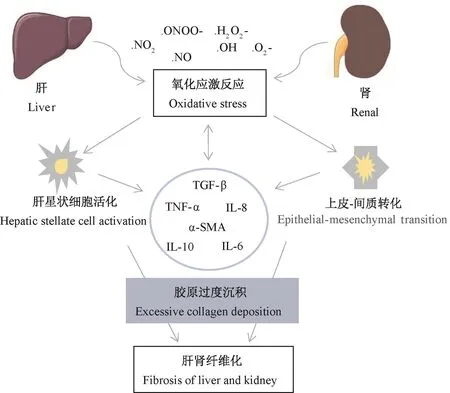
图1 肝肾纤维化的形成Note.The injury reaction can make the liver and kidney secrete inflammatory factors,activate hepatic stellate cells and promote renal epithelial mesenchymal transition.On the contrary,activation of hepatic stellate cells and epithelial mesenchymal transformation can promote the secretion of inflammatory factors,so that the injury continues,resulting in excessive deposition of extracellular matrix and organ fibrosis.Figure 1 Formation of liver and kidney fibrosis
CCl4通常与玉米油、花生油、橄榄油等按比例混合,通过灌胃、腹腔注射、吸入、皮下注射等方式给药。腹腔注射会造成更高的死亡率,但因建模快、稳定性好、成功率高得到更广泛的应用。一般根据不同实验动物品系,使用不同剂量CCl4均可在6~8周表现出炎症因子浸润、肝脂肪变性和坏死的明显的纤维化阶段特征。雌性啮齿类动物对CCl4表现出耐受难成模倾向,所以多数选取雄性大鼠进行造模。此模型具有缓慢形成肝纤维化的变化过程,形态学、病理学及血清生化指标的明显变化都具有类似人类肝纤维化的典型特征,适用于肝纤维化形成的动态研究和药物筛选。
1.1.2 硫代乙酰胺(thioacetamide,TAA)
硫代乙酰胺是无色或白色结晶,1948年被报导具有肝毒性[4],2017年WHO将其纳入2B类致癌物。TAA在体内和体外均可被CYP 2E1酶激活,代谢为不稳定的反应物TASO2与肝大分子共价结合而引发坏死。Bashandy等[5]人用TAA诱导肝纤维化时,肾同时表现出肾小球缩小、肾小管上皮变性、间质淋巴细胞浸润等损伤。
TAA可用蒸馏水或生理盐水配制,通过饮用水、腹腔注射等途径给药;饮用水给药可建立比较温和的肝纤维化模型,但饮用水给药会因为个体摄入差异造成剂量偏差,因此常采用腹腔注射,剂量范围150~250 mL/kg,最常用剂量200 mg/kg,大概4~6周即可成功建立肝纤维化模型[5-8]。TAA相比CCl4表现出更强肝毒性,造模过程中更高的死亡率要求实验人员扩大啮齿类动物数量,而集中在中央门静脉的病变、与人类肝纤维化血流动力学和代谢改变的相似性使其更适合肝纤维化向肝硬化发展的阶段研究。
1.1.3 N-亚硝基化合物
二甲 基 亚 硝 胺/二 乙 基 亚 硝 胺(dimethylnitrosamine/diethylnitrosamine,DMN/DEN)均属N-亚硝基化合物,在20世纪30年代先后报道具有强致癌性与肝毒性。N-亚硝基化合物在各器官主要依靠细胞色素P450代谢激活,转变为更具活性的代谢产物,导致烷基化DNA和活性氧产生,从而对器官产生氧化损伤[9-10]。虽然N-亚硝基化合物的主要损伤靶向器官除肝外还有肾,但其对肾的损伤研究较为缺乏,研究主要集中于肝毒性。
以肝萎缩、脾肿大、血小板减少和血清总胆红素水平显著升高为典型特征的N-亚硝基化合物模型是研究肝纤维化和肝硬化发展相关的生化、病理生理以及分子改变的优秀动物模型。
Dapito等[11]认为将DEN与CCl4合用,会促使肠道产生更多内毒素,可更好的模拟人类肝癌的微环境。Ding等[12]利用SD大鼠建立了完整的肝炎-肝纤维化-肝癌模型轴,为不同阶段疾病模型的准确建立提供了参考,此研究显示每周两次注射DEN(30 mg/kg),8~12周肝即处在明显肝纤维化阶段。
1.2 手术法
肝纤维化手术法是通过手术将胆管暴露并结扎,直接人为造成胆汁淤积,是一种以胆管增生为病变特点的胆汁淤积型肝纤维化模型。
胆管结扎可通过手术在动物体内结扎胆总管,也可在体外对细胞使用抑制剂,造成胆汁阻塞性病变。胆管结扎一定程度上可较好的模拟人类因长期胆汁淤积而引起的肝细胞增殖和凋亡、门静脉纤维化及肝硬化过程,以及伴有常见的胆汁性急性肾损伤并发症[13-14]。但手术结扎会阻断所有的胆汁流通,因此,无法更完全复制人类临床具有一定胆汁通量的原发性硬化性胆管炎和原发性胆源性胆管炎的病理过程。
Ghallab等[15]利用荧光胆汁盐和非胆汁盐有机阴离子的双光子成像技术对胆管结扎的病理机制进行研究,结扎胆总管后,肝内和胆内胆汁酸水平急剧升高损伤细胞。氧化应激和炎症反应在胆管结扎损伤肝中起重要作用[16]。Yang等[17]用SD大鼠结扎总胆管不同位置进行研究发现,胆总管上端结扎比胆总管中部结扎可用更小的死亡率诱导更严重的胆汁淤积性肝纤维化。胆管结扎建模周期大概在2~4周,在7 d左右开始看见病理变化,结扎时间不宜过长,否则啮齿类动物死亡率会大幅度升高以致数据缺失;手术法在所有方法中建模最快,但其病变也近似于急性损伤的变化,而纤维化是一种慢性疾病的过程,因此胆管结扎可能对于慢性疾病模型来说不够典型。
1.3 免疫诱导法
免疫反应本是机体免疫系统对抗外侵的正常反应,但大量免疫细胞和蛋白的堆积又会损伤正常组织细胞。免疫诱导法正是利用此原理在啮齿类动物体内模拟人类的免疫性纤维化病变,因此,免疫诱导应用的前提是作为模型的动物源要具有正常免疫系统。
1.3.1 刀豆蛋白(concanavalin A,Con A)
刀豆蛋白是从植物中提取的凝集素,具有强烈的促有丝分裂和促淋巴转化反应作用,是重要的生化和免疫研究试剂。Con A诱导的免疫性肝炎模型可用于人类免疫性肝炎、急性病毒性肝炎等疾病或药物筛选的研究。Con A的肝毒性依赖于激活体内T淋巴细胞和巨噬细胞,和内皮细胞表面糖蛋白结合,激活自身免疫系统分泌 TNF-α、IFN-γ、TGF-β1等炎症因子,从而损伤肝细胞。因此,造模时不能选用免疫缺陷无T细胞应答的啮齿类动物[18-19]。
本方法建模采用小鼠居多,造模周期约4~8周。造模时Con A可用生理盐水或PBS配制,通过尾静脉或腹腔注射给药,关于剂量Heymann等[20]建议具有更多Th1亚系的T细胞免疫反应的啮齿类动物,例如C57BL/6、C3H小鼠对刀豆蛋白更加敏感,只需要15~20 mg/kg体重;而具有更多Th2亚系的免疫应答啮齿类动物,例如BALB/c品系的近交或杂交NMRI小鼠对刀豆蛋白不敏感则至少需要30 mg/kg体重的量。
1.3.2 猪/牛血清蛋白
血清蛋白是凭借引起自身过激免疫反应产生全身性的损伤,因此本模型更适合于免疫性纤维化病理学研究,但本模型存在自愈的问题。其所致免疫性肝纤维化模型是研究细胞水平上纤维化隔膜形成的模型,以及肝纤维化后的结构变化,例如毛细血管化和静脉化;但目前未见血清蛋白诱导肝肾纤维化复合模型的诱导研究。
猪/牛血清蛋白无法在免疫缺陷或免疫耐受啮齿类动物中诱导肝纤维化,因其免疫性损伤依赖于一定周期的激活巨噬细胞、Kupffer细胞,释放炎症因子,进而激活星状细胞和成纤维细胞纤维化[21]。用猪血清蛋白诱导的免疫性纤维化程度与血清蛋白剂量并无依赖关系,只会随时间不同呈现不同病理变化[22]。You等[23]用牛血清蛋白(BSA)致SD大鼠肝小叶结构严重受损,炎性细胞浸润,广泛的纤维组织增生,纤维组织通过中央小叶增生并扩展为肝实质。
2 肾纤维化模型
2.1 化学试剂法
重金属化合物、腺嘌呤和手术法在国内建立慢性肾病模型的应用属最为广泛。建立肾纤维化模型的几种化学物质相较肝纤维化模型的几种物质,明显缺少对肾损伤的高度靶向性,且研究多集中于肾的急性损伤研究。
2.1.1 氯化汞(mercury dichloride,HgCl2)
重金属汞是主要以金属汞、无机汞、有机汞三种形式普遍存在于自然环境中的污染物,对环境和人体有极大的伤害。肾是受无机汞毒性影响的主要器官之一,因为无机汞更容易在肾中累计,使肾成为受伤最严重的器官。
Zalups[24]发现 HgCl2静脉注射 0.5 μmol/kg或2.0 μmol/kg后3 h,超过总剂量55%的Hg2+都集中在肾近段小管上皮细胞中。HgCl2可诱导T细胞死亡和破坏细胞中线粒体膜,当线粒体电子传输链功能受损会产生过量活性氧自由基(ROS),氧化应激反应可激活细胞死亡程序。HgCl2造模时多选取大鼠进行实验,原因是小鼠对HgCl2显示出一定的耐药性,难成模。本方法可通过皮下注射、静脉注射、灌胃等途径给药。造模中HgCl2剂量非常关键,过小难成模,剂量稍大啮齿类动物容易大批死亡,因此,预实验时,对于大鼠的剂量,应多进行尝试或采取梯度给药。在国内多采用每日8 mg/kg HgCl2水溶液灌胃给药,8周左右即可建立肾小管间质纤维化模型[25]。
2.1.2 腺嘌呤
腺嘌呤可在体内代谢为2,8-二羟基腺嘌呤(DHA),DHA在肾小管积累,形成晶体(结石)堵塞肾小管造成肾损伤,虽然DHA的致病机理还尚未完全清楚,但已知TGF-β在其中起到重要作用[26]。
用腺嘌呤诱导的慢性肾病(chronic kidney disease,CKD)模型会增加增加尿酸的排泄,形成蛋白尿,游离氨基酸减少,肾外表颗粒化且伴有肾纤维化,同时还会出现心血管系统的结构和功能损伤,无论是缓慢变化的慢性肾病还是并发症均与临床人类CKD表现高度一致。
腺嘌呤诱导肾纤维化多采用大鼠进行含有0.75%腺嘌呤的饲料喂食,可引起肾迅速且严重的变化,伴随肾小管损伤、肾小球、肾间质纤维化及炎症。但 Tamura等[26]和 Imamura等[27]仅用含有0.2%和0.25%腺嘌呤饲料喂食C57BL/6小鼠,也成功诱导肾纤维化,可能说明小鼠比大鼠对腺嘌呤更敏感。
2.1.3 硝酸铀酰(uranyl nitrate)
硝酸铀酰目前在国外诱导急性肾损伤模型应用较多,其急性肾毒性和急性肾衰竭的病理机制有很多深入的研究和详细的描述。向啮齿类动物注射硝酸铀酰之后,50%的铀化合物通过肾排出,铀化合物在肾中又集中在肾皮质部分,在其他器官分布的数量微不足道,具有较好的肾靶向性[28]。硝酸铀酰可使啮齿类动物尿量和肾小球过滤率减少,近端肾小管萎缩;其慢性肾毒性多与重金属汞、锌等对肾损伤的机理类似,硝酸铀酰同样可以破坏线粒体电子传输链功能,产生的氧化应激反应损伤肾[29]。
在国内不仅对硝酸铀酰的慢性肾毒性研究不多,应用都非常少,但基于硝酸铀酰对肾的靶向性,我们应尝试扩大对硝酸铀酰的慢性肾毒性研究,也许可以建立良好的慢性肾纤维化模型。在为数不多的硝酸铀酰诱导纤维化模型文章中,多采用雌性啮齿类动物,硝酸铀酰的给药方式和剂量都比较统一,多采用单次腹腔注射5 mg硝酸铀酰/kg体重,大约8~10周即可见肾间质纤维化。
2.2 手术法
对肾纤维化的研究中更多会采取手术法建立模型,一般手术法有单侧输尿管结扎、5/6肾切除手术和缺血再灌注法;其中结扎单侧输尿管最经典,应用也是最为广泛,而缺血再灌注法则因其临床实际应用的高度需求性同样被研究的较多。5/6肾切除法虽然也能快速建立肾的损伤,但因其需要切除大部分肾,对机体产生过大的损伤且并不是很符合临床需求的研究。
2.2.1 单侧输尿管结扎(unilateral ureteral ligation,UUO)
本方法适用于大鼠和小鼠,输尿管结扎后阻碍尿液正常排泄,短时间便可造成尿潴留,肾肿大,肾小管细胞坏死,肾组织结构完全被破坏从而导致肾功能不全。此模型已经成为了研究尿路梗阻肾小管间质纤维化原因和机制的标准模型。但UUO模型同样存在慢性病变特点不够典型的问题,并且伴随结扎时间延长,啮齿类动物死亡率会加速提升。此模型病变只发生在结扎输尿管一侧,对侧肾功能依旧正常。
单侧输尿管结扎后,从第3天起有肾髓质和皮质减少的病理变化,且有少量纤维化出现,随时间推移,结扎7 d后血清肌酐和尿素氮成倍增长,单核巨噬细胞浸润,间质水肿,部分近端小管上皮空泡变性[30],两周后即可形成以小管细胞坏死和萎缩、炎症细胞渗透、细胞外基质和I型胶原蛋白大量沉积为特点的严重的结构破坏[31]。刘克剑等[32]等发现从侧腹开口结扎单侧输尿管两端后,不离断输尿管,可保证不影响造模效果的同时大幅提升啮齿类动物的存活率。
2.2.2 缺血再灌注
在临床的外科手术、器官移植、烧伤等过程均可出现缺血再灌注损伤,然而短暂缺血并不足以引起器官细胞损伤,反而缺血后的血液再灌注可造成微血管和实质细胞更严重的损伤。因此缺血再灌注模型具有高度应用局限性,基本全部用于缺血再灌注引起肾损伤的相关研究。
缺血再灌注引起的肾损伤主要与活性氧自由基和Ca2+超载有关,在缺血组织中清除自由基的酶类合成能力受损,并且缺血再灌注可以直接损伤肾小球内毛细血管内皮细胞,引起炎症级联反应。因此,抑制TLR4通路和增强清除自由基能力可减少缺血再灌注造成的损伤[33]。张蕊[34]利用动态对比增强MRI监测大鼠缺血再灌注后的肾损伤,发现当大鼠肾缺血30~45 min时可在保证大鼠存活率的条件下对肾造成不可逆转的伤害。
3 肝肾纤维化复合模型
作为人体两大免疫器官,肝肾总是有千丝万缕的联系,不仅临床上的肝肾综合征、乙肝相关性肾病、胆汁性肾病等,中医的肾病从肝论治,肝病从肾论治等均体现着肝肾协作、互滋的能力;此外,为了深入研究一些传统中药对肝肾的异病同治功效,开始尝试建立肝肾纤维化复合模型。基于以往建立肝纤维化和肾纤维化模型的经验之上,几乎所有肝损伤药物和手术法都具有高度肝靶向性的同时可轻损肾,而致肾损伤的化学药物往往肾靶向性较低,因此在建立肝肾纤维化复合模型时多采用肝靶向性损伤药物结合肾损伤药物或直接采用能造成全身损伤的化学试剂、药物。
3.1 四氯化碳和牛血清
Manoj[35]联合四氯化碳和牛血清蛋白腹腔注射。在本研究中,四氯化碳主要造成肝损伤,牛血清蛋白主要通过免疫复合物形成蛋白尿造成肾损伤;10周后肝病理切片可见明显的纤维化,肾仅见结缔组织增生和炎症细胞浸润。
四氯化碳具有较高肝靶向性的同时对肾也有损伤,牛血清蛋白作为免疫性损伤药物配合四氯化碳,使肝肾损伤程度均大致处于纤维化阶段,但本试验最终并未显示严重的肾纤维化结果;反而发现牛血清蛋白对四氯化碳的肝损伤有拮抗作用,为日后造模方法提供了新发现。
3.2 DMN和汞
姜哲浩等[36]在研究扶正化瘀方对大鼠肝肾纤维化的影响时采用了腹腔注射DMN和喂食含有重金属汞的饲料建立肝肾纤维化复合模型。8周之后,肝组织坏死、肝细胞肿胀、大量炎症细胞浸润、假小叶形成;肾间质水肿伴炎细胞浸润、肾间质中大量胶原纤维。汞在诱导肾纤维化单独使用时,剂量难以控制,但配合对肝肾都有损伤的DMN使用大大提高了成功诱导肝肾纤维化的几率。
3.3 酪氨酸氧化产物
酪氨酸是常见的食品添加剂和药原料,容易被氧化修饰[37];因此在售卖的牛奶、奶粉、动物饲料中等均可检测到酪氨酸及其氧化产物的存在。因此,酪氨酸及其氧化产物对人体的影响成为了研究热点。李竹青[38]发现短期28 d喂食酪氨酸氧化产物可对肝肾均产生损伤,随喂食时间增长,会引起肝肾炎症因子大量分泌,产生氧化应激反应,紧接着激活肝星状细胞与内质网应激反应,促进肾小球内皮细胞-间质转化反应,引起肝肾纤维化。
3.4 环孢菌素A(cyclosporine,CsA)
从20世纪80年代CsA作为免疫抑制剂应用于临床,主要用于器官移植手术后的排异反应,但由于较严重的肝、肾毒性副作用,使其应用受限。短期注射CsA可使肾血流减少,长期注射会导致具有广泛的肾小管纤维化的肾衰竭。CsA的急性肾毒性与激活肾素-血管紧张素系统有关,慢性肾毒性是因为可触发机体分泌TGF-β,大量的TGF-β是触发上皮间质转化的关键因素。CsA可破坏肾近端管状细胞的形态、连接结构、细胞骨架,并且在上皮-间质转化后,成肌纤维细胞可以自由迁移到间质中,并释放出大量的细胞外基质(ECM),促进纤维化发展[30-40]。程根阳[41]先建立低盐饮食(low salt diet,LSD)喂养,然后每日皮下注射CsA,14 d后即显示肝肾功能受损、炎症细胞浸润,35 d试验结束时,间质炎性细胞浸润减少,纤维化程度明显。
4 总结与展望
4.1 总结
现有建立肝、肾纤维化模型的方法在建模难易程度、临床相似性、重复程度都各有千秋。化学诱导法建模耗时较长,但比较符合慢性疾病病变过程,个别毒性化学物质,如氯化汞、DMN等由于安全管控原因难以购买,因此模型出现空缺,丞待开发新的模型;手术法虽然建模过程耗时短,但对于慢性疾病的慢性病变过程来讲不够典型,同时术后感染、啮齿类动物撕咬造成刀口撕裂、结扎时间过长等使死亡率升高;免疫法虽能引起全身性的炎症,但却存在停药后可自愈的问题,这并不利于肝肾纤维化的治疗药物筛选。
现有造模方法基本可以实现从不同发病原因来模拟人类临床中出现的肝、肾纤维化的一些病理变化,可以适用于不同科研目的。相对来讲肝肾纤维化复合模型现在处于较空白的阶段,由于胆管结扎、注射硫代乙酰胺等方法能同时引起肝肾的损伤,是对肝肾同时的直接毒性还是基于肝肾功能交互的损伤,对其潜在机制及诱导复合模型的潜力还有待深入研究。近年仅有两篇报道称酪氨酸氧化产物和环孢菌素A均可同时引起肝肾纤维化,但在大鼠体内引起的病理变化及模型特点还需进行大量且深入的研究;而能够引起全身性损伤的阿霉素和免疫性血清可能成为诱导肝肾纤维化复合模型的潜力物质;同时也可以尝试分别选取建立肝纤维化和肾纤维化模型的经典方法,结合使用建立肝肾纤维化复合模型,例如经典四氯化碳模型、硫代乙酰胺模型结合单侧输尿管结扎法等。
4.2 展望
人类慢性肝病和慢性肾病作为全球健康问题,其药物研究日益迫切。而实验性动物模型不仅可以从群体数量上满足疾病实验和药物筛选实验的要求,还可以在实验中各个环节实现条件控制,可以人为的剔除一些干扰因素,从而实现对发病机制、疾病进程、药物筛选等进行深入的研究。但现有的肝、肾纤维化动物模型依旧存在问题:(1)对动物模型本身的发病机制尚未完全清楚;(2)肝肾纤维化动物模型大多在大、小鼠身上建立,模型的动物种类较少;(3)无法完全模拟人类肝、肾纤维化进展所引起的所有变化;(4)造模过程中死亡的啮齿类动物无法确认死因,且可能会在啮齿类动物体内引发并发症或其他变化我们也无法详尽得知;(5)造模过程至今并未有统一化的规范操作标准,会因为啮齿类动物品种、实验人员操作、药品配置等方面造成成模差异。
因此,对现有建模方法继续优化以及对所有动物模型进行发病机制的探讨,都将是日后重点研究的领域。

