磁吻合实现犬下腔静脉人工血管置换快速无缝线吻合实验与效果
刘仕琪,慈红波,雷 鹏,吕 毅,宋宇龙,王善佩,白纪刚
(1. 西京学院医学院,陕西西安 710123;2. 新疆维吾尔自治区人民医院血管外科,新疆乌鲁木齐 830001;3. 宁夏医科大学总医院肝胆外科,宁夏银川 750004;4. 西安交通大学第一附属医院肝胆外科,陕西西安 710061;5. 陕西省人民医院麻醉科,陕西西安 710068)
腹腔内或腹膜后肿瘤侵犯腹腔大血管中,以下腔静脉(inferior vena cava, IVC)受累最为常见[1],由于IVC解剖位置深且为膈肌平面以下绝大部分器官的血流回心通道,因此IVC显露、切除、重建等技术水平直接影响腹膜后肿瘤预后,从而对外科医生的技术提出巨大挑战。目前人工血管置换技术已广泛应用于IVC受侵犯的肿瘤患者,并扩大了肿瘤的可切除性[2-3]。但目前人工血管吻合仍普遍延用传统的手工缝合,不仅吻合速度慢,血管阻断时间长,易引起相应器官缺血-再灌注损伤,且由于缝合材料对血管壁不可避免的损伤及血管腔内缝线等异物存留引起的相关并发症,成为人工血管置换技术进一步发展的技术瓶颈[4-6]。基于前期研究关于磁吻合技术(magnetic compression anastomosis, MCA)可实现血管无缝线吻合研究经验[7],本研究尝试利用自主设计并制作的人工血管-磁吻合环模块完成大动物腹腔大血管切除后人工血管快速置换的可行性。
1 材料与方法
1.1 实验动物及分组健康成年杂交犬16只,购自西安市长安区教学动物养殖场,12~18月龄,体质量(20.5±4.6)kg,雌雄不限,按照人工血管吻合方式不同随机分2组:MCA组(n=8)采用人工血管-磁吻合环模块完成IVC人工血管置换,手工缝合(manual suture, MS)组(n=8)采用传统方法缝合完成IVC人工血管置换。本实验经西安交通大学医学部伦理委员会批准。
1.2 人工血管-磁吻合环模块设计与制作根据成年杂种犬IVC个体差异选择不同管径膨体聚四氟乙烯(expanded polytetrafluomethylene, ePTFE)人工血管,结合前期设计,制作用于大血管无缝线吻合的磁性吻合环(专利号:ZL 2014 2 0371869.2),组合成ePTFE人工血管-磁吻合环模块(图1A),每段人工血管两端各配1对相同规格椭圆形磁性吻合环(由西北有色金属研究院防腐研究所加工制作),以适应不同管径人工血管吻合。此项研究中所选成年犬IVC人工血管置换的复合材料磁吻合环规格(内孔短径8.0~15.0 mm,内孔长径16.0~20.0 mm,外径较内径增加约3.5 mm,高2.0 mm,重约2.0 g,最大磁通密度100~185 mT)。
1.3 动物模型制备及分组处理
1.3.1动物模型制备 MCA组与MS组术前准备及下腔静脉游离方法相同,术前3 d每只犬给予300 mg/d阿斯匹林口服。术前常规禁食、水,腹腔注射30 g/L戊巴比妥钠(1 mL/kg)全身麻醉。完成气管插管后,采用仰卧位束缚带固定犬爪,40 g/L硫化钠除去腹部术野和左后肢大隐静脉体表投影区域毛发。左侧大隐静脉切开置管,建立静脉通道,开腹前30 min开始静脉滴注头孢唑林钠1 g,术中以乳酸林格氏液(500 mL)维持静脉输液。腹部常规消毒铺巾后经腹正中切口入腹。以温盐水纱布覆盖并向左推开胃肠以显露IVC并游离周围结缔组织,于肾静脉下方仔细游离IVC至6~8 cm长度,距离拟切除段IVC约2 cm处,血管阻断钳分别阻断IVC远近端,切除两阻断部位之间IVC长5~6 cm。
1.3.2IVC人工血管置换MCA快速吻合方法 选择与试验犬IVC相适用的ePTFE人工血管-磁吻合环模块,IVC断端分别套上配对的磁吻合环,将血管边缘均匀固定在吻合环针尖上(图1B),以低浓度肝素盐水(100 IU/mL)冲洗血管末端与e-PTFE人工血管腔,用无磁镊子分别夹持人工血管一端磁环与IVC末端配对磁吻合环相互靠近,使吻合环上针尖与针孔相对应后,随即两个配对磁性吻合环在磁场作用下相互吸引自动完成吻合,同法完成另一端人工血管快速吻合,松开远端血管阻断钳排出人工血管腔内空气,松开近端阻断钳,血流恢复通畅(图1C),吻合口无渗漏,血管壁无湍流形成的波动。
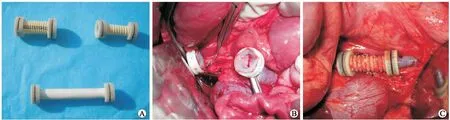
图1 ePTFE人工血管-磁吻合环模块与IVC切除后MCA人工血管快速吻合
1.3.3IVC手工缝合方法 以5-0 prolene线按两定点法分别在人工血管与IVC远端吻合口两端做定点缝线。先连续缝合吻合口后壁,至另一端后打结,再连续缝合前壁,在一端打结;同法缝合人工血管近端,吻合口暂不打结,松开远端阻断钳,排出人工血管腔内空气再打结,松开近端阻断钳,恢复IVC血流。若有渗漏血的情况则用5-0 prolene线修补。
1.4 术后处理及观察仔细检查术野无出血及渗漏后,以2-0 PDSII缝合腹膜与腹白线,再以3-0丝线间断缝合皮肤与皮下组织。术后自然苏醒,第1天仅饮水,第2天即恢复正常饮食,术后连续3 d给予阿司匹林口服(200 mg/d)并经留置的大隐静脉通道给予静点头孢唑林钠(1 g,Bid)。
术后3 d及1、2、4、12周分别定期行吻合口多普勒超声(APOGEE 3500,国产)与血管照影(WINMEDIC 2000,国产)检查,人工血管造影检查时通过大隐静脉插管推注300 g/L复方泛影葡胺观察吻合口有无狭窄及血栓形成;4、8、12周时各组分别取2只犬IVC吻合口标本肉眼观察,并常规制作石蜡包埋切片,行HE与Masson染色,进行病理组织学观察。检查前均给予腹腔注射30 g/L戊巴比妥钠(1 mL/kg)全身麻醉。
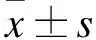
2 结 果
2.1 MCA与MS组IVC人工血管置换手术时间的比较MCA组利用ePTFE人工血管-磁吻合环模块完成IVC人工血管置换时间为(6.25±2.25)min,MS组所需时间约(27.32±5.12)min,两组手术时间差异有统计学意义(t=10.658,P<0.001)。
2.2 术中吻合口情况的比较MCA组术中吻合口无渗漏血及狭窄情况发生。MS组有4例在缝合完毕释放阻断钳后出现吻合口渗漏血情况(P=0.077),需要用5-0 prolene线局部修补,其中1例人工血管远端吻合口因反复渗血进行修补出现轻度狭窄。
2.3 术后吻合口彩色多普勒血流动力学检测与X线影像观察所有实验犬术后恢复顺利且健康状况良好。术后吻合口超声检查显示,MCA组人工血管远近端血流速度正常,未发现吻合口狭窄、血栓形成或湍流引起的血管壁波动(图2A),血管造影结果显示血流通畅,吻合口无狭窄及血栓形成(图2B)。MS组术后4~8周时共发现3例吻合口轻度狭窄并发症,与MCA组比较差异无统计学意义(P=0.200)。
2.4 术后吻合口标本观察结果IVC人工血管置换术后4、8、12周进行IVC肉眼观察,见两组吻合口血管腔内皮细胞覆盖完整,但MS组由于缝线异物存留致吻合口内壁欠光滑。HE染色显示,吻合4周后,MCA组吻合口表面即有较完整内膜覆盖,血管内皮化顺利完成;12周时,MCA组吻合口部位仅有极少数的炎性细胞浸润,但在MS组人工血管吻合口部位覆盖内皮细胞层明显增厚且血管腔内可以看到明显的缝线残留痕迹,表面凸凹不平,吻合口周围仍有较多炎性细胞浸润。Masson染色显示在术后12周时的吻合口愈合情况及局部纤维组织增生程度,MS组人工血管表面内皮细胞层较MCA组明显增厚,缝线周围纤维化组织增生明显(图3)。
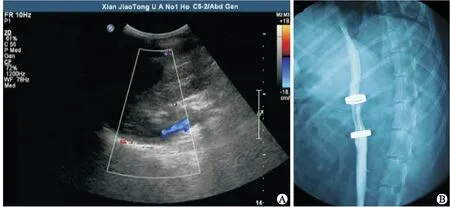
图2 MCA方法完成IVC人工血管置换术后影像学检查结果
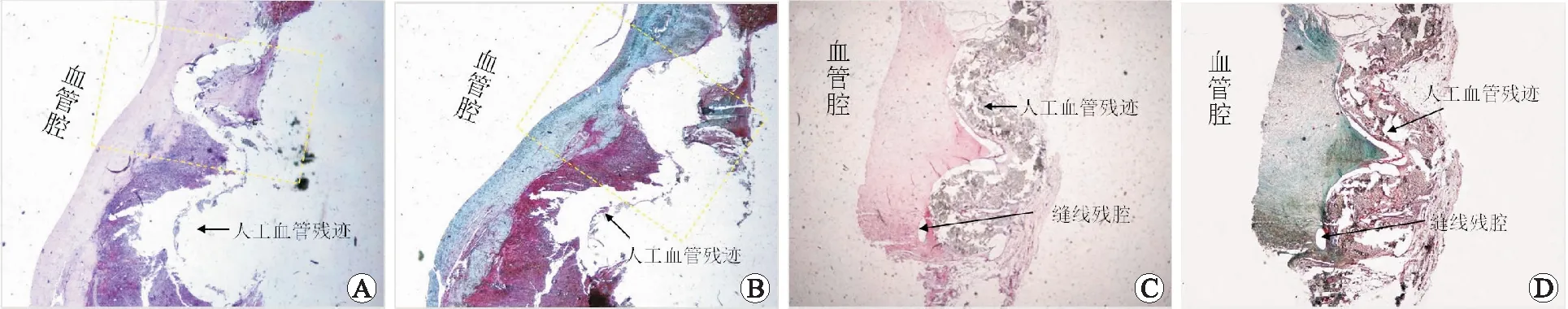
图3 IVC人工血管置换术后12周吻合口HE与Masson染色情况(黄色虚框为吻合口区域)
3 讨 论
腹膜后肿瘤常由于起病隐匿而错失早期治疗机会,待出现症状在临床就诊时,常已发生后腹膜后广泛转移并累及IVC,需要手术彻底切除病灶等根治性手术才能延长患者生存期[1,8]。此外,部分累及IVC的腹腔包虫病或源于IVC的原发肿瘤亦涉及大血管切除并重建外科手术。由于IVC独特的解剖特点与生理功能,手术风险大,其显露、切除、重建等问题对临床医生外科技术与经验提出巨大挑战,并直接影响着腹膜后肿瘤患者的预后。目前,人工血管置换技术已广泛应用于 IVC受侵犯的肿瘤患者,并扩大了肿瘤的可切除性[3,9]。但长期以来,人工血管吻合过程仍沿用传统的手工缝合,手术耗时为常规血管吻合时间两倍以上,不仅吻合速度慢,IVC阻断时间也较长,易引起腹部以下机体大部分器官缺血-再灌注损伤[4],且由于缝合材料对血管壁不可避免的损伤[5],以及术后血管腔内缝线等异物存留引起的相关并发症,成为人工血管置换技术进一步发展的技术瓶颈[6]。因此,腹腔大血管人工血管置换手术期待一种新的吻合方法以克服传统缝合方法的不足。本研究在前期自主设计制备的大血管磁性吻合装置基础上[7,10],进一步设计完善了人工血管-磁吻合环模块以完成腹腔大血管切除后人工血管快速置换手术。
根据实验犬IVC直径,本研究设计并制作了不同规格磁吻合环与相应管径的ePTFE人工血管组合成模块,磁吻合环轴向最大磁场强度为100~185 mT,可确保吻合口保持紧密对合,避免了渗漏血的情况发生[10-11]。在手术操作过程中仅需根据直视下所见受术者IVC实际直径选择相应人工血管模块,利用磁场作用力即可实现IVC快速置换。这种技术可有效克服传统手工缝合人工血管两端吻合口的繁琐程序,方法简便可靠,学习曲线短,使复杂的大血管吻合技术得以极大程度简化。
此项研究中,MCA组在IVC部分切除并利用ePTFE人工血管-磁吻合环模块历时仅6~8 min即完成人工血管置换,吻合完成后松开阻断钳恢复IVC血流通畅未见渗漏血情况发生,吻合速度仅为MS组1/4,耗时较MS组显著缩短(P<0.001),可有效避免组织器官因长时间阻断IVC血流而导致器官淤血水肿及缺血-再灌注损伤,相关基础研究尚在持续研究中。
人工血管-磁吻合有效克服了传统缝合过程中针线对血管壁完整性破坏及针距间渗漏血等技术性并发症。术后行IVC与人工血管吻合口多普勒超声与IVC造影检查发现,MS组有3例出现吻合口不同程度狭窄,MCA组未见此并发症,这与术中选择与受术者血管大小相对应的人工血管有关,但尚未有统计学差异。利用人工血管-磁吻合环组合模块可能有助于避免或者减少手工缝合方法诸多并发症,还有待进一步基础研究。
IVC人工血管置换术后,不同时期吻合口标本的HE与Masson染色结果显示,相较于传统缝合方法,e-PTFE人工血管-磁吻合环组合模块与自体血管吻合口无狭窄,无异物残留于血管腔内,内膜层相较MS组更加平整光滑,吻合口炎性反应轻微,纤维组织形成少,可见吻合口质量优于后者。
e-PTFE人工血管-磁吻合环组合模块为涉及腹腔大血管疾病的外科手术提供了一种简单、快速、吻合效果可靠的人工血管置换吻合装置与技术。利用这种吻合装置,可以显著缩短手术时间,保持高通畅率;可能有助于减少传统缝合技术与材料导致的吻合口并发症,有利于手术后恢复。其不足之处在于磁吻合环将长期滞留体内,且影响MRI检查。本研究小组目前已经开始着手进行可吸收纳米磁性材料的研制,有望克服此类缺点与不足。人工血管-磁吻合环组合模块实现人工血管无缝线化置换的吻合口愈合质量及对全身器官缺血-再灌注损伤的影响将在后续研究中进一步完善。
致谢:感谢西安交通大学第一附属医院精准外科与再生医学国家地方联合工程研究中心、陕西省再生医学与外科工程研究中心及西北有色金属研究院为此项研究提供的支持与帮助。

