核心素养理念下的电化学命题特点探析
◇ 河北 高孝强
电化学是化学学科模型认知、宏观辨识与微观探析、变化观念、社会责任等核心素养体现的最主要载体之一,是高考命题的必考知识点,常同时出现在选择题与非选择题中,选择题难度较大、题境较新颖,常以电化学研究的新成果、新应用为素材,展示电化学工作原理模型;在非选择题中常常以拓展知识宽度、角度及深度来凸显命题的综合性、创新性,常以简单的电化学装置图或文字描述来展示,这不仅利于考查氧化还原反应知识、电化学模型、方程式的书写等必备化学知识,同时也利于对识图分析与信息整合、推理与计算等关键能力的考查.
1 考查电化学装置的工作原理,凸显知识的基础性
电化学考查内容尽管主要体现在电极类型判断、电极反应式书写、总反应方程式书写、电子转移数目以及电解液中离子浓度变化等方面,但其命题的基础就是电化学的基本工作原理,其工作原理就是在电极上发生电极反应,进而可以明确有关微粒的得失电子及存在状态.
例1一种水基二次电池原理如下,
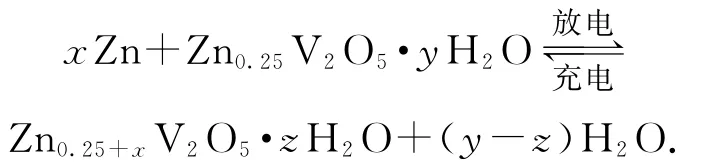
电解液为含Zn2+的水溶液,该电池可用于电网贮能.下列说法正确的是( ).

图1
A.放电时,Zn2+脱离插层
B.放电时,溶液中Zn2+浓度一直减小
C.充电时,电子由Zn0.25V2O5·yH2O层经电解质溶液流向Zn0.25+xV2O5·zH2O 层
D.充电时,阳极反应为:Zn0.25+xV2O5·zH2O+(y-z)H2O-2xe-=Zn0.25V2O5·yH2O+xZn2+
解析
以一种水基二次电池为题材,考查原电池、电解池的工作原理.从图示及提供的反应方程式角度来看,有点复杂,但耐心分析就会发现知识落脚点很简单,无非就是电极判断、电子(或离子)移动、电极反应式书写等常规内容.放电时,Zn作负极,Zn0.25V2O5·yH2O得电子,并与Zn2+结合进入插层,选项A错误;由反应方程式可知,Zn2+没有在总反应方程式中出现,故Zn2+浓度不变,选项B错误;电子只能通过导线转移,不能通过电解质溶液转移,选项C错误;充电是与放电完全相反的过程,充电时,阳极的电极反应式为Zn0.25+xV2O5·zH2O+(y-z)H2O-2xe-=Zn0.25V2O5·yH2O+xZn2+,选项 D正确.答案为D.
解题策略电化学的实质就是氧化还原反应,因而在熟练掌握氧化还原反应中的氧化剂与还原产物、还原剂与氧化产物等基本概念的基础上,理解电化学装置的工作原理(如图2),并结合转化中箭头指向或信息提示,就可以顺利判断出电极反应类型.
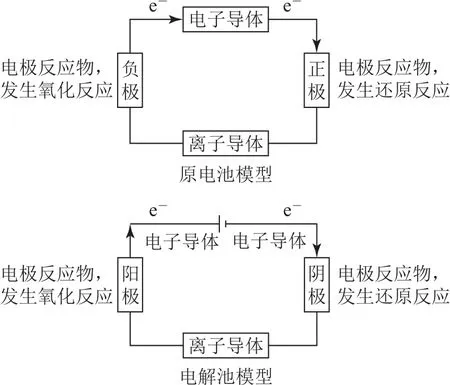
图2
2 展示新型电池的最新研究成果,凸显化学的使命感
能源是人类社会可持续发展的三大因素之一,因而对能源危机的解决主要集中在提高现有燃料的利用率与寻找新能源两个方面,可以说是化学面临的极大社会责任问题,需要不断研究创新.
例2微生物燃料电池是指在微生物的作用下将化学能转化为电能的装置,某微生物燃料电池的工作原理如图3所示,下列说法错误的是( ).
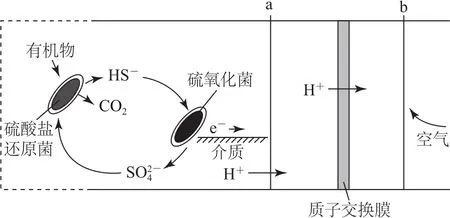
图3
A.b电极发生还原反应:4H++O2+4e-=2H2O
B.电路中有4mol电子发生转移,大约消耗标准状况下22.4L空气
C.维持两种细菌存在,该装置才能持续将有机物氧化成CO2并产生电子
D.HS-在硫氧化菌作用下转化为的反应是
解析
以微生物燃料电池为情境素材,展现了电化学研究的多角度.由图示可知,通O2的b电极为正极,发生的电极反应为4H++O2+4e-=2H2O,选项A正确;电路中有4mol电子发生转移时,消耗O2为在标准状况下体积为22.4L,则大约消耗标准状况下空气22.4L×5=112 L,选项B错误;硫酸盐还原菌可以将有机物氧化成CO2,硫氧化菌可以将HS-氧化成,故两种细菌存在时就会循环把有机物氧化成CO2并释放出电子,所以选项C正确;HS-在硫氧化菌作用下转化为,其电极反应式是HS-+4H2O-8e-=+9H+,选项D正确.答案为B.
例3一种钌(Ru)基配合物光敏染料敏化太阳能电池的示意图如图4所示.电池工作时电极上发生的反 应 为:(激发态),RuⅡ∗-e-→RuⅢ,I-3+2e-→3I-.下列关于该电池的叙述正确的是( ).
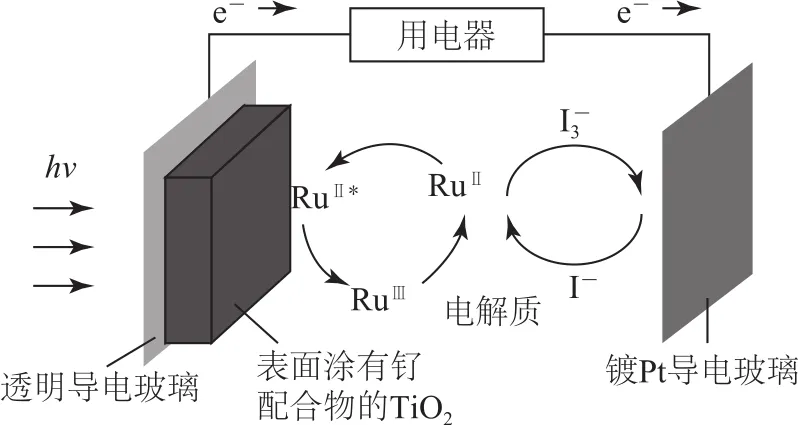
图4
A.电池工作时,是将化学能转化为电能
B.电池工作时,电解质溶液中I-和浓度不断降低
C.透明导电玻璃上的电势比镀Pt导电玻璃上的电势高
D.电解质溶液中发生反应2Ru3++3I-=2Ru2++
解析
本题以太阳能电池为情境素材,既体现科学家在新能源研究方面的成果,同时也从微观角度图了解发电的工作原理.根据图示可知,太阳能电池是将太阳能转化为电能的装置,选项A错误;电池工作时,电解质溶液中I-3转化为I-,选项B错误;电子由透明导电玻璃经用电器转移至镀Pt导电玻璃上,说明透明导电玻璃上的电势比镀Pt导电玻璃上的电势低,选项C错误;由图示可知,电解质溶液中发生协同反应:2Ru3++3I-=2Ru2++,选项D正确.答案为D.
解题策略在关注物质中元素价态的变化及微粒实际存在状态前提下,利用守恒思想书写电极反应式及总反应方程式.书写电极反应式时,首先通过价态升降关系找出氧化剂与还原产物(或还原剂与氧化产物),然后写出氧化剂+ne-→还原产物(或还原剂-ne-→氧化产物),最后利用电荷守恒、原子守恒配平即可,其中配平电荷守恒时一定要运用离子导体中的导电离子(或电解质溶液中的H+或OH-).
3 以电化学应用为情境,体现社会责任感
化学源于生活又服务于社会,这就是化学不断向前发展的动力,因此涉及电化学在三废处理、海水淡化、物质制备与测定等方面的新应用逐渐成为命题的热点.
例4三室式电渗析法处理含NH4NO3废水的原理如图5所示,在直流电场的作用下,两膜中间的和可通过离子交换膜,而两端隔室中的离子被阻挡不能进入中间隔室.工作一段时间后,在两极区均得到副产品NH4NO3.下列叙述正确的是( ).

图5
A.a极为电源负极,b极为电源正极
B.c膜是阴离子交换膜,d膜是阳离子交换膜
D.当电路中通过1mol电子的电荷量时,会有5.6LO2生成
解析
这是一道涉及废水处理、变废为宝的电化学试题.由“工作一段时间后,在两极区均得到副产品NH4NO3”及装置图可知,Ⅱ室中的阳离子NH+4、H+向Ⅰ室移动,并与Ⅰ室中的稀硝酸反应生成了NH4NO3,故c膜为阳离子交换膜,Ⅰ室中石墨为电解池阴极,a极为电源负极,阴极电极反应式为2H2O+2e-=H2↑+2OH-;Ⅱ室中的阴离子、OH-向Ⅲ室移动,并与Ⅲ室中的稀氨水反应生成NH4NO3,故d膜为阴离子交换膜,Ⅲ室中石墨为电解池的阳极,b极为电源正极,阳极电极反应式为2H2O-4e-=O2↑+4H+,所以选项A正确、选项B与C错误;选项D中没有给出标准状况下,无法用气体摩尔体积公式计算气体体积,故错误.答案为A.
例5我国科学家开发设计出一种天然气脱硫装置,利用图6装置可实现反应H2S+O2=H2O2+S↓.已知甲池中有如图7所示的转化:

图6

图7
下列说法错误的是( ).
A.该装置将光能只转化为电能
B.该装置工作时,溶液中的H+从甲池经过全氟磺酸膜进入乙池
C.甲池碳棒上发生电极反应:

D.乙池①处发生反应:H2S+=3I-+S↓+2H+
解析
这是利用原电池原理来脱硫的试题.由图中信息知光能转化为电能和化学能,选项A错误;根据甲池中碳棒上发生消耗H+的反应可知,H+应从乙池移向甲池,选项B错误;甲池中碳棒是正极,电极反应式为AQ+2H++2e-=H2AQ,选项C正确;根据乙池①处箭头方向知,发生的协同反应为H2S+I-3=3I-+S↓+2H+,选项D正确.答案为A、B.
知识延伸:电极反应是指在电极表面上进行的反应,其他发生的反应都不属于电极反应.离子移动的目的一是为了形成闭合电路,二是为了中和(或减少)电极附近多余的电荷,以确保电极附近呈电中性.
4 与实验探究、平衡与速率等知识相融合,凸显学科内知识的综合性
化学是一门以实验为基础,以理论与计算为指导的学科,因而诸多化学知识点不是孤立的,而是有机融合在一起成为一个较为完整的系统.
例6(2020年新课标Ⅰ)为验证不同化合价铁的氧化还原能力,利用图8所示电池装置进行实验.
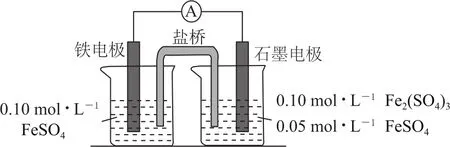
图8
回答下列问题:
(1)由 FeSO4·7H2O 固体配制0.10mol·L-1FeSO4溶液,需要的仪器有药匙、玻璃棒、________(从图9中选择,写出名称).
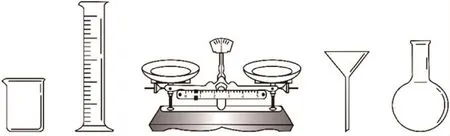
图9
(2)电池装置中,盐桥连接两电极电解质溶液.盐桥中阴、阳离子不与溶液中的物质发生化学反应,并且电迁移率(μ∞)应尽可能地相近.根据表1数据,盐桥中应选择________作为电解质.
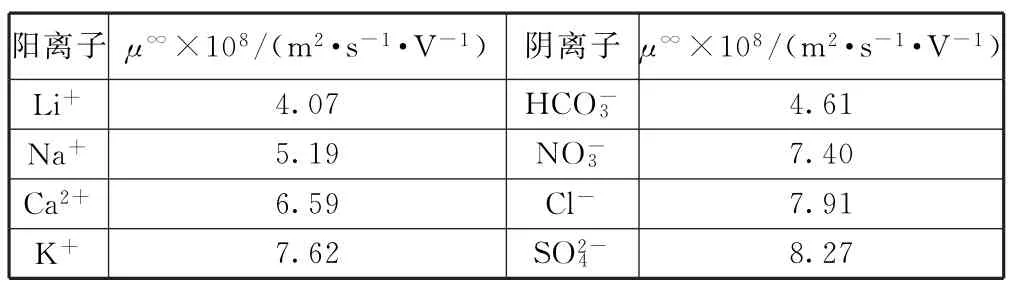
表1
(3)电流表显示电子由铁电极流向石墨电极.可知,盐桥中的阳离子进入________电极溶液中.
(4)电池反应一段时间后,测得铁电极溶液中c(Fe2+)增加了0.02mol·L-1.石墨电极上未见Fe析出.可知,石墨电极溶液中c(Fe2+)=________.
(5)根据(3)、(4)实验结果,可知石墨电极的电极反应式为________,铁电极的电极反应式为________.因此,验证了Fe2+氧化性小于________,还原性小于________.
(6)实验前需要对铁电极表面活化.在FeSO4溶液中加入几滴Fe2(SO4)3溶液,将铁电极浸泡一段时间,铁电极表面被刻蚀活化.检验活化反应完成的方法是________.
解析
这是一道实验探究与电化学知识相融合的试题.(1)由 FeSO4·7H2O 固体配制0.10 mol·L-1FeSO4溶液的步骤为计算、称量、溶解并冷却至室温、移液、洗涤、定容、摇匀、装瓶、贴标签,因而需要的仪器有药匙、托盘天平、合适的量筒、烧杯、玻璃棒、合适的容量瓶、胶头滴管.(2)FeSO4、Fe2(SO4)3都属于强酸弱碱盐,水溶液呈酸性,故Fe2+、Fe3+能与HCO-3反应,酸性条件下NO-3能与Fe2+反应,又因Ca2+能与SO2-4反应,所以根据题意“盐桥中阴、阳离子不与溶液中的物质发生化学反应”,故盐桥中阴离子不能选择HCO-3、NO-3,阳离子不能选择Ca2+,又因“盐桥中阴、阳离子的迁移率(μ∞)应尽可能地相近”,故盐桥中选择KCl作为电解质.(3)根据“电流表显示电子由铁电极流向石墨电极”知,铁电极为负极,石墨电极为正极,所以盐桥中的阳离子进入石墨电极溶液中.(4)铁电极上的反应式为Fe-2e-=Fe2+,石墨电极上的反应式为Fe3++e-=Fe2+,根据“电池反应一段时间后,测得铁电极溶液中c(Fe2+)增加了0.02mol·L-1”,又由得失电子守恒,石墨电极溶液中c(Fe2+)增加0.04mol·L-1,故c(Fe2+)=0.05mol·L-1+0.04mol·L-1=0.09mol·L-1.(5)电池总反应为Fe+2Fe3+=3Fe2+,根据氧化还原反应强弱规律知:Fe2+氧化性小于Fe3+,还原性小于Fe.(6)铁电极表面被刻蚀活化,发生的反应为Fe+Fe2(SO4)3=3FeSO4,要检验活化反应是否完成,只要检验溶液中不含Fe3+即可.
解题策略读取题干,明确题意要求,运用所学知识及题干中的文字描述或图示信息提示,解答具体问题即可.
电化学的命题素材比较新颖,命题的方式可以多变,但考查的知识点仍落到电化学的基本原理上,故学习或复习时一定要深度理解电化学的工作原理,以不变应万变.

