Fe3O4@GO@TiO2的制备及光催化降解综合化学实验的设计
焦琳娟,卓银珊,唐家惠,张家伟
(韶关学院 化学与土木工程学院,广东 韶关 512005)
《高等学校“十三五”科学和技术发展规划》中明确指出:“科教融合是现代高等教育的核心理念,支撑人才培养是高校科技工作的内在要求”[1].可见,培养应用型创新人才离不开科教融合.综合化学实验是本科化学专业人才培养中一门重要课程,是通过探究性实验来培养学生的科学创新能力、独立思维能力与综合研究能力.以科教融合为切入点,将教师的最新科研成果转化为综合化学实验,是该课程改革的必然趋势[2].
“TiO2光催化降解甲基橙”是化工类专业经典的基础实验之一,已有文献对TiO2合成方法及实验装置进行了改进,可提高TiO2的纯度、分散性以及缩短实验时间[3].但TiO2存在催化率不高、难回收等缺点,目前解决办法之一就是将TiO2负载在磁性碳基材料上[4-8].为了把这前沿的科研成果引入到大学实验教学中,本文结合课题组的科研成果,以自制的氧化石墨和Fe3O4为主要原料,采用溶胶-凝胶法制备了磁性氧化石墨烯/二氧化钛(Fe3O4@ GO@ TiO2)复合光催化剂[9-10],使用扫描电镜、X-射线衍射、红外光谱对复合光催化剂的形貌、晶型结构及官能团进行了表征,并考察其对甲基橙的光催化性能,设计了一个综合性的化学实验.实验内容包括洗涤、常温过滤、真空干燥、煅烧、超声等基本操作技术,以及X-射线衍射仪、扫描电子显微镜、红外光谱仪、光化学反应仪等现代化实验仪器的使用,适合作为化学、应用化学、环境工程等专业的综合化学实验项目.
1 实验目的
(1)掌握制备光催化剂的实验技能,熟悉光催化材料的表征方法;
(2)理解光催化原理,熟悉光催化性能实验的测定方法;
(3)学习撰写学术论文.
2 实验原理
氧化石墨烯(GO)具有良好的导电性、热稳定性,以及比表面积大等优点[11],在波长小于或等于387 nm的紫外光照射下,负载在GO表面的TiO2被激发,价带(VB)中的电子接受光子能量跃迁至导带(CB),在导带形成光生电子(e-),在价带相应位置产生光生空穴(h+),组成光生电子-空穴对(e-/ h+).随之光生电子和空穴对被具有良好导电性的GO转移到表面,分别和表面物质反应生成高活性的氧化自由基.主要反应如下:
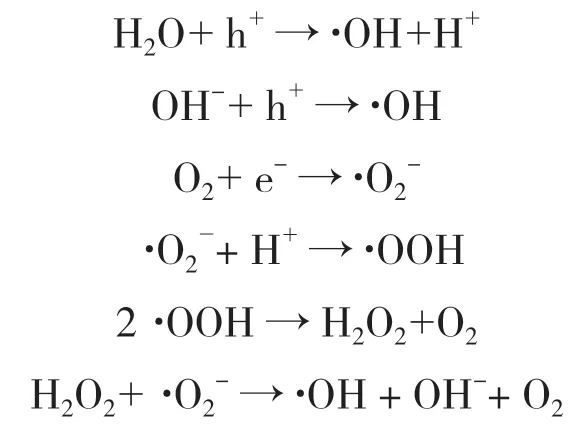
大多数的有机污染物能被具有强氧化性的羟基自由基(·OH)和超氧负离子(·O2-)氧化为CO2和H2O,从而达到去除污染的目的. GO较大的比表面积以及GO和有机物分子之间的π-π键的相互作用,使得大量目标污染物被吸附到催化剂表面,提高单位时间被·O2-和·OH氧化降解为CO2和H2O的目标污染物数量,从而提高TiO2光催化活性[11-12].
3 仪器与试剂
实验所用仪器主要为:Ultima IV X-射线衍射仪,Zeiss Gemini500 扫描电子显微镜,IRTracer-100傅立叶红外光谱仪,BL-GHX-Ⅳ光化学反应仪,722s分光光度计等.
甲基橙、钛酸四丁酯(TBT)、无水乙醇、浓盐酸等试剂均为分析纯.氧化石墨和Fe3O4为实验室自制.
4 实验内容
4.1 光催化剂的制备
4.1.1 制备GO@TiO2光催化剂
实验过程分为4步:第1步,在40 mL无水乙醇中加入0.3 g氧化石墨,超声振荡1 h,得GO溶液A.第2步,向35 mL无水乙醇中添加11.9 mL TBT,接着一边搅拌一边滴加由35 mL无水乙醇、0.2 mL浓HCl和3 mL去离子水组成的混合溶液,滴加完后继续搅拌至出现溶胶状物质B.第3步,缓慢将溶液A加入到溶胶B中,搅拌至凝胶状后再在80 ℃下搅拌12 h,接着冷却至室温、过滤、洗涤至滤液呈中性.第4步,80 ℃下真空干燥产物12 h,研细后在450 ℃马弗炉中煅烧3.5 h,即得GO@TiO2.
4.1.2 制备Fe3O4@GO@TiO2光催化剂
将0.3 g Fe3O4加入到200 mL含有1.0 g GO@TiO2的水溶液中,搅拌1 h后用永磁铁将产物分离、洗涤、真空干燥12 h即得Fe3O4@GO@TiO2光催化剂.
4.2 标准曲线的绘制
用去离子水将250 mg·L-1的甲基橙储备液逐级稀释为2.50、5.00、7.50、10.0和12.5 mg·L-1标准溶液.选择溶剂空白为参比溶液,在464 nm处测定各标准溶液吸光度,绘制标准曲线.
4.3 光催化性能实验
将40.0 mg Fe3O4@GO@TiO2光催化剂分散于盛有50 mL 10.0 mg·L-1甲基橙溶液的石英管中,在光催化反应仪的暗箱中搅拌30 min后,以高压汞灯为光源,每隔一定时间取出1支石英管,并依次进行磁性分离、高速离心、过滤、测定滤液吸光度、根据4.2标准曲线得到对应浓度,然后通过(1)式得到甲基橙溶液降解率Dr:

式中,c0、ct分别为暗处放置30 min、光照tmin后溶液中甲基橙浓度.
5 结果与讨论
5.1 催化剂的表征
5.1.1 扫描电镜及EDS分析
图1a清晰地反映出氧化石墨为表面光滑的片层结构.图1b可知,在GO的片层结构上,分散着TiO2纳米粒子.图1c显示随着负载量的增加,GO表面上的颗粒越来越均匀.图1d出现了 C、Fe、O、Ti元素的对应峰.结合扫描电镜图、XRD图、红外光谱图可以证明 Fe3O4和 TiO2粒子成功附着在氧化石墨烯上.

图1 扫描电镜图及EDS分析图
5.1.2 X-射线衍射
图2在2θ=10.46处出现了氧化石墨特征衍射峰[13-14],但图3显示两种复合光催化剂均无此峰,说明氧化石墨已被完全剥离,形成氧化石墨烯.图3b表明,GO@TiO2只在25.38°、37.96°、48.12°、53.88°、55.12°、62.7°、69.08°、70.24°、75.12°出现了衍射峰,分别对应于锐钛型TiO2的(101)、(004)、(200)、(105)、(211)、(204)、(116)、(220)、(215)晶面,说明GO@TiO2中的TiO2为锐钛型.对比图3a和图3b可以发现,图3a中除了有锐钛型TiO2特征衍射峰外,在2θ=30.5°、35.6°、43.5°、62.7°处出现了Fe3O4(311)、(400)、(422)和(440)特征衍射峰,说明Fe3O4@GO@TiO2中各物质为共存状态.
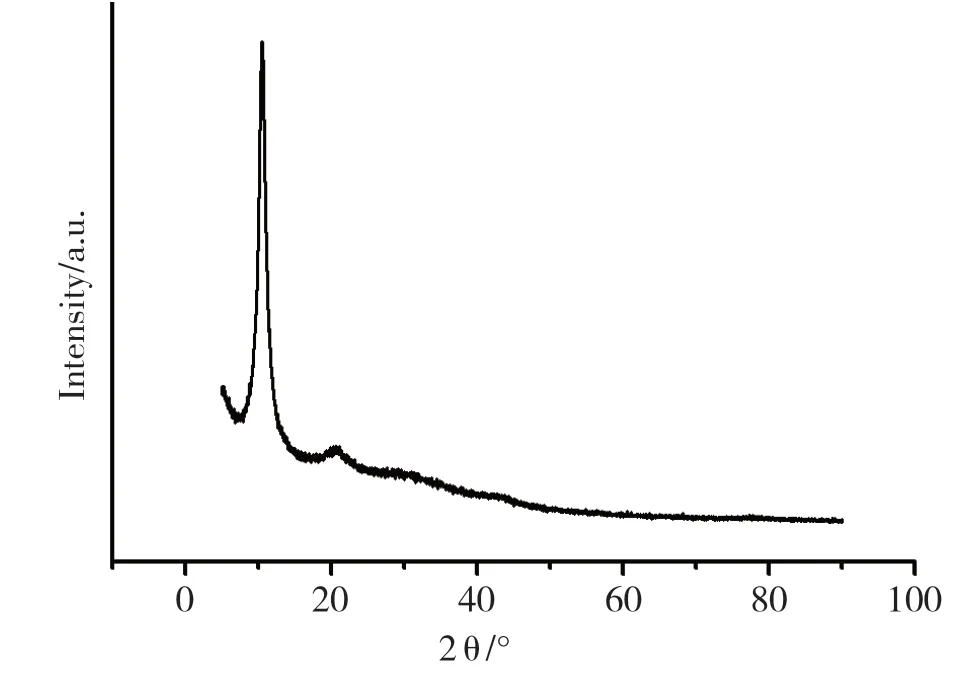
图2 氧化石墨XRD图

图3 磁性和非磁性GO@ TiO2 XRD图
5.1.3 红外光谱
如图4所示,3 430 cm-1和1 430 cm-1是-OH的伸缩振动峰,1 640 cm-1是C=C的伸缩振动峰,565 cm-1是Fe3O4的Fe-O 振动吸收峰,447 cm-1和401 cm-1是Ti-O键的伸缩振动峰,这些说明Fe3O4和TiO2已经成功复合到GO上.
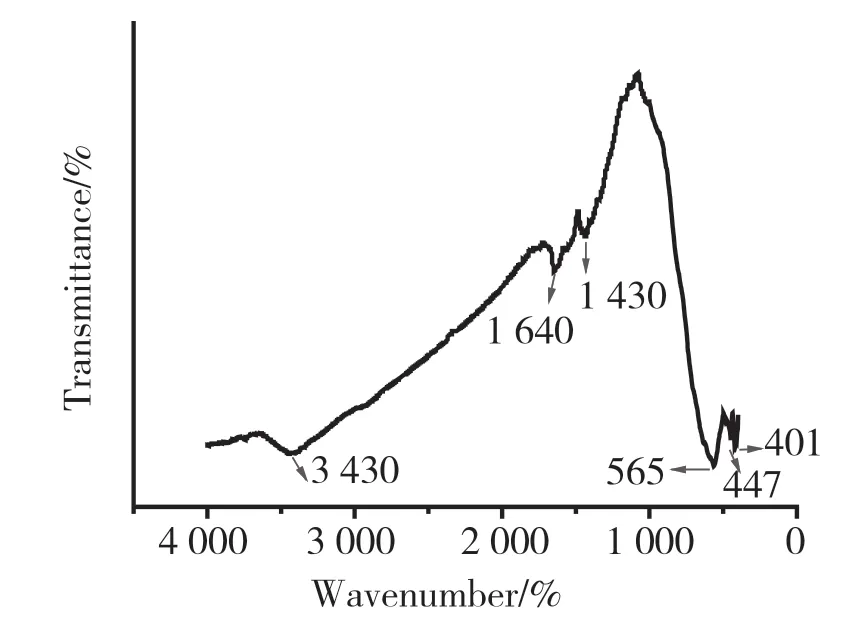
图4 Fe3O4@GO@TiO2 FT-IR谱图
5.2 光催化性能
以y表示吸光度A,x表示甲基橙浓度,实验测得y=0.066 74x+0.002 86,R2=0.999 82,说明在实验浓度范围内,甲基橙浓度与吸光度成良好的线性关系,如图5所示.
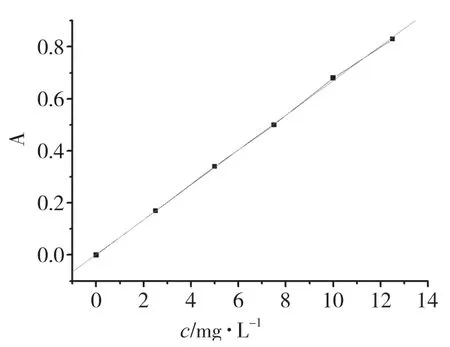
图5 甲基橙标准曲线
图6为Fe3O4@GO@TiO2作为光催化剂时,不同光照时间内对甲基橙的降解曲线.由图6可以看出,在光催化剂Fe3O4@GO@TiO2存在下,高压汞灯连续照射70 min后,甲基橙的降解率达到94.5%.
利用Langmiur-Hinshelwood模型,采用积分法拟合图6数据,得到图7 ln(c0/ct)与time回归方程:ln(c0/ct)= -0.071 67+0.040 08t,R2=0.995 20,说明本实验遵循一级动力学方程.
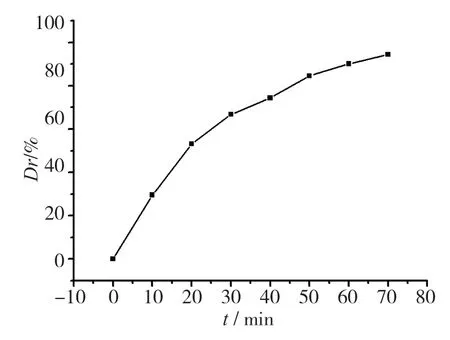
图6 Fe3O4@GO@TiO2降解曲线

图7 ln(c0 /ct)与time的线性回归方程
6 教学安排与要求
(1)实验预习.通过查阅文献,了解TiO2光催化的研究进展,重点了解半导体固定化提高TiO2光催化性能的主要方法;熟悉GO、纳米TiO2和Fe3O4的制备方法及操作注意事项;熟悉X-射线衍射仪、扫描电子显微镜、红外光谱仪等现代化仪器的原理和使用方法.
(2)实验教学安排与分组.本实验共分3个阶段,第一阶段8学时,制备Fe3O4@GO@TiO2复合光催化剂.第二阶段3学时,材料的表征分析.第三阶段3学时,甲基橙标准曲线的绘制和Fe3O4@GO@TiO2光催化性能实验.按照5~6人一组,将学生分成若干组.
(3)实验结果表达与要求.根据氧化石墨、GO@TiO2和Fe3O4@GO@TiO2电镜扫描图,分析彼此之间在形貌,粒径等方面的差异,再根据EDS能谱表征图,确定Fe3O4@GO@TiO2复合光催化剂的元素组成.对照文献,分析GO@TiO2、Fe3O4@ GO@TiO2两种复合光催化剂XRD图谱中主要特征衍射峰的归属,确定TiO2在复合材料中的晶型.根据红外光谱图,分析主要官能图的归属.通过光催化性能实验数据,分析Fe3O4@GO@TiO2光催化效果及其遵循的动力学方程.最后每位学生以科技论文的形式撰写实验报告.
7 结语
易于分离的高活性光催化材料成为目前科学研究的热点之一,本综合化学实验旨在以科教融合为切入点,将科研与教学密切结合,培养学生实验操作技能、文献查阅能力以及实验设计能力、操作使用现代化分析仪器能力以及谱图分析能力,提高学生的团队合作精神、综合实验素质和解决实际问题的能力,为毕业论文(或设计)及尽快适应今后的工作岗位打下坚实的基础.同时,本实验还有很多可以拓展的空间,例如探讨氧化石墨、TiO2及Fe3O4不同质量比对Fe3O4@GO@TiO2光催化效果的影响、Fe3O4@GO@TiO2光催化降解甲基橙溶液的最优化条件、Fe3O4@GO@TiO2对其他染料的光催化降解性能等.因此,该实验覆盖面较广,实际教学内容可根据学生专业、实验室条件等进行灵活调节和改变.

