MLH1、PD-L1、HSF1、SIRT1在胃癌中的表达及临床意义
孔琼琼 钱立勇 (舟山医院病理科,浙江 舟山 312000)
胃癌发病率和死亡率呈不断上升趋势〔1〕。目前,手术切除是治疗胃癌主要手段,且取得很大进步。但由于大部分发病初期无明显症状,就诊时通常已进入中晚期,从而错失了最佳手术治疗时机,且很多患者在手术切除后出现复发或转移,影响预后,严重威胁患者生命健康〔2~4〕。胃癌发生发展是多个基因调节的多因素和多步骤的复杂过程,近年研究发现错配修复蛋白(MLH)1、程序性死亡受体配体(PD-L)1、热休克因子(HSF)1、沉默信息调节因子(SIRT)1在癌组织中异常表达,但在胃癌中研究甚少,缺乏可靠的参考价值〔5,6〕。本研究探讨MLH1、PD-L1、HSF1、SIRT1在胃癌中的表达及临床意义。
1 资料与方法
1.1一般资料 选择舟山医院于2014年1月至2018年12月143例胃癌患者癌组织标本及癌旁正常组织作为研究对象。纳入标准:①经临床表现、影像学及组织病理学证实为胃癌;②病理分期Ⅰ~Ⅲ期;③行胃癌根治性手术切除肿瘤;④临床资料完整。排除标准:①合并其他恶性肿瘤;②术前采用放疗、化疗者;③无完整规范的术后病理报告及随访资料。纳入的143例患者中,男85例,女58例;年龄41~79〔平均(62.74±7.18)〕岁;TNM分期:Ⅰ期35例,Ⅱ期67例,Ⅲ期41例;分化程度:高分化32例,中分化76例,低分化35例;肿瘤复发转移34例。
1.2免疫组化法测定MLH1、PD-L1、HSF1、SIRT1蛋白表达 取胃癌组织和癌旁组织标本石蜡包埋切片,以免疫组织化学SP法检测MLH1、PD-L1、HSF1、SIRT1蛋白表达。采用MLH1单克隆抗体、PD-L1单克隆抗体、HSF1单克隆抗体和SIRT1单克隆抗体工作浓度分别为1∶100、1∶100、1∶500和1∶500,由同一病理科人员严格依据北京中杉金桥生物公司免疫组织化学SP法试剂盒检测,以已知抗体阳性标本作为阳性对照,并且以磷酸盐缓冲液(PBS)代替一抗作为阴性对照。
1.3结果判定 每张切片选取连续5个高倍视野,每个视野计数200个细胞,对其中所有阳性染色分别计数,计算阳性细胞率。①按照阳性细胞率进行评分,0%~5%计为0分,6%~25%计为1分,26%~50%计为2分,>50%计为3分;②按照细胞染色强度进行评分,细胞未着色计为0分,淡黄色计为1分,棕黄色计为2分,棕褐色计为3分。将上述2种评分相乘,判定阳性表达,其中0~1分为阴性,2~5分为弱阳性,6~8分为阳性,9分为强阳性。
1.4统计学方法 采用SPSS19.0软件行χ2检验。
2 结 果
2.1MLH1、PD-L1、HSF1、SIRT1蛋白表达阳性率比较 癌组织MLH1、PD-L1、HSF1、SIRT1蛋白表达阳性率明显高于癌旁组织(P<0.05)。见表1。
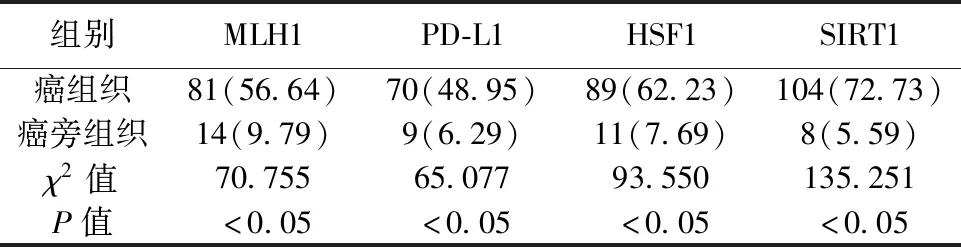
表1 两组MLH1、PD-L1、HSF1、SIRT1蛋白表达阳性率比较〔n=143,n(%)〕
2.2不同病理特征MLH1蛋白表达阳性率比较 不同性别、年龄、TNM分期和分化程度MLH1蛋白表达阳性率比较无明显差异(P>0.05);肿瘤复发转移者MLH1蛋白表达阳性率明显高于无肿瘤复发转移者(P<0.05)。见表2。
2.3不同病理特征PD-L1蛋白表达阳性率比较 不同性别、年龄和TNM分期PD-L1蛋白表达阳性率比较无明显差异(P>0.05);分化程度低和肿瘤复发转移者PD-L1蛋白表达阳性率明显高于分化程度较高无肿瘤复发转移者(P<0.05)。见表2。
2.4不同病理特征HSF1蛋白表达阳性率比较 不同性别、年龄、TNM分期和分化程度HSF1蛋白表达阳性率比较无明显差异(P>0.05);肿瘤复发转移者HSF1蛋白表达阳性率明显高于无肿瘤复发转移者(P<0.05)。见表2。
2.5不同病理特征SIRT1蛋白表达阳性率比较 不同性别、年龄、TNM分期和分化程度征SIRT1蛋白表达阳性率比较无明显差异(P>0.05);肿瘤复发转移者SIRT1蛋白表达阳性率明显高于无肿瘤复发转移者(P<0.05)。见表2。
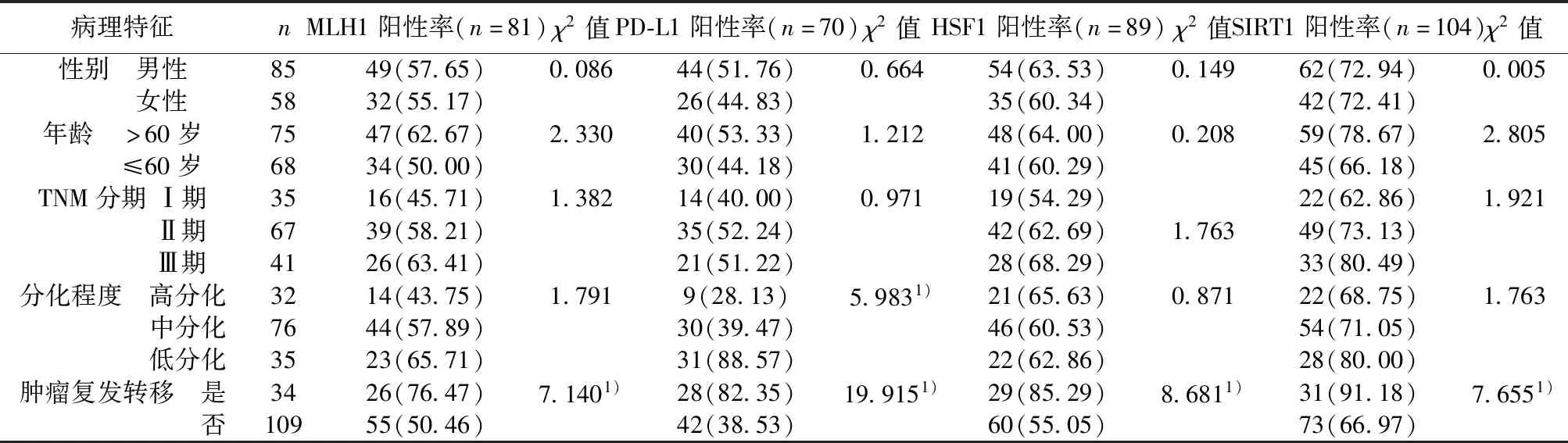
表2 不同病理特征MLH1、PD-L1、HSF1、SIRT1蛋白表达阳性率比较〔n(%),n=81〕
3 讨 论
胃癌具体发病机制尚未完全阐明,认为可能是多因素、多基因参与共同发病〔7,8〕。MLH1是错配修复酶,是遗传易感基因,具有降低自发性突变、维持基因组稳定、增强DNA复制的忠实性及修复DNA碱基错配的功能〔9〕。临床研究显示,恶性肿瘤组织中MLH1异常表达〔10,11〕。本研究结果表明胃癌组织中MLH1表达升高,且与肿瘤复发转移相关,故认为MLH1可作为推测胃癌复发转移潜能的敏感指标之一。PD-L1是B7家族成员,并且是程序性死亡分子1的配体,其在T细胞、B细胞、树突细胞和巨噬细胞中广泛表达,在上述细胞中表达受干扰素-γ刺激后;提呈抗原细胞表面的PD-L1分子及T细胞表面的成形死亡分子-1结合发挥作用,在免疫耐受的维持和诱导方面具有重要作用〔12,13〕。在多种恶性肿瘤细胞中PD-L1异常表达,并且和恶性肿瘤细胞的预后及恶性程度有关,和肿瘤浸润淋巴细胞密切相关;PD-L1和肿瘤浸润淋巴细胞表达的程序性死亡分子1结合,抑制肿瘤浸润淋巴细胞的功能,导致肿瘤免疫逃逸〔14,15〕。此外研究发现,肿瘤微环境中调节性T细胞(Treg)存在PD-L1分子表达〔16〕。目前,临床上关于PD-L1在胃癌中表达甚少,缺乏可靠的参考价值。本研究表明,胃癌组织中PD-L1表达升高,且与分化程度和肿瘤复发转移相关,故而认为PD-L1可作为推测胃癌复发转移和分化程度潜能的敏感指标之一。HSF1是真核细胞热休克应激反应的一种主要转录因子,且可编程肿瘤间质细胞,促进恶性肿瘤形成。HSF1在应激条件下可改变蛋白质的稳定性,促使细胞转化及恶性增殖,从而促使肿瘤细胞的生存和增殖;HSF1作为一种转录因子,可使肿瘤间质发生功能和结构上的重塑。研究报道显示,在食管鳞癌、前列腺癌、乳腺癌和肝癌等多种癌组织中HSF1表达上调〔17〕。本研究表明,胃癌组织中HSF1表达升高,且与肿瘤复发转移相关,故而认为HSF1可作为推测胃癌复发转移潜能的敏感指标之一。最新研究发现,SIRT1可依赖尼克酰胺腺嘌呤二核苷酸,使多种蛋白质的赖氨酸残基发生去乙酰化〔18〕。SIRT1属SIRTUIN家族,可调节基因表达,参与调节机体细胞内多种生物学事件,特别是细胞生存、凋亡及分化等代谢中具有重要作用。近期相关研究报道显示,SIRT1在急性髓细胞性白血病、前列腺癌及肝癌中的表达显著升高〔19,20〕。本研究表明,胃癌组织中SIRT1表达升高,且与肿瘤复发转移相关,故而认为SIRT1可作为推测胃癌复发转移潜能的敏感指标之一。

