L-半胱氨酸配位合成CdTe量子点的理论研究
陈 晓, 罗 惠, 李来才
(1.四川文理学院 化学化工学院, 达州 635000; 2. 四川师范大学 化学与材料科学学院, 成都 610066)
量子点(QDs)是一种新型无机纳米材料,由于其吸收范围广、发射范围窄、可调谐、量子产率高、光稳定性好等特点,在光学设备、生物传感和分析检测等领域引起了人们的日益关注[1-2]. 在分析检测方面,有研究者提出了一种基于生物分子介导合成的发光量子点用于无标记检测生物分子的新方法[3],其原理是量子点的信号强度与生物分子的含量密切相关. 例如,多肽被用于仿生合成CdZnTeS量子点,用于高度敏感的检测蛋白酶[4];以二硫醇为表面配体制备的CdTe/CdS量子点具有较高的量子产率和较好的稳定性,用于简便有效的检测碱性磷酸酶[5];将甲基丙烯酸磷酰胺基功能寡核苷酸与水溶性硫化镉锌芯/硫化锌壳量子点 (CdZnS/ZnS QDs)结合之后,合成了DNA传感器,用于无标记DNA检测[6];透明质酸功能化的MoS2量子点作为荧光探针检测透明质酸酶[7].
最近,有研究者通过L-半胱氨酸配体介导合成了CdTe QDs荧光材料[8]. 该量子点荧光材料有明显的红色荧光色,若在H2O2存在下,L-半胱氨酸会被I-催化氧化成L-胱氨酸,然而L-胱氨酸不是CdTe QDs合成的良好配体,从而导致荧光效应减弱. 该仿生合成材料有望用于生物体内的H2O2和葡萄糖的可视检测. 目前关于L-半胱氨酸配位合成CdTe量子点研究侧重于实验研究,相关理论研究报道较少. 本文旨在通过理论计算,从吸附能、键长、前沿分子轨道、电子构型等方面探究L-半胱氨酸和L-胱氨酸在基底CdTe上的吸附稳定性以及发光性能.
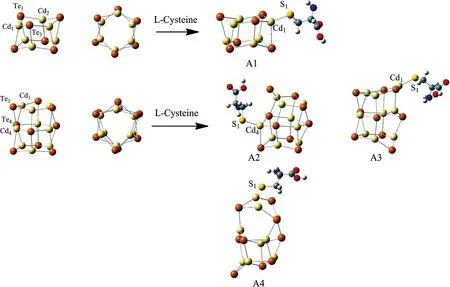

图1 L-Cysteine及L-Cystine分别在(CdTe)n(n=6,9)上的稳定吸附构型Fig.1 Stable adsorption configurations of L-Cysteine and L-Cystine adsorbed on (CdTe)n (n = 6,9)
2 计算方法
本文采用密度泛函理论(DFT)[9-11]进行分子结构优化,在Gaussian09软件中采用混合M05方法进行. 对于Cd和Te原子,采用LANL2DZ基组[12]. 对于C、H、O、S原子,采用6-31+G*基组[13]. 频率分析表明,最优结构是一个稳定的最小点,没有虚频率.
对于荧光激发波长,则采用含时密度泛函理论(TDDFT)[14-15]在基态优化的结构下计算基态到一批激发态的激发能和振子强度,把每个跃迁根据这两个量用高斯函数展宽,再把所有跃迁进行叠加,即得到UV-Vis光谱图. 吸附能定义为:
Eads=Eadsorbate+Ecluster-Eadsorbate/cluster
Eabsorbate为游离被吸附物质的能量,Ecluster为裸簇的能量,Eabsorbate /cluster为吸附后的簇的总能量. 因此,Eads正值越大,吸附能越高.
3 计算结果与讨论
3.1 稳定吸附构型的吸附能与键长分析
我们选择了合适的(CdTe)n簇作为模型,研究了L-半胱氨酸(L-Cysteine)及L-胱氨酸(L-Cystine)在CdTe QDs上的吸附. 考虑计算效率,选取(CdTe)n(n=6,9)进行优化. 我们尝试了点、线、面等不同的吸附位点,发现当(CdTe)n(n=6)吸附L-Cysteine和L-Cystine时,只有Cd原子点位能生成稳定的吸附结构. 当(CdTe)n(n=9)吸附L-Cysteine和L-Cystine时,Cd原子点位和面位点均能生成稳定的吸附结构. 这些簇的结构如图1所示. 吸附能和部分表征参数如表1所示.
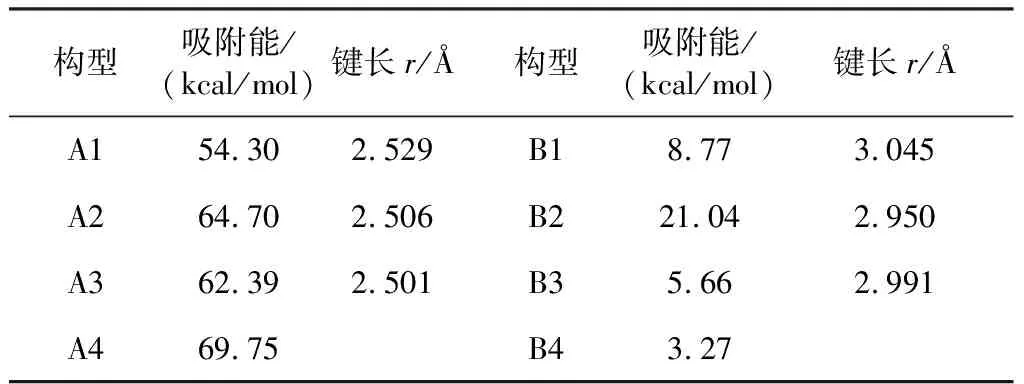
表1 L-Cysteine及L-Cystine分别在(CdTe)n(n = 6,9)上的吸附能及键长r
对L-半胱氨酸吸附而言,A1是(CdTe)6上最稳定的吸附构型,吸附能为54.30 kcal/mol(1 kcal/mol=4.186 kJ/mol),键长为2.529 Å;A4是(CdTe)9上最稳定的吸附构型,吸附能为69.75 kcal/mol. 对L-胱氨酸吸附,B1是(CdTe)6上最稳定的吸附构型,吸附能为8.77 kcal/mol,键长为3.045 Å. B2是(CdTe)9上最稳定的吸附构型,吸附能为21.04 kcal/mol,键长为2.950 Å. 对比表中数据可知,相比于L-半胱氨酸,L-胱氨酸在(CdTe)n(n=6,9)上各个吸附位点的吸附能更小,键长更大,吸附构型不稳定. 说明L-胱氨酸确实不是CdTe QDs合成的良好配体[8].
3.2 稳定吸附构型的能级分析
为了比较L-半胱氨酸、L-胱氨酸在(CdTe)n上的吸附能力,我们分别研究了吸附之前底物与被吸附物的前沿分子轨道(图2),以及吸附之后稳定吸附结构的前沿分子轨道(表2).

图2 吸附之前L-Cysteine、L-Cystine和(CdTe)n(n=6,9)的前沿分子轨道Fig.2 The frontier molecular orbitals of L-Cysteine,L-Cystine and (CdTe)n(n=6,9) before adsorption

表2 吸附之前(CdTe)n(n=6,9)以及吸附之后稳定结构的HOMO (eV),LUMO (eV),能隙值△Eq (eV)
从图2a中可以看出,吸附前,无论是(CdTe)6还是(CdTe)9,L-半胱氨酸的HOMO能量都要比它们的LUMO能量大,这有利于L-半胱氨酸向(CdTe)n(n=6,9)的电子转移,可以预测它们之间的电子相互作用较强. 然而,从图2b中可以看出,无论是(CdTe)6还是(CdTe)9,L-胱氨酸的HOMO能量值都比它们的LUMO能量要小,这表明从L-胱氨酸向(CdTe)n(n=6,9)的电子转移可能受到阻碍,相互作用可能较弱. 从表2中可以看出,L-半胱氨酸吸附之后,稳定吸附物的HOMO能级与LUMO能级均大幅度降低,稳定吸附构型的能隙值也有明显降低. 而L-胱氨酸吸附之后,稳定吸附物的HOMO能级和LUMO能级升降变化不明显,且稳定吸附构型的能隙值降低得也不如L-半胱氨酸的多. 以上分析可以看出,L-半胱氨酸吸附在(CdTe)n(n=6,9)上的稳定构型的△Eq较小,说明L-半胱氨酸内部的垂直跃迁能较小,有利于分子内部电子的激发,从而更容易产生分子荧光.
3.3 稳定吸附构型的电子结构分析
为了进一步比较L-半胱氨酸、L-胱氨酸与(CdTe)n(n= 6,9) 之间的电子相互作用强弱,我们列出了吸附之前(CdTe)n(n= 6,9)的净电荷值及吸附之后各种稳定构型的净电荷值(表3),以及稳定吸附构型的电子密度图(图3).
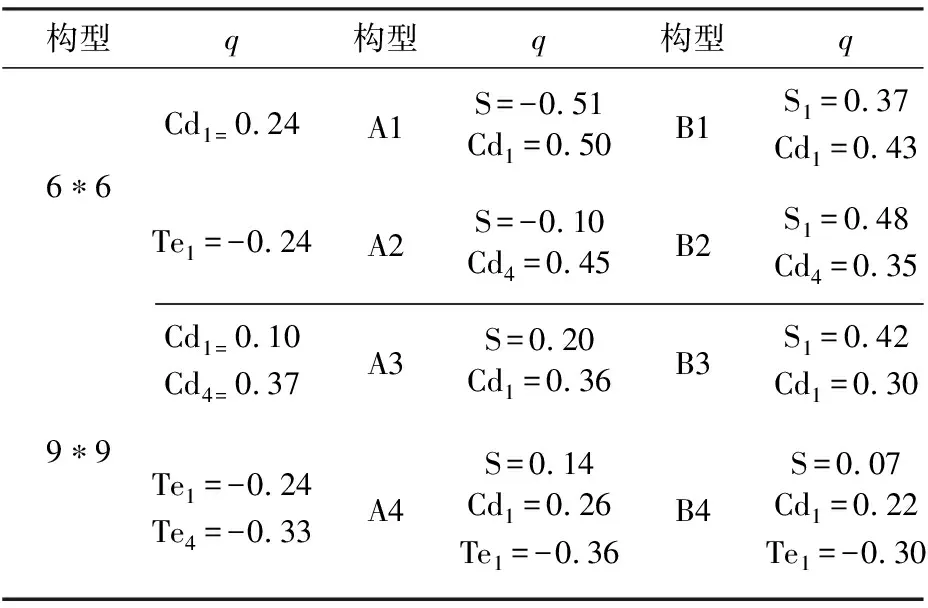
表3 吸附之前(CdTe)n(n = 6,9)的净电荷值及吸附之后各种稳定构型的净电荷值
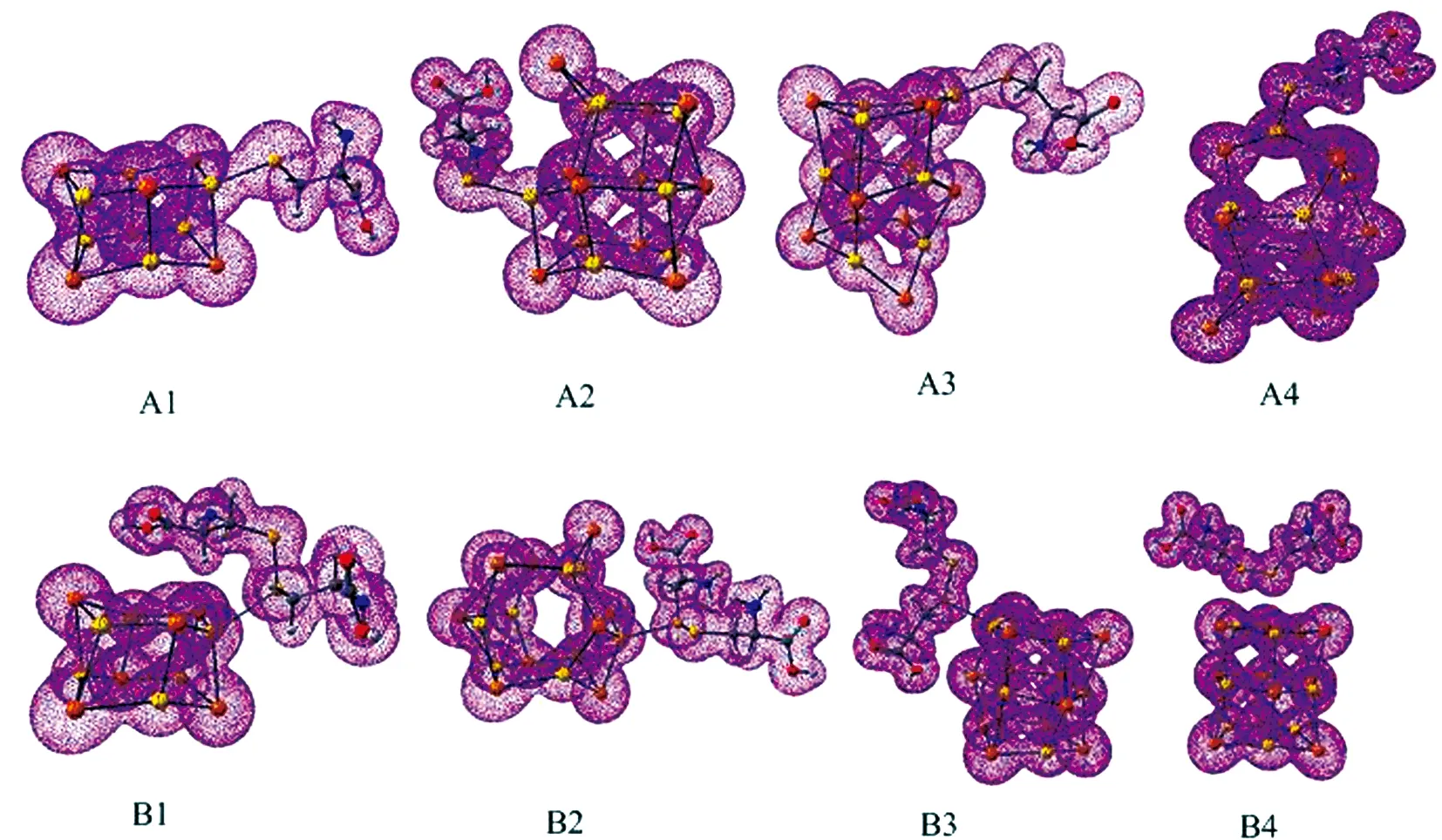
图3 L-半胱氨酸和L-胱氨酸在(CdTe)n(n = 6,9)上的稳定吸附构型的电子密度图Fig.3 The electron density maps of stable adsorption structures ofL-Cysteine and L-Cystine on (CdTe)n(n = 6,9)
对比表3中数据可看出,L-半胱氨酸和L-胱氨酸吸附之后,净电荷值都有明显变化,其中Cd原子的净电荷值增加,而Te原子的净电荷值减小,但是L-半胱氨酸吸附之后的净电荷变化值比L-胱氨酸的更大. 由此可进一步验证,L-半胱氨酸与基底之间的电子相互作用确实比L-胱氨酸的强. 从图3可以看出,无论是吸附在(CdTe)6还是(CdTe)9上,L-半胱氨酸与基底之间都存在电子云的重叠,可说明它们产生了一定程度的电子相互作用,而L-胱氨酸与基底之间的电子云有相互靠近的趋势,但看不出明显的重叠,说明其与基底之间的电子相互作用较弱. 以上可进一步说明,L-半胱氨酸在(CdTe)n(n= 6,9)上的吸附比L-胱氨酸的更稳定.
3.4 稳定吸附构型的荧光激发波长与吸收强度
为了探究荧光激发波长与吸附构型的稳定程度之间的关系,我们计算了各种稳定吸附构型在紫外可见光区的吸收情况,最大吸收波长如表4 所示,紫外可见吸收光谱如图4 所示.

表4 各种稳定吸附构型对紫外可见光的最大吸收波长λ
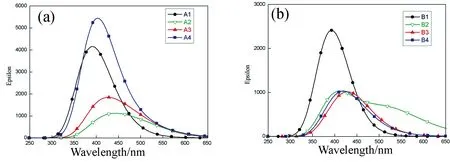
图4 L-半胱氨酸和L-胱氨酸在(CdTe)n(n=6,9)上的稳定吸附构型的紫外可见光谱图Fig.4 UV-Vis spectra of stable adsorption configurations of L-Cysteine and L-Cystine on (CdTe)n(n=6,9)
由表4可知,(CdTe)n(n=6,9)吸附L-半胱氨酸所有稳定吸附物荧光激发波长: 390~455 nm;(CdTe)n(n=6,9)吸附L-胱氨酸所有稳定吸附物荧光激发长:386~429 nm. 在图4中,若横向比较,可以看出无论是(CdTe)6还是(CdTe)9,在同一吸附位点,L-半胱氨酸吸附之后在最大吸收波长处对光的吸收强度都要比L-胱氨酸的大得多;若纵向比较,可以看出,仅对L-半胱氨酸在(CdTe)9上吸附而言,A4构型是(CdTe)9上最稳定的吸附构型,其在最大吸收波长处对光的吸收强度又比A2、A3构型的都要大;仅对L-胱氨酸在(CdTe)9上的吸附而言,B2是最稳定的吸附构型且其在最大吸收波长处对光的吸收强度比B3、B4构型的都略大.
由此可见,无论是(CdTe)n(n=6,9)上同一位点吸附不同的物质还是(CdTe)n(n=6,9)上不同位点吸附同一种物质,对紫外可见光的吸收程度与吸附构型的稳定程度之间均存在一定的相关性,即吸附构型最稳定,其在最大吸收波长处对光的吸收强度也最大. 此外,我们观察到L-半胱氨酸CdTe QDs的最大吸收波长大约是455 nm,与实验值570 nm[8]相比有一些偏差,可能存在部分能量损失.
4 结 论
本文采用密度泛函理论,研究了 L-半胱氨酸和L-胱氨酸在(CdTe)n(n=6,9)上的吸附特征. L-半胱氨酸能吸附在CdTe QDs上且吸附较稳定,L-胱氨酸在CdTe QDs上吸附稳定性较差. 通过电子密度、能级以及紫外可见吸收光谱分析可得出:L-半胱氨酸吸附之后对光的吸收更强,更容易吸收光能而产生分子荧光效应,而L-胱氨酸在(CdTe)n(n=6,9)上的吸附稳定性很差,对光的吸收也很弱,与实验中的结论符合. 该研究为L-半胱氨酸配位合成的CdTe QDs荧光材料用于生物体内H2O2和葡萄糖的检测提供理论支撑.

