盐酸埃克替尼片治疗晚期非小细胞肺癌的临床疗效及对免疫功能的影响
陈昕,薛璐,王鸣,刘春梅,于丽丽,王松,孙梯业,周静
(河北燕达医院 a.肿瘤科,b.病案统计室,河北 三河 065201)
肺癌是目前全球范围内发病率、病死率最高的恶性肿瘤疾病之一,其中非小细胞肺癌(non-small cell lung cancer,NSCLC)占80%~85%[1],但75%~80%的NSCLC患者确诊时已为晚期,5年总生存率为15%~25%[2]。化疗是大多数晚期肺癌的主要治疗手段,虽然可选择的化疗方案多样,但患者不耐受以及耐药问题的出现,严重影响患者的生活质量,故单纯化疗效果欠佳[3]。目前靶向治疗是临床癌症治疗的新方向,靶向药物进入体内后会使肿瘤细胞发生特异性死亡,且损伤正常组织的程度明显减轻,患者的药物不良反应发生率明显下降,能够有效提高癌症患者生活质量,延长生存期[4]。自2004年起,NSCLC的表皮生长因子受体(epidermal growth factor receptor,EGFR)基因突变与EGFR酪氨酸激酶抑制剂(EGFR-tyrosine kinase inhibitor,EGFR-TKI)之间的关系逐渐被报道[5]。EGFR是一类与细胞增殖、分化、黏附及迁移等相关的多功能跨膜糖蛋白,其在机体内的水平与肿瘤的发生、发展关系密切[6]。通过对NSCLC临床病理检测发现,EGFR基因突变在NSCLC发生、发展和转移过程中发挥重要作用[7]。目前EGFR-TKI在肺癌患者临床治疗中的应用最为广泛,对患者产生的影响也越来越大[8]。有研究报道,在完全切除的EGFR突变阳性的NSCLC患者中,辅助EGFR-TKIs可能是一种潜在的治疗选择[9]。盐酸埃克替尼片是我国自主研发的一种特异性选择EGFR-TKI,作用机制类似于吉非替尼和厄洛替尼,通过高效性能有效抑制表皮生长因子酪氨酸激酶,进而抑制肺癌细胞侵袭和增殖,促进肺癌细胞快速凋亡,延缓肺癌进展速度,延长患者生存期,改善生活质量,且价格低廉,易被患者接受[10],但有关其对晚期NSCLC患者免疫功能影响的研究较少。本研究旨在探讨盐酸埃克替尼片靶向治疗晚期NSCLC患者的临床疗效和对免疫功能的影响。
1 资料与方法
1.1一般资料 选取2012年1月至2013年6月河北燕达医院肿瘤科收治的225例经病理学确诊的晚期NSCLC患者作为研究对象。根据治疗方法不同分为靶向组(n=112)和化疗组(n=113),其中靶向组男58例、女54例,年龄30~83岁,平均(59±24)岁;TNM分期[11]:Ⅲa期43例,Ⅲb期35期,Ⅳ期 34例。化疗组男59例、女54例,年龄30~81岁,平均(56±25)岁;TNM分期:Ⅲa期43例,Ⅲb期 37期,Ⅳ期33例。两组患者的性别、年龄、TNM分期比较差异无统计学意义(P>0.05)。本研究经河北燕达医院医学伦理委员会批准。
1.2纳入与排除标准 纳入标准:①符合2014版《NCCN非小细胞肺癌临床实践指南》[12]中关于NSCLC的诊断标准,初治且经组织学或细胞学确诊,并证实为Ⅲ~Ⅳ期NSCLC患者;②年龄≥30岁,均有可测量的病灶,既往未行相关治疗;③预计生存时间≥3个月;④患者无严重心、肝、肾、脑等重要器官障碍;⑤入组时未发生转移者;⑥对本研究所用药物成分无禁忌;⑦基因检测EGFR为突变型;⑧患者及其家属均同意参与本研究;⑨所有患者依从性良好,配合治疗,随访资料完整。排除标准:①Ⅰ期、Ⅱ期NSCLC患者;②妊娠期妇女;③对所用抗癌药物过敏;④精神性疾病无法配合治疗;⑤自身免疫系统、血液系统疾病者;⑥存在放化疗禁忌证。
1.3治疗方法 靶向组患者给予盐酸埃克替尼片(浙江贝达药业股份有限公司生产,批号:A190404,规格:125 mg/片)125 mg口服治疗,每日3次,持续服药至患者无法耐受不良反应或病情进展时停药,改用吉非替尼片(英国阿斯利康制药有限公司生产,批号:190203)250 mg,口服,每日1次。化疗组患者采用培美曲塞(山东齐鲁制药有限公司生产,批号:0611804032,规格:100 mg/支)联合顺铂(山东齐鲁制药有限公司生产,批号:FA4A9019B,规格:10 mg/支)化疗方案:培美曲塞推荐剂量为500 mg/m2,仅可静脉滴注,临用前用0.9%氯化钠注射液20 mL溶解后,再用0.9%氯化钠注射液稀释后静脉滴注超过10 min,21 d为1个周期,在每周期的第1天给药。顺铂推荐剂量为75 mg/m2,培美曲塞滴注结束后30 min开始滴注,滴注时间超过2 h。接受顺铂治疗前或后应有适宜的水化方案,21 d为1个周期,治疗结束3个月后评价各项指标,后续采用同样的治疗方法进行治疗。
1.4观察指标 所有患者均于治疗前及治疗结束3个月后,于清晨5∶00采集空腹静脉血3~5 mL,采用CytoFLEX LX流式细胞仪[贝克曼库尔特商贸(中国)有限公司生产]检测CD4+和CD8+水平,计算CD4+/CD8+比值,严格按照说明书进行操作。首次治疗前1周内完成胸部X线或CT及头颅CT、骨扫描等影像学检查,治疗期间每周复查血常规、血生化和血清CD4+、CD8+水平,治疗结束后3个月评价疗效,以后每3个月、6个月复查胸腹部CT、头颅磁共振成像、骨扫描等检查及血常规、血生化和血清CD4+、CD8+等检验,1年后每年复查1次,必要时可6个月复查1次,出现新的症状及原有症状加重时随时复查,治疗前后影像学检查方法一致。所有患者均观察至随访结束,随访结束时间为2016年6月30日。本研究仅对患者治疗3年后的临床治疗效果和免疫功能进行评价,若患者病情没有进展,则采用最后一次联系患者的时间进行计算。无进展生存期:开始治疗至首次记录肿瘤进展的时间或死亡时间;总生存期:开始治疗至任何原因导致患者死亡的时间。
1.5疗效判断标准 治疗3年后,根据世界卫生组织实体肿瘤疗效评价标准[13]评定肿瘤控制效果:完全缓解,治疗后原有病灶完全消失并维持时间超过4周;部分缓解,治疗后病灶体积缩小>50%并维持时间超过4周,且未发现新的肿瘤病灶;病情稳定,治疗后病灶缩小25%~50%,且未出现新的肿瘤病灶;病情进展,治疗后病灶增大>25%或出现新病灶。疾病控制率=(完全缓解例数+部分缓解例数+病情稳定例数)/总例数×100%,总缓解率=(完全缓解例数+部分缓解例数)/总例数×100%。
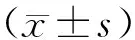
2 结 果
至2016年6月30日末次随访时间,225例患者中,有27例失访,失访率为12.00%,其中靶向组13例、化疗组14例。
2.1两组患者的临床疗效比较 靶向组的疾病控制率显著高于化疗组[67.68%(67/99)比38.38%(38/99)](χ2=17.053,P<0.001),总缓解率高于化疗组[42.42%(42/99)比21.21%(21/99)](χ2=10.267,P=0.010),靶向组的临床疗效优于化疗组(Z=3 297.000,P<0.001)。见表1。
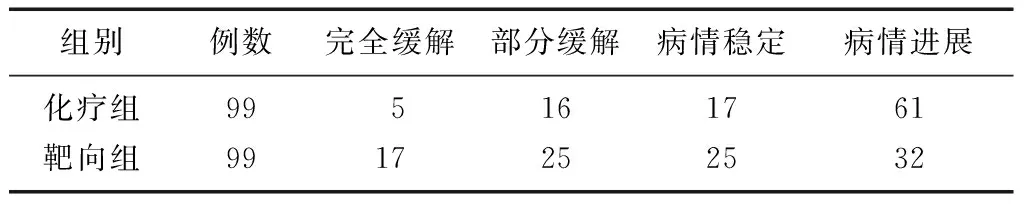
表1 两组晚期NSCLC患者的临床疗效比较 (例)
2.2两组患者治疗前后血清T细胞亚群水平比较 治疗前后血清CD4+、CD8+和CD4+/CD8+水平的主效应差异有统计学意义(P<0.01);不考虑测量时间,两组间血清CD4+、CD8+和CD4+/CD8+水平的主效应差异有统计学意义(P<0.01);血清CD4+、CD8+和CD4+/CD8+水平的时点间与组间存在交互作用(P<0.01),两组治疗前后各指标变化幅度不同,化疗组治疗后各指标低于治疗前,靶向组高于治疗前,且靶向组高于化疗组。见表2。
2.3两组患者无进展生存期比较 靶向组的无进展生存期为25.8个月(95%CI22.1~28.7个月),化疗组的无进展生存期为16.5个月(95%CI13.5~20.4个月),靶向组的无进展生存期明显长于化疗组(χ2=6.799,P=0.009),见图1。
2.4两组患者的总生存期比较 靶向组的总生存期为36.0个月,化疗组的总生存期为16.8个月,靶向组的总生存期显著长于化疗组(χ2=12.624,P=0.002),见图2。198例患者中有20例死亡,156例带瘤生存,22例无瘤生存。靶向组99例患者中,

表2 两组晚期NSCLC患者治疗前后血清T细胞亚群水平比较

NSCLC:非小细胞肺癌

NSCLC:非小细胞肺癌
无1例死亡,3年生存率为100.00%(99/99);化疗组99例患者中,79例仍然存活,3年生存率为79.80%(79/99),20例死于肺癌进展,3年死亡率为20.20%(20/99)。靶向组的3年生存率高于化疗组(χ2=22.247,P<0.001)。
3 讨 论
NSCLC是最常见的肺癌类型,其病因复杂,与吸烟、电离辐射、遗传等因素有关,早期无明显症状,约75%的患者到院时已处于中晚期,临床尚无有效的治疗手段。近年来,随着分子靶向药物研究的深入,NSCLC治疗取得了较大突破。其中,分子靶向治疗是通过针对性抑制基因转录和蛋白表达,调控细胞增殖分化,从而延缓肿瘤病灶的进展。EGFR-TKI属于一种新型的分子靶向治疗药物,其能与ATP竞争性结合,且能作用于EGFR受体酪氨酸区域,有助于抑制酪氨酸磷酸化和肿瘤的增殖、生长,对改善患者症状、生活质量均具有良好的效果[14]。
目前,EGFR-TKI已成为EGFR敏感突变阳性晚期肺癌患者常用的治疗方法之一。我国自主研发的EGFR-TKI盐酸埃克替尼片已于2014年11月13日获得国家食品药品监督管理局批准用于EGFR敏感性突变的晚期NSCLC患者,其主要通过抑制EGFR的酪氨酸激酶活性、阻断信号传递、抑制肺癌细胞的增殖和侵袭转移,发挥抑制肿瘤的作用,从而缓解肺癌患者的临床症状,提高生存率[15]。董燕等[16]研究表明,埃克替尼对EGFR21外显子突变和19外显子缺失突变的晚期NSCLC患者治疗效果显著。裴斐等[17]认为,盐酸埃克替尼一线治疗晚期NSCLC能延长患者生存期,改善预后生活质量。
现阶段,临床治疗晚期NSCLC仍以化疗为主,培美曲塞联合铂类被认为是标准的一线治疗方案[18]。培美曲塞是一种含有吡咯嘧啶基团的新型多靶点抗叶酸制剂,为第三代抗肿瘤新药,主要通过破坏癌细胞内叶酸正常代谢而达到控制肿瘤生长的目的[19]。顺铂为第一代铂类抗肿瘤药物,具有广谱抗癌作用,可对肿瘤细胞DNA复制起到抑制作用,并可损伤肿瘤细胞细胞膜结构,发挥抗肿瘤效果。本研究结果显示,靶向组的疾病控制率、总缓解率、3年生存率均显著高于化疗组(P<0.01),说明盐酸埃克替尼治疗EGFR基因突变晚期NSCLC患者效果比较理想,有助于提高临床疗效,促进患者早期恢复。这与Miyauchi等[20]的研究结果基本一致。故推测,盐酸埃克替尼可能通过选择性抑制ATP与EGFR酪氨酸激酶结合,从而有效降低EGFR-TKI的生物活性,阻断信号转导,有助于阻止肺癌细胞的增殖、侵袭与转移,促进肺癌细胞的凋亡,提高靶向药物治疗的准确性[21]。
近年来研究发现,免疫功能低下与恶性肿瘤的发生和发展密切相关[22]。有学者报道,NSCLC在发生和发展过程中常会导致患者免疫功能下降,出现免疫逃逸现象,从而促进NSCLC的发生发展[23],故在治疗过程中,对患者免疫机制的修复也成为抗癌的重要手段[24]。机体T淋巴细胞亚群主管细胞免疫,具有抵抗病毒和调节免疫系统的作用,其细胞功能取决于T淋巴细胞总值(CD3+)及其亚群(CD4+、CD8+)的相对组成。正常情况下,亚群间互相拮抗达到平衡,免疫失衡时,易引发疾病。CD3+CD4+T细胞和CD3+CD8+T细胞是两类重要的T淋巴细胞,其中前者能够分泌多种细胞因子并启动免疫应答、发挥抗肿瘤作用;后者能够抑制细胞免疫功能。当CD4+/CD8+T细胞比例降低时,细胞免疫功能受到抑制,进而造成癌细胞发生免疫逃逸[25]。王小磊和刘微微[26]报道,盐酸埃克替尼可以促进T细胞亚群的分化和白细胞介素-2的分泌,有利于机体发挥免疫作用,同时加强巨噬细胞的吞噬功能、激活自然杀伤细胞活性,增强机体发挥免疫功能,从而提高自然杀伤细胞活性和CD3+、CD4+、CD4+/CD8+细胞比例。有研究表明,埃克替尼在发挥抗癌治疗的同时不会损伤患者机体,且可通过下游的靶分子作用增强患者的免疫机制的应答,T淋巴细胞是机体发挥细胞免疫的主要细胞,CD4+能加强患者机体的免疫功能,CD8+能抑制细胞免疫的过程[27]。本研究结果显示,治疗后,靶向组的CD4+、CD8+表达水平均显著高于化疗组(P<0.01),说明埃克替尼可有效改善晚期NSCLC患者的免疫功能,与王小磊和刘微微[26]的研究结果基本一致,故推测盐酸埃克替尼片能有效调节和强化患者的免疫功能,有效控制肿瘤细胞的增殖,对正常细胞的影响较小[28],同时也能促进血清T淋巴细胞生长,调节T细胞亚群的表达水平,参与正向免疫调节[29],减少肿瘤负荷,增强机体抗肿瘤免疫功能,具有调节晚期NSCLC患者机体内环境的保护作用,从而提高患者临床治疗效果。
综上所述,盐酸埃克替尼片治疗EGFR突变型晚期NSCLC患者有助于提高临床疗效和血清T细亚群表达水平,安全性、依从性较高。但本研究的样本量较少,仅对埃克替尼靶向和一线化疗对晚期NSCLC患者治疗3年后的临床效果和免疫功能进行对比,缺乏与二代、三代靶向药物(吉非替尼、奥西替尼等)临床治疗效果的比较,今后需扩大样本量进一步研究。

